53
của nhóm methoxy trong khoảng δC 58,0-61,0 và cacbon oximethine trong khoảng 70,0-80,0 ppm.
- Các hợp chất pregnane glycoside thường được gắn thêm hợp phần benzoyl, cinnamoyl, tigloyl, acetyl và nicotiloyl. Đặc trưng phổ 13C-NMR của các nhóm này như sau:
Nhóm acetyl: 1 píc khoảng δC 165,0-170,0 ppm (O - C = O) và 1 píc trong vùng δC 20,0-25,0 ppm (cacbon methyl).
Nhóm benzoyl: 1 cacbon cacbonyl δC 165,0-170,0 ( O - C = O) và 4 cacbon vùng thơm, δC 100,0 – 150,0. Trong đó C-2 và C-6 chập tín hiệu, C-3 và C-5 chập tín hiệu, do đó đặc thù sẽ có 2 píc có cường độ cao gấp đôi các píc còn lại của vùng thơm.
Nhóm cinnamoyl: Có các píc tương tự như benzoyl. Khác biệt duy nhất là xuất hiện thêm 2 píc của nối đôi ngoài vòng trong khoảng δC 110,0 -130,0.
Nhóm tigloyl (Tig): 1 cacbon cacbonyl 165,0-170,0 ppm ( O - C = O), 1 nối đôi ngoài vòng với hai tín hiệu trong khoảng 120,0-140,0 ppm và 2 nhóm methyl.
3.1.2. Xác định cấu trúc của các hợp chất phân lập được từ loài G. sylvestre
3.1.2.1. Hợp chất GS1: gymsyloside A
Hình 3.4. Cấu trúc hóa học của hợp chất GS1
Hợp chất GS1 thu được dưới dạng bột vô định hình màu trắng. Công thức phân tử của hợp chất GS1 được xác định là C47H76O17 bởi sự xuất hiện của píc ion giả phân
54
tử m/z 935,4986 [M + Na]+ trên phổ khối lượng phân giải cao HR-ESI-MS (tính toán lý thuyết cho công thức [C47H76O17Na]+ là 935,4975). Kết quả trên cho thấy độ bất bão hòa của phân tử là 10. Phổ 1H NMR của GS1 cho tín hiệu của ba nhóm methyl ở δH 1,13 (3H, s), 1,53 (3H, s) và 1,05 (3H, d, J = 6,4 Hz); một proton olefin ở δH 5,32 (1H, br s), gợi ý đây là một aglycone pregnane, một khung chất chính và phổ biến nhất xuất hiện trong thành phần hóa học của chi Gymnema [5-7]; hai nhóm methyl ở δH 1,80 (3H, d, J = 7,2 Hz) và 1,85 (3H, s) và một proton olefin ở δH 6,98 (1H, q, J = 7,2 Hz) gợi ý sự có mặt của một gốc tigloyl; ba proton anome xuất hiện tại δH 4,84 (br d, J = 9,6 Hz), 4,57 (br d, J = 9,2 Hz) và 4,41 (br d, J = 8,0 Hz) cho thấy sự có mặt của 3 phân tử đường. Các giá trị hằng số tương tác J nêu trên khá lớn cho thấy các phân tử đường đều có liên kết β-glycoside. Ba nhóm methoxy có độ dịch chuyển hóa học khá thấp tại δH 3,39 (3H, s), 3,42 (3H, s) và 3,60 (3H, s) cùng với ba nhóm methyl bậc 2 tại δH 1,19 (3H, d, J = 6,0 Hz), 1,25 (d, J = 6,0 Hz) và 1,35 (d, J = 6,0 Hz) cho thấy ba phân tử đường nêu trên là ba đơn vị đường deoxy, một loại đường rất đặc trưng có mặt trong các hợp chất phân lập từ chi Gymnema [5, 8, 10]. Các dữ liệu phổ 1H NMR gợi ý hợp chất GS1 là một pregnane glycoside. Phổ 13C NMR và DEPT cho thấy hợp chất GS1 chứa 47 nguyên tử cacbon, trong đó có 21 nguyên tử cacbon rất đặc trưng thuộc khung pregnane (δC 39,8 × 2, 30,2, 79,2, 140,0, 120,0,
35,2, 74,9, 44,7, 38,0, 26,0, 75,1, 57,6, 89,3, 34,3, 33,5, 89,1, 11,2, 18,5, 71,5 và 18,9)
[6-8], [73], [74], 5 cacbon của gốc tigloyl (δC 169,1, 130,0, 139,5, 14,8 và 12,2) và 21 cacbon cũng rất đặc trưng cho ba phân tử đường cymaropyranose (Cym), oleandropyranose (Ole) và thevetopyranose (Thv) có mặt trong chi Gymnema. Các giá trị độ dịch chuyển hóa học cụ thể của ba phân tử đường nêu trên như sau: cym (δC 97,2 36,6, 78,5, 83,8, 69,9, 18,5, 58,5), Ole (102,6, 37,6, 80,2, 84,1, 72,5, 18,9, 57,6),
thv (104,3, 75,6, 87,7, 76,6, 73,2, 18,1 và 61,0) (Bảng 3.1). Tiến hành thủy phân hợp chất GS1 trong môi trường axit thu được các đường đơn. Chúng được xác định là D- cymarose, D-oleandrose và D-thevetose bởi sự phù hợp về giá trị độ quay cực riêng của chúng với các dữ liệu tương ứng đã được công bố (xem mục 2.2.2.4). Kết quả này cũng hoàn toàn phù hợp với các đường đơn có mặt trong chi Gymnema [5, 8, 10]. Để xác định vị trí của các nhóm thế cũng như trật tự liên kết của các phân tử đường, phổ HSQC, 1H-1H COSY và HMBC đã được thực hiện (Hình 3.5). Phổ HSQC để xác định các proton liên kết trực tiếp với cacbon, phổ HMBC để xác định tương tác xa 2J
55
và 3J giữa các proton và cacbon. Trên phổ HSQC, các tương tác giữa các proton và cacbon của các phân tử đường đã được xác định bao gồm Cym: H-1 (δH 4,84)/C-1 (δC 97,2), H-2 (δH 1,52 và 2,05)/C-2 (δC 36,6), H-3 (δH 3,82)/C-3 (δC 78,5), H-4 (δH
3,24)/C-4 (δC 83,8), H-5 (δH 3,79)/C-5 (δC 69,9), H-6 (δH 1,19)/C-6 (δC 18,5), OCH3
(δH 3,42)/C-6 (δC 58,5); Ole: H-1 (δH 4,57)/C-1 (δC 102,6), H-2 (δH 1,40 và 2,30)/C-2
(δC 37,6), H-3 (δH 3,36)/C-3 (δC 80,2), H-4 (δH 3,18)/C-4 (δC 84,1), H-5 (δH 3,36)/C-
5 (δC 72,5), H-6 (δH 1,35)/C-6 (δC 18,9), OCH3 (δH 3,39)/C-6 (δC 57,6); Thv: H-1 (δH
4,41)/C-1 (δC 104,3), H-2 (δH 3,18)/C-2 (δC 75,6), H-3 (δH 3,00)/C-3 (δC 87,7), H-4
(δH 3,00)/C-4 (δC 76,6), H-5 (δH 3,25)/C-5 (δC 73,2), H-6 (δH 1.25)/C-6 (δC 18.1),
OCH3 (δH 3,60)/(δC 61,0). Trên phổ 1H-1H COSY, các tương tác COSY giữa các proton của các phân tử đường đã được xác định cho phép xác định các giá trị độ dịch chuyển hóa học của cả proton và cacbon trong từng phân tử đường.
![]()
Hình 3.5. Các tương tác HMBC, COSY và NOESY chính của hợp chất GS1
Mặt khác, tương tác HMBC giữa H-19 (δH 1,13) và C-1 (δC 39,8)/C-5 (δC 140,0)/C- 9 (δC 44,7)/C-10 (δC 38,0), giữa H-6 (δH 5,32) với C-8 (δC 74,9)/C-10 (δC 38,0) khẳng
định vị trí của liên kết đôi tại C-5/C-6; tương tác HMBC giữa H-18 (δH 1,53) với C- 13 (δC 57,6)/C-14 (δC 89,3)/C-17 (δC 89,1); giữa H-21 (δH 1,05) với C-17 (δC 89,1)/C-
20 (δC 71,5) và giữa H-6 (δH 5,32)/H-7 (δH 2,11)/H-9 (δH 1,49) với C-8 (δC 74,9)
chứng minh vị trí của các nhóm hydroxyl tại C-8, C-14, C-17, C-20. Tương tác
56
HMBC giữa Tig H-5 (δH 1,85) và Tig C-1 (δC 169,1)/Tig C-2 (δC 130,0)/Tig C-3 (δC 139,5) và giữa Tig H-4 (δH 1,80) với Tig C-2/Tig C-3 xác định hợp phần tigloyl. Và tương tác ROESY giữa Tig H-4 (δH 1,80) và Tig H-5 (δH 1,85) cho thấy hợp phần tigloyl này có cấu hình (E). Ngoài ra, vị trí của nhóm tigloyl này tại C-12 (OH) đã được khẳng định bởi tương tác HMBC từ H-12 (δH 4,68) đến Tig C-1 (δC 169,1). Tương tác HMBC giữa Thv H-1 (δH 4,41) và Ole C-4 (δC 84,1); giữa Ole H-1 (δH 4,57) và Cym C-4 (δC 83,8); Cym H-1 (δH 4,84) và aglycone C-3 (δC 79,2) chỉ ra các liên kết của chuỗi đường là β-D-thevetopyranosyl-(1→4)-β-D-oleandropyranosyl- (1→4)-β-D-cymaropyranoside và vị trí của các liên kết đường tại C-3 của aglycone. Kết quả phân tích chi tiết các giá trị độ dịch chuyển hóa học của proton và cacbon của phần aglycon cũng như các tương tác giữa các proton và hằng số tương tác proton của hợp chất GS1 với các hợp chất pregnane thuộc chi Gymnema cho thấy sự phù hợp hoàn toàn với các dữ liệu đã được công bố về aglycon (20S)- 3β,8β,12β,14β,17β,20-hexahydroxypregn-5-ene, khung sarcostin đặc trưng, cũng như cấu hình D-cymarose, D-oleandrose và D-thevetose của tất cả các đường có mặt trong chi này. Đây là một đặc điểm thú vị về quá trình sinh tổng hợp của các hợp chất thứ cấp có khung pregnane glycoside của chi Gymnema [6, 7]. Ngoài ra, cấu hình tương đối của GS1 được khẳng định thêm một lần nữa bằng phân tích phổ ROESY. Tương tác NOESY giữa Hβ-1 (δH 1,80) với H-19 (δH 1,13) đã xác định được proton Hβ-1, suy ra được Hα-1 (δH 1,09), tương tác giữa Hα-1 (δH 1,09) với H-3 (δH 3,50) khẳng định Hα-3, suy ra nhóm 3-OHβ, tương tác giữa Hα-12 (δH 4,68) với Hα-9 (δH 1,49) khẳng định nhóm thế tại C-12 chiếm vị trí β. Bên cạnh đó, hằng số tương tác lớn Jaa Ha-12 và Ha-11 (J = 11,6 Hz) cho thấy H-12 chiếm vị trí axial,tương tác giữa Hα-12/axial với H-15 (δH 1,88) chứng tỏ cacbon CH2 tại C-15 cùng chiếm vị trí α/axial, tức là nhóm OH tại C-14 sẽ chiếm vị trí β (Hình 3.5). Ngoài ra tương tác NOESY giữa H-12 và H-20 (δH 3,45) xác định nhóm OH tại C-20 chiếm vị trí β. Nhóm OH tại C-17 được đề xuất có cấu hình β dựa trên kết quả công bố của tất cả các pregnan đã được phân lập từ chi Gymnema đều có nhóm 17-OHβ. Đây cũng là một đặc điểm về sinh tổng hợp các hợp chất pregnane từ chi này mà đã được các nhà khoa học trên thế giới đều khẳng định [5, 8, 10]. Bằng các phân tích phổ trên, cấu trúc của GS1 đã được làm sáng tỏ là (20S)-12β-tigloyloxy-3β,8β,14β,17β,20- pentahydroxypregn-5-ene 3-O-β-D-thevetopyranosyl-(1→4)-β-D-oleandropyranosyl-
(1→4)-β-D-cymaropyranoside. Đây là một hợp chất mới và được đặt tên là gymsyloside A.
Bảng 3.1. Số liệu phổ NMR của hợp chất GS1
a,b a,c a,b a,c
C δC δH (độ bội, J = Hz) C δC δH (độ bội, J = Hz)
39,8 | 1,09 (m, α)/1,80 (m, β) | 5 | 12,2 | 1,85 (s) | |
2 | 30,2 | 1,57 (m, β)/1,84 (m, α) | Cym | ||
3 | 79,2 | 3,50 (m) | 1 | 97,2 | 4,84 (br d, 9,6) |
4 | 39,8 | 2,20 (m, β)/2,33 (m, α) | 2 | 36,6 | 1,52 (m)/2,05 (m) |
5 | 140,0 | - | 3 | 78,5 | 3,82, m |
6 | 120,0 | 5,32 (br s) | 4 | 83,8 | 3,24, m |
7 | 35,2 | 2,11 (m) | 5 | 69,9 | 3,79, m |
8 | 74,9 | - | 6 | 18,5 | 1,19 (d, 6,0) |
9 | 44,7 | 1,49 (m) | 3-OMe | 58,5 | 3,42, s |
10 | 38,0 | - | Ole | ||
11 | 26,0 | 1,63 (m, α)/2,00 (m, β) | 1 | 102,6 | 4,57 (br d, 9,2) |
12 | 75,1 | 4,68 (dd, 4,0, 11,6) | 2 | 37,6 | 1,40 (m)/2,30 (m) |
13 | 57,6 | - | 3 | 80,2 | 3,36 (m) |
14 | 89,3 | - | 4 | 84,1 | 3,18 (m) |
15 | 34,3 | 1,83 (m, β)/1,88 (m, α) | 5 | 72,5 | 3,36 (m) |
16 | 33,5 | 1,74 (m) | 6 | 18,9 | 1,35 (d, 6,0) |
17 | 89,1 | - | 3-OMe | 57,6 | 3,39 (s) |
18 | 11,2 | 1,53 (s) | Thv | ||
19 | 18,5 | 1,13 (s) | 1 | 104,3 | 4,41 (br d, 8,0) |
20 | 71,5 | 3,45 (m) | 2 | 75,6 | 3,18 (m) |
21 | 18,9 | 1,05 (d, 6,4) | 3 | 87,7 | 3,00 (t, 6,8) |
Tig | 4 | 76,6 | 3,00 (t, 6,8) | ||
1 | 169,1 | - | 5 | 73,2 | 3,25 (m) |
2 | 130,0 | - | 6 | 18,1 | 1,25, d (6,0) |
3 | 139,5 | 6,98 (q, 7,2) | 3-OMe | 61,0 | 3,60 (s) |
4 | 14,5 | 1,80 (d, 7,2) |
Có thể bạn quan tâm!
-
 Phương Pháp Phân Lập Các Hợp Chất
Phương Pháp Phân Lập Các Hợp Chất -
 Các Thông Số Vật Lí Của Các Hợp Chất Phân Lập Được Từ Loài G. Sylvestre
Các Thông Số Vật Lí Của Các Hợp Chất Phân Lập Được Từ Loài G. Sylvestre -
 Các Thông Số Vật Lí Của Các Hợp Chất Phân Lập Được Từ Loài G. Latifolium
Các Thông Số Vật Lí Của Các Hợp Chất Phân Lập Được Từ Loài G. Latifolium -
 Nghiên cứu thành phần hóa học và hoạt tính ức chế enzym α-glucosidase và α-amylase của loài dây thìa canh - Gymnema sylvestre Retz. R.BR. EX SM. và dây thìa canh lá to - Gymnema latifolium Wall. EX wight - 10
Nghiên cứu thành phần hóa học và hoạt tính ức chế enzym α-glucosidase và α-amylase của loài dây thìa canh - Gymnema sylvestre Retz. R.BR. EX SM. và dây thìa canh lá to - Gymnema latifolium Wall. EX wight - 10 -
 Nghiên cứu thành phần hóa học và hoạt tính ức chế enzym α-glucosidase và α-amylase của loài dây thìa canh - Gymnema sylvestre Retz. R.BR. EX SM. và dây thìa canh lá to - Gymnema latifolium Wall. EX wight - 11
Nghiên cứu thành phần hóa học và hoạt tính ức chế enzym α-glucosidase và α-amylase của loài dây thìa canh - Gymnema sylvestre Retz. R.BR. EX SM. và dây thìa canh lá to - Gymnema latifolium Wall. EX wight - 11 -
 Nghiên cứu thành phần hóa học và hoạt tính ức chế enzym α-glucosidase và α-amylase của loài dây thìa canh - Gymnema sylvestre Retz. R.BR. EX SM. và dây thìa canh lá to - Gymnema latifolium Wall. EX wight - 12
Nghiên cứu thành phần hóa học và hoạt tính ức chế enzym α-glucosidase và α-amylase của loài dây thìa canh - Gymnema sylvestre Retz. R.BR. EX SM. và dây thìa canh lá to - Gymnema latifolium Wall. EX wight - 12
Xem toàn bộ 255 trang tài liệu này.
a đo trong methanol-d4, b100 MHz, c400 MHz
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
Hình 3.6. Phổ HR-ESI-MS của hợp chất GS1
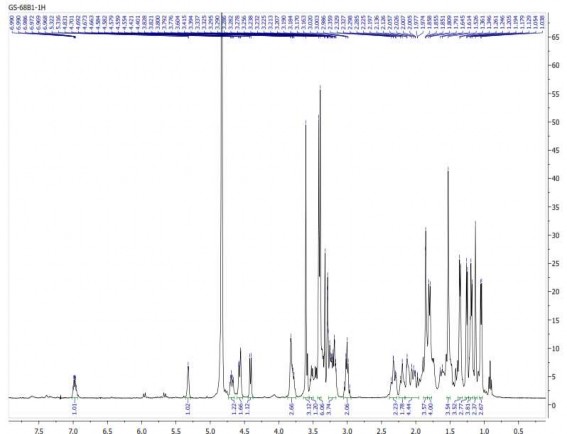
Hình 3.7. Phổ 1H NMR của hợp chất GS1
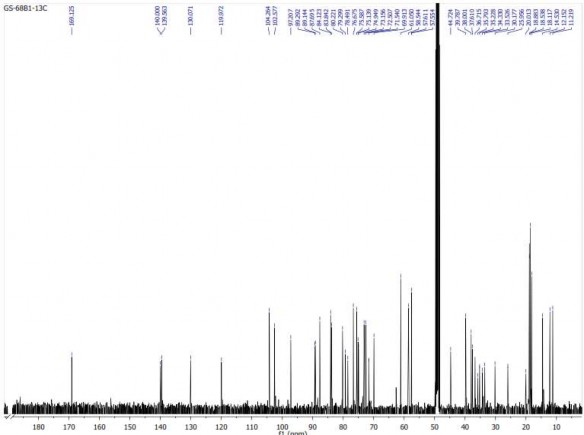
Hình 3.8. Phổ 13C-NMR của hợp chất GS1
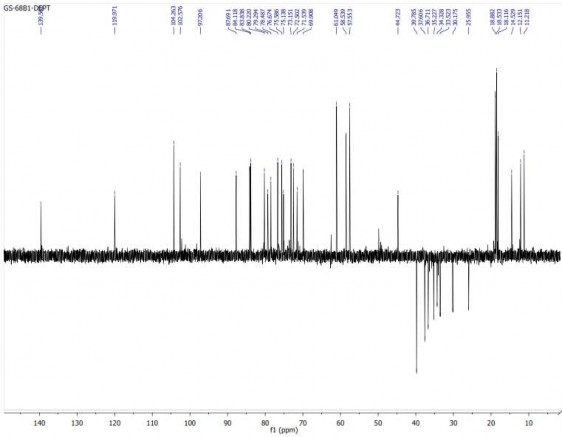
Hình 3.9. Phổ DEPT-135 của hợp chất GS1
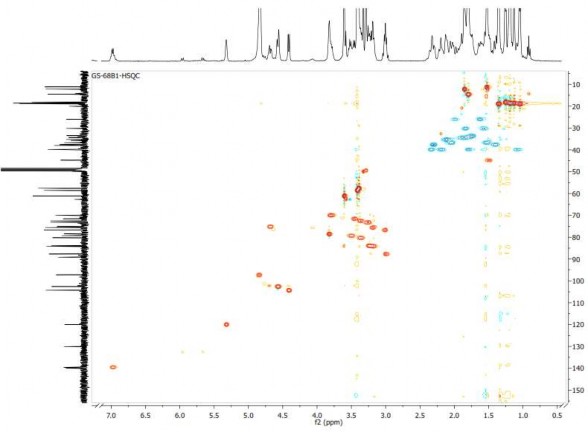
Hình 3.10. Phổ HSQC của hợp chất GS1
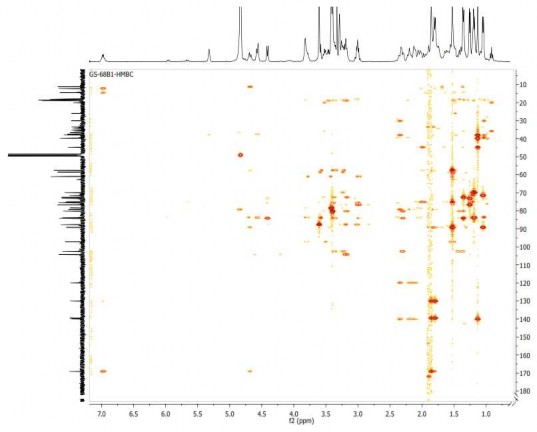
Hình 3.11. Phổ HMBC của hợp chất GS1






