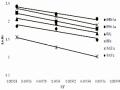
Như vậy, nhóm OH-/OH2 trong các tác nhân biến tính đã bị thay thế bởi ion H2PO4- (loại ion chiếm ưu thế trong khoảng pH 3 – 6). Kết quả trong các thí nghiệm nghiên cứu động học hấp phụ phù hợp với phương trình biểu kiến bậc 2 được đề nghị
cho quá trình hấp phụ hoá học. Tại pH cao, tâm hấp phụ bị thuỷ phân tạo thành kết tủa hiđroxit. Các hiđroxit này hấp phụ phốtpho trên bề mặt thông qua tương tác Van de Van. Do vậy có thể nói quá trình hấp phụ phốtpho trên bentonit biến tính xảy ra chủ yếu thông qua tương tác tĩnh điện, trao đổi phối tử ở pH thấp và hấp phụ thông qua tương tác Van de Van ở pH cao. Sự tham gia của anion phốtphat phải xuất hiện tại các tâm hoạt động trên bề mặt của bentonit biến tính. Vì vậy, quá trình hấp phụ các loại anion phốtphat có thể được suy đoán xảy ra theo 2 bước sau: (1) quá trình chuyển anion phốtphat từ dung dịch đến các tâm hoạt động của chất hấp phụ; (2) quá trình tạo phức hoá học/trao đổi ion tại các tâm hoạt động này [63, 148, 149, 161].
3.5.2. Thành phần hoá học và tính chất bề mặt của vật liệu sau khi hấp phụ
Thành phần hoá học của các mẫu bentonit biến tính sau khi hấp phụ phốtpho được trình bày trong Bảng 3.31 nhận thấy rằng, phần trăm khối lượng của K2O tăng lên một ít so với phần trăm khối lượng của các mẫu bentonit biến tính chưa hấp phụ phốtpho. Trong khi đó phần trăm khối lượng của P2O5 tăng lên đáng kể trong các mẫu sau khi hấp phụ phốtpho, điều này được giải thích là do các tâm hoạt động trên bentonit biến tính đã hấp phụ phốtpho vào trong cấu trúc của lớp aluminosilicat. Phần trăm khối lượng các thành phần còn lại thay đổi không đáng kể sau khi hấp phụ phốtpho.
Bảng 3.31. Thành phần hoá học của vật liệu sau khi hấp phụ phốtpho
SiO2 | Al2O3 | Fe2O3 | CaO | Na2O | K2O | La | P2O5 | |
B40-La-P | 51,25 | 17,82 | 7,76 | 1,82 | 0,69 | 1,65 | 4,68 | 0,42 |
B90-La-P | 52,82 | 15,79 | 7,03 | 1,98 | 0,92 | 1,72 | 5,51 | 0,57 |
BAl-P | 45,81 | 27,51 | 6,03 | 0,41 | 0,87 | 1,98 | 0,02 | 0,73 |
BFe-P | 37,01 | 10,16 | 34,78 | 0,23 | 0,72 | 1,96 | 0,01 | 0,77 |
BAlLa-P | 48,87 | 22,09 | 6,62 | 0,14 | 0,88 | 1,62 | 2,08 | 0,55 |
BAlFe-P | 36,91 | 12,14 | 34,71 | 0,16 | 0,69 | 1,94 | 0,04 | 0,96 |
Có thể bạn quan tâm!
-
 Giản Đồ Xrd Của Mẫu A) Balla-Tx Và B) Balfe-Tx Điều Chế Ở Nhiệt Độ
Giản Đồ Xrd Của Mẫu A) Balla-Tx Và B) Balfe-Tx Điều Chế Ở Nhiệt Độ -
 Sự Phụ Thuộc Của Dung Lượng Hấp Phụ Phốtpho Của Bentonit Biến Tính Theo Thời Gian.
Sự Phụ Thuộc Của Dung Lượng Hấp Phụ Phốtpho Của Bentonit Biến Tính Theo Thời Gian. -
 Các Tham Số Nhiệt Động Học Hấp Phụ Phốtpho Trên Bentonit Biến Tính
Các Tham Số Nhiệt Động Học Hấp Phụ Phốtpho Trên Bentonit Biến Tính -
 Sự Biến Đổi Nồng Độ Pht Trong Cột Đối Chứng Và Cột Xử Lý Với Tỉ Lệ B90- La:p Là 230:1, 340:1 Và 450:1.
Sự Biến Đổi Nồng Độ Pht Trong Cột Đối Chứng Và Cột Xử Lý Với Tỉ Lệ B90- La:p Là 230:1, 340:1 Và 450:1. -
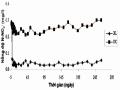
 Nồng Độ N-No2- (Mg/l) Của Khu Vực Xử Lý Và Khu Vực Đối Chứng Trong Thời Gian Thử Nghiệm: (♦) Khu Vực Xử Lý, (■) Khu Vực Đối Chứng.
Nồng Độ N-No2- (Mg/l) Của Khu Vực Xử Lý Và Khu Vực Đối Chứng Trong Thời Gian Thử Nghiệm: (♦) Khu Vực Xử Lý, (■) Khu Vực Đối Chứng. -
 Biến Đổi Mật Độ Tảo Của Nước Hồ Hoà Mục Trước Và Sau Khi Xử Lý Bằng B90-La: A) Khu Vực Xử Lý, B) Khu Vực Đối Chứng.
Biến Đổi Mật Độ Tảo Của Nước Hồ Hoà Mục Trước Và Sau Khi Xử Lý Bằng B90-La: A) Khu Vực Xử Lý, B) Khu Vực Đối Chứng.
Xem toàn bộ 213 trang tài liệu này.
c)
d)
Ảnh SEM của vật liệu bentonit biến tính (La, Al, Fe, Al/La, Al/Fe) sau khi hấp phụ phốtpho được chỉ ra trong Hình 3.33 cho thấy, khác biệt đáng kể về hình thái bề mặt của vật liệu trước và sau khi hấp phụ phốtpho. Đối với các mẫu B90-La, B40-La (Hình 3.9), BFe (Hình 3.15) và BAlFe (Hình 3.22) có hình thái kết bông và xuất hiện các mảng lớp được quan sát thấy trên bề mặt. Sau khi hấp phụ phốtpho, một số lá mỏng xuất hiện hình thành cấu trúc sắp xếp rất chặt làm giảm kích thước của các lớp sét. Đặc biệt đối với mẫu BAl-P và BAlLa-P có một số bọt nhỏ xuất hiện trên bề mặt, khác biệt nhiều so với các mẫu BAl (Hình 3.15) và BAlLa (Hình 3.22). Điều này cho thấy, phốtphat hấp phụ trên cách tâm hoạt động nằm ở giữa lớp sét, thay đổi cơ bản tính chất bề mặt của bentonit biến tính do sự nén mạng tinh thể [148]. Ngoài ra còn một số ít anion phốtphat hấp phụ trên bề mặt lớp sét, thấy rõ ràng nhất là các mẫu BAl-P và BAlLa-P [89].
a)
b)
c)
d)
e)
f)
e)
f)
Hình 3.33. Ảnh SEM của vật liệu sau khi hấp phụ phốtpho: (a) B40-La-P, b) B90- La-P, c) BAl-P, d) BFe-P, e) BAlLa-P và f) BAlFe-P.
3.5.3. Kết luận về khả năng hấp phụ phốtpho trong dung dịch nước bằng vật liệu bentonit biến tính
Đã khảo sát các yếu tố ảnh hưởng đến quá trình hấp phụ phốtpho trong nước của các vật liệu đã điều chế cho thấy, tốc độ hấp phụ xảy ra nhanh trong 1 giờ đầu, giảm dần khi thời gian tăng và đạt cân bằng sau 4 giờ hấp phụ. Dung lượng hấp phụ phốtpho của B90-La, B40-La, BAl, BFe, BAlLa và BAlFe thay đổi không nhiều trong khoảng pH 3 – 6, dung lượng hấp phụ giảm dần khi pH tăng lên 7 – 11. Động học hấp phụ phốtpho trên bentonit biến tính phù hợp với mô hình động học biểu kiển bậc
2 (R2 > 0,99) tốt hơn so với mô hình Elovich (R2 > 0,86). Dung lượng hấp phụ qe (mg/g)
tăng dần theo thứ tự sau: B40-La < B90-La < BAlLa < BAl < BFe < BAlFe. Hằng số tốc độ hấp phụ (k) của B90-La và B40-La lớn hơn nhiều so với các mẫu còn lại và được sắp xếp theo thứ tự: k(B90-La) >k(B40-La) >k(BAl) >k(BAlLa) >k(BFe) >k(BAlFe). Phương trình đẳng nhiệt Langmuir mô tả quá trình hấp phụ phốtpho trên bentonit biến tính tốt hơn so với phương trình Freundlich trong khoảng nhiệt độ khảo sát từ 25oC đến 35oC
Tính toán các tham số nhiệt động học ở các nhiệt độ khác nhau cho thấy quá trình hấp phụ phốtpho trên bentonit biến tính tự xảy ra trong điều kiện nhiệt động và thu nhiệt. Bentonit biến tính có khả năng hấp phụ tốt phốtpho trong dung dịch nước và giữ chặt chúng không cho giải phóng trở lại cột nước. Cơ chế hấp phụ phốtpho trong nước trên bentonit biến tính xảy ra chủ yếu thông qua tương tác tĩnh điện, trao đổi phối tử ở pH thấp và hấp phụ thông qua tương tác Van de Van ở pH cao. Phốtphat đã hấp phụ vào các tâm hoạt động nằm ở lớp xen giữa sét và trên bề mặt của bentonit biến tính thể hiện qua phân tích ảnh SEM.
3.6. KHẢO SÁT HẤP PHỤ PHỐTPHO CỦA BENTONIT BIẾN TÍNH LANTAN TRONG PHÒNG THÍ NGHIỆM
Trong phần nghiên cứu này, vật liệu hấp phụ được sử dụng là bentonit 90% montmorillonit biến tính lantan (B90-La) với lý do chính: (i) tốc độ hấp phụ phốtpho của B90-La lớn hơn nhiều so với các loại bentonit biến tính còn lại và (ii) khả năng lưu giữ phốtpho của B90-La là tốt nhất. Tiến hành khảo sát ảnh hưởng của lượng chất hấp phụ đến khả năng hấp phụ loại bỏ phốtpho trong dung dịch nước tổng hợp và nước hồ Hoà Mục phú dưỡng tiến hành với điều kiện khuấy liên tục và theo mô hình cột thí nghiệm.
3.6.1. Ảnh hưởng của lượng chất hấp phụ
Thí nghiệm tiến hành khảo sát ảnh hưởng của lượng chất hấp phụ được mô tả trong mục 2.6.1, với nồng độ phốtphat cố định là 10 mg/l, còn lượng chất hấp phụ sử dụng với tỉ lệ B90-La:P là 100:1, 230:1, 340:1 và 450:1 (tương ứng với 1; 2,3; 3,4 và 4,5 g/L). Lượng phốtpho hấp phụ tính toán từ phương trình (2.1) và sự phụ thuộc của dung lượng hấp phụ phốtpho vào lượng chất hấp phụ được trình bày trong Hình 3.34.
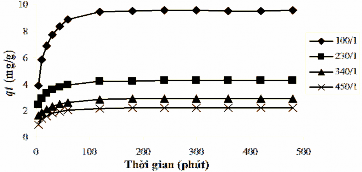
Hình 3.34. Dung lượng hấp phụ phốtpho của bentonit biến tính lantan theo thời gian trong điều kiện khuấy liên tục với dung dịch nước tổng hợp.
Từ Hình 3.34 nhận thấy rằng, lượng chất hấp phụ có ảnh hưởng đáng kể đến dung lượng hấp phụ phốtpho (qt) theo thời gian. Lượng phốtpho hấp phụ giảm khi khi lượng chất hấp phụ tăng, khả năng hấp phụ tăng mạnh trong thời gian 1 giờ đầu, sau đó giảm dần theo thời gian khảo sát. Đường thẳng tuyến tính vẽ t/qt qua t của phương trình động học biểu kiến bậc 2 chỉ ra trong Hình 3.35.
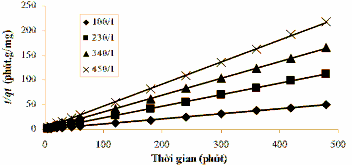
Hình 3.35. Phương trình động học biểu kiến bậc 2 áp dụng cho quá trình hấp phụ phốtpho trên bentonit biến tính lantan với dung dịch nước tổng hợp.
Trên cơ sở xác định hằng số tốc độ hấp phụ (k) và dung lượng hấp phụ phốtpho biểu kiến với lượng chất sử dụng từ phương trình động học biểu kiến bậc 2 (2.8). Bảng 3.32 cho biết hằng số tốc độ hấp phụ (k) và dung lượng hấp
phụ phốtpho biểu kiến (qe) của quá trình hấp phụ khi sử dụng lượng chất hấp phụ khác nhau. Từ kết quả chỉ ra trong Bảng 3.32 cho thấy, tất cả các hệ số tương quan của phương trình động học biểu kiến bậc 2 đều cao (R2 > 0,99), điều đó có nghĩa là quá trình hấp phụ phốtpho của bentonit biến tính lantan tuân theo phương trình động học biểu kiến bậc 2. Dung lượng hấp phụ phốtpho biểu kiến (qe) giảm khi lượng chất hấp phụ tăng và được sắp xếp theo thứ tự: qe(100:1) >qe(230:1) >qe(340:1) >qe(450:1).
Bảng 3.32. Các tham số động học hấp phụ phốtpho trên B90-La trong nước tổng hợp trong điều kiện khuấy liên tục với lượng chất hấp phụ là 1; 2,3; 3,4 và 4,5 g/L
Phương trình | qe (mg/g) | k (g/mg.phút) | R2 | |
100:1 | y = 0,1034x + 0,6334 | 9,6712 | 0,0169 | 0,9999 |
230:1 | y = 0,2313x + 1,1609 | 4,3234 | 0,0461 | 0,9999 |
340:1 | y = 0,3389x + 2,1591 | 2,9507 | 0,0532 | 0,9999 |
450:1 | y = 0,4460x + 2,9498 | 2,2422 | 0,0674 | 0,9998 |
Hằng số tốc độ hấp phụ (k) của quá trình hấp phụ tăng cùng chiều tăng với lượng chất hấp phụ chỉ ra trong Bảng 3.32. Sự phụ thuộc của hằng số tốc độ hấp phụ (k) vào lượng chất hấp phụ (W) được tính từ phương trình: k = ko.Wn [78], trong đó n là bậc của lượng chất hấp phụ. Lấy ln 2 vế của phương trình ta được: lnk = lnko
+ n.lnW. Kết hợp với số liệu chỉ ra trong Bảng 3.32 xây dựng đồ thị tuyến tính sự phụ thuộc của lnk vào lnW chỉ ra trong Hình 3.36.
lnk = 0.9157.lnW - 1.904
R2 = 0.9641
n
-2.5
-3
lnk
-3.5
-4
-4.5
-2.5 -2 -1.5 -1 -0.5
lnW
Hình 3.36. Sự phụ thuộc của lnk vào lnW.
Từ Hình 3.36 tính được bậc của chất hấp phụ (n) xấp xỉ 1, cho thấy tính chất bề mặt bao gồm diện tích bề mặt và tâm hấp phụ của B90-La không thay đổi nhiều
khi thay đổi lượng chất hấp phụ. Điều này cũng khẳng định thêm về tính đồng nhất về mặt hình thái và năng lượng của các tâm trên bề mặt vật liệu B90-La. Sự đồng nhất về mặt năng lượng này một lần nữa khẳng định đường đẳng nhiệt hấp phụ tuân theo phương trình Langmuir là hợp lí.
3.6.2. Khảo sát hấp phụ phốtpho của nước hồ bị phú dưỡng
Thí nghiệm được tiến hành khảo sát được mô tả trong mục 2.6.1 trong phần thực nghiệm, với lượng bentonit biến tính lantan sử dụng với tỉ lệ B90-La:P là 230:1; 340:1 và 450:1. Độ pH và nồng độ phốtpho hoà tan ban đầu của hồ Hoà Mục là 8,75 và 0,22 mgP/L. Sự biến đổi nồng độ phốtpho hoà tan (PHT) theo thời gian xử lý được chỉ ra trong Hình 3.37.
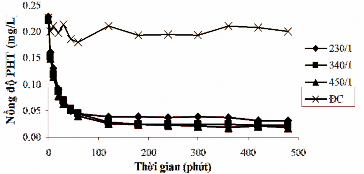
Hình 3.37. Sự biến đổi nồng độ PHT trong thí nghiệm đối chứng và thí nghiệm xử lý với tỉ lệ B90-La:P khác nhau theo thời gian.
Từ Hình 3.37 cho thấy rằng, nồng độ PHT trong thí nghiệm xử lý với nước hồ giảm nhanh trong thời gian đầu. Sau 2 giờ xử lý, nồng độ PHT giảm trong các thí nghiệm xử lý với tỉ lệ B90-La:P là 230:1, 340:1 và 450:1 lần lượt: từ 0,228 mg/l xuống 0,037 mg/l (83,77%), 0,221 mg/l xuống 0,028 mg/l (87,33%) và 0,224 mg/l xuống 0,025 mg/l (88,84%). Khi thời gian xử lý tăng từ 2 giờ lên 6 giờ thì nồng độ PHT trong các thí nghiệm xử lý giảm chậm, phần trăm nồng độ PHT giảm khi tỉ lệ xử lý B90-La:P là 230:1, 340:1 và 450:1 lần lượt 86,84%; 90,05% và 91,96% (Phụ lục P19.1). Nồng độ PHT trong thí nghiệm đối chứng thay đổi không đáng kể trong suốt thời gian khảo sát chỉ ra trong Hình 3.37. Như vậy nồng độ phốtpho hoà tan trong nước hồ Hoà Mục giảm là do bentonit biến tính lantan đã hấp phụ. Phần trăm hấp phụ phốtpho trong nước hồ thấp hơn so với nước tổng hợp là do trong hồ còn chứa các thành phần khác có khả năng cạnh tranh hấp phụ với phốtpho, chẳng hạn: axit humic, axit fluvic,v.v..
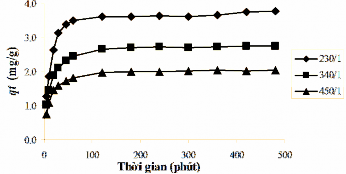
Dung lượng hấp phụ phốtpho biểu kiến (qt) tính từ phương trình (2.1) theo thời gian khảo sát được chỉ ra trong Hình 3.38 cho thấy rằng, khả năng hấp phụ phốtpho của vật liệu tăng theo thời gian, tăng nhanh trong 1 giờ đầu, sau đó giảm dần. So sánh dung lượng hấp phụ phốtpho biểu kiến với nước tổng hợp và nước hồ Hoà Mục chỉ trong Hình 3.34 và Hình 3.38 cho thấy, khả năng hấp phụ phốtpho trong nước hồ phú dưỡng thấp hơn trong nước tổng hợp. Khả năng hấp phụ phốtpho trong nước hồ với tỉ lệ xử lý khác nhau được sắp xếp theo thứ tự: qe(230/1) >qe(340/1) >qe(450/1).
Hình 3.38. Dung lượng hấp phụ phốtpho của B90-La theo thời gian trong điều kiện khuấy liên tục với nước hồ Hoà Mục ở liều lượng dùng khác nhau.
Mô hình động học biểu kiến bậc 2 thường được áp dụng để mô tả động học hấp phụ phốtpho trong nước hồ Hoà Mục trên vật liệu B90-La với liều lượng B90- La:P là 230:1, 340:1 và 450:1. Đường thẳng tuyến tính t/qt qua t được chỉ ra trong Hình 3.39 và các tham số động học tính toán từ Hình 3.39 chỉ ra trong Bảng 3.33.
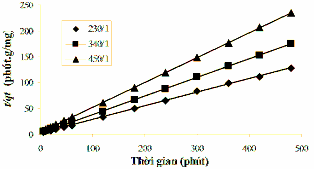
Hình 3.39. Phương trình động học biểu kiến bậc 2 áp dụng cho quá trình hấp phụ phốtpho trong nước hồ Hoà Mục trên B90-La với liều lượng dùng khác nhau.
Từ Bảng 3.33 nhận thấy rằng, tất cả các thí nghiệm xử lý với liều lượng sử dụng khác nhau đều tuân theo phương trình động học biểu kiến động học bậc 2 (2.8) với hệ số tương quan cao (R2 > 0,99). Dung lượng hấp phụ phốtpho biểu kiến
(qe) của bentonit biến tính lantan với liều lượng sử dụng với tỉ lệ B90-La:P là 230:1, 340:1 và 450:1 lần lượt là 3,8 mg/g, 2,80 mg/g và 2,08 mg/g. Giá trị này thấp hơn so với nước tổng hợp với tỉ lệ xử lý tương ứng lần lượt là 4,32 mg/g, 2,95 mg/g và 2,24 mg/g. Hằng số tốc độ (k) của quá trình hấp phụ tăng cùng với sự tăng lượng chất xử lý và giá trị này thấp hơn so với quá trình xử lý trong nước tổng hợp với tỉ lệ tương ứng chỉ ra trong Bảng 3.32.
Bảng 3.33. Các tham số động học hấp phụ phốtpho của B90-La trong nước hồ Hoà Mục với điều kiện khuấy liên tục ở liều lượng dùng khác nhau
Phương trình | qe (mg/g) | k (g/mg.phút) | R2 | |
230:1 | y = 0,2631x + 2,1664 | 3,8008 | 0,0320 | 0,9996 |
340:1 | y = 0,3574x + 3,0117 | 2,7980 | 0,0424 | 0,9999 |
450:1 | y = 0,4812x + 4,1211 | 2,0781 | 0,0562 | 0,9999 |
3.6.3. Khảo sát hấp phụ phốtpho trong nước hồ của vật liệu bằng cột
Thí nghiệm được tiến hành như mô tả trong mục 2.6.2 trong phần thực nghiệm. Nồng độ phốtpho hoà tan và một số đặc tính lý hoá của nước hồ Hoà Mục trước khi xử lý được trình bày trong Bảng 3.34.
Bảng 3.34. Nồng độ PHT và một số chỉ tiêu lý hoá của nước hồ Hoà Mục trước khi xử lý bằng B90-La
PHT (mg/l) | pH | DO (mg/l) | Độ dẫn điện (mS) | Ngày lấy mẫu | |
230:1 | 0,202 | 8,79 | 1,84 | 0,32 | 10/05/2010 |
340:1 | 0,205 | 8,84 | 1,92 | 0,31 | 24/05/2010 |
450:1 | 0,204 | 8,82 | 1,94 | 0,31 | 31/05/2010 |
ĐC | 0,211 | 8,76 | 1,82 | 0,32 | 10/05/2010 |
Sự biến đổi của nồng độ PHT trong cột đối chứng và cột xử lý với tỉ lệ B90- La:P là 230:1, 340:1 và 450:1 sau 72 giờ xử lý chỉ ra trong Hình 3.40 nhận thấy rằng, nồng độ PHT trong cột xử lý giảm dần theo thời gian khảo sát, khả năng hấp phụ phốtpho của bentonit biến tính lantan xảy ra nhanh trong thời gian đầu, sau đó chậm dần. Khả năng hấp phụ phốtpho trong cột chậm hơn so với khả năng hấp phụ phốtpho trong thí nghiệm với điều kiện khuấy liên tục (Hình 3.37). Sau 6 giờ xử lý, nồng độ PHT giảm khoảng 50%, trong khi đó khả năng hấp phụ phốtpho trong thí