Vm : Thể tích môi trường hòa tan (ml) Vl : Thể tích lấy mẫu (ml)
P : Hàm lượng hoạt chất theo nhãn
X: % lượng hoạt chất giải phóng trong môi trường ở giai đoạn trước
Đánh giá hình ảnh bề mặt và mặt cắt ngang lớp bao
Quan sát đặc điểm hình thái học của bề mặt và mặt cắt ngang của pellet bao film bằng kính hiển vi điện tử quét (SEM).
2.2.4.5. Đánh giá viên nang cứng chứa pellet bao
Hình thức
Viên nang chứa pellet hình cầu, màu vàng bên trong.
Định lượng mesalamin trong viên nang cứng chứa pellet bao
Phương pháp định lượng mesalamin trong viên nang cứng được tiến hành giống như định lượng mesalamin trong pellet nhân
Đánh giá độ hòa tan in vitro của viên nang cứng chứa pellet bao
Tiến hành giống điều kiện 2 của mục đánh giá độ hòa tan in vitro của pellet bao ở trên.
Đánh giá độ ổn định
Việc khảo sát độ ổn định của thuốc được thực hiện theo ASEAN [24]
Đối tượng thử: 3 mẻ viên nang mesalamin giải phóng tại đại tràng (quy mô 2 kg pellet nhân / mẻ bao) được đóng trong lọ thủy tinh nâu được đậy nút cao su và khằn bằng nắp nhôm.
Điều kiện bảo quản và thời điểm lấy mẫu kiểm tra như ghi ở bảng 2.10
Bảng 2.10. Điều kiện bảo quản và thời gian kiểm tra độ ổn định
Nhiệt độ (oC) | Độ ẩm tương đối (%) | Thời điểm kiểm tra | |
Điều kiện thực | Nhiệt độ phòng thí nghiệm (15 – 350C) | 60 - 90 % | 0, 3, 6, 9, 12 tháng |
Lão hóa cấp tốc | 40 ± 20C | 75 ± 5 % | 0, 3, 6 tháng |
Có thể bạn quan tâm!
-
 Thành Phần Pellet Nhân Tính Cho Lượng Pellet Chứa 500 Mg Mesalamin
Thành Phần Pellet Nhân Tính Cho Lượng Pellet Chứa 500 Mg Mesalamin -
 Thẩm Định Các Phương Pháp Định Lượng Mesalamin
Thẩm Định Các Phương Pháp Định Lượng Mesalamin -
 Đánh Giá Nghiên Cứu Tiền Công Thức
Đánh Giá Nghiên Cứu Tiền Công Thức -
 Đồ Thị Biểu Diễn Mối Tương Quan Giữa Nồng Độ Mesalamin Và Diện Tích Pic
Đồ Thị Biểu Diễn Mối Tương Quan Giữa Nồng Độ Mesalamin Và Diện Tích Pic -
 Độ Ổn Định Của Mes Huyết Tương Trong Các Điều Kiện Khác Nhau (N=6)
Độ Ổn Định Của Mes Huyết Tương Trong Các Điều Kiện Khác Nhau (N=6) -
 Kết Quả Thử Độ Hòa Tan Của Các Mẫu Pellet Sử Dụng Chất Hóa Dẻo Khác Nhau (N = 6)
Kết Quả Thử Độ Hòa Tan Của Các Mẫu Pellet Sử Dụng Chất Hóa Dẻo Khác Nhau (N = 6)
Xem toàn bộ 299 trang tài liệu này.
Các chỉ tiêu theo dõi: Hình thức, độ hòa tan, hàm lượng mesalamin trong viên. Dự đoán sự biến thiên của hàm lượng mesalamin trong thời gian bảo quản và dự đoán tuổi thọ của thuốc bằng phần mềm Minitab 17.
2.2.5. Phương pháp đánh giá in vivo trên chó
2.2.5.1. Đánh giá sự dịch chuyển pellet in vivo trên chó bằng phương pháp hình ảnh X-quang
Chó thử nghiệm
Tiến hành thí nghiệm trên 5 chó ta trưởng thành, giống đực, khỏe mạnh, cân nặng 10 đến 18 kg. Tất cả các chó được cho ăn uống và nuôi trong khi thử nghiệm với cùng điều kiện và được theo dõi về thể trạng trước khi uống thuốc, trong quá trình thử nghiệm và khi kết thúc giai đoạn lấy mẫu. Trước ngày dùng thuốc, chó ăn nhẹ trước 10 giờ đêm. Ngày dùng thuốc, chó không ăn sáng và uống thuốc trong tình trạng không gây mê. Chó ăn nhẹ sau 2 giờ uống thuốc. Sau 4 và 10 giờ, chó ăn chính. Chó uống nước tự do sau uống thuốc
Cách cho chó uống thuốc
Chó uống thuốc bằng cách cho thuốc trực tiếp vào họng chó, sau đó cho chó uống khoảng 50 ml nước kèm theo. Cho chó uống 1 viên nang đóng pellet nhân chứa chất cản quang bari sulfat, chất kích quang (dung dịch xenetix 6 mg/ml) và khoảng 125 mg mesalamin được bao film theo công thức màng bao tối ưu bằng cách cho thuốc trực tiếp vào họng chó, sau đó cho chó uống khoảng 50 ml nước kèm theo. Chụp X-quang ở thời điểm 2; 4; 7; 9 và 11 giờ sau khi uống.
2.2.5.2. Đánh giá hấp thu in vivo trên chó
Chó thử nghiệm
Số lượng chó thử nghiệm và điều kiện nuôi, ăn uống của chó được thực hiện giống mục 2.2.5.1.
Cách cho chó uống thuốc
Chó uống thuốc bằng cách cho thuốc trực tiếp vào họng chó, sau đó cho chó uống khoảng 50 ml nước kèm theo. Mỗi chó thí nghiệm được uống 4 viên nang cứng đóng pellet nhân. Mỗi viên nang cứng đóng pellet nhân chứa khoảng 125 mg mesalamin. Sau 1 tuần, chó sau khi uống pellet nhân được uống 4 viên nang cứng
đóng pellet bao giải phóng tại đại tràng bằng công thức tối ưu. Mỗi viên nang cứng đóng pellet bao chứa khoảng 125 mg mesalamin.
Lấy máu và xử lý mẫu
Mỗi lần lấy 2 ml máu, đựng vào ống nghiệm có chất chống đông Na2EDTA. Mẫu máu được lấy ở các thời điểm 0; 1; 2; 3; 4; 5; 6; 7; 8; 9; 10; 12; 15; 17 và 24 giờ. Các mẫu máu được ly tâm với tốc độ 5000 vòng / phút trong 15 phút ở nhiệt độ phòng. Tách lấy huyết tương và bảo quản ở tủ lạnh âm sâu -250C cho đến khi phân tích.
Định lượng mesalamin trong huyết tương
Bằng phương pháp ghi ở mục 2.2.4.1 thẩm định phương pháp phân tích khối phổ LC-MS/MS
2.2.6. Xử lý số liệu
Thiết kế thí nghiệm và tối ưu hóa bằng phần MODDE 12.0
Sử dụng add-in DDsolver [114] trong Microsoft Excel để xác định các mô hình động học giải phóng như động học bậc 0, động học bậc 1, động học bậc 2, Higuchi, Korsmeyer-peppas, Hixson-Crowell, Hopfenberg, Baker-Lonsdale, Makoid-Banakar, Peppas-Sahlin 1, Peppas-Sahlin 2, Quadratic, Weilbull 1, Weilbull
2, Weilbull 3, Weilbull 4, Logistic 1, Logistic 2, Logistic 3 của các công thức thí nghiệm. Mô hình động học giải phóng phù hợp nhất dựa trên tiêu chuẩn thông tin Akaike (AIC) và giá trị R2hiệu chỉnh để xác định T10 và T80.
Công thức tính AIC:
AIC= n×ln(δ2) +2×p
Trong đó:
- n là cỡ mẫu
- δ2 là phương sai
- p là tham số trong mô hình. Công thức tính R2hiệu chỉnh
R2hiệu chỉnh = 1 - (𝑛−1) x (1-R2)
(𝑛−𝑝)
Trong đó:
- n là số điểm lấy mẫu
- p là tham số của mô hình
So sánh các giá trị AIC và R2hiệu chỉnh khi khớp các mô hình động học. Giá trị AIC nhỏ nhất hoặc/và R2hiệu chỉnh lớn nhất tương ứng với mô hình phù hợp nhất, từ đó tính ra T10 và T80 dựa trên mô hình động học đã lựa chọn.
Dự đoán tuổi thọ của thuốc bằng phần mềm minitab 17.
Các kết quả nghiên cứu được xử lý và biểu thị trong luận án dưới dạng: giá trị trung bình ± độ lệch chuẩn (TB ± SD), n là số lần lặp lại thí nghiệm và RSD % là độ lệch chuẩn tương đối.
2.2.7. Dự đoán hấp thu mesalamin trong đường tiêu hóa chó từ viên nang chứa pellet mesalamin bao bằng phần mềm GastroPlusTM
Tiến hành khớp mô hình dược động học sinh lý bằng phần mềm GastroPlusTM xác định tỷ lệ dược chất hấp thu ở từng đoạn của đường tiêu hóa.
3. CHƯƠNG 3. KẾT QUẢ NGHIÊN CỨU
3.1. KẾT QUẢ THẨM ĐỊNH CÁC PHƯƠNG PHÁP ĐỊNH LƯỢNG MESALAMIN
3.1.1. Kết quả thẩm định phương pháp quang phổ tử ngoại UV-VIS
Tiến hành thẩm định phương pháp quang phổ tử ngoại – khả kiến UV-VIS như phương pháp trình bày ở mục 2.2.4.1 được kết quả như sau:
Độ đặc hiệu
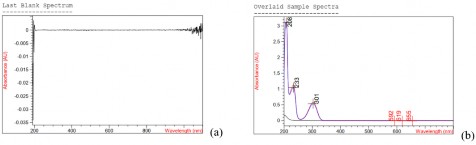
Hình 3.1. Phổ hấp thụ của (a) mẫu trắng, (b) mẫu chuẩn, thử, placebo trong môi trường pH 1,2
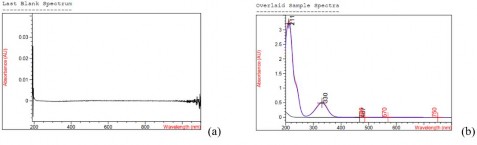
Hình 3.2. Phổ hấp thụ của (a) mẫu trắng, (b) mẫu chuẩn, thử, placebo trong môi trường pH 6,8
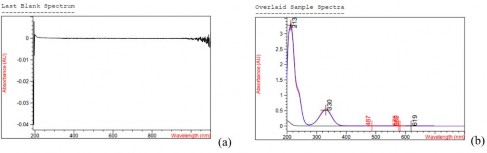
Hình 3.3. Phổ hấp thụ của (a) mẫu trắng, (b) mẫu chuẩn, thử, placebo trong môi trường pH 7,4
Kết quả so sánh phổ cho thấy phổ mẫu chuẩn trùng với phổ mẫu thử, có cực đại hấp thụ tương đương nhau trong môi trường pH 1,2; pH 6,8 và pH 7,4. Ngoài ra, ảnh hưởng của mẫu placebo trong 3 môi trường pH 1,2; pH 6,8 và pH 7,4 lần lượt là - 0,19 %, - 0,41 % và 0,53 % đạt yêu cầu ≤ 2 %
Độ phù hợp của hệ thống
Bảng 3.1. Kết quả khảo sát tính phù hợp của hệ thống (n=6)
Độ hấp thụ | |||
TB | SD | RSD | |
pH 1,2 | 0,64499 | 0,00113 | 0,18 % |
pH 6,8 | 0,57719 | 0,00087 | 0,15 % |
pH 7,4 | 0,62664 | 0,00141 | 0,22 % |
Kết quả phân tích cho thấy RSD của độ hấp thụ từ 6 lần đo mẫu chuẩn ≤ 2,0 %, vậy quy trình phân tích đạt tính phù hợp hệ thống.
Tính tuyến tính
1.0
0.8
0.6
0.4
0.2
0.0
pH 1,2
y = 0.0234x + 0.0016 R² = 0.9993
0 10 20 30 40
Nồng độ (µg/ml)
Độ hấp thụ (ABS)
Kết quả khảo sát tính tuyến tính như sau
0.8
0.6
pH 6,8
y = 0.021x + 0.0017 R² = 0.9987
0.4
0.2
0.0
0
10
20
30
40
Nồng độ (µg/ml)
Độ hấp thụ (ABS)
(a)
(b)
pH 7,4
1.0
0.8
y = 0.0218x - 0.0034
R² = 0.9974
0.6
0.4
0.2
0.0
0
10
20
30
40
Nồng độ (µg/ml)
Độ hấp thụ (ABS)
Hình 3.4. Đồ thị biểu diễn mối tương quan giữa độ hấp thụ và nồng độ mesalamin trong môi trường (a) pH 1,2; (b) pH 6,8 và (c) pH 7,4
Kết quả cho thấy nồng độ mesalamin trong dung dịch các môi trường pH 1,2; pH 6,8 và pH 7,4 và độ hấp thụ có mối quan hệ tuyến tính trong khoảng nồng độ khảo sát 0,3 – 34,7 µg/ml với hệ số tương quan R2 khoảng 0,99. Do đó, phương pháp đạt chỉ tiêu tính tuyến tính.
Độ đúng
Kết quả khảo sát độ đúng như sau:
Bảng 3.2. Kết quả khảo sát độ đúng
Mức nồng độ | Tỷ lệ hồi phục trung bình (%) | RSD (%) | |
pH 1,2 | 1% (0,3 µg/ml) | 100,57 | 0,95 |
10% (2,8 µg/ml) | 101,65 | 0,24 | |
80% (22,3 µg/ml) | 100,35 | 0,46 | |
125% (34,7 µg/ml) | 100,91 | 0,71 | |
pH 6,8 | 1% (0,3 µg/ml) | 101,29 | 0,91 |
10% (2,8 µg/ml) | 100,95 | 0,45 | |
80% (22,3 µg/ml) | 100,39 | 0,41 | |
125% (34,7 µg/ml) | 100,06 | 0,48 | |
pH 7,4 | 1% (0,3 µg/ml) | 99,50 | 1,02 |
10% (2,8 µg/ml) | 100,26 | 0,82 |
80% (22,3 µg/ml) | 100,23 | 0,93 |
125% (34,7 µg/ml) | 100,56 | 0,52% |
Kết quả ở bảng trên cho thấy tỷ lệ hồi phục nằm trong khoảng 97 – 103 % và RSD tỉ lệ thu hồi ở mỗi mức nồng độ ≤ 2,0 % đạt yêu cầu độ đúng.
Khoảng xác định
Từ kết quả thẩm định độ đúng và tính tuyến tính suy ra khoảng xác định của phương pháp: 0,3 µg/ml đến 34,7 µg/ml.
Độ chính xác
Kết quả độ lặp lại và độ chính xác trung gian như sau
Bảng 3.3. Kết quả khảo sát độ chính xác của phương pháp
Độ lặp lại (RSD, n = 6) | Độ chính xác trung gian (RSD, n = 12) | |
pH 1,2 | 0,87% | 0,95% |
pH 6,8 | 0,88% | 0,82% |
pH 7,4 | 0,32% | 0,69% |
Kết quả cho thấy độ chính xác đạt yêu cầu (RSD < 2 %).
3.1.2. Kết quả thẩm định phương pháp sắc ký lỏng hiệu năng cao
Tiến hành thẩm định như đã mô tả ở mục 2.2.4.1, thu được kết quả như sau:
3.1.2.1. Độ đặc hiệu
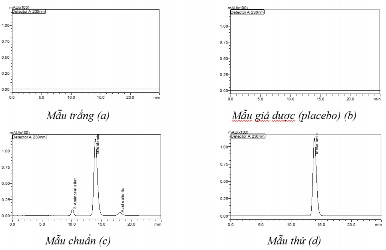
Hình 3.2. Sắc ký đồ mẫu trắng (a), mẫu placebo (b), mẫu chuẩn (c) và mẫu thử (d)






