![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
Ngoài ra, nhóm nghiên cứu Ph.D.Ty cũng đã xác định một cách tương đối hàm lượng của một số triterpene khung lupane có trong loài này:
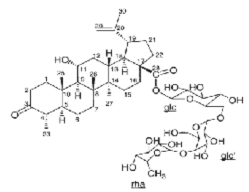
Tiếp tục nghiên cứu về loài cây này của Việt Nam, trong một số công bố gần đây, Phan Van Kiem và các cộng sự cho thấy ngoài những hợp chất trên, trong loài cây Ngũ gia bì hương thu hái ở miền Bắc Việt Nam còn chứa nhiều các hợp chất khác như quercitrin (22), eleutheroside E (23), 1-(3-D-glucopyranosyl-2,6- dimethoxy-4-propenylphenol (acantrifoside E) (24), 1-[β-D-glucopyranosyl- (1→6)-β-D-glucopyranosyl]-2,6-dimethoxy-4-propenylphenol (acantrifoside F) (25), syringin (26), (2R,3R)-2,3-di-(3,4-methylenedioxybenzyl)-butyrolactone (27), 3α-acetoxy-30-hydroxylup-20(29)-ene-23,28-dioic acid (acantrifoic acid A) (28), 3α-acetoxy-30-hydroxylup-20(29)-ene-23,28-dioic acid 28-O-α-L- rhamnopyranosyl-(1→4)-β-D-glucopyranosyl-(1→6)-β-D-glucopyranosyl ester (acantrifoside C) (29), 24-nor-11α-hydroxy-3-oxo-lup-20(29)-ene-28-oic acid 28-O- α-L-rhamnopyranosyl-(l→4)-β-D-glucopyranosyl-(1→6)-β-D- glucopyranosyl ester (acantrifoside B) (30), ent-kaur-16-ene-19-oic acid (31), ent-pimara-8(14),15-dien- 19-oic acid (32). Trong đó, các chất 24, 25, 28, 29 và 30 là những hợp chất lần đầu tiên phân lập được từ tự nhiên và chất 27 lần đầu tiên phân lập từ chi này [21], [22],
[23], [24], [25].
![]()
![]()
![]()
30
![]()
![]()
Bên cạnh đó, hai triterpene năm vòng thuộc khung taraxerane cũng được nhóm nghiên cứu phân lập được từ loài này [21]:
Như vậy, các kết quả nghiên cứu về thành phần hóa học của cây Ngũ gia bì hương (A. trifoliatus, họ Araliaceae) đã chỉ ra cây này có chứa nhiều triterpene, đặc biệt là triterpene khung lupane và trong đó nhiều chất có hàm lượng cao.
b. Hoạt tính sinh học
Bên cạnh nghiên cứu về thành phần hóa học, Phan Van Kiem và cộng sự cũng đã tiến hành nghiên cứu về hoạt tính của một dãy các chất được tách ra từ cây này. Kết quả cho thấy, các chất 22, 28 có hoạt tính kháng MAO khá cao ngay cả ở nồng độ thấp với các IC50 tương ứng là 0,12 và 0,18 mM. Các chất 31, 32 có hoạt tính kháng enzim COX-1 với giá trị IC50 = 0,15 và 0,19 μg/ml, do đó có hoạt tính kháng viêm rất tốt. Kiểm tra khả năng kháng vi khuẩn kiểm định, các chất 24, 31 lại có thể kháng vi khuẩn Gr (+) là B. subtilis và chủng S. aureus. Đặc biệt hợp chất phenylpropenyl glycosid mới, acantrifoside E (24) có hoạt tính kháng mạnh cả ba dòng tế bào ung thư người là tế bào ung thư biểu mô người (KB) IC50 = 1,22 μg/ml, tế bào ung thư màng tim người (RD) IC50 = 2,06 μg/ml, và tế bào ung thư gan người (Hep-2) IC50 = 0,75 μg/ml [26].
Năm 2004, Xing Fu Cai và các cộng sự cũng tiến hành khảo sát hoạt tính một số các hợp chất triterpene khung lupane có trong rễ loài A. koreanum. Kết quả cho thấy impressic acid (20), hợp chất có trong loài A. trifoliatus với hàm lượng lớn, thể hiện hoạt tính ức chế yếu tố sao chép (transcription factor) ở giá trị IC50 = 12,65 µM [27].
Ở một công bố mới nhất, năm 2013, một nhóm nghiên cứu đã tiến hành thử khả năng kháng viêm, chống phù nề ở chuột với ba dịch chiết n-hexane, dichloroform, methanol của lá A. trifoliatus. Kết quả cho thấy, dịch chiết methanol có khả năng chống viêm đáng kể, ở nồng độ cao nhất 500mg/kg thì có thể kháng đến 77,24% [28]. Bên cạnh đó, một nhóm nghiên cứu khác lại tiến hành thử khả năng cải thiện trí nhớ, chống trầm cảm với dịch nước từ lá loài này và cũng cho kết quả tốt [29].
Từ các kết quả đã được công bố về hai loài nghiên cứu cho thấy thành phần chính của chúng chủ yếu là các hợp chất flavonoid và triterpene khung lupane. Vì
vậy dưới đây là vài nét tổng quan về hóa học và hoạt tính sinh học của hai lớp chất chính này từ hai cây nghiên cứu.
1.2. Các hợp chất flavonoid
Flavonoid là lớp hợp chất có cấu trúc phenolic, tồn tại phổ biến trong thực vật. Có thể nói flavonoid được độc quyền hình thành trong thực vật (exclusively produced in plants), chỉ có thực vật mới có khả năng sinh tổng hợp flavonoid và được tìm thấy trong hầu như tất cả các loài thực vật nghiên cứu. Theo tính toán của các nhà khoa học, mỗi năm có khoảng 2% lượng cacbon được thực vật quang hợp (khoảng 109 tấn) được chuyển hóa thành các flavonoid và các hợp chất liên quan
[30]. Các hợp chất flavonoid được các nhà khoa học bắt đầu nghiên cứu từ những năm 1940, đến nay có hơn 9000 flavonoid đã được phân lập và xác định cấu trúc, hoạt tính sinh học. Thuật ngữ “Flavonoid” xuất phát từ chữ Latin flavus nghĩa là màu vàng – màu sắc của phần lớn các hợp chất flavonoid. Tuy nhiên, một số hợp chất có màu xanh, tím đỏ, một số khác lại không có màu cũng thuộc lớp này [31].
1.2.1. Cấu trúc hóa học
Flavonoid là những hợp chất tự nhiên có cấu tạo khung cacbon theo kiểu C6– C3–C6 hay nói cách khác khung cơ bản gồm hai vòng benzene A, B nối với nhau qua một mạch 3C. Trừ một số trường hợp mạch 3C hở như chalcone, đa số trường hợp mạch 3C đóng vòng với vòng A và tạo nên dị vòng C chứa O như [32]:
![]()
Hình 1.3: Vòng benzopyrano của hợp chất flavonoid [31]
Dựa trên mức độ oxi hóa của mạch 3C và vị trí của gốc aryl (vòng B) liên kết với vòng benzopyrano, người ta chia flavonoid thành các loại khác nhau như:
Euflavonoid: Các flavonoid có gốc aryl gắn ở vị trí C2 như anthocyanidin, flavan, flavan 3-ol, flavan 4-ol, flavan 3,4-diol, flavanone, 3-hydroxy flavone, flavone flavonol, dihydro chalcone, chalcone, aurone.
Isoflavonoid: Các flavonoid có gốc aryl gắn ở vị trí C3 như isoflavan, iso flav-3-ene, isoflavan-4-ol, isoflavanone, isoflavone, rotenoid, pterocarpan, coumestan, 3-arylcoumarin, coumaronochromen, coumaronochromon, dihydroisochalcon, homo-isoflavone.
Neoflavonoid: Các flavonoid có gốc aryl gắn ở vị trí C4. Nhóm hợp chất này chỉ mới thấy giới hạn trong một số loài thực vật như 4-arylchroman, 4-aryl couramin, dalbergion, 3,4-dihydro-4-arylcouramin, neoflavene.
Ngoài ra, người ta còn phân loại thành flavonoid, biflavonoid (những flavonoid dimer), triflavonoid (cấu tạo bởi 3 monomer flavonoid), flavonlignan (những flavonoid mà phân tử có phần cấu trúc lignan).
Trong thực vật flavonoid tồn tại ở nhiều dạng nhóm thế khác nhau như thêm nhóm hydroxyl, methyl hóa và quan trọng nhất là glycosyl hóa. Đôi khi, các nhóm thế khác như vòng thơm, aliphatic acid, sunfate, prenyl, methylendioxy hay isoprenyl cũng đính vào nhân flavonoid và các glycoside của chúng.
3' | O OH Flavanol | ||||
7 | 8 A | 2' 9 O 2 1' C | B 6' | 4' 5' | |
6 | 5 | 4 3 10 | |||
O | |||||
Flavone | |||||
Flavanone | Anthocyanidin | ||||
Isoflavone |
Chalcone | ||||
Có thể bạn quan tâm!
-
 Nghiên cứu hóa học và thăm dò hoạt tính sinh học của loài thông lá dẹt (pinus krempfii lecomte) và ngũ gia bì hương (acanthopanax trifoliatus L. Merr) - 1
Nghiên cứu hóa học và thăm dò hoạt tính sinh học của loài thông lá dẹt (pinus krempfii lecomte) và ngũ gia bì hương (acanthopanax trifoliatus L. Merr) - 1 -
 Nghiên cứu hóa học và thăm dò hoạt tính sinh học của loài thông lá dẹt (pinus krempfii lecomte) và ngũ gia bì hương (acanthopanax trifoliatus L. Merr) - 2
Nghiên cứu hóa học và thăm dò hoạt tính sinh học của loài thông lá dẹt (pinus krempfii lecomte) và ngũ gia bì hương (acanthopanax trifoliatus L. Merr) - 2 -
 Tình Hình Nghiên Cứu Về Thành Phần Hóa Học Và Hoạt Tính Sinh Học Loài Thông Lá Dẹt
Tình Hình Nghiên Cứu Về Thành Phần Hóa Học Và Hoạt Tính Sinh Học Loài Thông Lá Dẹt -
 Chuyển Hóa Hóa Học Hợp Chất Triterpene Khung Lupane Và Hoạt Tính Sinh Học Của Chúng
Chuyển Hóa Hóa Học Hợp Chất Triterpene Khung Lupane Và Hoạt Tính Sinh Học Của Chúng -
![Khử Hoá Nối Đôi 20(29) Của Betulinic Acid [65], [66]](data:image/svg+xml,%3Csvg%20xmlns=%22http://www.w3.org/2000/svg%22%20viewBox=%220%200%2075%2075%22%3E%3C/svg%3E) Khử Hoá Nối Đôi 20(29) Của Betulinic Acid [65], [66]
Khử Hoá Nối Đôi 20(29) Của Betulinic Acid [65], [66] -
![Hoạt Tính Chống Oxi Hóa: Thực Hiện Theo Phương Pháp Dpph [80], [81]](data:image/svg+xml,%3Csvg%20xmlns=%22http://www.w3.org/2000/svg%22%20viewBox=%220%200%2075%2075%22%3E%3C/svg%3E) Hoạt Tính Chống Oxi Hóa: Thực Hiện Theo Phương Pháp Dpph [80], [81]
Hoạt Tính Chống Oxi Hóa: Thực Hiện Theo Phương Pháp Dpph [80], [81]
Xem toàn bộ 169 trang tài liệu này.
Bảng 1.3. Một số khung flavonoid thường gặp
1.2.2. Hoạt tính sinh học
Flavonoid là một nhóm các hợp chất được gọi là “những người thợ sửa chữa sinh hóa của thiên nhiên” nhờ vào khả năng sửa chữa các phản ứng cơ thể chống lại các hợp chất khác trong các dị ứng nguyên, virus và các chất sinh ung. Nhờ vậy chúng mang lại những hoạt tính quý báu.
Có thể nói hoạt tính chống oxi hóa là hoạt tính đặc trưng của các hợp chất flavonoid. Theo Rice-Avans và các cộng sự [33], khả năng chống oxi hóa có thể được giải thích dựa vào các đặc điểm cấu trúc phân tử của chúng như: Trong phân tử có chứa các nhóm hydroxy liên kết trực tiếp với vòng thơm có khả năng nhường hydro giúp các flavonoid có thể tham gia vào các phản ứng oxi hóa khử, bắt giữ các gốc tự do; chứa các vòng thơm (vòng benzene, vòng dị nguyên tố) và các liên kết bội (liên kết C=C, C=O) tạo nên hệ liên hợp giúp bền hóa các gốc tự do được hình thành khi chúng bắt giữ các phần tử oxi hoạt động; chứa nhóm có thể tạo phức chuyển tiếp với các ion kim loại như catechol…giúp làm giảm quá trình sản sinh ra các phần tử oxi hoạt động. Ví dụ, từ rễ loài Scutellaria baicalensis đã phân lập được ba flavonoid chính là wogonin (5,7-dihydroxy-8-methoxyflavonoid) (35), baicalein (5,6,7-trihydroxy-flavone) (36) và dẫn xuất 7-glucuronid của nó (baicalin) (37). Kết quả thử hoạt tính chống oxi hóa của các chất này cho thấy baicalin có hoạt tính chống oxi hóa tốt nhất (72%). Như vậy, việc gắn thêm một nhóm glucuronid tại C-7 làm cho khả năng chống oxi hóa tăng lên đáng kể [34].
![]()
![]()
![]()
Trong một nghiên cứu, Das và Pereira chỉ ra rằng trong phân tử flavonoid có chứa các nhóm cacbonyl ở C-4 và liên kết đôi giữa C-2, C-3 thì có khả năng chống oxi hóa cao như butein (38) [35]:
![]()
Rất nhiều công trình nghiên cứu đã cho thấy sự kỳ diệu của các hợp chất flavonoid trong việc điều trị các căn bệnh ung thư. Hai flavones 39, 40 đã được tìm thấy từ lá của loài Baeckea frutescens (Myrtaceae) có khả năng gây độc tế bào rất mạnh (IC50 = 0,25μg/ml) đối với dòng tế bào bạch cầu (L1210) [36]:
![]()
![]()
![]()
Hoạt tính chống ung thư bằng cách thay đổi hình thái tế bào dẫn đến khả năng ức chế sự phân bào của các dòng tế bào ung thư đã được tìm thấy ở các hợp chất naringenin (41) và kaempferol 3-O-(2’’,6’’-di-O-p-trans-coumaroyl) glucosid (42), phân lập từ hoa của loài Melastoma malabathricum trên dòng tế bào ung thư vú (MCF-7) với các giá trị tương ứng là 0,28 và 1,3μM [37].
Bên cạnh đó, các hợp chất flavonoid còn cho thấy khả năng kháng virus HIV. Baicalin (5,6,7-trihydroxy-flavon 7-glucuronide) (37) được phân lập từ cây Scutellaria baicalensis có khả năng ức chế trực tiếp lên virus HIV; hay hai biflavone là hinokiflavone (43) và robustafavone (44) có thể ức chế enzym phiên mã ngược HIV-1 với IC50 = 65µM [38], [39].
![]()
![]()
Ngoài ra, các hợp chất flavonoid còn thể hiện các hoạt tính như kháng viêm, kháng khuẩn, tiểu đường…Do sự gia tăng số người mắc bệnh tiểu đường và các biến chứng nguy hiểm mà căn bệnh này gây ra nên các hoạt tính của chúng đối với căn bệnh tiểu đường đang được các nhà khoa học đặc biệt quan tâm. Các kết quả nghiên cứu đã chỉ ra rằng các flavonoid tự nó có vai trò như chất kích thích insulin hay bắt chước chức năng của insulin; ngoài ra chúng còn có sự ảnh hưởng đến hoạt động của các enzym trong quá trình chuyển hóa đường…[40],[41]. Từ rễ của cây Dorstenia psilurus (họ Dâu tằm, Moraceae), Tabopda và cộng sự đã phân lập được hợp chất dạng prenyl flavonol dorsilurin F (45) có hoạt tính ức chế enzym α- glucosidaza tốt với giá trị IC50 = 4,13μM. Đặc biệt, cũng với enzym α-glucosidaza, một dẫn xuất của luteolin là 6-hydroxyluteolin (46) có thể ức chế đến 92% ở nồng
độ 500μM [42].
OH
HO O
OH
OH O
45
OH
O
OH
HO
HO
OH O
46
O
O
OH
HO H OH O
47
Từ cây Eysenhardtia platycarpa (họ Đậu, Fabaceae), 5,4,1”-trihydroxyy-6,7- (3”,3”-dimethylchromano) flavone (47) đã được phân lập. Chất này có khả năng chống lại sự tăng đường huyết ở chuột với liều lượng 30 mg/kg trọng lượng cơ thể [43].





![Khử Hoá Nối Đôi 20(29) Của Betulinic Acid [65], [66]](https://tailieuthamkhao.com/uploads/2022/05/09/luanghien-cuu-hoa-hoc-va-tham-do-hoat-tinh-sinh-hoc-cua-loai-thong-la-det-6-120x90.jpg)
![Hoạt Tính Chống Oxi Hóa: Thực Hiện Theo Phương Pháp Dpph [80], [81]](https://tailieuthamkhao.com/uploads/2022/05/10/luanghien-cuu-hoa-hoc-va-tham-do-hoat-tinh-sinh-hoc-cua-loai-thong-la-det-7-120x90.jpg)