3.1.1.4. Chất 70 (LHRn7 = LHRn3): Stigmast-4-en-3-on.
- Phổ hồng ngoại của chất 70 cho đỉnh hấp thụ của nhóm carbonyl liên hợp (1678 cm-1).
- Phổ 1H-NMR (Hình 3.10, 3.11, 3.12) cho thấy có hai nhóm metyl với các tín hiệu singlet tại H = 0,71 (3H, s, CH3-18) và H = 1,18 (3H, s, CH3-19), ba nhóm metyl gắn với –CH với các tín hiệu doublet tại: H = 0,82 (3H, d, J = 6,7 Hz, CH3-26); 0,84 (3H, d, J = 7,0 Hz, CH3-27), 0,86 (3H, d, J = 7,4 Hz,
CH3-21) và nhóm metyl gắn với – CH2 với tín hiệu triplet tại : H = 0,92 (3H, t, J = 6,3 Hz, H-29). Sự có mặt của nhóm carbonyl liên hợp cũng được thấy rõ trong phổ 13C-NMR (Hình 3.13) với các tín hiệu C =199,598 (s, C- 3), 171,653 (s, C-5) và 123,754 (d, C-4) cũng như tín hiệu H = 5,72 (1H, br s, H-4).
- Phổ 13C-NMR và phổ DEPT của chất 70 có tín hiệu của 29 nguyên tử carbon, trong đó có 6 nhóm CH3, 11 nhóm CH2, 8 nhóm CH và 4 nguyên tử carbon bậc 4.
- Phổ khối phân giải cao (HR-ESI-MS) cho pic ion phân tử tại m/z = 413,37162 [M+H]+. Như vậy công thức phân tử của chất 70 sẽ là C29H48O (M=412).
- Phổ 1H- và 13C-NMR của chất 70 hoàn toàn phù hợp với phổ của chất stigmast-4-en-3-on trong tài liệu [64] (xem Bảng 3.4). Như vậy chất 70 chính
là stigmast-4-en-3-on. Chất này đã được tách trước đây từ cây Nauclea officinalis thuộc họ Cà phê [64].
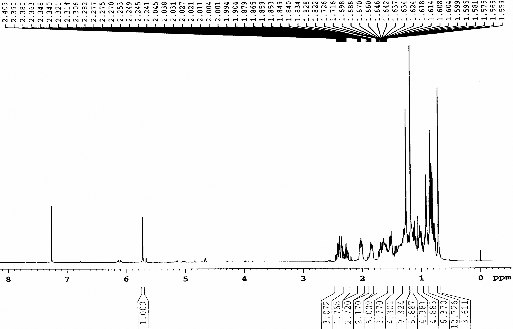
Hình 3.10. Phổ 1H-NMR (CDCl3, 500 MHz) của chất 70 (Stigmast-4-en-3-on)
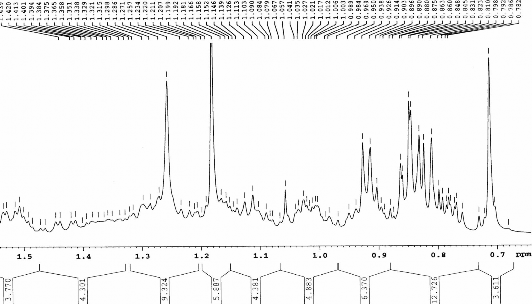
Hình 3.11. Phổ 1H-NMR dãn rộng (CDCl3, 500 MHz) của chất 70
(Stigmast-4-en-3-on)
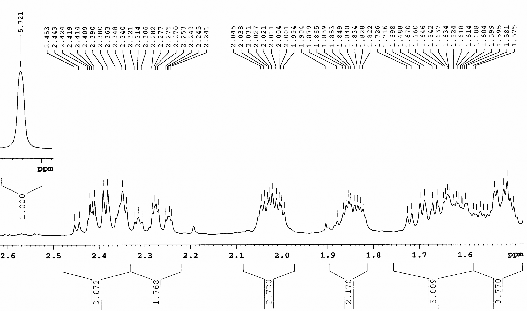
Hình 3.12. Phổ 1H-NMR dãn rộng (CDCl3, 500 MHz) của chất 70
(Stigmast-4-en-3-on)
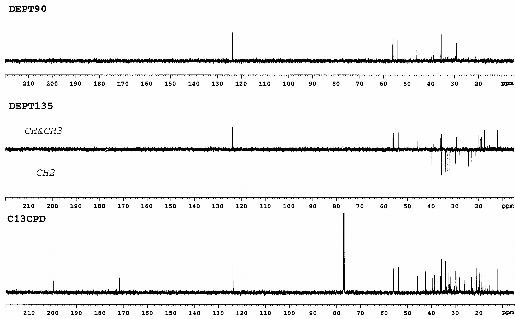
Hình 3.13. Phổ 13C-NMR và phổ DEPT của chất 70 (Stigmast-4-en-3-on)
Bảng 3.4. Số liệu phổ 1H- và 13C-NMR (CDCl3) của hợp chất 70 và Stigmast-4-en-3-on
Chất 70 | Stigmast-4-en-3-on [64] | |||
C | C | H (J=Hz) | C | H (J=Hz) |
1 | 35,7 | 34,8 | ||
2 | 34,0 | 2,26 (1H, ddd, J=2.4, 3.9, 14.5 Hz, H-2A) | 32,8 | |
3 | 199,6 | 198,5 | ||
4 | 123,8 | 5,72 (1H,br.s, H-4) | 122,7 | 5,72 (1H, s, H-4) |
5 | 171,7 | 170,5 | ||
6 | 33,0 | 31,9 | ||
7 | 32,1 | 31,0 | ||
8 | 35,7 | 34,6 | ||
9 | 53,9 | 52,7 | ||
10 | 38,6 | 37,5 | ||
11 | 23,1 | 22,0 | ||
12 | 39,7 | 38,5 | ||
13 | 42,4 | 41,3 | ||
14 | 55,9 | 54,9 | ||
15 | 26,2 | 25,0 | ||
16 | 28,2 | 27,1 | ||
17 | 56,1 | 54,9 | ||
18 | 12,0 | 0,71 (3H, s, CH3-18) | 10,9 | 0,71(3H, s, H-18) |
19 | 19,1 | 1,18 (3H, s, CH3-19) | 18,0 | 1,18(3H, s, H-19) |
20 | 36,1 | 35,0 | ||
21 | 17,4 | 0,86 (3H, d, J=7,4 Hz, CH3-21) | 16,3 | 0,84 (3H, d, 7,4Hz, H-21) |
22 | 33,9 | 32,9 | ||
23 | 24,2 | 23,1 | ||
24 | 45,9 | 44,7 | ||
25 | 29,2 | 27,1 | ||
26 | 19,8 | 0,82 (3H, d, J=6,7 Hz, CH3-26) | 18,7 | 0,82 (3H, d, 6,7Hz, H-26) |
27 | 18,7 | 0,84 (3H, d, J=7,0 Hz, CH3-27) | 17,6 | 0,84 (3H, d, 7,0Hz, H-27) |
28 | 24,2 | 23,1 | ||
29 | 12,0 | 0,92 (3H, t, J=6,3 Hz, CH3-29) | 10,9 | 0,92(3H, t, J=6,4Hz, H-29) |
Có thể bạn quan tâm!
-
 Β -Sitosterol-3- O- Β –D -Glucopyranosid ( Β -Sitosterol Glucosid), (Lhrm3)
Β -Sitosterol-3- O- Β –D -Glucopyranosid ( Β -Sitosterol Glucosid), (Lhrm3) -
 Số Liệu Phổ Của Các Chất Phân Lập Được Từ Cây Rau Má
Số Liệu Phổ Của Các Chất Phân Lập Được Từ Cây Rau Má -
![Nghiên cứu cấu trúc và hoạt tính sinh học một số hợp chất phân lập từ cây cọ hạ long (Livistona halongensis T.H. Nguyen & Kiew) và cây rau má [Centella asiatica(Linn.) Urban] - 9](data:image/svg+xml,%3Csvg%20xmlns=%22http://www.w3.org/2000/svg%22%20viewBox=%220%200%2075%2075%22%3E%3C/svg%3E) Nghiên cứu cấu trúc và hoạt tính sinh học một số hợp chất phân lập từ cây cọ hạ long (Livistona halongensis T.H. Nguyen & Kiew) và cây rau má [Centella asiatica(Linn.) Urban] - 9
Nghiên cứu cấu trúc và hoạt tính sinh học một số hợp chất phân lập từ cây cọ hạ long (Livistona halongensis T.H. Nguyen & Kiew) và cây rau má [Centella asiatica(Linn.) Urban] - 9 -
![Nghiên cứu cấu trúc và hoạt tính sinh học một số hợp chất phân lập từ cây cọ hạ long (Livistona halongensis T.H. Nguyen & Kiew) và cây rau má [Centella asiatica(Linn.) Urban] - 11](data:image/svg+xml,%3Csvg%20xmlns=%22http://www.w3.org/2000/svg%22%20viewBox=%220%200%2075%2075%22%3E%3C/svg%3E) Nghiên cứu cấu trúc và hoạt tính sinh học một số hợp chất phân lập từ cây cọ hạ long (Livistona halongensis T.H. Nguyen & Kiew) và cây rau má [Centella asiatica(Linn.) Urban] - 11
Nghiên cứu cấu trúc và hoạt tính sinh học một số hợp chất phân lập từ cây cọ hạ long (Livistona halongensis T.H. Nguyen & Kiew) và cây rau má [Centella asiatica(Linn.) Urban] - 11 -
 R ,3 R -3,7,3’-Trihydroxy-5’-Metoxyflavan 5- O - - D - Glucopyranosid
R ,3 R -3,7,3’-Trihydroxy-5’-Metoxyflavan 5- O - - D - Glucopyranosid -
 Nghiên Cứu Thành Phần Hóa Học Của Cây Rau Má
Nghiên Cứu Thành Phần Hóa Học Của Cây Rau Má
Xem toàn bộ 129 trang tài liệu này.
![]()
![]()
3.1.1.5. Chất 71 (CT1): Stigmasterol
![]()
![]()
![]()
![]()
Chất 71: Được phân lập dưới dạng tinh thể màu trắng, điểm nóng chảy 169- 171oC.
- Phổ 13C-NMR và DEPT cho tín hiệu cộng hưởng của 29 cacbon, trong đó có 3 cacbon bậc bốn, 11 cacbon bậc ba, 9 cacbon bậc hai và 6 nhóm metyl. Phổ 13CNMR cũng cho tín hiệu cộng hưởng của hai liên kết đôi ở vị trí C5 = C6: ( = 140,8 và 121,7) và vị trí C22 = C23: ( = 138,3 và 129,3).
- Phổ 1H-NMR cho thấy có hai nhóm metyl với các tín hiệu singlet tại H = 0,70 (3H, s, H-18) và H = 1,01 (3H, s, H-19), ba nhóm metyl gắn với –CH với các tín hiệu doublet tại: H = 0,798 (3H, d, J = 6,4 Hz, H-26), 0,848 (3H, d, J = 6,4 Hz, H-27), 1,02 (3H, d, J = 6,7 Hz, H-21) và một nhóm metyl gắn với – CH2 với tín hiệu triplet tại : H = 0,807 (3H, t, J = 7,5 Hz, H-29). Ở vùng trường thấp cho tín hiệu cộng hưởng của một olefin proton ( = 5,35 (1H, br s, H-6) và hai olefin proton ( = 5,02 (1H, dd, J = 8,7, 15.2 Hz, H-22) và 5,16 (1H, dd, J = 8,6, 15,2Hz,
H-23) ; một proton carbinol: = 3,51 (1H, m, H-3) chứng minh cho nhóm β- OH ở vị trí C3.
- Phổ khối ESI-MS cho pic ion phân tử tại m/z = 414,8 phù hợp với công thức phân tử là (C29H50O) [M+2H]+. Như vậy công thức phân tử của chất 71 sẽ là (C29H48O) với M = 412. Ngoài ra ta còn thấy pic ở m/z = 395,8 [M- H2O +1] . Pic này là pic cơ bản, hình thành do tạo thành dẫn xuất dien liên hợp (3,5-dien) sau khi phân tử 71 bị tách một phân tử nước. Kết hợp các dữ kiện phổ ESI-MS, phổ 1HNMR, 13C-NMR và phổ DEPT cho phép xác định cấu trúc của chất 71 là stigmasterol [64, 65].
Stigmasterol là hợp chất thiên nhiên có hoạt tính sinh học, tồn tại khá phổ biến trong giới thực vật, ví dụ như trong vỏ chuối [66], trong lá cây Euphorbia heterophylla thuộc họ Thầu dầu [67], trong lá cây phèn đen (Phyllanthus reticulatas Poir) [68]. Itoh và cộng sự đã nghiên cứu khả năng phân biệt các sterol khác nhau thông qua hiệu số của thời gian lưu của dẫn xuất 3-oxo của chúng trong sắc ký khí [69].
3.1.1.6. Chất 72 ( LHVH2): β-Sitosterol
Chất 72 được xác định là β-sitosterol qua so sánh số liệu phổ 1H-NMR và 13C- NMR của chúng với số liệu trong tài liệu [64, 70] .
3.1.2. Xác định cấu trúc hóa học của các chất phân lập được từ rễ cây cọ hạ long (Livistona halongensis)
3.1.2.1. Chất 73 (LHRn2): 6-O-acetyl-2R,8-dimetyl-2-(4R,8R,11-trimetyltridecence- 12)chroman
73: (LHR.n2)
Chất 73 thu được dưới dạng bột vô định hình, có pic ion phân tử trong phổ khối phân giải cao ESI-HRMS tại m/z = 457,36838 [M + H]+ (theo tính toán cho C30H49O3 là 457,36817). Phổ FT-IR của nó cho thấy các đỉnh hấp thụ ở 2936, 2857 (CH3, CH2), 1760 và 1209 cm-1 (phenyl axetat).
- Phổ 1H-NMR cho biết phân tử chất 73 có 7 nhóm metyl, trong đó có 3 nhóm thể
hiện dưới dạng tín hiệu dublet ở H= 0,84 (J = 5,9 Hz); 0,85 (J = 5,9 Hz); 0,99 (J
= 6,8 Hz). Một tín hiệu metyl singlet ở H= 2,13 có thể được gán cho nhóm metyl đính vào vòng thơm; tín hiệu metyl của nhóm axetyl cộng hưởng ở 2,24 ppm và metyl của nhóm isopropenyl xuất hiện ở 1,64 ppm. Ngoài ra, các tín hiệu của hai proton thơm có tương tác meta ở 6,60 và 6,66 ppm (mỗi tín hiệu d, J = 2,6Hz), hai
proton olefin (>C=CH2) ở 4,66 ppm cũng như các proton no trong vùng từ 0,80 – 2,80 ppm cũng được quan sát thấy trong phổ 1H-NMR.
- Chất 73 cho tín hiệu của 30 nguyên tử cacbon trong phổ 13C-NMR và DEPT, bao gồm 7 nhóm metyl, 8 cacbon thơm, 11 nhóm metylen, 2 nhóm metin và 2 cacbon bậc 4. Sự có mặt của phần 2-methylchroman axetat trong phân tử 73 được chứng minh qua 3 nhóm tín hiệu: vòng thơm, aliphatic metylen và metyl. Các tương tác trong phổ HMBC đã khẳng định cấu trúc của phần 2-methylchroman
axetat trong phân tử chất 73. Các tương tác đó là tương tác giữa một cacbon trong cầu ete (C= 150,37, C-8a) với hai proton thơm ở H= 6,60; 6,66 (H-5, H-7), hai proton ở H= 2,72 (2H-4), proton của nhóm methyl gắn với vòng thơm H= 2,13 (8-CH3) và tương tác của cacbon thứ 2 trong cầu ete (C= 76,16, C-2) với bốn proton ở H= 2,72 (2H-4); 1,73; 1,79 (2H-3); 1,56 (2H-1'); nhóm metyl ở H= 1,25. Sự nối kết của nhóm axetyl ở C-6 và nhóm metyl ở C-2 được xác định bằng sự dịch chuyển về phía trường thấp của C-6 (142,51 ppm) và các tương tác quan sát được trong phổ HMBC giữa C-6 và H-5, H-7 (H= 6,60; 6,66); giữa C-2 (76,16 ppm) và 2-CH3(1,25 ppm). Các dữ liệu phổ đã phân tích cho phép kết luận cấu trúc của đơn vị 2-metylchromanol-6-axetat trong chất 73. Cấu trúc của mạch nhánh được chứng minh qua các tương tác giữa C-12' (C= 149,82) và nhóm metyl bậc 3 ở H= 1,64 (s, 3H-13'), nhóm metyl bậc hai ở H= 1,00 (d, 3H-11') trong phổ HMBC. Vị trí nối kết của mạch nhánh được xác định ở C-2 là do tương tác của 2H-1' (H= 1,56) với C-2 (C= 76,16). Phổ H,H – COSY ( Hình 3.16 và hình 3.17) cho thấy các tương tác H,H phù hợp với cấu trúc dự đoán của chất 73, đặc biệt các tương tác giữa các proton trong đơn vị cấu trúc Chroman cũng như trong nhóm isopropenyl. Cấu hình tuyệt đối tại các vị trí C-2, 4’ và 8’ được xác định dựa vào so sánh với tài liệu tham khảo công bố bởi Browstein và Brem [71, 72]. Theo các tài liệu này, các đồng phân quang học khác nhau của α và δ- tocopherol cho độ chuyển dịch khác nhau nhiều nhất ở vị trí CH3-4’. Do đó, có thể xác định được cấu hình tuyệt đối của chất 73 dựa vào việc so sánh độ chuyển dịch hóa học tại vị trí CH3-4’ với một loạt các đồng phân quang học của δ- tocopherol đã được nghiên cứu và thống kê trong tài liệu. Qua đối chiếu với tài liệu tham khảo, độ chuyển dịch hóa học của CH3-4’ (δC19,65) hoàn toàn phù hợp với cấu hình tuyệt đối R, R, R của chất 3,4-dehydrotocopherol. Do đó cấu trúc của chất 73 được xác định là 6-O-acetyl-2R,8-dimetyl-2-(4R,8R,11-trimetyltridecence-



![Nghiên cứu cấu trúc và hoạt tính sinh học một số hợp chất phân lập từ cây cọ hạ long (Livistona halongensis T.H. Nguyen & Kiew) và cây rau má [Centella asiatica(Linn.) Urban] - 9](https://tailieuthamkhao.com/uploads/2022/05/09/nghien-cuu-cau-truc-va-hoat-tinh-sinh-hoc-mot-so-hop-chat-phan-lap-tu-cay-9-1-120x90.png)
![Nghiên cứu cấu trúc và hoạt tính sinh học một số hợp chất phân lập từ cây cọ hạ long (Livistona halongensis T.H. Nguyen & Kiew) và cây rau má [Centella asiatica(Linn.) Urban] - 11](https://tailieuthamkhao.com/uploads/2022/05/09/nghien-cuu-cau-truc-va-hoat-tinh-sinh-hoc-mot-so-hop-chat-phan-lap-tu-cay-11-1-120x90.png)

