Sấy kết tủa thu được trong tủ sấy ở 50 oC trong 24 giờ. Sơ đồ 2.1 minh họa sơ đồ tổng hợp ZnO.
ZnO cũng được tổng hợp trong dung môi với các tỉ lệ ethanol - nước khác nhau bao gồm: (90:10), (75:25), (50:50), (25:75) và (0:100) theo quy trình trên.
50 mL cồn tuyệt đối + 50 mL nước + 0,2195 g kẽm acetate + 0,1402 g C6H12N4
Dung dịch chứa hỗn hợp trên đã đồng nhất
Khuấy đến khi dung dịch đồng nhất
Các hạt nano/micro ZnO
Lọc kết tủa, sấy 50 oC, 24 giờ
Hồi lưu ở 90 oC ổn nhiệt bằng glycerine
Kết tủa ZnO
Sơ đồ 2.1. Sơ đồ tổng hợp nano ZnO
2.4.2.2. Phương pháp tổng hợp ZnO pha tạp La
Tổng hợp ZnO và La - ZnO có kích thước nano bằng phương pháp thủy nhiệt gồm các bước sau (xem sơ đồ 2.2).
Bước 1: Cân Zn(CH3COO)2.2H2O.
Chuẩn bị lượng khác nhau La(NO3)3.6H2O (1%, 2% và 2,5%).
Bước 2:Hòa tan hỗn hợp vào ethanol nồng độ 98% bằng cách khuấy đều trong 2 giờ (thu được dung dịch 1).
Bước 3:Trong lúc đó, cân NaOH, hòa tan vào ethanol nồng độ 98% và khuấy đều trong 2h (thu được dung dịch 2).
Bước 4:Nhỏ từ từ dung dịch 1 vào dung dịch 2 (vừa nhỏ vừa khuấy).
Bước 5:Khuấy hỗn hợp thu được trong 1 giờ.
Bướ c6:Chuyển hỗn hợp sang bình teflon 200ml và cho vào lò sấy ở 150 oC trong 20 giờ.
Bước 7:Kết tủa thu được bằng cách ly tâm.
Rửa nhiều lần bằng nước và bằng ethanol.
Bước 8:Mẫu nano La - ZnO thu được khi sấy kết tủa trên ở 60oC trong 15 giờ và nung
ở 500oC trong 2 giờ và thu được mẫu cần tổng hợp.
NaOH + C2H5OH
0,86 g Zn(CH3COO)2.2H2O
+ x (g) (La(NO3)3.6H2O + C2H5OH
Khuấy 2h
Vừa nhỏ từ từ vừa khuấy
Khuấy 2h
Khuấy 1h
Huyền phù
Thủy nhiệt (teflon 200 mL, 150 oC,
Sản phẩm thủy nhiệt
Sản phẩm ướt
Sấy khô 60 oC, 15h và nung 500 oC, 2h
Sản phẩm khô
Sơ đồ 2.2. Sơ đồ tổng hợp nano La - ZnO dạng que bằng phương pháp thủy nhiệt
Dung dịch 2 | Dung dịch 1 | |
Có thể bạn quan tâm!
-
 Một Số Công Trình Đã Được Công Bố Ứng Dụng Zno Để Xác Định Một Số Hợp Chất Hữu Cơ Bằng Phương Pháp Điện Hóa
Một Số Công Trình Đã Được Công Bố Ứng Dụng Zno Để Xác Định Một Số Hợp Chất Hữu Cơ Bằng Phương Pháp Điện Hóa -
 Giản Đồ Mức Năng Lượng Chỉ Ra Những Trạng Thái Liên Quan Đến Phổ Raman
Giản Đồ Mức Năng Lượng Chỉ Ra Những Trạng Thái Liên Quan Đến Phổ Raman -
 Phương Pháp Sắc Ký Lỏng Hiệu Năng Cao Hplc (High Performance Liquid Chromatography)
Phương Pháp Sắc Ký Lỏng Hiệu Năng Cao Hplc (High Performance Liquid Chromatography) -
 Tổng Hợp Kiểm Soát Hình Thái Micro/nano Zno Từ Dạng Đĩa Đến Dạng Que Trong Hệ Kẽm Acetate – Ethanol – Nước Dùng Chất Hexamethylenetetramine (Hm) Tạo Môi
Tổng Hợp Kiểm Soát Hình Thái Micro/nano Zno Từ Dạng Đĩa Đến Dạng Que Trong Hệ Kẽm Acetate – Ethanol – Nước Dùng Chất Hexamethylenetetramine (Hm) Tạo Môi -
 A. Chỉ Số Hướng Mặt Phẳng Của Cấu Trúc Lục Lăng; B. Cấu Trúc Tinh Thể Lục Lăng
A. Chỉ Số Hướng Mặt Phẳng Của Cấu Trúc Lục Lăng; B. Cấu Trúc Tinh Thể Lục Lăng -
 Tổng Hợp Zno Dạng Cầu Trong Hệ Kẽm Acetate – Ethanol - Koh
Tổng Hợp Zno Dạng Cầu Trong Hệ Kẽm Acetate – Ethanol - Koh
Xem toàn bộ 207 trang tài liệu này.
2.4.2.3. Phương pháp tổng hợp ZnO trong hệ kẽm acetate – ethanol dùng KOH/NaOH làm chất tạo môi trường kiềm
Qui trình tổng hợp ZnO trong hệ này, tương tự như quy trình tổng hợp ZnO pha tạp La (phần 2.4.2.2). Riêng bước 8, mẫu ZnO chỉ sấy kết tủa trong 15 giờ ở nhiệt độ 60 oC thì thu được vật liệu cần tổng hợp.
2.4.2.4. Phương pháp xác định hoạt tính xúc tác
Hoạt tính xúc tác của phản ứng phân hủy methyl xanh trong hệ xúc tác ZnO/H2O2 có sự hỗ trợ của sóng siêu âm được thực hiện theo hình 2.9. Mẫu được rút ra bằng xilanh (có đầu lọc) theo thời gian (hình 2.9 a) và phân tích methyl xanh còn lại bằng phương
pháp đo quang trên máy 722N-VS Spectrophotometer; hoạt tính xúc tác của phản ứng phân hủy quang hóa methyl xanh trong hệ xúc tác La – ZnO được thực hiện như hình 2.9
Cốc thủy tinh
b
a
Đèn UV
b. Sau đó, mẫu (được lọc bằng xilanh có đầu lọc) đem ly tâm và phân tích methyl xanh còn lại bằng phương pháp đo quang trên máy 722N-VS Spectrophotometer..
Hình 2.9. a. Sơ đồ hệ phản ứng phân hủy methyl xanh trong hệ xúc tác ZnO/H2O2 có sự hỗ trợ của sóng siêu âm: 1. Thiết bị phát siêu âm, 2. Bộ điều biến, 3. Đầu dò, 4 Nhiệt kế, 5. bình nước điều nhiệt, 6. Hỗn hợp phản ứng; b. Hệ phản ứng quang hóa (bước sóng λ = 356 nm)
2.4.2.5. Phương pháp đo nhu cầu oxy hóa học (COD)
Chuyển 10 mL mẫu vào bình phản ứng, thêm đúng 5 mL dung dịch K2Cr2O7, thêm vài hạt thủy tinh nhỏ đã được làm sạch vào phần mẫu thử và lắc trộn đều. Thêm từ từ 15 mL dung dịch Ag2SO4 trong acid sunfuric và lắp bình vào ống sinh hàn, đưa hỗn hợp phản ứng tới sôi trong 10 phút và tiếp tục đun sôi 110 phút nữa (ở nhiệt độ 148 oC). Làm nguội ngay bình phản ứng đến 60 oC, pha loãng hỗn hợp phản ứng đến 75 mL và làm nguội đến nhiệt
độ phòng. Chuẩn độ lượng dư Cr O 2- bằng Fe(II) amonium sulphate với chất chỉ thị feroin.
2 7
Nhu cầu oxy hóa học COD (mg/L), được tính bằng công thức:
COD =
8000 x C x (V1-V2)
Vo
(2.25)
Trong đó: - C: Nồng độ Fe (II) amonium sulphate đã được biết trước (mol/L)
- Vo: Thể tích mẫu thử (mL)
- V1: Thể tích Fe (II) amonium sulphate sử dụng chuẩn độ mẫu trắng (mL)
- V2: Thể tích Fe (II) amonium sulphate sử dụng chuẩn độ mẫu thử (mL)
- 8000: khối lượng mol 0,5 O2 (mg/L)
2.4.2.6. Phương pháp xác định điểm đẳng điện
Cho vào một loạt 7 bình tam giác (dung tích 50 mL) 25 mL dung dịch NaCl 0,1M. Giá trị pH ban đầu của dung dịch (pHi) được điều chỉnh nằm trong khoảng 2 đến 12 bằng HCl 0,1 M hay NaCl 0,1 M. Cho vào mỗi bình tam giác trên một lượng 0,05 gam vật liệu tổng hợp, đậy kín và lắc bằng máy lắc trong 48 giờ. Sau đó, để lắng và lọc bằng giấy lọc, đo lại các giá trị pH gọi là pHf. Đồ thị biểu diễn mối quan hệ khác nhau giữa các giá trị pH ban đầu và sau cùng (ΔpH = pHf - pHi) theo pHi là đường cong cắt trục hoành tại ΔpH = 0 cho ta giá trị pH đẳng điện (pHi.e.p.).
2.4.2.7. Phương pháp đo cảm biến khí
Để khảo sát đặc tính nhạy khí, chúng tôi sử dụng điện cực răng lược Pt trên đế Si/SiO2 được chế tạo bằng công nghệ vi điện tử truyền thống (hình 2.10). Cảm biến chế tạo bằng phương pháp nhỏ phủ sử dụng điện cực răng lược này. Đối với điện cực để mọc trực tiếp dây nano lên điện cực, ngoài lớp Pt chúng tôi phủ thêm một lớp Au (10 nm) lên trên Pt để làm xúc tác trước khi liff off tạo điện cực.
Trộn vật liệu nano ZnO với nước rồi nhỏ phủ lên điện cực răng lược. Sau đó mẫu được ủ ở nhiệt độ 600 oC trong không khí để vật liệu ổn định và có độ nhạy tốt khi đo nhạy khí. Khó khăn nhất của quá trình này là làm sao để vật liệu nano bám dính và tiếp xúc với điện cực răng lược không chỉ ở nhiệt độ phòng mà cả khi cảm biến hoạt động ở nhiệt độ cao.
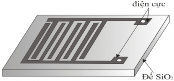

Hình 2.10. Điện cực răng lược trên đế Si/SiO2
(a)
(b)
(c) 
Hình 2.11. a, b. Điện cực răng lược trước khi phủ dây nano SnO2
c. Điện cực răng lược sau khi nhỏ phủ dây nano SnO2
Chúng tôi tiến hành khảo sát đặc trưng I - V của cảm biến màng điện trở. Qua đó kiểm tra tính chất ohmic tại các cực tiếp xúc giữa chất bán dẫn với điện cực Pt. Khi vật liệu có tiếp xúc ohmic thì sự thay đổi tính chất điện là do sự thay đổi của vật liệu nhạy khí chứ không phải do tiếp xúc giữa vật liệu và điện cực. Thiết bị dùng đo đặc trưng I - V là máy HP 4156A tại viện Itims – Đại học bách khoa Hà Nội.
Để đo đặc trưng nhạy khí, chúng tôi sử dụng các khí chuẩn và các bộ điều khiển lưu lượng khí để pha trộn khí tạo ra nồng độ khí cần đo. Sơ đồ nguyên lý của hệ đo như hình 2.12.
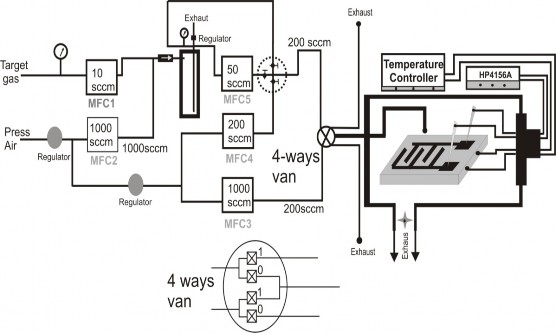
Hình 2.12. Sơ đồ nguyên lý của hệ trộn khí
Các bộ phận chính của hệ đo này là:
- Bộ điều khiển lưu lượng khí (MFC): Hệ dùng 5 bộ điều khiển lưu lượng khí để
pha trộn khí nhằm tạo ra nồng độ khí cần đo.
- Bộ điều khiển nhiệt độ: Dùng nguồn điện đốt nóng dây điện trở và tạo ra nhiệt
độ cần thiết để cảm biến làm việc. Nhiệt độ tối đa của lò là 450 oC.
- Đầu đo: Áp vào 2 điện cực của điện cực răng lược để đo điện trở của cảm biến.
Đầu đo này được nối với máy đo điện trở Keithley 2700.
- Máy đo điện trở Keithley 2700 và phần mềm VEE Pro đọc và ghi giá trị điện trở từ máy Keithley 2700. Giao diện của phần mềm này như trên hình 2.9.
Dải nồng độ khí cần đo được tính toán như trên bảng 2.1, 2.2 và 2.3.
Bảng 2.2. Dải nồng độ khí NH3 cần đo (Sử dụng khí chuẩn NH3 1%)
MFC2 | MFC3 | MFC4 | MFC5 | C (ppm) | |
(sccm) gas | (sccm) Air | (sccm) Air | (sccm) Air | (sccm) gas | |
Off | Off | 350 | 400 | 0.4 | 10 |
Off | Off | 350 | 399 | 1 | 25 |
Off | Off | 350 | 398 | 2 | 50 |
Off | Off | 350 | 396 | 4 | 100 |
10 | Off | 350 | 390 | Off | 250 |
20 | Off | 350 | 380 | Off | 500 |
40 | Off | 350 | 360 | Off | 1000 |
Bảng 2.3. Dải nồng độ hơi ethanol cần đo (Sử dụng khí chuẩn ethanol 1%) | |||||
MFC1 | MFC2 | MFC3 | MFC4 | MFC5 | C (ppm) |
(sccm) gas | (sccm) Air | (sccm) Air | (sccm) Air | (sccm) gas | |
Off | Off | 350 | 400 | 0.4 | 10 |
Off | Off | 350 | 399 | 1 | 25 |
Off | Off | 350 | 398 | 2 | 50 |
Off | Off | 350 | 396 | 4 | 100 |
10 | Off | 350 | 390 | Off | 250 |
20 | Off | 350 | 380 | Off | 500 |
40 | Off | 350 | 360 | Off | 1000 |
Bảng 2.4. Dải nồng độ khí H2 cần đo (Sử dụng khí chuẩn H2 0,5%) | |||||
MFC1 | MFC2 | MFC3 | MFC4 | MFC5 | C (ppm) |
(sccm) gas | (sccm) Air | (sccm) Air | (sccm) Air | (sccm) gas | |
Off | Off | 350 | 398 | 2 | 25 |
Off | Off | 350 | 396 | 4 | 50 |
Off | Off | 350 | 392 | 8 | 100 |
20 | Off | 350 | 380 | Off | 250 |
40 | Off | 350 | 360 | Off | 500 |
80 | Off | 350 | 350 | Off | 1000 |
2.4.2.8. Biến tính điện cực GC bằng ZnO dạng đĩa lục lăng
![]()
10 mg ZnO (dạng đĩa lục lăng được tổng hợp ở phần 3.4.2.1) sau khi được tổng hợp được tạo thành thể huyền phù bằng cách sử dụng 10 mL dung môi DMF (dimethyl formamide) với kỹ thuật rung siêu âm trong 20 phút. Quá trình biến tính điện cực được trình bày qua sơ đồ 2.3.
Chuẩn bị điện cực làm việc:
- Mài GCE với Al2O3 (0,05 m); rửa bằng nước cất 2 lần.
- Siêu âm bằng dung dịch H2SO4 1 M trong 1 giờ.
- Rửa lại bằng nước cất 2 lần.
Biến tính điện cực Glassy carbon (GCE): GCE/P(BCP)/ ZnO
- Tạo poly(bromocresol purple): quét von – ampe vòng (CV): 50 vòng, từ -0,4 (V) đến 1,8 (V) ; v = 100 (mV/s), trong nước cất chứa BCP 0,5 (mM). Sau đó rửa sạch, để khô ở nhiệt độ phòng.
- Nhỏ lên bề mặt GCE, 8 (L) dung dịch ZnO sao cho phủ kín toàn bộ bề mặt GCE, để dung môi bay hơi ở nhiệt độ phòng không ánh sáng trong 3 giờ thu được GCE biến tính – GCE/P(BCP)/ZnO.
Sơ đồ 2.3. Quy trình chuẩn bị điện cực và biến tính điện cực làm việc
Phương pháp von – ampe hòa tan anot xung vi phân (DP-ASV) xác định UA dùng GCE/P(BCP)/ZnO với quy trình thí nghiệm được thể hiện qua sơ đồ 2.4.
1. Giai đoạn làm giàu:
- Dung dịch phân tích: 1 mL đệm PBS (0,1(M), pH = 5,3); 50 (µL) UA 5.10-3 (M), nước cất 2 lần vừa đủ 10 (mL);
- Áp thế và thời gian điện phân: Edep (mV) và tdep (s), (vòng/phút).
![]()
Nghỉ 15 s
2. Giai đoạn hòa tan:
- Quét thế theo chiều anot, khoảng quét thế từ E1 = 0 (mV) đến E2 = 800 (mV);
- Sử dụng kỹ thuật DP để đo tín hiệu hòa tan (Ep và Ip).
- Tín hiệu hòa tan: Ip và Ep, trong đó Ip,UA CUA.
- Tiến hành định lượng bằng phương pháp thêm chuẩn.
![]()
Sơ đồ 2.4 Sơ đồ tiến trình thí nghiệm theo phương pháp ASV
Các điều kiện thí nghiệm (ĐKTN) của phương pháp DP-ASV được cố định ở
bảng 3.5 [35, 142, 178].
Bảng 2.5. Các thông số được cố định trong phương pháp DP – ASV.
Các yếu tố hoặc thông số | Ký hiệu | Đơn vị | Giá trị | |
1 | Đệm photphat (pH = 7) | PBS | M | 0,1 |
2 | Thế điện phân làm giàu | Edep | mV | 0 |
3 | Thời gian điện phân làm giàu | tdep | s | 60 |
4 | Tốc độ quay điện cực | vòng/phút | 2000 | |
5 | Thời gian nghỉ | trest | s | 15 |
6 | Khoảng quét thế | Erange | mV | 0 – 800 |
Các thông số kỹ thuật DP: | ||||
+ Biên độ xung | E | mV | 50 | |
+ Bề rộng xung | tpulse | ms | 50 | |
7 | + Bước nhảy thế | Ustep | mV | 6 |
+ Thời gian mỗi bước thế | tstep | s | 0,2 | |
+ Thời gian đo dòng | tmeas | ms | 20 | |
+ Tốc độ quét thế | v | mV/s | 30 |