rắn.
N: Số gam đạm tổng số có trong 1 lít nguyên liệu loãng hay 1kg nguyên liệu
V = V0 – V
V0: thể tích NaOH N/100 mẫu thử không. V: thể tích NaOH N/100 mẫu thử thật.
2.2.6 Phương pháp xác định đạm formol (phương pháp Sorensen)[1, 4]
2.2.6.1 Nguyên tắc
Trong phân tử acid amin, peptid, protein có một đầu chức là nhóm –COOH như là một acid còn đầu kia là nhóm –NH2 được xem như là một base, còn các amin tự do cũng như amoniac khi hòa tan thường ở dưới dạng amonium NH4+ kết hợp với một anion thường là clorur, sulfat, phosphat…
Như vậy khi ta cho tác dụng các phân tử “phi protein” này với formol, formol sẽ tác dụng lên nhóm -NH2 để tạo thành phức chất methylen (mono, tri hoặc hexamethylen).
H H
HOOC C
NH2
+ HCHO HOOC C
N CH2 + H2O
R
RNH4+Cl-
R
+ HCHO R N CH2 + H2O + HCl
Sản phẩm của phản ứng là hợp chất methylen và một chức –COOH tự do (trong trường hợp acid amin) hoặc HCl (trong trường hợp amin tự do hoặc amoniac). Nên ta có thể định phân bằng NaOH, từ đây cho phép ta xác định một cách gián tiếp được lượng –NH2.
Khi hàm lượng đạm formol không tăng theo thời gian có nghĩa là phản ứng
thủy phân đã kết thúc
2.2.6.2 Tiến hành
Trung hòa formol ½: lấy 50ml formol ½, thêm vào đó vài giọt phenolphtalein 3%, cho NaOH N/10 từng giọt cho đến khi dung dịch chuyển màu hồng nhạt, ta được formol ½ đã trung hòa.
Hút 10ml dung dịch nguyên liệu đã pha loãng từ 5 đến 20 lần (trong đề tài này chúng tôi tiến hành pha loãng mẫu 10 lần) thêm vào đó 10ml dung dịch formol
½ đã trung hòa và vài giọt phenolphtalein 3%, lắc đều để phản ứng xảy ra hoàn toàn, sau đó định phân bằng NaOH x N/10 cho đến khi dung dịch chuyển màu hồng.
Thực hiện ba sự thử thật và ba sự thử không (thay dung dịch đạm bằng nước cất) lấy trị số trung bình.
2.2.6.3 Cách tính
Số gam đạm formol có trong 1 lít nguyên liệu = 1.4*V (g/lít) Trong đó:
V = V – V0
V0: thể tích NaOH N/10 mẫu thử không. V: thể tích NaOH N/10 mẫu thử thật.
2.2.7 Xác định đạm amoniac[1, 4]
2.2.7.1 Nguyên tắc
Trong nguyên liệu chứa đạm thường có một loại đạm nằm dưới dạng “vô cơ” (muối amonium hay những amin dễ bay hơi). Đây là dạng đạm tạo thành do sự phân hủy của protein (bị lên men thối hoặc quá trình khử carboxyl của acid amin), vì thế nếu đứng về khía cạnh dinh dưỡng thì loại đạm này không cần cho cơ thể, nếu có sự hiện diện của nó với hàm lượng cao thì nguyên liệu được đánh giá là “mất phẩm chất’.
Những loại đạm này thường có tính kiềm yếu, vì vậy khi cho tác dụng với MgO thì những loại đạm này sẽ bị đuổi ra khỏi dung dịch, nên chúng sẽ được lôi cuốn theo hơi nước qua một bình đựng lượng thừa acid. Sau đó đem định phân lượng acid dư, cho phép chúng ta xác định được loại đạm này.
2(NH4)+ + Mg(OH)2 ---> 2NH3 + 2H2O + Mg2+
2NH3 + H2SO4 ----> (NH4)2SO4
2.2.7.2 Tiến hành
Lấy 50ml dung dịch nguyên liệu đã pha loãng 20 lần (hoặc cân chính xác một lượng m gam nguyên liệu đã nghiền nhuyễn cho đồng nhất) cho vào trong bình cầu 500ml, thêm vào đó 150ml nước cất và vài giọt phenolphtalein, tiếp tục thêm vào bình cầu 5g MgO, dung dịch phải có màu hồng nhạt, đậy nút ngay để tránh amoniac bay ra, lắc đều, đun sôi và hơi nước được chưng cất sang một bình tam giác có chứa sẵn 10ml H2SO4 N/10 và vài giọt thuốc thử Tashiro, đầu nhọn của ống sinh hàn nhúng chìm trong dung dịch H2SO4 N/10. Chưng cất trong 15-20 phút kể từ khi dung dịch trong bình cầu sôi. Sau 15-20 phút chất đạm amoniac sẽ được hấp thụ vào dung dịch H2SO4. Lấy bình tam giác ra (rửa đầu ống sinh hàn trước khi lấy ra).
Định phân lượng acid dư bằng NaOH có chuẩn độ là x N/10 từ màu xanh tím sang màu xanh xám, nếu dư NaOH thì chuyển thành màu xanh ve chai. Thực hiện ba lần thử thật và ba lần thử không.
2.2.7.3 Cách tính
Số gam đạm NH3 có trong 1 lít nguyên liệu = (1.4*V)/2.5
V = (Vt – V0) là lượng NaOH tương đương với lượng đạm phóng thích đã được hấp thụ trong H2SO4.
2.2.8 Phương pháp chung tiến hành phản ứng thủy phân bánh dầu đậu phộng với xúc tác papain thô.[15, 27]
2.2.8.1 Phương pháp loại béo:
Sử dụng dung môi eter dầu hỏa: cho dung môi vào bánh dầu đậu phộng đã xay nhuyễn với tỷ lệ khối lượng dung môi trên cơ chất là 3:2. Khuấy đều trong 3 giờ ở 70oC, sau đó lọc bỏ dung môi (tiến hành 3 lần). Sau đó cho nước vào với tỷ lệ trên sản phẩm là 2:1, khuấy đều, đem lọc. Thực hiện sự rửa này 7 lần. Sản phẩm thu được đem sấy khô ta được bánh dầu đậu phộng đã loại béo.
2.2.8.2 Phương pháp thực hiện phản ứng[5, 30, 31, 37]
Phản ứng thủy phân được thực hiện tại tỉ lệ của bánh dầu đậu phộng với dung dịch đệm phosphate là 1:10. Cân 5g bánh dầu đậu phộng đã loại béo cho vào
erlen 100ml, thêm vào 50ml dung dịch đệm phosphate 0.1M. Bánh dầu đậu phộng được trộn với dung dịch đệm phosphate để đạt được pH mong muốn, hỗn hợp sau đó được gia nhiệt và khuấy từ liên tục. Khi phản ứng đạt đến nhiệt độ cần khảo sát, cho enzyme vào với tỉ lệ thích hợp, phản ứng được tiến hành trong 26 giờ. Sau mỗi 2 giờ phản ứng, lấy 0.1 gam dịch thủy phân từ erlen trên, thêm nước sôi để ngừng phản ứng, định mức thành 100ml dung dịch, đem lọc. Hút 10ml dịch lọc đem xác định hàm lượng đạm formol theo phương pháp Sorensen, phần dung dịch còn lại trong bình định mức dùng để xác định lượng protein theo phương pháp Lowry.
2.2.8.3 Hiệu suất thủy phân[39]
Papain có tính chất của endopeptidase thủy phân protein trong bánh dầu đậu phộng chủ yếu thành peptide theo phản ứng sau:
H R3 R4 H R3 R4
R1 N C C N
H O H
C C R2 +
H O
HOH
R1 N C H
C OH O
+ H2N C H
CO R2
Ngoài ra, papain còn có tính chất của exopeptidase thủy phân các peptide thành các acid amin theo phản ứng sau:
R2
H2N C C N
H O H
R3
C C R1 +
H O
HOH
R3
H2N C C
H O
OH +
R4
H2N C H
CO R1
Hiệu suất gần đúng của phản ứng thủy phân (%) được tính dựa trên tỉ lệ hàm lượng acid amin hòa tan trong nước của dung dịch sau phản ứng so với hàm lượng protein ban đầu được xác định thông qua hàm lượng nitơ tổng.
Hiệu suất gần đúng của phản ứng thủy phân H(%) được tính theo công thức như sau:
Trong đó:
H G *100
P
H: hiệu suất gần đúng của phản ứng thủy phân (%).
G: hàm lượng acid amin tan của dung dịch sau thủy phân xác định theo phương pháp Lowry.
P: hàm lượng protein ban đầu trong bánh dầu đậu phộng xác định theo phương pháp Kjeldahl.
Chương 3 KẾT QUẢ VÀ THẢO LUẬN
3.1 KHẢO SÁT LƯỢNG NHỰA Ở QUẢ ĐU ĐỦ
Chúng tôi đã tiến hành khảo sát lượng nhựa ở ba loại quả (quả non, quả già xanh, quả gần chín) ở trên cùng một loài và cùng một phương pháp làm khô. Kết quả được trình bày trong bảng 3.1
Bảng 3.1. Hàm lượng phần trăm của nhựa đu đủ trong các loại quả khác nhau.
Khối lượng quả (g) | Khối lượng nhựa lấy (g) | Tỉ lệ nhựa thô trên quả (%) | |
Quả non (dưới 40 ngày tuổi) | 120 | 0.2576 | 0.21 |
Quả già xanh (50-100 ngày tuổi) | 580 | 1.5153 | 0.26 |
Quả gần chín (100-120 ngày tuổi) | 1700 | 3.0292 | 0.18 |
Có thể bạn quan tâm!
-
 Thu nhận Enzym Papain để ứng dụng vào phản ứng thủy phân Protein trong bánh dầu đậu phộng - 2
Thu nhận Enzym Papain để ứng dụng vào phản ứng thủy phân Protein trong bánh dầu đậu phộng - 2 -
 Thành Phần Hóa Học Của Bã Đậu Phộng Đã Loại Béo
Thành Phần Hóa Học Của Bã Đậu Phộng Đã Loại Béo -
![Phương Pháp Trích Nhựa Đu Đủ Từ Trái[3, 8, 11, 16, 10, 20]](data:image/svg+xml,%3Csvg%20xmlns=%22http://www.w3.org/2000/svg%22%20viewBox=%220%200%2075%2075%22%3E%3C/svg%3E) Phương Pháp Trích Nhựa Đu Đủ Từ Trái[3, 8, 11, 16, 10, 20]
Phương Pháp Trích Nhựa Đu Đủ Từ Trái[3, 8, 11, 16, 10, 20] -
 Đường Chuẩn Biểu Diễn Sự Phụ Thuộc Của Mật Độ Quang Vào Nồng Độ Albumin.
Đường Chuẩn Biểu Diễn Sự Phụ Thuộc Của Mật Độ Quang Vào Nồng Độ Albumin. -
 Khảo Sát Sự Biến Đổi Hoạt Tính Của Các Chế Phẩm Theo Thời Gian.
Khảo Sát Sự Biến Đổi Hoạt Tính Của Các Chế Phẩm Theo Thời Gian. -
 Khảo Sát Phản Ứng Thủy Phân Ở Hàm Lượng Xúc Tác Là 0.25% So Với Cơ Chất Theo Thời Gian
Khảo Sát Phản Ứng Thủy Phân Ở Hàm Lượng Xúc Tác Là 0.25% So Với Cơ Chất Theo Thời Gian
Xem toàn bộ 96 trang tài liệu này.
Nhận xét: lượng papain thô thu được ở quả già xanh cao hơn so với quả non và quả gần chín đồng thời chiếm hàm lượng khá cao. Qua kết quả này, chúng tôi nhận thấy thời gian thích hợp để thu nhận nhựa thô là khi quả đu đủ được 50 – 100 ngày tuổi.
3.2 KHẢO SÁT ĐIỀU KIỆN SƠ CHẾ NHỰA TƯƠI
Nhựa tươi được làm khô ngay, ở nhiệt độ nhỏ hơn 50oC bằng các phương pháp khác nhau. Kết quả được trình bày trong bảng 3.2
Bảng 3.2. Các phương pháp làm khô nhựa đu đủ
Hình thức cảm quan | |
Phơi nắng 1-2 nắng | Vón cục,vàng nâu |
Sấy nóng, có quạt gió 24 giờ | Vón cục, vàng nhạt |
Đông khô chân không 8 giờ | Vẩy mỏng, óng ánh và trắng sáng |
Nhận xét:
Chất lượng papain thô thu được từ các phương pháp xử lý khác nhau rất khác nhau. Hình thức cảm quan phản ánh rõ chất lượng của sản phẩm: màu càng thẫm chất lượng càng kém.
Tuy có nhiều phương pháp khác nhau để làm khô nhựa tươi nhưng phương pháp đông khô chân không là phương pháp hiệu quả nhất và ít ảnh hưởng đến chất lượng nhựa. Do đó, toàn bộ nhựa tươi được đông khô chân không để loại nước và nhựa sau đông khô được bảo quản trong tủ lạnh để tiến hành các nghiên cứu tiếp theo.
Từ 100ml dung dịch nhựa tươi, chúng tôi tiến hành đông khô trong 8 giờ và thu được 5 gam chế phẩm đông khô.
3.3 KHẢO SÁT ĐIỀU KIỆN THU NHẬN PAPAIN TỪ NHỰA KHÔ
Nhựa tươi sau khi đã đông khô chân không, chúng tôi tiến hành sơ chế bằng dung môi hữu cơ được làm lạnh để loại bỏ các tạp chất. Sản phẩm sau quá trình sơ chế được chạy điện di để phân tích sơ bộ thành phần protein. Kết quả chạy điện di của sản phẩm sau giai đoạn sơ chế được trình bày trong hình 3.1a:
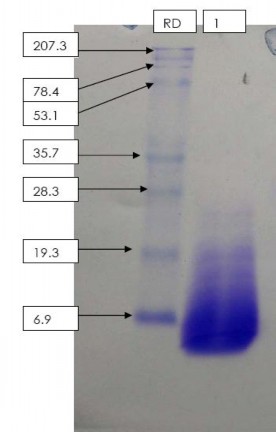
Hình 3.1a. Điện di đồ của nhựa khô ở trái non sơ chế bằng dung môi etanol
1 – thang protein chuẩn
2 – nhựa đu đủ non đông khô sơ chế bằng etanol
Nhận xét: quá trình sơ chế bằng dung môi còn lẫn khá nhiều protein tạp, do đó chúng tôi tiến hành qui trình tinh chế với các phân đoạn khác nhau để tinh sạch protein. Đồng thời, chúng ta cũng dễ dàng nhận thấy rằng trong vạch điện di của nhựa đu đủ non không có xuất hiện enzyme papain do đó chúng tôi tiến hành lấy nhựa trên trái trưởng thành để thu nhận papain. Điều này hoàn toàn phù hợp với các nghiên cứu trước đây về enzyme trong nhựa đu đủ: enzyme papain chỉ hình thành trong giai đoạn trưởng thành của trái.
Tinh chế:
Tiến hành tinh chế papain từ nhựa đông khô theo phương pháp đã trình bày trong phần thực nghiệm, từ 90 gam nhựa khô ban đầu chúng tôi thu được 1g papain. Kết quả điện di được trình bày trong hình 3.1b:

Hình 3.1 b. Điện di đồ của chế phẩm Merk và papain tinh chế từ nhựa đu đủ đông khô.
1- Thang protein chuẩn 2- Chế phẩm Merck
3 - papain



![Phương Pháp Trích Nhựa Đu Đủ Từ Trái[3, 8, 11, 16, 10, 20]](https://tailieuthamkhao.com/uploads/2023/06/13/thu-nhan-enzym-papain-de-ung-dung-vao-phan-ung-thuy-phan-protein-trong-banh-dau-4-1-120x90.jpg)


