- Đánh giá khách quan kết quả thực nghiệm của phương pháp đã chọn.
- Tìm hiểu thêm về các phương pháp quang phổ và so sánh các phương pháp phân tích định lượng với nhau.
Kết quả ghi đo một số mẫu hải sản bằng phương pháp GFAAS được tổng kết trong bảng 3.44.
Bảng 3.44: Kết quả ghi đo quang phổ hấp thụ nguyên tử lò graphit của một số mẫu hải sản
Ngao | Tôm Sú | Cá Thu | |
Lần 1 | 115,73 | 16,79 | 88,23 |
Lần 2 | 117,54 | 13,98 | 89,67 |
Lần 3 | 120,52 | 16,24 | 89,58 |
Giá trị trung bình | 117,93 | 15,67 | 89,16 |
Độ lệch chuẩn | 2,419 | 1,489 | 0,807 |
Độ lệch chuẩn trung bình | 1,396 | 0,860 | 0,466 |
Có thể bạn quan tâm!
-
 Sự Phụ Thuộc Của I P Vào Nồng Độ Các Ion Zn(Ii), As(V)
Sự Phụ Thuộc Của I P Vào Nồng Độ Các Ion Zn(Ii), As(V) -
 Đường Dpcsv Và Đường Chuẩn Của Se(Iv) Vùng Nồng Độ (0,8 ÷ 10) Ppb
Đường Dpcsv Và Đường Chuẩn Của Se(Iv) Vùng Nồng Độ (0,8 ÷ 10) Ppb -
 Kết Quả Nghiên Cứu Ảnh Hưởng Của Nồng Độ Hcl
Kết Quả Nghiên Cứu Ảnh Hưởng Của Nồng Độ Hcl -
 Đường Dpcsv Và Đồ Thị Thêm Chuẩn Xác Định Dạng Selen Trong Pha Nước Sau Khi Loại Chất Béo Bằng 5Ml N-Hexan (1 Lần)
Đường Dpcsv Và Đồ Thị Thêm Chuẩn Xác Định Dạng Selen Trong Pha Nước Sau Khi Loại Chất Béo Bằng 5Ml N-Hexan (1 Lần) -
 Đường Dpcsv Xác Định Dạng Selen Trong Pha Nước Sau Khi Tách Dạng Dmdse Bằng 5,5Ml Ch 2 Cl 2
Đường Dpcsv Xác Định Dạng Selen Trong Pha Nước Sau Khi Tách Dạng Dmdse Bằng 5,5Ml Ch 2 Cl 2 -
 Sơ Đồ Chiết Tách Và Xác Định Một Số Dạng Selen Trong Mẫu Hải Sản
Sơ Đồ Chiết Tách Và Xác Định Một Số Dạng Selen Trong Mẫu Hải Sản
Xem toàn bộ 165 trang tài liệu này.

Kết quả nghiên cứu thu được cho thấy, phương pháp GFAAS có độ chính xác cao, xác định hàm lượng các nguyên tố trong mẫu một cách nhanh chóng, điều này rất thuận tiện để xác định hàm lượng mẫu hàng loạt, đặc biệt là xác định hàm lượng tổng nguyên tố trong mẫu cần phân tích. Tuy nhiên, dựa vào độ lệch chuẩn và độ lệch chuẩn trung bình giữa các kết quả ghi đo thì phương pháp DPCSV cho độ lặp lại tốt hơn phương pháp GFAAS.
Bảng 3.45: So sánh kết quả nghiên cứu thu được theo hai phương pháp: DPCSV và GFAAS
Ngao | Tôm Sú | Cá Thu | |
DPCSV | 105,78 | 15,16 | 86,47 |
GFAAS | 117,93 | 15,67 | 89,16 |
Sai số tương đối giữa hai phương pháp | 11,49% | 3,36% | 3,11% |
Kết quả nghiên cứu chỉ ra rằng giữa hai phương pháp DPCSV và GFAAS sai lệch không đáng kể. Cùng với kết quả phân tích mẫu chuẩn, chứng tỏ phương pháp
DPCSV xây dựng được có độ tin cậy và độ chính cao, cho phép xác định nhạy lượng vết selen trong các mẫu sinh học.
Qua kết quả nghiên cứu cho thấy, hàm lượng selen trong mẫu Ngao lớn nhất, tiếp đến là cá Thu, cá Khoai, Mực và nhỏ nhất là trong tôm Sú. Các kết quả chứng tỏ rằng những động vật sống dưới đáy tích lũy selen lớn hơn so với những động vật sống ở tầng cao hơn.
3.6.2. Định lượng một số dạng selen trong mẫu hải sản
Trên cơ sở quy trình xác định một số dạng selen trong trầm tích, trong nước bằng phương pháp Von-Ampe hòa tan tham khảo từ các tài liệu, chúng tôi tiến hành nghiên cứu, xây dựng quy trình xác định một số dạng selen trong hải sản bằng phương pháp DPCSV dựa trên tính chất điện hóa của chúng.
3.6.2.1. Xây dựng sơ đồ chiết tách và xác định một số dạng selen trong mẫu hải sản
a. Chọn dung môi chiết các dạng selen trong mẫu hải sản
Để chiết các dạng selen trong hải sản, qua tham khảo tài liệu và để phù hợp với nền điện li khi xác định bằng phương pháp Von-Ampe hòa tan cũng như thuận lợi cho việc chiết tách loại bỏ protein và chất béo, chúng tôi chọn dung dịch axít HCl 0,5M để ngâm chiết mẫu.
b. Chiết tách và xác định dạng DMDSe trong pha hữu cơ
Để tiến hành nghiên cứu các điều kiện chiết tách tối ưu, chúng tôi chuẩn bị 50ml dung dịch mẫu pha chuẩn gồm: Se(IV) 1µg/l, Se-Cyst 20µg/l, DMDSe 2µg/l, axit béo 20000µg/l và HCl 0,5M.
Chúng tôi dùng dung môi diclometan (CH2Cl2) để chiết tách làm giàu dạng DMDSe từ dung dịch mẫu pha chuẩn. Do đó, chúng tôi tiến hành nghiên cứu, lựa chọn thể tích dung môi chiết, số lần chiết và thời gian lắc chiết tối ưu.
Nghiên cứu ảnh hưởng của số lần chiết và thể tích dung môi chiết diclometan
Lấy những thể tích khác nhau của CH2Cl2 để chiết tách dạng DMDSe trong mẫu pha chuẩn và tiến hành chiết nhiều lần.
- Chiết bằng 3,5ml diclometan:
Thêm 3,5ml diclometan vào 50ml mẫu pha chuẩn và lắc trong 15 phút, sau đó để yên, chờ phân lớp trong ngăn mát của tủ lạnh. Lấy 3ml dịch chiết pha hữu cơ, thêm vào 2ml diclometan, thêm tiếp 0,3ml HCl 2M, 1ml LiClO4 2M/etanol và định
mức bằng etanol đến 10ml. Làm lạnh hỗn hợp về khoảng 60C và tiến hành ghi đo DPCSV theo các điều kiện tối ưu đưa ra ở bảng 3.28. Chiết lặp lại lần 2 tương tự như lần 1. Kết quả thu được được trình bày trên các hình 3.47, 3.48.
DMDSe
c = 7.151 µg/L
+/- 0.002 µg/L (0.03%)
-100n
-80.0n
-60.0n
-40.0n
-7.2e-006
-20.0n
0
-5.00e-6
0
c (g/L)
5.00e-6 1.00e-5
+ Chiết lần 1:
I (A)
Hình 3.47: Đường DPCSV và đồ thị thêm chuẩn xác định dạng DMDSe trong dịch chiết CH2Cl2 lần 1
DMDSe
c = 1.456 µg/L
+/- 0.028 µg/L (1.94%)
-30.0n
-20.0n
-10.0n
-1.5e-006
0
-2.00e-6 -1.00e-6 0 1.00e-6 2.00e-6 3.00e-6
c (g/L)
+ Chiết lần 2:
I ( A )
Hình 3.48: Đường DPCSV và đồ thị thêm chuẩn xác định dạng DMDSe trong dịch chiết CH2Cl2 lần 2
- Chiết bằng 5,5ml diclometan:
Thêm 5,5ml diclometan vào 50ml mẫu pha chuẩn và lắc trong 15 phút, sau
đó để yên, chờ phân lớp trong ngăn mát của tủ lạnh. Lấy 5ml dịch chiết pha hữu cơ,
thêm vào 0,3ml HCl 2M, 1ml LiClO4 2M/etanol và định mức bằng etanol đến 10ml. Làm lạnh hỗn hợp về khoảng 60C và tiến hành ghi đo DPCSV theo các điều kiện tối
ưu đưa ra ở bảng 3.28. Chiết lặp lại lần 2 tương tự như lần 1. Kết quả thể hiện trên hình 3.49.
DMDSe
c = 8.978 µg /L
+/- 0.383 µg /L (4.27 %)
-100n
-80.0n
-60.0n
-40.0n
-9e-006
-20.0n
0
-1.00e-5 -5.00e-6 0 5.00e-6 1.00e-5
c (g/L)
+ Chiết lần 1:
DMDSe
c = 8.978 µg /L
+/- 0.383 µg /L (4.27 %)
-100n
-80.0n
-60.0n
)
A (
I -40.0n
-9e-006 -20.0n
0
-1.00e-5 -5.00e-6 0 5.00e-6 1.00e-5
c (g/L)
I (A)
Hình 3.49: Đường DPCSV và đồ thị thêm chuẩn xác định dạng DMDSe trong dịch chiết CH2Cl2 lần 1
+ Chiết lần 2: Không tìm thấy dạng DMDSe do hàm lượng dạng DMDSe trong dịch chiết pha hữu cơ nhỏ hơn giới hạn phát hiện.
- Chiết bằng 10ml diclometan:
Thêm 10ml diclometan vào 50ml mẫu pha chuẩn và lắc trong 15 phút, sau đó để yên, chờ phân lớp trong ngăn mát của tủ lạnh. Lấy 5ml dịch chiết pha hữu cơ, thêm vào 0,3ml HCl 2M, 1ml LiClO4 2M/etanol và định mức bằng etanol đến 10ml.
Làm lạnh hỗn hợp về khoảng 60C và tiến hành ghi đo DPCSV theo các điều kiện tối
ưu đưa ra ở bảng 3.28. Chiết lặp lại lần 2 tương tự như lần 1. Kết quả thu được thể hiện trên hình 3.50.
DMDSe
c = 4.938 µg/L
+/- 0.439 µg/L (8.89%)
-60.0n
-50.0n
-40.0n
) A
( -30.0n
I
-20.0n
-4.9e-006 -10.0n
0
-4.00e-6-2.00e-6 0 2.00e-64.00e-66.00e-6
c (g/L)
DMDSe
c = 4.938 µg/L
+/- 0.439 µg/L (8.89%)
-60.0n
-50.0n
-40.0n
-30.0n
-20.0n
-4.9e-006 -10.0n
0
-4.00e-6-2.00e-6 0 2.00e-64.00e-66.00e-6
c (g/L)
+ Chiết lần 1:
I ( A )
Hình 3.50 : Đường DPCSV và đồ thị thêm chuẩn xác định dạng DMDSe trong dịch chiết CH2Cl2 lần 1
+ Chiết lần 2: Không tìm thấy dạng DMDSe, tương tự như trường hợp chiết lần 2
khi dùng 5,5ml CH2Cl2.
Tổng hợp các kết quả thu được chỉ ra trong bảng 3.46.
Thể tích diclometan (ml) | % DMDSe tìm thấy (TB) | |
Chiết lần 1 (n=3) | Chiết lần 2 (n=3) | |
3,5 | 83,50 | 16,41 |
5,5 | 98,76 | Không tìm thấy |
10 | 99,14 | Không tìm thấy |
Bảng 3.46 : Kết quả nghiên cứu ảnh hưởng của số lần chiết và thể tích dung môi chiết CH2Cl2 đến hiệu suất chiết DMDSe
Từ kết quả nghiên cứu cho thấy, với 5,5ml CH2Cl2 thì hiệu suất chiết đã đạt được trên 98% ngay ở lần chiết đầu tiên. Ở lần chiết thứ hai không tìm thấy DMDSe, do nồng độ DMDSe còn lại trong dịch chiết mẫu rất ít và mặc dù đã được làm giàu vào pha hữu cơ nhưng vẫn nhỏ hơn giới hạn phát hiện. Do đó, chúng tôi chọn thể tích CH2Cl2 để chiết lấy dạng DMDSe là 5,5ml và tiến hành chiết 1 lần.
Nghiên cứu ảnh hưởng của thời gian lắc chiết
Để nghiên cứu ảnh hưởng của thời gian lắc chiết đến hiệu suất chiết, chúng tôi sử dụng 5,5ml diclometan để chiết tách dạng DMDSe và thay đổi thời gian lắc chiết.
Thêm 5,5ml diclometan vào 50ml mẫu pha chuẩn và lắc trong những thời gian khác nhau (5, 10, 15, 20 phút), sau đó để yên, chờ phân lớp trong ngăn mát của
tủ lạnh. Lấy 5ml dịch chiết pha hữu cơ, thêm vào 0,3ml HCl 2M, 1ml LiClO4 2M/etanol và định mức bằng etanol đến 10ml. Làm lạnh hỗn hợp về khoảng 60C và
tiến hành ghi đo DPCSV theo các điều kiện tối ưu đưa ra ở bảng 3.28. Kết quả thu
DMDSe
c = 3.320 µg/L
+/- 0.175 µg/L (5.27 %)
-60.0n
-50.0n
-40.0n
-30.0n
-20.0n
-3.3e-006-10.0n
0
-4.00e-6-2.00e-6 0 2.00e-6 4.00e-6 6.00e-6
c (g/L)
được thể hiện ở các hình từ 3.51 đến 3.54.
DMDSe
c = 3.320 µg/L
+/- 0.175 µg/L (5.27 %)
-60.0n
-50.0n
-40.0n
) A
( -30.0n
I
-20.0n
-3.3e-006-10.0n
0
-4.00e-6-2.00e-6 0 2.00e-6 4.00e-6 6.00e-6
c (g/L)
DMDSe
c = 5.845 µg /L
+/- 0.265 µg/L (4 .53 %)
-50.0n
-40.0n
(A -30.0n
)
I
-20.0n
-10.0n
-5.8e-006
0
-5.00e-6-2.50e-6 0 2.50e-6 5.00e-6
c (g/L)
DMDSe
c = 5.845 µg /L
+/- 0.265 µg/L (4 .53 %)
-50.0n
-40.0n
-30.0n
-20.0n
-10.0n
-5.8e-006
0
-5.00e-6-2.50e-6 0 2.50e-6 5.00e-6
c (g/L)
I (A)
Hình 3.51: Đường DPCSV và đồ thị thêm chuẩn xác định dạng DMDSe trong dịch chiết CH2Cl2 khi lắc chiết 5 phút
I (A)
Hình 3.52: Đường DPCSV và đồ thị thêm chuẩn xác định dạng DMDSe trong dịch chiết CH2Cl2 khi lắc chiết 10 phút
DMDSe
c = 8 .934 µg/L
+/- 0.671 µg/L (7.51 %)
-150n
-125n
-100n
)
A -75.0n
( I
-50.0n
-8.9e-006-25.0n
0
-1.00e-5 0 1.00e-5 2.00e-5
c (g/L)
DMDSe
c = 9 .060 µg/L
+/- 0.414 µg/L (4.57%)
-150n
-125n
-100n
)
A -75.0n
( I
-50.0n
-9.1e-00-256 .0n
0
-1.00e-5 0 1.00e-5 2.00e-5
c (g/L)
DMDSe
c = 8 .934 µg/L
+/- 0.671 µg/L (7.51 %)
-150n
-125n
-100n
-75.0n
-50.0n
-8.9e-006-25.0n
0
-1.00e-5
0
c (g/L)
1.00e-5 2.00e-5
DMDSe
c = 9 .060 µg/L
+/- 0.414 µg/L (4.57%)
-1.00e-5
0
c (g/L)
1.00e-5
2.00e-5
I (A)
Hình 3.53: Đường DPCSV và đồ thị thêm chuẩn xác định dạng DMDSe trong dịch chiết CH2Cl2 khi lắc chiết 15 phút
0 |
I (A)
Hình 3.54: Đường DPCSV và đồ thị thêm chuẩn xác định dạng DMDSe trong dịch chiết CH2Cl2 khi lắc chiết 20 phút
Tổng hợp các kết quả nghiên cứu thời gian lắc chiết được trình bày ở bảng 3.47.
Bảng 3.47: Kết quả nghiên cứu ảnh hưởng của thời gian lắc chiết
đến hiệu suất chiết DMDSe
5 phút (n=3) | 10 phút (n=3) | 15 phút (n=3) | 20 phút (n=3) | |
% DMDSe tìm thấy (TB) | 36,89 | 64,13 | 98,45 | 99,22 |
Từ kết quả nghiên cứu cho thấy, từ 15 phút trở đi hiệu suất chiết đạt được trên 98%. Tuy nhiên, khi phân tích mẫu cần rút ngắn thời gian phân tích, do đó chúng tôi chọn thời gian lắc chiết là 15 phút.
c. Chiết loại chất béo để xác định dạng Se-Cyst và Se(IV) trong pha nước
Như đã nghiên cứu trong mục 3.3, chất béo gây cản trở đến việc ghi đo mẫu xác định các dạng selen trong pha nước, cần phải loại bỏ. Chúng tôi tiến hành nghiên cứu các điều kiện tối ưu để chiết loại chất béo bằng n-hexan dựa trên mẫu pha chuẩn được chuẩn bị như ở phần b.
Nghiên cứu, lựa chọn số lần chiết và thể tích dung môi chiết n-hexan tối ưu
Se-cyst
c = 19.081 µg/L
+/- 0.052 µg/L (0.27%)
-200n
-150n
-100n
-50.0n
-1.9e-005
0
-2.00e-5
0
2.00e-5
c (g/L)
4.00e-5
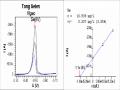
Trước khi sử dụng n-hexan để loại bỏ chất béo, chúng tôi tiến hành chiết tách dạng DMDSe vào pha hữu cơ bằng 5,5ml diclometan, sau đó lấy 10ml dịch chiết pha nước đem ghi đo DPCSV theo các điều kiện tối ưu đưa ra ở bảng 3.14, kết quả thể hiện trên hình 3.55.
I (A)
Hình 3.55: Đường DPCSV và đồ thị thêm chuẩn xác định dạng selen trong pha nước sau khi chiết tách dạng DMDSe bằng 5,5ml CH2Cl2
Trên hình 3.55 cho thấy, chỉ xuất hiện pic của Se-Cyst, còn Se(IV) chỉ thấy ở dạng vai nhỏ so với pic của Se-Cyst. Điều này có thể giải thích như sau: khi dùng CH2Cl2 để chiết dạng DMDSe thì lượng axít béo trong mẫu pha chuẩn sẽ bị chiết một phần cùng với DMDSe vào pha hữu cơ. Do đó hàm lượng axít béo còn lại trong pha nước không còn đủ để gây biến dạng hay làm giảm cường độ pic của Se-Cyst nhưng lại đủ để gây biến dạng và làm giảm cường độ pic của Se(IV). Vì vậy, chỉ xác định được dạng Se-Cyst mà không xác định được dạng Se(IV).