- Dung dịch thử (định lượng nystose trong dược liệu rễ Ba kích): Nghiền dược liệu rễ Ba kích thành bột mịn và rây qua rây 250 µm. Cân chính xác khoảng 0,5 g bột dược liệu rễ Ba kích vào bình nón nút mài 100 ml, thêm chính xác 50 ml pha động, đậy nắp, cân xác định khối lượng. Đun sôi hồi lưu trong cách thủy 30 phút, để nguội, cân lại, bổ sung pha động nếu thiếu so với khối lượng ban đầu.
* Tiến hành
- Độ thích hợp của hệ thống sắc ký: Độ lệch chuẩn tương đối của thời gian lưu và Ln(diện tích pic) của pic nystose trong 6 lần tiêm lặp lại dung dịch chuẩn không được lớn hơn 2,0 %. Số đĩa lý thuyết tính theo pic nystose không thấp hơn 2.000.
- Tiêm lần lượt dung dịch chuẩn và dung dịch thử vào hệ thống sắc ký. Tiến hành sắc ký theo điều kiện đã nêu, ghi thời gian lưu và diện tích của các pic nystose.
* Tính toán kết quả
- Hàm lượng (%) nystose (C24H42O41), tính theo nguyên trạng trong nguyên liệu
được tính theo công thức:
𝑋 (%) = 𝑒
𝑙𝑛𝐶
𝑐
(ln 𝑆𝑇×𝑙𝑛𝑆𝐶)
25
×
𝑚 × 1000
1
×
1000
× 100
- Hàm lượng (%) nystose (C24H42O41), tính theo dược liệu khô kiệt được tính theo công thức:
trong đó:
𝑋 (%) = 𝑒
𝑙𝑛𝐶
𝑐
(ln 𝑆𝑇×𝑙𝑛𝑆𝐶)
50
× ×
𝑚 × 1000
100
100 − 𝐴
1
×
1000
× 100
SC: diện tích pic nystose trên sắc ký đồ của dung dịch chuẩn ST: diện tích pic nystose trên sắc ký đồ của dung dịch thử CC: nồng độ nystose trong dung dịch chuẩn (µg/ml)
m: lượng cân mẫu thử (g).
A: hàm ẩm của dược liệu rễ Ba kích (%).
b. Thẩm định phương pháp định tính, định lượng nystose
Tiến hành thẩm định phương pháp định tính, định lượng nystose bằng HPLC- ELSD dựa trên các chỉ tiêu tại Bảng 2.3.
Bảng 2.3. Nội dung thẩm định phương pháp định lượng nystose [52]
Cách xác định/ đánh giá | Giới hạn chấp nhận | ||||
Độ thích hợp của hệ thống | Hiệu lực phân tách của cột | Số đĩa ≥ 2.000 | lý | thuyết | (N) |
Độ lệch chuẩn tương đối (RSD) của thời gian lưu, ln(diện tích pic) nystose trong dung dịch chuẩn | RSD ≤ 2,0 % (n = 6) | ||||
Độ đặc hiệu | Thời gian lưu của pic nystose trên sắc ký đồ của dung dịch chuẩn, dung dịch thử. | Thời gian lưu tương ứng | |||
Sắc ký đồ dung dịch mẫu dung môi | Không có pic tại thời gian lưu của pic monotropein | ||||
Độ tính | tuyến | Hệ số tương quan giữa ln(diện tích pic) và ln(nồng độ) | r ≥ 0,995 | ||
Độ chính xác | |||||
Độ lặp lại | Giá trị định lượng | RSD | kết | quả | RSD ≤ 2,0% (n = 6) |
Độ chính xác trung gian | Xác định giá trị RSD kết quả định lượng | RSD ≤ 2,0% (n = 12) | |||
Xác định tỷ lệ thu hồi của chất | |||||
Độ đúng | chuẩn nystose trong các dung dịch tự tạo có mức nồng độ tương ứng 80%, 100% và 120% so với nồng | 98,0 % - 102,0 % RSD ≤ 2,0% (n = 9) | |||
độ định lượng. | |||||
Có thể bạn quan tâm!
-
 Tình Hình Thiết Lập Chất Chuẩn Monotropein Và Nystose
Tình Hình Thiết Lập Chất Chuẩn Monotropein Và Nystose -
![Sơ Đồ Và Các Chu Kỳ Của Phản Ứng Chuỗi Polymerase [15]](data:image/svg+xml,%3Csvg%20xmlns=%22http://www.w3.org/2000/svg%22%20viewBox=%220%200%2075%2075%22%3E%3C/svg%3E) Sơ Đồ Và Các Chu Kỳ Của Phản Ứng Chuỗi Polymerase [15]
Sơ Đồ Và Các Chu Kỳ Của Phản Ứng Chuỗi Polymerase [15] -
 Thẩm Định Phương Pháp Định Tính, Định Lượng Monotropein Và Nystose
Thẩm Định Phương Pháp Định Tính, Định Lượng Monotropein Và Nystose -
 Xây Dựng Tiêu Chuẩn Chất Lượng Chất Chuẩn Monotropein Và Nystose
Xây Dựng Tiêu Chuẩn Chất Lượng Chất Chuẩn Monotropein Và Nystose -
 Thẩm Định Phương Pháp Định Tính, Định Lượng Monotropein
Thẩm Định Phương Pháp Định Tính, Định Lượng Monotropein -
 Kết Quả Độ Chính Xác Trung Gian Của Phương Pháp Định Lượng Nystose Trong Nguyên Liệu
Kết Quả Độ Chính Xác Trung Gian Của Phương Pháp Định Lượng Nystose Trong Nguyên Liệu
Xem toàn bộ 226 trang tài liệu này.

Phương pháp tiến hành
Độ thích hợp của hệ thống
Tiến hành sắc ký lặp lại 6 lần dung dịch chuẩn vào hệ thống sắc ký, ghi lại sắc ký đồ. Xác định độ lặp lại của thời gian lưu, ln(diện tích pic) nystose và số đĩa lý thuyết.
Độ đặc hiệu
- Mẫu trắng (dung môi): Pha động.
- Dung dịch chuẩn, dung dịch thử: Tiến hành theo Mục 2.3.1.1 – b – Chuẩn bị dung dịch chuẩn, dung dịch thử.
Tiến hành sắc ký lần lượt các dung dịch chuẩn, dung dịch thử, dung môi vào hệ thống sắc ký, ghi lại sắc ký đồ.
Độ tuyến tính
- Dung dịch chuẩn gốc: Cân chính xác khoảng 10 mg chất chuẩn nystose, hoà
tan và định mức thành 10 ml dung dịch bằng pha động.
- Từ dung dịch chuẩn gốc, tiến hành pha loãng bằng pha động để thu được các dung dịch chuẩn có nồng độ nystose lần lượt bằng 25 %, 50 %, 100 %, 150 % và 200
% so với nồng độ định lượng.
Tiến hành sắc ký các dung dịch chuẩn trên, ghi lại sắc ký đồ. Xây dựng đường hồi qui tuyến tính giữa Ln(diện tích pic) và Ln(nồng độ) nystose trong các dung dịch chuẩn. Xác định hệ số tương quan tuyến tính (r).
Độ chính xác
Độ lặp lại:
- Sử dụng phương trình hồi quy tuyến tính.
- Dung dịch thử: Chuẩn bị 6 dung dịch thử theo phương pháp nêu tại Mục 2.3.1.1
– b – Chuẩn bị dung dịch thử.
Xác định hàm lượng nystose trong 6 dung dịch thử, tính độ lệch chuẩn tương đối của 6 giá trị hàm lượng.
Độ chính xác trung gian
Tiến hành tương tự như phần độ lặp lại nhưng khác ngày, khác người thử nghiệm. Tính độ lệch chuẩn tương đối của 6 kết quả định lượng khác ngày và 12 kết quả định lượng của độ lặp lại và khác ngày.
Độ đúng
* Định lượng nystose trong nguyên liệu: Sử dụng phương pháp mẫu tự tạo.
- Sử dụng phương trình hồi quy của mục Độ tuyến tính.
- Dung dịch 80%: Cân chính xác khoảng 8 mg chuẩn nystose, hòa tan và định mức thành 25 ml bằng pha động.
- Dung dịch 100%: Cân chính xác khoảng 10 mg chuẩn nystose, hòa tan và định mức thành 25 ml bằng pha động.
- Dung dịch 120%: Cân chính xác khoảng 12 mg chuẩn nystose, hòa tan và định mức thành 25 ml bằng pha động.
Tiến hành sắc ký các dung dịch chuẩn và dung dịch mẫu tự tạo, ghi lại sắc ký
đồ. Xác định tỷ lệ thu hồi của nystose trong 9 dung dịch mẫu tự tạo.
* Định lượng nystose trong dược liệu: Sử dụng phương pháp thêm chuẩn.
- Dung dịch chuẩn: Chuẩn bị theo phương pháp tại Mục 2.3.1.2 - a.
- Dung dịch thử: Thêm chính xác khoảng 9 mg, 14 mg và 19 mg chất chuẩn nystose vào các bình nón nút mài 100 ml đã chứa sẵn khoảng khoảng 0,25 g bột dược liệu rễ Ba kích, thêm chính xác 50 ml pha động, đậy nắp, cân xác định khối lượng. Đun sôi hồi lưu trong cách thủy 30 phút, để nguội, cân lại, bổ sung pha động nếu thiếu so với khối lượng ban đầu.
Tiến hành sắc ký các dung dịch chuẩn và dung dịch mẫu tự tạo, ghi lại sắc ký
đồ. Xác định tỷ lệ thu hồi của nystose trong 9 dung dịch mẫu thử.
2.3.1.3. Thẩm định phương pháp định tính nystose trong dược liệu rễ Ba kích bằng TLC
a. Phương pháp định tính nystose trong dược liệu bằng TLC
Tham khảo phương pháp định tính nystose trong dược liệu rễ Ba kích bằng phương pháp TLC trong Bộ tiêu chuẩn chất lượng dược liệu Hồng Kông [47], lựa chọn phương pháp định tính nystose trong dược liệu rễ Ba kích với điều kiện như sau:
Bản mỏng: Silica gel F254.
Dung môi khai triển: Ethyl acetat – nước – acid formic – acid acetic băng (6 : 3
: 2 : 2).
Thuốc thử hiện màu: Cho từ từ 11 ml acid sulfuric đặc vào 89 ml EtOH. Thêm 2,75 g alpha-naphthol và 7 ml nước.
Dung dịch chuẩn: Cân khoảng 5 mg chất chuẩn nystose, hoà tan và định mức thành 50 ml bằng MeOH.
Dung dịch thử: Cân khoảng 0,5 g bột dược liệu rễ Ba kích vào bình nón dung tích 50 ml, thêm 20 ml MeOH. Lắc siêu âm trong 15 phút. Lọc lấy dịch lọc.
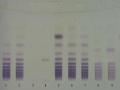
Tiến hành: Chấm lần lượt 15 µl dung dịch chuẩn và 1,5 µl dung dịch thử lên bản mỏng. Trước khi triển khai sắc ký, thêm pha động vào 1 ngăn, bản mỏng để vào ngăn còn lại, đậy nắp bình và để yên 15 phút. Nghiêng bình sắc ký để pha động tràn sang ngăn chứa bản mỏng. Triển khai sắc ký đến khi pha động đi được khoảng 8 cm,
lấy bản mỏng ra, đánh dấu mức di chuyển của pha động trước, sấy khô bản mỏng. Phun thuốc thử hiện màu lên bản mỏng, sấy ở nhiệt độ khoảng 100 oC đến khi xuất hiện vết. Trên sắc ký đồ của dung dịch thử phải có vết chính có cùng màu sắc và giá trị Rf với vết nystose trên sắc ký đồ của dung dịch chuẩn.
b. Thẩm định phương pháp định tính nystose trong dược liệu rễ Ba kích bằng TLC
Tính đặc hiệu
- Dung môi: MeOH
- Dung dịch chuẩn: Sử dụng chất chuẩn nystose, nguồn gốc Sigma Aldrich (lô: BCBT3105).
- Dung dịch dược liệu chuẩn: Sử dụng dược liệu chuẩn Ba kích (Morinda officinalis How, họ cà phê (Rubiaceae)): Nguồn gốc: Viện kiểm nghiệm thuốc và thực phẩm Trung ương Trung Quốc; Số lô: 121163-201405.
- Dung dịch thử: Sử dụng 6 mẫu dược liệu rễ Ba kích tại Bảng 2.1.
Tiến hành sắc ký các dung dịch trên theo điều kiện sắc ký ở Mục 2.3.1.3 – a. So sánh màu sắc, vị trí (Rf) của vết chính cho bởi các dung dịch dược liệu chuẩn, dung dịch thử, dung môi so với vết nystose cho bởi dung dịch chuẩn.
2.3.2. Chiết xuất, phân lập, tinh chế monotropein và nystose từ dược liệu rễ Ba kích
2.3.2.1. Chuẩn bị mẫu
- Dược liệu rễ Ba kích tươi thu hái tại Hoành Bồ, Quảng Ninh (BK4) được rửa sạch, bỏ lõi, thái nhỏ và sấy ở nhiệt độ 55 oC cho đến khi hàm ẩm dưới 12 %, sau đó xay và rây qua rây kích thước lỗ 2800 µm thu được bột khô Ba kích.
2.3.2.2. Chiết xuất cao chiết toàn phần chứa monotropein và nystose
- Lựa chọn MeOH để chiết các iridoid ra khỏi dược liệu. Phần bã sau khi chiết
được gom lại và chiết với nước để thu cao chiết nước có chứa nystose.
2.3.2.3. Phân lập và tinh chế monotropein
- Sử dụng phương pháp chiết phân đoạn, sắc ký cột, kết tinh lại để phân lập, tinh chế monotropein. Kết hợp với các phương pháp SKLM để kiểm tra sự có mặt của monotropein trong từng giai đoạn.
+ Chuẩn bị cột sắc ký cột silica gel: Sử dụng cột thuỷ tinh đường kính 2,5 cm, dài 40 cm. Cân 7 g silica gel vào cốc thuỷ tinh có chứa 20 ml chloroform, khuấy đều, chuyển lên cột. Tiếp tục cho khoảng 50 ml chloroform chảy qua cột với tốc độ 2 ml/phút, để yên khoảng 3 giờ cho cột ổn định.
Dịch chiết thu được tinh chế bằng phương pháp sắc ký lỏng bán điều chế với
điều kiện sắc ký như sau:
- Cột sắc ký: Gimitec HiQ sil C18-10 (250 mm x 10 mm).
- Detector UV tại bước sóng 237 nm.
- Lượng mẫu bơm: 100 µl.
- Tốc độ dòng: 2,5 ml/phút.
- Thời gian phân tích: 15 phút.
- Pha động: Gradient dung môi theo chương trình tại Bảng 2.4.
Bảng 2.4. Chương trình gradient pha động sắc ký lỏng điều chế.
Thời gian (phút) | % MeOH | % Dung dịch amoni acetat 20 mM | |
1 | 0 8 | 3 | 97 |
2 | 8 15 | 3 100 | 97 0 |
Hứng và gộp các dung dịch có thời gian lưu tương ứng với pic monotropein, cô
quay dưới áp suất giảm thu được sản phẩm kết tinh.
2.3.2.4. Phân lập và tinh chế nystose
- Sử dụng phương pháp chiết phân đoạn, sắc ký cột, kết tinh lại kết hợp phổ khối, SKLM để tiến hành phân lập tinh chế nystose.
2.3.2.5. Xác định cấu trúc và kiểm tra độ tinh khiết của các chất tinh chế được
- Xác định cấu trúc: Tiến hành đo phổ cộng hưởng từ hạt nhân, đo khối phổ, đo
phổ hồng ngoại
- Kiểm tra độ tinh khiết:
+ Đo điểm chảy của chất tinh chế được.
+ Sử dụng các phương pháp HPLC detector DAD (đối với monotropein) và
detector ELSD (đối với nystose) để định tính và đánh giá sơ bộ độ tinh khiết.
2.3.3. Thiết lập chất chuẩn monotropein và nystose
2.3.3.1. Kiểm tra chất lượng nguyên liệu monotropein và nystose
Lấy một lượng nguyên liệu (ở điều kiện nhiệt độ 22 – 25 oC, độ ẩm tương đối thích hợp tùy thuộc vào tính chất của chất đối chiếu đủ để đánh giá các tiêu chuẩn chất lượng theo qui trình thiết lập đối chiếu. Đánh giá nguyên liệu theo qui trình thiết lập chất đối chiếu [23], [24], [26], [85].
a. Nguyên liệu monotropein
* Định tính: Phương pháp đo quang phổ IR và sắc ký lỏng hiệu năng cao.
* Mất khối lượng do làm khô: Phương pháp phân tích nhiệt trọng lượng (TGA)
- Thiết bị: Máy phân tích nhiệt trọng lượng TGA.
- Chương trình gia nhiệt: 25 ºC đến 105 ºC, tốc độ gia nhiệt 10 oC/phút, giữ ở 105
ºC trong 180 phút.
- Lượng mẫu thử: Khoảng 5 mg chế phẩm.
* Nhiệt độ nóng chảy: Tiến hành theo Phụ lục 6.7 – Dược điển Việt Nam V.
* Định lượng: Theo phương pháp phân tích tại Mục 2.3.1 - a.
* Tạp chất liên quan:
+ Điều kiện sắc ký: Tương tự điều kiện sắc ký của chỉ tiêu định lượng, thời gian chạy sắc ký gấp 4 lần thời gian lưu của pic monotropein.
- Mẫu trắng: Nước.
- Dung dịch chuẩn: Cân chính xác khoảng 10 mg monotropein chuẩn, hòa tan và định mức thành 10 ml dung dịch bằng MeOH. Lấy chính xác 1 ml dung dịch pha loãng và định mức thành 20 ml bằng nước.
- Dung dịch thử: Cân chính xác khoảng 10 mg nguyên liệu monotropein, hòa
tan và định mức thành 10 ml dung dịch bằng pha động.
- Dung dịch đối chiếu: Lấy chính xác 1 ml dung dịch thử pha loãng và định mức thành 100 ml bằng pha động.
Tiến hành sắc ký lần lượt với dung dịch mẫu trắng, dung dịch chuẩn, dung dịch đối chiếu và dung dịch thử, ghi lại sắc ký đồ, thời gian lưu và diện tích của tất cả các pic ngoại trừ pic dung môi. Hàm lượng (%) từng tạp chất được tính theo công thức:
Trong đó:
X (%) =𝑆𝑇× 100
𝑆𝐶
- ST: Diện tích pic từng tạp trên sắc ký đồ dung dịch thử.
- SC: Diện tích pic monotropein trên sắc ký đồ dung dịch đối chiếu tương ứng.
Loại những pic phụ có diện tích pic 0,05 % so với diện tích pic monotropein
thu được trong dung dịch đối chiếu tương ứng.
b. Nguyên liệu nystose
- Định tính: Phương pháp đo quang phổ IR và sắc ký lỏng hiệu năng cao.
- Mất khối lượng do làm khô: Phương pháp phân tích nhiệt trọng lượng (TGA)
+ Thiết bị: Máy phân tích nhiệt trọng lượng TGA.
+ Chương trình gia nhiệt: 25 ºC đến 105 ºC, tốc độ gia nhiệt 10 ºC/phút, giữ ở 105
ºC trong 180 phút.
+ Lượng mẫu thử: Khoảng 5 mg chế phẩm.
- Nhiệt độ nóng chảy: Tiến hành theo Phụ lục 6.7 – Dược điển Việt Nam V.
- Định lượng: Theo phương pháp phân tích tại Mục 2.3.1 - b.
- Tạp chất liên quan: Phương pháp sắc ký lớp mỏng [47].
Điều kiện sắc ký:
+ Bản mỏng: Silica gel GF254.
+ Dung môi khai triển: Ethyl acetat – nước – acid formic – acid acetic (6 : 3 : 2
: 2).
+ Thuốc thử hiện vết: Thêm từ từ 11 ml dung dịch acid sulfuric đậm đặc vào 89
ml EtOH tuyệt đối, thêm 2,75 g α - naphthol và 7 ml nước, trộn đều.
Chuẩn bị các dung dịch thử, dung dịch đối chiếu:
+ Dung dịch chuẩn: Dung dịch chuẩn nystose trong MeOH có nồng độ 0,05 mg/ml.
+ Dung dịch thử: Cân chính xác khoảng 10 mg nguyên liệu nystose, hoà tan và
định mức thành 10,0 ml dung dịch bằng MeOH.


![Sơ Đồ Và Các Chu Kỳ Của Phản Ứng Chuỗi Polymerase [15]](https://tailieuthamkhao.com/uploads/2024/04/20/nghien-cuu-nang-cap-tieu-chuan-duoc-lieu-re-ba-kich-radix-morindae-officinalis-5-3-120x90.jpg)