Kết quả cho thấy có sự tương quan tuyến tính chặt chẽ giữa Ln(nồng độ) và Ln(diện tích pic) trong khoảng nồng độ từ 113,1 µg/ml – 904,4 µg/ml với hệ số tương quan gần bằng 1 (r = 0,9992).
3.1.2.4. Độ chính xác
a. Định lượng nystose trong nguyên liệu
- Ngày định lượng 1: Phương trình hồi quy: Y= 1,40 X + 4,48 (Kết quả của độ
lặp lại).
- Ngày định lượng 2: Phương trình hồi quy: Y= 1,40 X + 44,67.
Kết quả độ chính xác của phương pháp định lượng nystose trong nguyên liệu
được trình bày tại Bảng 3.9.
Bảng 3.9. Kết quả độ chính xác trung gian của phương pháp định lượng nystose trong nguyên liệu
Ngày định lượng 2 | |||||||||
Stt | Lượng cân (mg) | Diện tích pic (mV.s) | Ln (diện tích pic) | Hàm lượng (%) | Stt | Lượng cân (mg) | Diện tích pic (mV.s) | Ln (diện tích pic) | Hàm lượng (%) |
1 | 10,08 | 379241 | 12,85 | 96,61 | 1 | 10,63 | 482012 | 13,09 | 97,73 |
2 | 10,82 | 419806 | 12,95 | 96,76 | 2 | 10,82 | 497401 | 13,12 | 98,20 |
3 | 10,92 | 435786 | 12,98 | 98,47 | 3 | 10,53 | 470062 | 13,06 | 96,90 |
4 | 10,85 | 428230 | 12,97 | 97,87 | 4 | 10,90 | 501272 | 13,13 | 98,02 |
5 | 10,95 | 426456 | 12,96 | 96,69 | 5 | 10,74 | 488089 | 13,10 | 97,60 |
6 | 10,22 | 400765 | 12,90 | 99,11 | 6 | 10,35 | 469313 | 13,06 | 98,47 |
Trung bình | 97,59 | Trung bình | 97,82 | ||||||
RSD (%) | 1,09 | RSD (%) | 0,56 | ||||||
Kết quả định lượng trung bình (n=12): 97,71 %; RSD = 0,83 % | |||||||||
Có thể bạn quan tâm!
-
![Nội Dung Thẩm Định Phương Pháp Định Lượng Nystose [52]](data:image/svg+xml,%3Csvg%20xmlns=%22http://www.w3.org/2000/svg%22%20viewBox=%220%200%2075%2075%22%3E%3C/svg%3E) Nội Dung Thẩm Định Phương Pháp Định Lượng Nystose [52]
Nội Dung Thẩm Định Phương Pháp Định Lượng Nystose [52] -
 Xây Dựng Tiêu Chuẩn Chất Lượng Chất Chuẩn Monotropein Và Nystose
Xây Dựng Tiêu Chuẩn Chất Lượng Chất Chuẩn Monotropein Và Nystose -
 Thẩm Định Phương Pháp Định Tính, Định Lượng Monotropein
Thẩm Định Phương Pháp Định Tính, Định Lượng Monotropein -
 Sơ Đồ Phân Lập, Tinh Chế Nystose Từ Cao Chiết Nước
Sơ Đồ Phân Lập, Tinh Chế Nystose Từ Cao Chiết Nước -
 Kết Quả Định Lượng Độ Ổn Định Chất Chuẩn Monotropein (6 Tháng)
Kết Quả Định Lượng Độ Ổn Định Chất Chuẩn Monotropein (6 Tháng) -
 Kết Quả Định Lượng Nghiên Cứu Độ Ổn Định Chất Chuẩn Nystose (1 Năm)
Kết Quả Định Lượng Nghiên Cứu Độ Ổn Định Chất Chuẩn Nystose (1 Năm)
Xem toàn bộ 226 trang tài liệu này.
b. Định lượng monotropein trong dược liệu rễ Ba kích
- Mẫu thử: BK5 (độ ẩm: 10,49 %).
- Ngày định lượng 1: Phương trình hồi quy: Y = 1,57 X + 3,24 (Kết quả của độ
lặp lại).
- Ngày định lượng 2: Lượng cân chất chuẩn nystose: 11,21 mg. Diện tich pic nystose: 360921 mV.s.
Kết quả độ chính xác của phương pháp định lượng nystose trong dược liệu rễ Ba kích (BK5) được trình bày tại Bảng 3.10.
Bảng 3.10. Kết quả độ chính xác của phương pháp định lượng nystose trong dược liệu BK5
Ngày định lượng 2 | |||||||||
Stt | Lượng cân thử (g) | Diện tích pic (mV.s) | Ln (diện tích pic) | Hàm lượng (%) | Stt | Lượng cân thử (g) | Diện tích pic (mV.s) | Ln (diện tích pic) | Hàm lượng (%) |
1 | 0,5095 | 511805 | 13,15 | 6,1 | 1 | 0,5216 | 611805 | 13,32 | 6,13 |
2 | 0,5025 | 523556 | 13,17 | 6,2 | 2 | 0,5122 | 603556 | 13,31 | 6,20 |
3 | 0,5091 | 523556 | 13,17 | 6,2 | 3 | 0,5330 | 623556 | 13,34 | 6,06 |
4 | 0,5082 | 530254 | 13,18 | 6,2 | 4 | 0,5132 | 600254 | 13,31 | 6,18 |
5 | 0,5106 | 525952 | 13,17 | 6,2 | 5 | 0,5078 | 595952 | 13,30 | 6,22 |
6 | 0,5054 | 509592 | 13,14 | 6,1 | 6 | 0,5109 | 589592 | 13,29 | 6,15 |
Trung bình | 6,2 | Trung bình | 6,2 | ||||||
RSD (%) | 1,1 | RSD (%) | 1,0 | ||||||
Kết quả định lượng trung bình (n=12): 6,2 %; RSD = 1,0 % | |||||||||
Kết quả cho thấy phương pháp có độ chính xác cao, thể hiện độ lặp lại trong ngày với RSD ≤ 1,1 % và khác ngày RSD ≤ 1,0 %
3.1.2.5. Độ đúng
a. Định lượng nystose trong nguyên liệu
- Phương trình hồi quy: Y = 1,40 x + 4,48
Kết quả khảo sát độ đúng của phương pháp định lượng nystose trong nguyên liệu được trình bày tại Bảng 3.11.
Bảng 3.11. Kết quả khảo sát độ đúng phương pháp định lượng nystose trong nguyên liệu
Dung dịch | Lượng chất chuẩn nystose (mg) | Diện tích pic (mV.s) | Ln(diện tích pic) | Lượng chất chuẩn nystose tìm lại (mg) | Tỷ lệ thu hồi (%) | |
1 | 80% | 8,25 | 304064 | 12,63 | 8,29 | 101,2 |
2 | 80% | 8,00 | 290680 | 12,58 | 8,03 | 101,1 |
3 | 80% | 8,26 | 306790 | 12,63 | 8,35 | 101,8 |
4 | 100% | 10,61 | 431027 | 12,97 | 10,64 | 101,0 |
5 | 100% | 10,32 | 418658 | 12,94 | 10,42 | 101,7 |
6 | 100% | 10,29 | 408393 | 12,92 | 10,24 | 100,2 |
7 | 120% | 12,59 | 545036 | 13,21 | 12,57 | 100,6 |
8 | 120% | 12,01 | 503902 | 13,13 | 11,89 | 99,7 |
9 | 120% | 12,46 | 541811 | 13,20 | 12,52 | 101,2 |
Trung bình | 100,9 | |||||
RSD (%) | 0,7 | |||||
b. Định lượng nystose trong dược liệu rễ Ba kích
- Lượng cân chất chuẩn nystose trong dung dịch chuẩn: 10,29 mg.
- Mẫu thử Ba kích BK5: Hàm lượng nystose là 6,2 % (Bảng 3.10), độ ẩm: 10,49
%.
Kết quả khảo sát độ đúng của phương pháp định lượng nystose trong dược liệu
rễ Ba kích được trình bày ở Bảng 3.12.
Bảng 3.12. Kết quả khảo sát độ đúng phương pháp định lượng nystose trong dược liệu BK5
Dung dịch | Lượng cân mẫu thử BK5 (g) | Lượng chất chuẩn thêm vào (mg) | Diện tích pic (mV.s) | Ln(diện tích pic) | Lượng chất chuẩn nystose tìm lại (mg) | Tỷ lệ thu hồi (%) | |
1 | 80% | 0,2408 | 9,22 | 438521 | 12,99 | 9,12 | 99,6 |
2 | 80% | 0,2402 | 9,21 | 436880 | 12,99 | 9,12 | 99,7 |
3 | 80% | 0,2405 | 9,04 | 427050 | 12,96 | 8,86 | 98,7 |
4 | 100% | 0,2501 | 14,79 | 723167 | 13,49 | 14,54 | 99,0 |
5 | 100% | 0,2561 | 14,59 | 742109 | 13,52 | 14,56 | 100,5 |
6 | 100% | 0,2568 | 14,29 | 723417 | 13,49 | 14,18 | 99,9 |
7 | 120% | 0,2515 | 19,57 | 1004945 | 13,82 | 19,20 | 98,8 |
8 | 120% | 0,2618 | 19,25 | 1043908 | 13,86 | 19,23 | 100,6 |
9 | 120% | 0,2596 | 19,34 | 1029612 | 13,84 | 19,14 | 99,6 |
Trung bình | 99,6 | ||||||
RSD (%) | 0,7 | ||||||
Kết quả cho thấy phương pháp có độ đúng tốt (phần trăm tìm lại trong nguyên liệu và trong dược liệu lần lượt đạt từ 99,7 % - 101,8 % và 98,8 % - 100,6 %) với độ lệch chuẩn tương đối RSD = 0,7 % (< 2,0%).
3.1.3. Thẩm định phương pháp định tính nystose trong dược liệu rễ Ba kích bằng
phương pháp sắc ký lớp mỏng
Tiến hành theo phương pháp tại Mục 2.3.1.3.
Kết quả thẩm định phương pháp định tính nystose trong dược liệu được trình bày tại Hình 3.5.
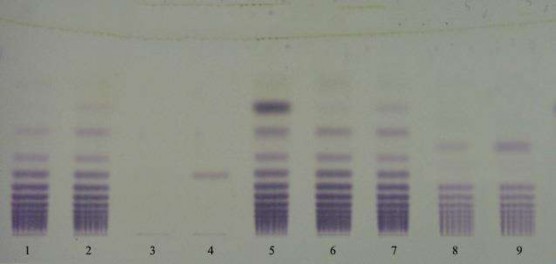
(3): Dung môi (1): Dung dịch thử BK1 (6): Dung dịch thử BK4 (4): Dung dịch chuẩn nystose (2): Dung dịch thử BK3 (7): Dung dịch thử BK5 (5): Dung dịch dược liệu chuẩn Ba kích (8): Dung dịch thử BK2 (9): Dung dịch thử BK6
Hình 3.5. Kết quả đánh giá độ đặc hiệu phương pháp định tính nystose trong dược liệu rễ Ba kích
Kết quả tại Hình 3.5 cho thấy:
- Dung môi không cho vết chính tương ứng với vết nystose cho bởi dung dịch chuẩn.
- Dung dịch dược liệu chuẩn, dung dịch thử BK1, BK3, BK4 và BK5 cho vết chính có vị trí tương ứng với vết nystose của dung dịch chuẩn.
- Dung dịch thử BK2, BK6 không cho vết chính tương ứng với vết nystose cho bởi dung dịch chuẩn (Mẫu BK2, BK6 được xác định không phải là Ba kích).
Như vậy, phương pháp TLC có tính đặc hiệu với nystose và phù hợp để định tính nystose trong dược liệu rễ Ba kích.
3.2. Chiết xuất, phân lập, tinh chế monotropein và nystose từ dược liệu rễ Ba kích
3.2.1. Chiết xuất cao chiết toàn phần chứa monotropein và nystose
Cho bột khô Ba kích lần lượt vào các bình thủy tinh (1kg/lần/bình), bổ sung MeOH theo tỷ lệ nguyên liệu/dung môi là 1/40 (khối lượng/thể tích), tiến hành chiết siêu âm ở nhiệt độ phòng, quá trình chiết siêu âm được lặp lại 3 lần, mỗi lần 1 giờ. Thu được dịch chiết MeOH và bã Ba kích.
- Dịch chiết MeOH được tiến hành lọc qua giấy lọc, gom lại dịch. Tiến hành cô quay chân không ở nhiệt độ 60 oC đến khi loại hết MeOH thu được cao chiết MeOH.
- Bã Ba kích ở trên được tiếp tục chiết với nước bằng đun hồi lưu trong 3 giờ. Gom dịch chiết, tiến hành cô quay chân không loại nước, sản phẩm thu được là cao nước Ba kích.
1 kg bột khô Ba kích thu được 300g cao chiết MeOH và 150 g cao chiết nước Qui trình chiết dịch chiết toàn phần MeOH và nước được mô tả theo Hình 3.6.
Bột khô Ba kích (1kg/lần)
Chiết siêu âm 3 lần bằng MeOH
ở nhiệt độ phòng trong 24 giờ
Dịch chiết MeOH
Cô quay duới áp suất giảm
Bã Ba kích
Đun hồi lưu bằng nước
trong 3 giờ
Cao chiết MeOH (300 g)
Dịch chiết nước
Cô quay duới áp suất giảm
Cao chiết nước (150 g)
Hình 3.6. Quy trình chiết xuất dịch chiết toàn phần
3.2.2. Phân lập và tinh chế monotropein
- Cao chiết MeOH (6000 g) được hòa với nước (80 lít), chiết phân đoạn lần lượt với n-hexan (40 lít x 3 lần) và ethyl acetat (40 lít x 3 lần) thu được các dịch chiết n- hexan và ethyl acetat, nước.
- Tiến hành sắc ký cột diaion HP-20 đối với dịch chiết nước, rửa giải bằng hệ dung môi gradient MeOH : nước (0 → 100% MeOH) thu được 3 phân đoạn kí hiệu A1, A2 và A3. Sử dụng phương pháp SKLM để kiểm tra sự có mặt của monotropein
trong 3 phân đoạn A1, A2, A3, kết quả phân đoạn A2 (tương ứng với hệ dung môi MeOH : nước theo tỷ lệ 25 : 75) có chứa monotropein.
- Phân đoạn A2 được triển khai sắc ký cột silica gel với hệ dung môi rửa giải dichlomethan – MeOH - nước theo tỷ lệ thể tích (2 : 1 : 0,1), hứng riêng từng phân đoạn vào các ống nghiệm đã đánh số thứ tự. Sử dụng phương pháp SKLM để kiểm tra sự có mặt của monotropein trong các phân đoạn, kết quả phân đoạn MO5.1 có chứa monotropein.
Phân đoạn MO5.1 được triển khai sắc ký cột pha đảo YMC-C18, dung môi rửa giải 100% nước. Cất cô quay chân không thu được sản phẩm MO6.2. Tiếp tục tiến hành sắc ký cột sephadex LH20 sản phẩm MO6.2, dung môi rửa giải 100% nước thu được hai phân đoạn MO7.1 và MO7.2. Sử dụng phương pháp SKLM để kiểm tra sự có mặt của monotropein trong phân đoạn MO7.2.
Tiến hành tinh chế phân đoạn MO7.2 bằng Hệ thống sắc ký lỏng bán điều chế theo điều kiện tại Mục 2.3.2.3, kết quả thu được 2,15 g sản phẩm. Kiểm tra phổ NMR (1H NMR, 13C NMR) và đo phổ khối ESI- sản phẩn thu được để xác định cấu trúc. Kết quả chất thu được có cấu trúc phù hợp với monotropein.
Qui trình phân lập và tinh chế monotropein từ cao chiết MeOH được thể hiện tại Hình 3.7.
Cao MeOH (6000g)
40 lít n-hexan × 3 lần
40 lít ethyl acetat x 3 lần
Sắc ký cột diaion HP20
Methanol – nước (25 : 75)
Sắc ký cột silica gel
Dichlomethan-MeOH-nước
![]()
MO5.1
Sắc ký cột YMC C18
100 % nước
MO6.2
Sắc ký lỏng bán điều chế, cột C18
Dung dịch chứa monotropein
Monotropein (2,15 g)
Dịch chiết n – hexan
Dịch nước
Dịch chiết ethyl acetat
Dịch nước
A2
MO7.2
Dịch nước
![]()
Sắc ký cột Sephadex LH20
Methanol – amoni acetat (gradient dung môi)
Cô bay hơi dung môi
80 lít nước
Hình 3.7. Sơ đồ phân lập, tinh chế monotropein từ cao chiết MeOH
3.2.3. Phân lập và tinh chế nystose
Cao chiết nước (250g) hòa trong 2,5 lít nước ấm, sau đó dịch chiết nước được triển khai lên cột diaion HP-20, rửa giải bằng hệ dung môi gradient MeOH : nước (0
→ 100 % MeOH) thu được 3 phân đoạn B1, B2 và B3 tương ứng với các tỷ lệ MeOH
: nước là (0 : 100), (25 :75) và (100 : 0). Kiểm tra sự có mặt của nystose bằng SKLM nhận thấy phân đoạn B2 có chứa nystose.
Phân đoạn B2 được cho lên cột chứa than hoạt tính, giải hấp phụ lần lượt bằng nước, EtOH 10 % và EtOH 20 % thu được các phân đoạn MO10.1, MO10.2 và MO10.3. Kiểm tra sự có mặt của nystose bằng SKLM nhận thấy dịch EtOH 20 % (tương ứng với MO10.3) có chứa nystose, cất loại dung môi thu được chất rắn MO10.3.
Hoà tan MO10.3 vào nước, triển khai sắc ký cột sephadex LH-20, rửa giải bằng hệ dung môi nước - MeOH với tỷ lệ thể tích (10 : 1) thu được 4 phân đoạn từ MO11.1
- MO11.4. Kiểm tra bằng SKLM xác định phân đoạn MO11.2 chứa nystose.
Phân đoạn MO11.2 được tinh chế bằng sắc ký cột silica gel với hệ dung môi isopropanol – EtOH - nước theo tỷ lệ thể tích (3:2:1). Dịch rửa giải được bổ sung thêm EtOH (1/5 thể tích) rồi để kết tinh qua đêm ở 4 ºC thu được sản phẩm kết tinh MO12.2.
Hòa tan MO12.2 và kết tinh lại 10 lần bằng EtOH 20 %.
Kết quả thu được 2,21 g sản phẩm. Tiến hành kiểm tra phổ NMR (1H NMR, 13C NMR) và đo phổ khối ESI+ cắn thu để xác định cấu trúc. Chất thu được có cấu trúc phù hợp với nystose.
Qui trình phân lập và tinh chế nystose từ cao chiết nước được thể hiện tại Hình
3.8.

![Nội Dung Thẩm Định Phương Pháp Định Lượng Nystose [52]](https://tailieuthamkhao.com/uploads/2024/04/20/nghien-cuu-nang-cap-tieu-chuan-duoc-lieu-re-ba-kich-radix-morindae-officinalis-7-120x90.jpg)