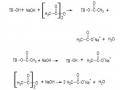hành phản ứng ở nhiệt độ cao hơn nhiệt độ hồ hoá c a tinh bột và khống chế một cách dễ dàng để tạo ra các sản phẩm có mạch phân tử như mong muốn với hiệu suất thu hồi cao. Bằng cách lựa chọn loại ancol, nồng độ axit, loại tinh bột và nồng độ tinh bột có thể tạo ra các dextrin có giá trị trùng hợp chọn lọc trong khoảng rộng [101-103].
Quá trình thuỷ phân tinh bột bằng axit trong môi trường ancol diễn ra theo mô hình 2 giai đoạn, giai đoạn đầu chậm và giai đoạn sau nhanh. Hiệu suất thu hồi đạt > 0% và kích thước hạt trung bình giảm nhẹ. Độ trùng hợp giảm dần khi tăng số nguyên tử cacbon c a ancol và sản phẩm có độ tan cao hơn gấp 4-9 lần so với tinh bột tự nhiên. Tinh bột sau khi xử lý axit trong ancol cho thấy những vết nứt bên trong hay những mao quản ở một số hạt, và số hạt bị nứt hoặc có mao quản tăng khi tăng số nguyên tử cacbon c a ancol. Mức độ phân huỷ c a phân tử sau khi xử lý axit trong ancol có liên hệ trực tiếp với sự luân phiên c a cấu trúc bên trong hạt tinh bột [104- 107].
Việc thuỷ phân tinh bột bằng axit trong môi trường ancol đã được Small đề xuất nhằm biến đổi các loại tinh bột tự nhiên thành dễ tan. Để so sánh ảnh hưởng c a các loại ancol khác nhau đến mức độ thuỷ phân tinh bột Robyt [98] đã thực hiện việc biến tính tinh bột ngô và khoai tây bằng axit HCl trong các môi trường ancol khác nhau là metanol, etanol, 2-propanol và 1-butanol. Kết quả nghiên cứu chỉ ra rằng cả hai loại tinh bột bị thuỷ phân mạnh nhất trong môi trường metanol, sau đó là etanol. Kết quả này được các tác giả giải thích là do
metanol có kích thước phân tử nhỏ hơn nên dễ khuếch tán và mang ion H+ vào
sâu trong mạch phân tử tinh bột hơn etanol. Kết quả là có nhiều ion H+ tấn công vào mạch tinh bột hơn do đó có khả năng phân cắt mạch tinh bột lớn hơn.
b. Tính chất của tinh bột biến tính bằng axit
- Việc sử lý tinh bột biến tính bằng axit làm thay đổi nhiều tính chất so với tinh bột chưa biến tính và có thêm những tính chất mới, chỉ còn giống tinh bột ban đầu ở hình dạng vật lý, không có sự thay đổi trực tiếp về dạng hạt mà chỉ có sự thay đổi nhỏ về tính lưỡng chiết hạt. Tinh bột biến tính bằng axit so với tinh
bột ban đầu có những tính chất như độ kết tinh tương đối, giảm ái lực ion, độ nhớt đặc trưng bé hơn, nhiệt độ hồ hoá cao hơn, áp suất thẩm thấu cao hơn do khối lượng phân tử bé hơn, khi hồ hoá trong nước nóng hạt trương nở kém hơn. Trong nước ấm có nhiệt độ thấp hơn nhiệt độ hồ hoá thì độ hoà tan cao hơn. Tinh bột biến tính bằng axit có sự thay đổi nhiều về tính chất so với tinh bột chưa biến tính và có thêm những đặc tính mới, chỉ còn giống tinh bột ban đầu ở hình dạng vật lí, chỉ có sự thay đổi nhỏ vềtính lưỡng chiết mà không có sự thay đổi trực tiếp về hình dạng hạt, chỉ có thay đổi nhỏ về tính lưỡng chiết hạt [140].
- Khi thuỷ phân bằng axit sẽ làm thay đổi độ kết tinh tương đối c a hạt tinh bột. Thông thường độ kết tinh tương đối trong các loại hạt tinh bột chiếm từ 15 đến 45% tuỳ thuộc vào nguồn gốc và loại tinh bột [15]. Kawaljit Singh Sandhu [ 2] đã nghiên cứu sự biến đổi độ kết tinh tương đối c a tinh bột khoai tây khi bị thuỷ phân bằng axit H2SO4 và phát hiện ra rằng độ kết tinh tương đối c a tinh bột biến tính cao hơn so với tinh bột khoai tây tự nhiên, sự tăng này tỷ lệ với mức độ thuỷ phân. Các kết quả tương tự cũng xuất hiện khi thuỷ phân tinh bột ngô, gạo, sắn bằng các loại axit khác nhau. Hầu hết các tác giả đều cho rằng tác nhân axit ưu tiên tấn công vào vùng vô định hình trước, sau đó mới đến vùng kết tinh làm cho tỷ lệ vùng vô định hình giảm dần và tăng độ kết tinh tương đối. Ngoài ra các phân tử tinh bột nằm ở vùng vô định hình sau khi bị phân cắt có khả năng kết hợp với nhau bằng các liên kết hidro và tạo thành dạng xoắn ốc, các vòng xoắn ốc này bó chặt với nhau và hình thành nên các vùng kết tinh mới [122].
- Tinh bột biến tinh bằng axit có sự thay đổi lớn về cấu trúc mạch tinh bột làm cho nhiệt độ hồ hoá bị thay đổi. Nói chung tinh bột nào có mức độ phân cắt cao hơn thì nhiệt độ hồ hoá cao hơn. Jacobs và các cộng sự [11 ] đã nghiên cứu quá trình chuyển nhiệt c a tinh bột khoai tây và tinh bột mì biến tính axit bằng máy phân tích nhiệt DSC. Kết quả cho thấy nhiệt độ đầu và nhiệt độ đỉnh c a tinh bột biến tính cao hơn so với tinh bột tự nhiên. Các kết quả tương tự cũng nhận được khi nghiên cứu tính chất nhiệt c a tinh bột lúa mạch [105], gạo [104],
ngô [102]. Sự tăng nhiệt độ hồ hoá này có thể là do sự tăng tỷ lệ vùng kết tinh trong hạt tinh bột sau khi bị thuỷ phân và vì vùng kết tinh có nhiệt độ nóng chảy cao hơn vùng vô định hình [122]. Ngoài ra cũng có thể nhận thấy rằng khi bị phân cắt thành các phân tử nhỏ, tuy mạch tinh bột ngắn hơn nhưng không đồng đều. Phân tử tinh bột biến tính có kích thước ngắn hơn nên dễ dàng sắp xếp chặt chẽ hơn làm cản trở quá trình hydrat hoá và trương nở c a tinh bột. Mặt khác cũng có thể lúc đó trong hạt mức độ trật tự c a các mixen đã tăng lên, các mạch tinh bột nằm trong vùng vô định hình bị thuỷ phân nên các mixen đó liên kết với nhau, tạo ra những mảng mạch khá lớn và vì vậy nhiệt độ hồ hoá tăng lên.
- Hình dạng cơ bản c a hạt tinh bột sau khi biến tính bằng axit có thể thay đổi phụ thuộc vào điều kiện thuỷ phân, kích thước có thể bị thay đổi và bề mặt sần sùi hơn. Các ion H+ xâm nhập vào vỏ nhờ khuếch tán và tiến hành phân cắt các phân tử tinh bột trong hạt, tạo ra những phân tử mạch ngắn hơn, nhưng số lượng phân tử mạch ngắn sẽ tăng làm tăng thể tích c a các vi hạt, do đó kích thước vi hạt tăng lên ở giai đoạn đầu trong toàn bộ mẫu. Tuy nhiên nếu quá trình thuỷ phân tiếp tục được duy trì cho đến khi toàn bộ lớp vỏ ngoài c a hạt tinh bột
bị thuỷ phân hết và các lớp tiếp theo bắt đầu bị thuỷ phân thì kích thước vi hạt tinh bột cũng bắt đầu giảm dần [123].
- Độ nhớt c a hồ tinh bột biến tính bằng axit giảm thấp. Sự giảm độ nhớt c a hồ tinh bột biến tính bằng axit là do phá huỷ vùng định hình giữa các mixen c a hạt và làm yếu cấu trúc c a hạt rồi dẫn đến sự phá huỷ hạt ngay cả khi hạt trương không đáng kể. Theo Mukerjea [107] nguyên nhân làm giảm độ nhớt c a hồ tinh bột là do độ hoà tan c a nó trong nước sôi rất lớn cũng có nghĩa là pha gián đoạn c a nó giảm đi. Pha gián đoạn là huyền phù c a các hạt đã trương và các mảnh vỡ c a chúng ở trong dung dịch nước c a các chất tinh bột (pha lỏng liên tục) chính pha gián đoạn này làm tăng độ nhớt hồ tinh bột [140].
- Chỉ số kiềm c a tinh bột biến tính bằng axit tăng lên. Chỉ số kiềm là lượng kiềm 0,1 M tiêu tốn để hoà tan 10 g tinh bột khô ở nhiệt độ sôi trong thời gian 1 giờ. Chỉ số kiềm có liên quan đến nhóm andehit. Khi kích thước phân tử
tinh bột nhỏ thì số lượng nhóm andehit tăng lên. Điều này phản ánh sự tăng chỉ số kiềm theo quá trình thuỷ phân hay sự tăng c a độ lỏng [108- 110].
- Tinh bột biến tính bằng phương pháp axit có độ bền màng cao. Vì vậy nó thích hợp trong việc ứng dụng đặc tính tạo gel, tạo màng cho sản phẩm. Độ bền gel c a tinh bột tăng lên bằng cách hiệu chỉnh điều kiện sản xuất. Vì vậy nếu dưới điều kiện thường mà sự biến đổi được tiến hành với H2SO4 0,1 N ở thời gian phản ứng thì sẽ tạo thành tinh bột biến tính có độ bền gel lớn [111, 112].
c. Ứng dụng làm tá dược trong dược phẩm
Các sản phẩm tinh bột biến tính trong dung dịch axit HCl được sử dụng làm tá dược trong dược phẩm, ngoài ra còn sử dụng rộng rãi trong công nghiệp thực phẩm, công nghiệp vải sợi và công nghiệp giấy [118].
Thời gian gần đây, các công ty dược rất trú trọng việc ứng dụng rộng rãi nhiều loại tinh bột biến tính khác nhau trong nhiều công đoạn c a công nghệ sản xuất thuốc viên và viên nang. Theo xu hướng này, lượng tinh bột biến tính được sử dụng trong công nghiệp dược phẩm làm thành phần bổ trợ cũng tăng lên. Các thành phần bổ trợ trong thuốc viên có tác dụng tạo cho hỗn hợp ban đầu có những tính năng công nghệ cần thiết để cung cấp một liều lượng chính xác, độ bền cơ học, đặc tính phân rã và sự ổn định cho các viên nén trong quá trình bảo quản. Tuỳ thuộc vào các mục đích sử dụng khác nhau, các thành phần bổ trợ lại được chia thành các nhóm nhỏ [120, 122] (bảng 1.3).
Phân tích số liệu trong bảng 1.3 cho thấy tinh bột nằm ở hầu hết các nhóm, do đó nó đóng một vai trò cực kỳ quan trọng trong ngành công nghiệp dược phẩm. Các loại tinh bột biến tính đang thu hút sự chú ý c a các nhà nghiên cứu để phát triển dược phẩm với thành phần và tính chất dược lý mới. Những lý do làm cho các loại tinh bột này được quan tâm như khả năng kết dính, làm trương, bôi trơn [12 ]. Xu hướng tăng việc chế tạo các loại thuốc viên, sự đa dạng về mặt cấu trúc và tính chất c a tinh bột được tạo ra từ nhiều loại nguyên liệu chưa tinh chế khác nhau, khả năng c a tinh bột tự nhiên và tinh bột biến tính
làm đậm đặc và ổn định nhiều thành phần c a thuốc, khả năng làm tăng các tính chất tạo gel và huyền phù c a tinh bột bằng các phương pháp biến tính trực tiếp. khả năng làm tăng tính bền c a thuốc trong điều kiện c a chu trình làm lạnh rồi làm tan, nhiệt độ cao và trong môi trường axit cao.
Bảng 1.3. Các thành phần tá dược cho thuốc viên
Thành phần | |
Kết dính | Tinh bột: bột sắn, khoai tây, bột ngô, bột gạo; nước cất, etanol, sirô, cacboxymetyl cenllulozo, gelatin, hidroxy metyl cenlulozo, PVP, PVA, axit algic |
Chất làm trương Chất tạo khí Chất làm ướt | Tinh bột: bột mì, khoai tây, bột ngô, bột gạo; pectin, gelatin, metyl cenlulozo, aga- aga. Natri hidrocacbonat trộn với axit xitric hoặc axit tactaric. Tinh bột: bột mì, khoai tây, bột ngô, bột gạo; đường glucozơ. |
Chất bôi trơn Chất chống dính Chất độn | Axit steric, canxi sterat, magie sterat. Tinh bột, đá tan, axit steric. Tinh bột, glucozơ, lactozơ, gelatin, cenlullozơ và dẫn xuất c a nó, dextrin, amylopectin, sorbitol, mannitol, pectin. |
Có thể bạn quan tâm!
-
 Một Số Phương Pháp Biến Tính Bằng Phương Pháp Vật Lý
Một Số Phương Pháp Biến Tính Bằng Phương Pháp Vật Lý -
 Nghiên cứu biến tính tinh bột bằng một số tác nhân hóa học và ứng dụng - 5
Nghiên cứu biến tính tinh bột bằng một số tác nhân hóa học và ứng dụng - 5 -
 Cơ Chế Thuỷ Phân Tinh Bột Bằng Axit
Cơ Chế Thuỷ Phân Tinh Bột Bằng Axit -
 Biến Tính Tinh Bột Bằng Axit Acrylic Và Cryla It
Biến Tính Tinh Bột Bằng Axit Acrylic Và Cryla It -
 Tình Hình Nghiên Cứu Biến Tính Tinh Bột Trong Nước
Tình Hình Nghiên Cứu Biến Tính Tinh Bột Trong Nước -
 Dụng Cụ, Thiết Bị Và Phương Pháp Nghiên Cứu
Dụng Cụ, Thiết Bị Và Phương Pháp Nghiên Cứu
Xem toàn bộ 190 trang tài liệu này.

Viên nén là dạng thuốc được sử dụng rộng rãi nhất do có nhiều ưu điểm. Tuy nhiên về mặt sinh dược học, viên nén là dạng thuốc có nhiều yếu tố tác động đến khả năng giải phóng dược chất trong quá trình bào chế từ khâu xây dựng công thức đến quá trình sản xuất. Viên nén thông dụng có thể chia làm hai loại gồm: có loại đòi hỏi rã và loại không đòi hỏi rã. Để giải phóng dược chất đa số viên nén thông thường đều đòi hỏi quá trình phản ánh cấu trúc vật lý c a viên, từ đó tạo ra các hạt hay tiểu phân gọi là quá trình rã. Đối với viên không đòi hỏi rã thường chứa dược chất và tá dược tan được hòa tan nhanh chóng trong miệng hoặc dịch tiêu hóa.
Quá trình giải phóng dược chất c a viên nén gồm: rã và giải phóng một phần dược chất, hòa tan dược chất vào môi trường dịch tiêu hóa, hấp thụ dược
chất qua màng vào hệ tuần hoàn. Trong quá trình rã, hòa tan và hấp thu, nếu quá trình nào diễn ra chậm nhất sẽ là bước giới hạn tốc độ hấp thu dược chất vào hệ tuần hoàn.
Thông thường, quá trình rã c a viên xảy ra đầu tiên và là một yếu tố tiền đề c a quá trình hòa tan và hấp thu dược chất. Điều này đặc biệt đúng với dược chất ít tan. Mức độ hòa tan dược chất từ viên nén nguyên vẹn thường rất ít do diện tích tiếp xúc c a dược chất với dịch tiêu hóa rất nhỏ. Qúa trình rã viên nén thành hạt sẽ làm tăng diện tích bề mặt tiếp xúc c a dược chất với môi trường hoà tan và do đó sẽ làm tăng tốc độ hòa tan dược chất [130,147].
1.4.3.6. Oxy h á tinh bột
Tinh bột oxy hoá được tổng hợp nhờ phản ứng c a tinh bột với một lượng nhất định tác nhân oxy hoá trong điều kiện nhiệt độ và pH được khống chế. Phương pháp oxy hoá và thu hồi sản phẩm cũng khác nhau khi sử dụng các chất oxy hoá khác nhau. ất nhiều tác nhân oxy hoá đã được sử dụng để oxy hoá tinh bột như periodat, axit chromic, kali pemanganat, nitơ dioxyt, hydropeoxyt, natri hypochlorit, hydrgen peroxyt...mỗi loại đều có ưu và nhược điểm riêng.
a. Oxy hoá bằng periodat
Ion periodat phản ứng với nhóm 2, -glycol c a tinh bột để bẻ gãy liên kết cacbon-cacbon với sự hình thành hai nhóm cacbonyl. Các nhóm cacbonyl có khả năng tạo cấu trúc hemiaxetal và các cấu trúc andehyt hydrate hoá khác nhau cả nội và ngoại phân tử.
Kết quả là tinh bột diandehyt không cho dải hấp thụ cacbonyl trong vùng hồng ngoại. Các nhóm cuối D-glucozơ c a tinh bột chứa nhiều hơn một nhóm - glycol và quá trình oxy hoá periodat thu được 2 mol axit formic và 1 mol focmandehyt từ nhóm cuối khử và thêm một mol axit formic từ nhóm cuối không khử.
Định lượng axit formic sinh ra là một phương pháp ước lượng độ trùng hợp trung bình c a tinh bột.
Quá trình oxy hoá -glycol bằng periodat diễn ra theo cơ chế este vòng. Gần đây một phương pháp đã được phát triển để phân loại các kiểu nhóm cacbonyl khác nhau trong xenlulozơ oxy hoá theo tốc độ oxy hoá c a chúng. Periodat oxyxenlulozơ chứa 6 loại nhóm cacbonyl khác nhau, áp dụng phương pháp này cho diandehyt tinh bột làm sáng tỏ cấu trúc tinh vi c a nó [15 , 15].
b. Oxy hoá bằng axit cromic
Oxy hoá tinh bột bằng anhydrit cromic trong hệ không dung dịch hoặc trong axit sunfuric 0,2M làm xuất hiện các nhóm cacboxyl, xeton, andehyt. Tuy nhiên, kali dicromat ở pH = 0,7 cho sản phẩm chứa 60% nhóm 2, -diandehyt và chỉ 4-5% nhóm cacboxyl. Các kết quả này phù hợp với cơ chế được chấp nhận gần đây khi oxy hoá bằng axit cromic, một trong những cơ chế đầu tiên được giải thích.
Trong dung dịch loãng ion dicromat bị thuỷ phân thành ion cromat axit. Cr2O72- + H2O 2HCrO42- (29)
Khi có mặt axit, các nhóm glycol phản ứng với cromat để tạo ra một este
vòng, tương tự như đối với periodat. Giống như este periodat, este cromat phân huỷ để cho hai nhóm cacbonyl – andehyt trên tinh bột. Các nhóm cacboxyl được tạo ra bởi quá trình oxy hoá các nhóm andehyt.
Tuy nhiên, axit cromic có thể tạo ra este không vòng với ancol sau đó phân huỷ để cho các nhóm cacbonyl.Mặt khác, periodat, mặc dù có thể tạo este không vòng, lại không thể nhận ion trong bước phân huỷ este cần thiết cho qúa trình oxy hoá ancol thông thường [15].
c. Oxy hoá bằng permanganat
Hiệu quả tác dụng c a permanganat lên tinh bột được biết đến. Các nhóm cacbonyl và cacboxyl được tạo ra với tốc độ lớn nhất ở pH 10 và có thể lớn nhất ở pH = 1.
Cơ chế thích hợp nhất cho quá trình oxy hoá các nhóm ancol bằng permanganat trong môi trường kiềm liên quan đến việc tách một nguyên tử
hydro khỏi anion ancol, mặc dù chuyển ion hydrua từ anion cũng là một khả năng thuyết phục [15].
d. Oxy hoá bằng nitơdioxyt
Nitơ dioxyt (N2O4) oxy hoá nhóm ancol bậc 1 C-6 c a tinh bột thành cacboxyl với đặc trưng riêng để sau khi thuỷ phân thu được 26% sản phẩm là lactone axit D-glucuronic kết tinh. Quá trình oxy hoá có thể bị ảnh hưởng bởi hơi N2O4, dung dịch N2O4 trong carbon tetraclorua hoặc axit nitric chứa nitrit bổ sung. Mặc dù nitơ dioxyt được đưa vào olefin theo cơ chế gốc tự do, sự có mặt c a nitơ liên kết trong giai đoạn đầu c a quá trình oxy hoá xenlulozơ bằng hơi N2O4 chứng tỏ sự hình thành nitrit este qua ion nitroso (NO+).
N2O4 NO+ + NO3-
hay HNO3 + HONO NO+ + H2O + NO3-
TB -CH2OH + NO+ TB -CH2ONO + H+ (30)
Ankyl nitrit trải qua giai đoạn sự phân huỷ nhiệt để thu được andehyt và chắc chắn là tiếp tục oxy hoá andehyt này để thu được axit cacboxylic.
Nếu quá trình oxy hoá diễn ra qua một este trung gian phản ứng c a cả nitrit hoặc nitrat ở các nhóm hydroxyl bậc 2 cũng có thể xảy ra, ảnh hưởng c a natri bohydrua lên nitơ dioxyt oxy tinh bột chứng tỏ sự có mặt c a các nhóm 2- hoặc 3-keton [15].
e. Oxy hóa bằng hypoclorit
So với các phưong pháp phân huỷ tinh bột ở trên phưong pháp ôxi hoá tinh bột bằng natri hypoclorit là quá trình phổ biến nhất, cho sản phẩm có khối lượng nhỏ hơn, kích thước mạch ngắn hơn các hạt đồng đều, tạo điều kiện tốt cho quá trình biến tính bằng các tác nhân hoá học. Phản ứng thường tiến hành bằng phưong pháp huyền phù, môi trường là dung dịch natri hypoclorit và các hạt phân tán là tinh bột. Kết thúc phản ứng tinh bột được rửa rồi làm khô. Tính chất c a sản phẩm được quyết định bởi điều kiện c a phản ứng [132, 133] .