VITAMIN B6
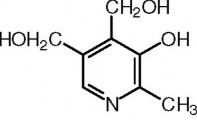
Tên khoa học: dạng pyridoxol = (5=hydroxyl-6-metylpyridin-3,4-diyl) dimethanol.
Tên khác: pyridoxine
Nguồn gốc:
Thực vật: trong mầm ngủ cốc, rau cải xanh, trái cây
Động vật: Thịt, sữa, gan, thận, long đỏ trứng.
Cấu trúc
Vitamin B6 dẫn xuất có cấu trúc pyridoxin là pyridin.
Có thể bạn quan tâm!
-
 Trình Bày Được Liên Quan Giữa Cấu Trúc Và Tác Động Của Các Vitamin.
Trình Bày Được Liên Quan Giữa Cấu Trúc Và Tác Động Của Các Vitamin. -
 Hóa dược trường CĐ phương đông Đà Nẵng - 33
Hóa dược trường CĐ phương đông Đà Nẵng - 33 -
 Hóa dược trường CĐ phương đông Đà Nẵng - 34
Hóa dược trường CĐ phương đông Đà Nẵng - 34 -
 Hóa dược trường CĐ phương đông Đà Nẵng - 36
Hóa dược trường CĐ phương đông Đà Nẵng - 36
Xem toàn bộ 293 trang tài liệu này.
Cả ba dạng pyridoxol, pyridoxal và pyridoxamin có tác dụng tương đương.
Tính chất

Bột kết tinh trắng. Dễ tan trong nước, tan được trong alcol, thực tế không tan trong ether.
Nhân pyridin:
Làm cho vitamin có tính base, tính chất này được ứng dụng trong sản xuất nguyên liệu, kiểm nghiệm:
- Có thể tạo muối với các acid: với hydrochloric tạo muối hydrcloric dễ tan là dạng dược dụng, với acid silico-vonframic, phosphovonframic, sulfuric tạo kết tủa có thể áp dụng để định lượng.
- Có thể định lượng bằng acid trong môi trường khan.
Nhóm –OH ở vị trí 3:
Tác dụng với các muối diazoni tạo phẩm màu azoic, tuy nhiên màu không bền nên chỉ được dùng để định tính, còn muốn để định lượng thì phải cho thêm các ion kim loại thích hợp để tạo ra phức chất kim loại có màu vững bền. Thí dụ: tác dụng với muối diazoni của sulfathiazole trong môi trường ethanol – nước, pH 6,5 – 7 có thêm kẽm clorid:
- Pyridoxol cho màu đỏ tím.
270
- Pyridoxal cho màu vàng da cam
- Pyridoxamin cho màu đỏ vững bền
Phản ứng này có thể dùng để định tính, phân biệt các pyridoxine, định lượng bằng phương pháp đo màu.
- Do nhóm –OH ở vị trí 3 và nhóm hydroxylmetyl ở vị trí 4: Chỉ có pyridoxin tạo ester vững bền với acid boric, pyridoxal và pyridoxamin thì không. Phản ứng này được dùng để phân biệt pyridoxol với hai chất kia.
- Do nhóm hydroxymetyl ở vị trí 5: ester hóa acid phosphoric tạo ra coenzyme của các men chuyển vận nitơ: transaminase.
- Do có H ở vị trí 6: Tác dụng với 2,6-dicloroquinon clorimid cho màu xanh.
Kiểm nghiệm:
Định tính:
Phổ IR, phản ứng của ion clorid, phổ UV, sắc ký lớp mỏng, phản ứng của kẽm clorid.
Thử tinh khiết
pH, tạp chất liên quan, kim loại nặng, giảm khối lượng do sấy, tro sulfat.
Định lượng
Phương pháp môi trường khan.
Tương kỵ lý hóa
Khoảng bền vững: pH: 3 – 4. Tương kỵ với các dung dịch tiêm: kiềm, trung tính.
Tác dụng
Pyridoxol là yếu tố chống đau dây thần kinh đầu chi (anti-acrodynie). Pyridoxal ảnh hưởng đến da và màng nhầy: chống tăng sừng, tiết bã nhờn.
Pyridoxamin là coenzyme trong nhiều phản ứng và có liên quan đến acid amin có lưu huỳnh và có nhóm hydroxyl như decarboxyl hóa, transamin hóa, racemin hóa.
Thiếu vitamin thường kéo theo thiếu máu tiểu hồng cầu, các rối loạn về thần kinh (co giật, viêm đa thần kinh).
Nhu cầu hàng ngày: 0,6 – 1,6mg ở trẻ em; 2mg ở người lớn; 2,5mg ở phụ nữ có thai và cho con bú.
271
Chỉ định:
Điều trị chứng thiếu vitamin B: người nghiên rượu, suy thận phải thẩm phân.
Tương tác thuốc
Vitamin ức chế tác động của levodopa cho nên không được phối hợp với thuốc này
Các chất làm gia tăng nhu cầu về vitamin B6: I.N.H., dihydralazin, thuốc ngừa thai, cycloserrin.
Dạng dùng:
Viên nén 250mg, ống tiêm 250mg/ml
Liều dùng
Uống 5-10mg/ ngày cho trẻ sơ sinh, 600mg/ ngày cho người lớn Tiêm bắp hoặc tiêm tĩnh mạch: 100 – 750mg/ ngày.
VITAMIN B9
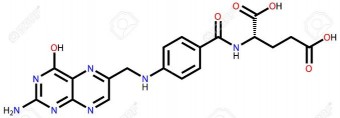
Tên khoa học: (2S)-2-[[4-[[(2amino-4-oxo-1,4-dihydropteridin-6-yl) methyl] amino]- benzoyl] amino]pentanedioic acid.
Tên khác: acid folic, hay pteroylglutamic
Liên quan cấu trúc – tác dụng:
Acid folic gồm: một phân tử pteroic (gồm hai vòng tương ứng với ptein gắn với acid para aminobenzoic) nối với chức amin của acid glutamic bằng liên kết peptid – RCO.NH-R’
Ở trạng thái thiên nhiên hay trong môi trường sinh học, acid folic hiện diện dưới dạng polyglutamat trong đó acid pteroic liên kết với nhiều phân tử acid glutamic. Do đó có thể nói rằng acid glutamic là cần thiết cho hoạt tính vitamin.
Trong các polyglutamat thì có 3 dạng acid glutamic (acid pteroyl-triglutamic) và acid glutamic (acid pteroyl-heptaglutamic) là dạng có hoạt tính sinh học nhưng phải được thủy phân trước khi hấp thu.
272
Nếu thay acid glutamic bằng acid aspartic (có ít hơn acid glutamic 1 nhóm –CH2-) thì được antivitamin.
Tính chất
Bột kết tinh vàng nhạt hoặc cam, thực tế không tan trong nước và phần lớn các dung môi trong hữu cơ. Acid folic tan trong acid loãng và trong dung dịch kiềm.
Dạng kết tinh bền với nhiệt, không khí trong môi trường trung tính hay kiềm, không bền trong môi trường acid, ánh sáng và tia UV.
Phổ hấp thu đặc trưng phụ thuộc pH của dung dịch và có cực đại trong vùng UV. Phổ hấp thu dặc trưng phụ thuộc pH của dung dịch và có cực đại trong vùng UV. Kiểm nghiệm
Định tính
Năng suất quay cực, phổ UV, sắc ký lớp mỏng
Thử tinh khiết
Amin tự do, nước, tro sulfat
Định lượng
Phương pháp phổ UV
Tác dụng
Acid folic có vai trò như một enzyme trong quá trình tổng hợp acid nucleic, purin của hồng cầu.
Chỉ định
Thiếu máu hồng cầu to do thiếu acid folic
Cung cấp acid folic khi điều trị bằng các thuốc làm giảm acid folic như pyrimethamin, trimethoprim, phenytoin, barbituric, sulfasalazine…
Tương tác thuốc
Acid folic làm giảm nồng độ của bacbituric và phenytoin trong máu khi dung đồng thời.
Liều dùng
Người lớn: 5-15mg/ ngày, trẻ em 5-10mg/ ngày, trẻ sơ sinh 2,5-5mg/ ngày.
Thận trọng khi dùng
273
Không được dùng acid folic riêng rẽ khi bị thiếu máu do bị thiếu vitamin hoặc do thiếu folic lẫn B12 vì acid folic sẽ làm thiếu hụt trầm trọng vitamin B12 dự trữ trong cơ thể, trong trường hợp này người ta dùng đồng thời acid folic và B12 hoặc cho bệnh nhân dùng B12 trước vài ngày.
VITAMIN B12
Vitamin B12 là tên chung của một số chất có cấu trúc hóa học và hoạt tính tương tự nhau. Dẫn chất thông dụng nhất là cyanocobalamin và hydroxocobalamin.
Tên khoa học: cyanocobalamin=α – (5,6-dimetylbenzimidazol-1-yl) cabalamin cyanid.
Nguồn gốc
Chỉ có động vật trong thịt, sữa.
Điều chế
Cyanocobalamin: lên men vi khuẩn Streptomyces friseus với các chất để hướng quá trình tổng hợp ra vitamin B12 thô rồi tinh chế bằng cách sắc ký.
Hydroxocobalamin: chuyển đổi giữa hydroxocobalamin và cyanocobalamin
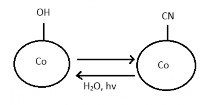
Tính chất
Tinh thể hoặc bột kết tinh màu đỏ đậm, rất dễ hút ẩm, có thể đến 12% khối lượng nếu tiếp xúc với không khí. Phân hủy ở trên 300 độ C, tan trong nước, ether và alcol, thực tế không tan trong aceton và chloroform.
Sự hiện diện của Co: vô cơ hóa bằng K2SO4 tạo thành CoSO4 cho màu xanh lơ với amoni cyanat.
Do base dimethyl-5,6-benzimidazol: cho sản phẩm phân hủy là dimethyl ortophenylen diamin, chất này ngưng tụ với acetylaceton tạo màu đỏ tía.
Do hệ thống nối đôi liên hợp , có chứa Co: vitamin B12 hấp thu mạnh bức xạ UV và khả kiến, có thể áp dụng tính chất này để định tính và định lượng.
Kiểm nghiệm
Định tính
274
Phổ UV, sắc ký lớp mỏng.
Thử tinh khiết
Tạp chất liên quan, giảm khối lượng do sấy.
Định lượng
Phương pháp phổ UV, đo ở 360nm
Tác dụng
Chống thiếu máu: vitamin B12 là yếu tố căn bản cho sự kích thích tạo máu cho nên thiếu vitamin này sẽ tăng dần dẫn đến thiếu máu.
Tác động lên sự tăng trưởng: là yếu tố tăng trưởng và đồng hóa protein, tổng hợp AND ở các mô phân chia (ruột non, mô tạo máu).
Tác động hướng thần kinh: có vai trò trong sự chuyển hóa nơron (không tạo được myelin), nếu thiếu sẽ xuất hiện các rối loạn về thần kinh.
Nhu cầu hằng ngày: Trẻ em 1-3µg, người lớn 3µg, phụ nữ có thai và cho con bú 4µg.
Chỉ định-liều dùng
Trị thiếu máu do thiếu vitamin B12 do không được cung cấp đầy đủ, thiếu máu hồng cầu to, hấp thu kém do thiếu yếu tố nội tại để hấp thu (bệnh thiếu máu Biermer).
Đường tiêm hữu hiệu hơn đường uống 50 lần. Chỉ được tiêm bắp.
Tác dụng phụ
Phản ứng dị ứng: ngứa, đỏ da, mề đay.
Đau nơi tiêm, nước tiểu có màu đỏ do thải qua đường này khi dùng liều cao.
Chống chỉ định
Bị dị ứng với cobaqlamin, khối u ác tính (do vitamin B12 có ảnh hưởng đến sự phân chia tế bào và phát triển của mô).
Dạng dùng
Viên nén 250mcg, ống tiêm 1mg, 10mg.
VITAMIN C
275
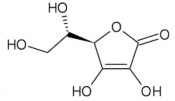
Tên khoa học: (R)-3,4-dihydroxy-5-(S)-1,2-dihydroxyethyl)furan-2(5H)-one
Tên khác: acid ascorbic
Nguồn gốc
Chủ yếu ở thực vật: trái xanh, xà lách, chanh, cam, chuối, đậu ve, sữa, yaourt…
Liên quan cấu trúc – tác dụng
Cấu trúc:
- Nhân furan, vòng 5 cạnh có dị tố õy
- Cầu oxyd giữa carbon 1 với 4
- Nhóm endiol ở vị trí 2 và 3
- Dây nhánh mang nhóm alcol ở vị trí 5 và alcol bậc I ở vị trí 6
- Hai carbon bất đối xứng C4 và C5
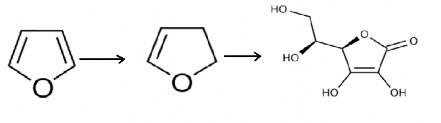
Furan dihydrofuran acid ascorbic
Liên quan cấu trúc – tác dụng:
- Dạng đồn phân: vitamin C là dạng acid L-ascorbic, dạng D không có hoạt tính.
- Nhân furan có gắn nhóm thế thì bị giảm hoặc mất tác động.
- Dây nhánh: thay 1 trong 2 nhóm alcol bậc 1 (vị trí 6) hoặc bậc II (vị trí 5) bằng nhóm methyl, vẫn giữ hoạt tính.
Nhóm dienol cần thiết để có hoạt tính nhưng không phải là quan trọng nhất.
276
Tính chất
Tinh thể không màu hoặc bột kết tinh trắng, màu sẫm dần khi để ngoài không khí ẩm. Dễ tan trong nước, tan trong alcol, thực tế không tan trong ether.
Nhiệt độ nóng chảy là 1900C kèm theo phân hủy.
Hấp thu bức xạ UV
Do nhóm endiol liên hợp với nhóm carbonyl nên acid ascorbic có thể được định tính bằng cách đo dung dịch này ở nồng độ 0,001% trong acid hydrocloric 0,01N cực đại hấp thu 243nm với A( 1%, 1cm) từ 545 đến 585nm.
Tính acid
Acid ascorbic được xem như một acid mạnh mặc dù không chứa nhóm –COOH. Kim loại Na có thể thế vào hydro ở vị trí 3 (nhóm endiol) rồi hỗ biến.
Tính khử
Oxy hóa-khử thuận nghịch: tính chất này rất quan trọng đối với tác dụng sinh học của acid ascorbic, nó có thể cho 2 nguyên tử hydro để trở thành acid dehydroascorbic, ở dạng này có thể nhận lại 2 hydro để trở lại acid ascorbic.
Như vậy acid ascorbic tham gia vận chuyển hydro, tức là tham gia vào các hệ thống xúc tác quá trình oxy hóa – khử xảy ra trong cơ thể.
Oxy hóa – khử không thuận nghịch tạo ra acid 2,3-dicetogulonic, furfurol, CO2, nước.
Nếu không có chất oxy hóa thì acid ascorbic bền vững. Ở dạng dung dịch, khi có mặt không khí thì acid ascorbic dễ bị oxy hóa. Các tác nhân xúc tác sự oxy hóa là ánh sáng, nhiệt độ, chất kiềm, vết đồng, sắt, các enzyme.
Acid ascorbic có thể khử thuốc thử Fehling, bạc nitrat, 2,6-diclorophenol indophenol. Làm mất màu iod.
Kiểm nghiệm
Định tính
Phổ IR, phổ UV, phản ứng với bạc nitrat
Thử tinh khiết
Năng suất quay cực, acid oxalic, đồng, kim loại nặng, tro sulfat.
Định lượng
Phương pháp iod
277