tự nhiên của cơ thể (serotonin) là nguyên nhân chính gây nôn mửa. Bên cạnh đó, indole còn là khung cấu trúc của indigo, một loại phẩm nhuộm được sử dụng trong ngành dệt nhuộm, có trong nhựa của cây chàm Indigofera tinctoria, Poligonum tinctorium, Isatis tinctoria… Cấu tạo của indigo được công bố xác định năm 1880, không lâu sau đó thì nó được tổng hợp thành công, indigo là sản phẩm oxi hoá của indole bằng oxigen không khí [58] (hình 1.4).
1.3.2. Tình hình nghiên cứu về hoạt tính gây độc tế bào ung thư của các hợp chất có khung indole
Pei-Liang-Zhao (2015) đã tổng hợp 19 dẫn xuất aminopyrimidine ghép với piperazine ở vị trí số 3 trên khung indole và đánh giá hoạt tính của chúng trên các dòng tế bào ung thư HT-29 – tế bào ung thư ruột kết ở người, A549, MDA-MB-231 và MCF-7. Kết quả cho thấy với các yếu tố sau trong cấu trúc: nguyên tử hydro ở vị trí N-1 được giữ nguyên, vị trí C-2 là một nhóm carbonyl đính kèm vòng thiophene, vị trí C-3 là sự lai ghép giữa pyrimidine và 1-methylpiperazine gắn với C-3 thông qua nhóm amin, vị trí C-6 là một nhóm halogen; thì kết quả thu được dẫn xuất 34 ức chế tốt trên cả 4 dòng tế bào thử nghiệm với IC50 lần lượt là 5,56; 14,36; 5,01 và 13,93
µM [59].
Hai-Liang Zhu (2016) đã nghiên cứu SAR của một chuỗi các dẫn xuất 1- methyl-1H-indole-pyrazoline ở vị trí số 3 trên 4 dòng tế bào ung thư HeLa, MCF-7, A549 và Hep G2. Trong đó dẫn xuất e19 có IC50 ấn tượng trên cả 4 dòng tế bào thử nghiệm, lần lượt là 0,21; 0,29; 0,26 và 0,31 µM. Nghiên cứu cấu trúc của chuỗi 28 dẫn xuất tổng hợp, tác giả đề xuất vị trí số 5 nên là nguyên tử Br, gắn ở vị trí 3’ là vòng phenyl chứa 3 nhóm methoxy [60].
Có thể bạn quan tâm!
-
 Nghiên cứu tổng hợp và đánh giá hoạt tính gây độc tế bào các dẫn xuất của benzimidazole và indole - 2
Nghiên cứu tổng hợp và đánh giá hoạt tính gây độc tế bào các dẫn xuất của benzimidazole và indole - 2 -
 Một Số Thuốc Điều Trị Ung Thư Chứa Khung Benzimidazole
Một Số Thuốc Điều Trị Ung Thư Chứa Khung Benzimidazole -
 Cấu Trúc Của Các Dẫn Xuất Benzimidazole- 1,3,4-Oxadiazole
Cấu Trúc Của Các Dẫn Xuất Benzimidazole- 1,3,4-Oxadiazole -
 Phép Tam Giác Phân Đặt Ligand Vào Điểm Gắn Kết Của Protein
Phép Tam Giác Phân Đặt Ligand Vào Điểm Gắn Kết Của Protein -
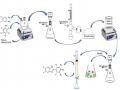
 Các Dụng Cụ Và Thiết Bị Sử Dụng Trong Tổng Hợp
Các Dụng Cụ Và Thiết Bị Sử Dụng Trong Tổng Hợp -
 Các Bước Tổng Hợp Các Dẫn Xuất 3-Aminoalkylated Indole
Các Bước Tổng Hợp Các Dẫn Xuất 3-Aminoalkylated Indole
Xem toàn bộ 186 trang tài liệu này.
Ahmed Kamal (2017) sử dụng curcumin ghép với indole ở vị trí số 3 nhằm tăng cường hoạt tính kháng ung thư của các dẫn xuất thu được, các dòng tế bào được sử dụng trong nghiên cứu này là A549, MDA-MB-231, BT-549 – tế bào ung thư vú ở người, 4T1- tế bào ung thư tuyến vú giai đoạn 4 ở chuột, PC3 – tế bào ung thư tuyến tiền liệt ở người, DU-145, HGC-27- tế bào ung thư dạ dày ở người và HeLa. Để tìm hiểu SAR, nhóm tác giả đã thay các nhóm thế khác nhau, kết quả cho thấy tác giả đề xuất vị trí N-1 không nên chứa nhóm thế thì hoạt tính sẽ tốt hơn khi xuất hiện nhóm thế, vòng phenyl trên khung lai ghép với curcumin nên là các nhóm đẩy điện tử như methoxy. Trong đó hợp chất 11c và 11f thể hiện hoạt tính ức chế tốt trên các dòng tế bào thử nghiệm với IC50 = 5,21-18,96 µM (11c) và 3,15-11,44 µM (11f) [61].

![]()
![]()
Guangsen Xu (2017) đã đánh giá hoạt tính ức chế dòng tế bào ung thư MDA- MB-231, hợp chất 9c, 9d và 9h – chứa đồng thời nhóm chức ở cả ba vị trí 1, 2 và 3 – có chỉ số IC50 tương ứng là 33,55; 38,62 và 42,06 µM. Từ các chỉ số IC50 thu được, các hợp chất này được dự đoán là có tiềm năng làm chất kháng ung thư mới [62].
HN O HN O
O HN O O S
O HN O O S
CH3
N
CH3
N NO2
O CH3 Cl
9c 9d 9h
Dựa vào các nghiên cứu trên cho thấy, các dẫn xuất indole có hoạt tính ức chế tế bào ung thư tốt nhất trên 3 dòng A549, MDA-MB-231 và PC3 có các đặc điểm chung là: vị trí số 1 được giữ nguyên nguyên tử H; vị trí số 3 trên khung indole thường là các nhóm thế lớn chứa vòng phenyl thế, các dị vòng no hoặc các mạch alkyl hoặc nhóm amine; vị trí số 5 và 6 là các nhóm thế nhỏ, thường là nguyên tử halogen hoặc không chứa nhóm thế. Do đó, nghiên cứu tập trung vào sự ảnh hưởng do biến đổi các nhóm chức cùng lúc ở các vị trí C-2, C-3 và C-5 đến hoạt tính kháng tế bào ung thư ở các dẫn xuất indole thu được. Ngoài ra, các nhóm chức được lựa chọn trong nghiên cứu là các nhóm chức phổ biến có mặt trong các phân tử có hoạt tính sinh học (ether, amine bậc 3, các halogen, alcohol, phenol…) [44], kết hợp với điều kiện thực tế, các nhóm thế khác nhau như: OCH3, N(CH3)2, CF3, I, Cl, OH, NO2, O-CH2-Ph, CH3 đã được sử dụng để đưa vào các cấu trúc indole trong nghiên cứu này.
1.3.3. Một số phương pháp tổng hợp các dẫn xuất indole
1.3.3.1. Phản ứng đóng vòng indole
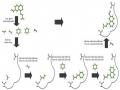
Phản ứng đóng vòng indole được chia làm hai loại: một loại sử dụng xúc tác là các kim loại chuyển tiếp (sơ đồ 1.6) và một loại cổ điển không sử dụng xúc tác (sơ đồ 1.7) [63]. Hai loại phản ứng đóng vòng này đều có khả năng tạo các dẫn xuất indole thế ở vị trí 2 và 3.
Sơ đồ 1.6. Các phản ứng đóng vòng indole sử dụng xúc tác kim loại chuyển tiếp
Sơ đồ 1.7. Các phản ứng đóng vòng indole cổ điển không sử dụng xúc tác kim loại chuyển tiếp
Mặc dù các điều kiện, tác nhân phản ứng đã được cải tiến, tuy nhiên tác chất ban đầu của các phản ứng đóng vòng indole vừa nêu thường không có sẵn hoặc không có lợi về mặt kinh tế để có thể dễ dàng sử dụng và tổng hợp một chuỗi các dẫn xuất indole thế ở vị trí 2 và 3, do đó cần có một phương án khác để tạo dẫn xuất thế indole này. Có thể thấy rằng, indole được ngưng tụ từ một vòng benzene và một vòng pyrrole, do đó nó có đầy đủ tính chất của một hợp chất hydrocarbon thơm và tính chất của một hợp chất chứa dị vòng nitơ như: tham gia phản ứng thế ái điện tử ở các vị trí CH trên hệ vòng indole, phản ứng thế nguyên tử hydro tại vị trí N-H, phản ứng oxy hóa và phản ứng khử trong vòng indole. Tuy nhiên, vị trí C-3 có khả năng phản ứng thế với các tác nhân electrophin cao hơn các vị trí khác trong vòng benzene, vì vậy phản ứng với các tác nhân electrophin xảy ra ở phía dị vòng pyrrole, với sự ưu tiên vào vị trí 3 (trạng thái (1)) vì tạo sản phẩm trung gian bền hơn (trạng thái (2)) [55].
N
N
H H
E
E
H (1)
H
(2)
Từ những lý do nêu trên, nhóm nghiên cứu quyết định tổng hợp các dẫn xuất indole bằng phản ứng thế vào vị trí số 3 trên khung indole bằng các tác nhân khác nhau, ngoài ra, với mục tiêu tìm kiếm các tác nhân indole mới ức chế tế bào ung thư, phản ứng đa hợp phần là một đối tượng nghiên cứu tiềm năng, khả thi để hoàn thành mục tiêu này.
1.3.3.2. Phản ứng đa hợp phần và phản ứng Mannich trên khung indole
a) Phản ứng đa hợp phần và phản ứng Mannich
Phản ứng đa hợp phần là phản ứng có từ 3 hoặc lớn hơn 3 tác chất phản ứng ban đầu hình thành được 1 sản phẩm duy nhất sau phản ứng, hoặc có hơn 2 tác chất ban đầu kết hợp tuần tự nhau để cho ra sản phẩm có độ chọn lọc cao và giữ được phần lớn các nguyên tử có mặt trong nguyên liệu ban đầu [64]. Trong những năm gần đây, phản ứng đa hợp phần (Multicomponent reactions – MCRs) đã thu hút sự quan tâm của nhiều nhà hóa học do khả năng tạo ra được sản phẩm đa dạng và phức tạp chỉ trong một lần phản ứng (one-pot) [65, 66]. MCRs còn nhận được sự yêu thích của nhiều nhà khoa học ở những lĩnh vực đòi hỏi phải luôn tìm tòi ra những cấu trúc chất mới có hoạt tính tốt hơn các cấu trúc chất ở thế hệ trước đó, nhưng lại không tốn nhiều chi phí và thời gian cũng như nhiều bước phản ứng, đặc biệt là không cần thiết
24
sử dụng phương án bảo vệ và giải bảo vệ nhóm chức thường phải sử dụng trong tổng hợp hữu cơ [66]. Ngoài ra với tính chọn lọc hóa học và chọn lọc lập thể cao, MCRs rất được chú ý trong tổng hợp dị vòng [67].
Trong số đó, phản ứng Mannich là một phản ứng hữu cơ quan trọng được sử dụng khá phổ biến trong việc hình thành liên kết C-C và C-N [68]. Sản phẩm cuối của nó thông thường là các base Mannich hoàn toàn mới [68, 69]. Phản ứng Mannich là phản ứng ngưng tụ giữa hợp chất chứa H linh động với aldehyde và amine, sẽ tạo nên hợp chất chứa aminomethyl được gọi là base Mannich [70]. Môi trường của phản ứng đa số là acid, vì thế sản phẩm tạo là muối của amine. Trong phản ứng Mannich, các hợp chất chứa C-H linh động khác nhau phản ứng với các amine khác nhau và các aldehyde khác nhau, vì thế chúng tạo ra một số lượng lớn các hợp chất hữu cơ. Chính vì thế phản ứng Mannich được sử dụng trong công nghiệp tổng hợp hữu cơ và trong công nghiệp hoá dược [69].
Cơ chế của phản ứng [70]: phản ứng thường xảy ra trong môi trường acid, các amine tự do phản ứng với các aldehyde tạo ra các dẫn xuất hydroxymethylamine, sau đó nhận thêm proton và tách ra một phân tử nước để hình thành nên cation aminomethyl hay còn gọi là iminium ion:
Các iminium ion này phản ứng với dạng enol của các hợp chất chứa liên kết C-H hoạt động (trường hợp hợp chất có H linh động nằm bên cạnh nhóm carbonyl của phân tử). Liên kết đôi C=C của dạng enol như một tác nhân nucleophile tấn công vào iminium ion để tạo ra hợp chất chứa nhóm aminomethyl (base Mannich).
![]()
![]()
![]()
![]()
Sơ đồ 1.8. Cơ chế của phản ứng Mannich
b) Phản ứng Mannich trên khung indole
25
![]()
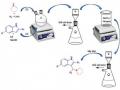
Nhóm nghiên cứu của Shchekotikhin (2005) sử dụng phản ứng Mannich ba hợp phần bao gồm dẫn xuất indole, formaldehyde, piperazine/1-methylpiperazine trong môi trường AcOH ở 60 °C để tạo ra sản phẩm 3-aminomethyl 6 và 7 trong chuỗi phản ứng [71].
Sơ đồ 1.9. Tổng hợp các dẫn xuất 3-aminomethyl indole
Kumar và các cộng sự (2012) đã thực hiện phản ứng Mannich để tổng hợp nên dẫn xuất thế của indole ở vị trí số 3 với các tác chất phản ứng indole, amine bậc hai và benzaldehyde. Phản ứng được thực hiện ở điều kiện không dung môi và nhiệt độ phòng với xúc tác là L-proline. Tuy độ chuyển hóa chỉ là 87% nhưng thu được sản phẩm mong muốn và không sinh ra sản phẩm phụ là bis-indole indole [72] .
Sơ đồ 1.10. Tổng hợp các dẫn xuất indole bằng phản ứng Mannich sử dụng xúc tác L-proline (trên), chất hoạt động bề mặt SDS và nước (dưới)
26
Nhóm nghiên cứu của Kumar (2013) tiếp tục thực hiện phản ứng Mannich giữa các amine bậc hai, các benzaldehyde và các indole khác nhau ở 80 °C, sử dụng chất hoạt động bề mặt SDS và nước để tạo thành hệ micelle có tác dụng làm bền iminium ion trung gian, từ đó tạo thành các sản phẩm 3-aminoalkylated indole (sơ đồ 1.10). Ưu điểm của phương pháp là hiệu suất cao, quy trình đơn giản và thân thiện môi trường [73].
Rajeswari và cộng sự (2015) đã tiến hành phản ứng Mannich giữa indole, benzaldehyde và succinimide trong DMF (sơ đồ 1.11), 48h thu được sản phẩm 1- ((1H-indol-3-yl)(phenyl)methyl)pyrrolidine-2,5-dione có hiệu suất 93% [74].
Sơ đồ 1.11. Phản ứng Mannich của indole, benzaldehyde và succinimide trong dung môi DMF
Liang-Hui Xie (2018) đã khảo sát các xúc tác acid và dung môi cho phản ứng Mannich cùng với các chất phụ gia để tìm ra điều kiện tối ưu nhất để thực hiện phản ứng Mannich, dung môi và phụ gia gồm MsOH và TBAI (Tetra-n-butylammonium iodide) (sơ đồ 1.12) để phản ứng Mannich đạt hiệu quả cao nhất [75].
Sơ đồ 1.12. Phản ứng Mannich trong tổng hợp các dẫn xuất indole sử dụng MsOH và TBAI
1.4. Nghiên cứu docking phân tử (molecular docking) và phức hợp camptothecin-topoisomerase I-DNA
1.4.1. Docking phân tử (molecular docking)
Mô hình gắn kết phân tử docking được xem là một phương pháp có vai trò lớn trong thiết kế thuốc với sự trợ giúp của máy tính (CADD – Computer-Aided Drug