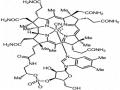
Bùi Thị Bửu Huê (2016) tổng hợp 12 dẫn xuất benzimidazole và thử hoạt tính gây độc tế bào của chúng trên dòng MFC-7, kết quả cho thấy hợp chất 13c và 13f – chứa dẫn xuất của naphtalen ở vị trí C-2 và nhóm Cl (13c), OCH3 (13f) ở vị trí C-5 – có hoạt tính ức chế mạnh trên dòng tế bào MCF-7, với CC50 lần lượt là 7,48 ± 1,19
µM và 6,43 ± 1,17 µM [41].
![]()
![]()
Cevik (2019) đã tổng hợp 18 dẫn xuất benzimidazole với vị trí C-2 là dẫn xuất oxadiazole và đánh giá hoạt tính kháng ung thư trên các dòng tế bào A549, Hep G2 và NIH 3T3 – tế bào của nguyên bào sợi phôi chuột (bảng 1.3). Kết quả cho thấy có 6/18 dẫn xuất có hoạt tính tốt hơn hoặc bằng chứng dương cisplatin, riêng hợp chất 4a -với vị trí số 5 và 6 là nguyên tử hydro, vị trí số 2 được thay thế bằng các nhóm chức khác nhau đính trên vòng oxadiazole - có hoạt tính ức chế trên cả 3 dòng tế bào thử nghiệm, giá trị IC50 (µM) thấp hơn cisplatin từ 4 – 20 lần [42].
Bảng 1.3. Giá trị IC50 của các dẫn xuất 4a-4s
I | C50 (µM) | ||||||
R1 | R2 | R3 | R4 | A549 | Hep G2 | NIH 3T3 | |
4a | H | H | H | H | 13 ± 1 | 3 ± 0,7 | 130 ± 8 |
4b | H | H | H | CH3 | 310 ± 20 | 170 ± 10 | >1000 |
4c | H | H | H | CN | 370 ± 20 | 50 ± 1 | 550 ± 20 |
4d | H | H | H | NO2 | 1000 ± 170 | 80 ± 2 | >1000 |
4e | H | H | H | Cl | 130 ± 10 | 40 ± 5 | 130 ± 20 |
4f | H | H | H | Br | 260 ± 60 | 40 ± 8 | 660 ± 80 |
4g | H | F | H | F | 30 ± 8 | 40 ± 7 | 40 ± 5 |
4h | H | Cl | H | Cl | 100 ± 20 | 60 ± 7 | 560 ± 70 |
4i | H | H | OH | OH | >1000 | >1000 | >1000 |
4j | CH3 | H | H | H | 90 ± 8 | 50 ± 3 | 300 ± 70 |
4k | CH3 | H | H | CH3 | 700 ± 9 | 80 ± 9 | >1000 |
4l | CH3 | H | H | CN | 60 ± 12 | 80 ± 1 | >1000 |
4m | CH3 | H | H | NO2 | 290 ± 40 | 20 ± 6 | 70 ± 10 |
4n | CH3 | H | H | Cl | 160 ± 40 | 60 ± 10 | 250 ± 60 |
4o | CH3 | H | H | Br | 450 ± 30 | 470 ± 10 | >1000 |
4p | CH3 | F | H | F | 110 ± 32 | 110 ± 20 | 110 ± 10 |
4r | CH3 | Cl | H | Cl | 300 ± 181 | 60 ± 3 | 450 ± 50 |
4s | CH3 | H | OH | OH | >1000 | >1000 | >1000 |
Cisplatin | 60 ± 9 | 60 ± 4 | >1000 |
Có thể bạn quan tâm!
-
 Nghiên cứu tổng hợp và đánh giá hoạt tính gây độc tế bào các dẫn xuất của benzimidazole và indole - 1
Nghiên cứu tổng hợp và đánh giá hoạt tính gây độc tế bào các dẫn xuất của benzimidazole và indole - 1 -
 Nghiên cứu tổng hợp và đánh giá hoạt tính gây độc tế bào các dẫn xuất của benzimidazole và indole - 2
Nghiên cứu tổng hợp và đánh giá hoạt tính gây độc tế bào các dẫn xuất của benzimidazole và indole - 2 -
 Một Số Thuốc Điều Trị Ung Thư Chứa Khung Benzimidazole
Một Số Thuốc Điều Trị Ung Thư Chứa Khung Benzimidazole -
 Tình Hình Nghiên Cứu Về Hoạt Tính Gây Độc Tế Bào Ung Thư Của Các Hợp Chất Có Khung Indole
Tình Hình Nghiên Cứu Về Hoạt Tính Gây Độc Tế Bào Ung Thư Của Các Hợp Chất Có Khung Indole -
 Phép Tam Giác Phân Đặt Ligand Vào Điểm Gắn Kết Của Protein
Phép Tam Giác Phân Đặt Ligand Vào Điểm Gắn Kết Của Protein -
 Các Dụng Cụ Và Thiết Bị Sử Dụng Trong Tổng Hợp
Các Dụng Cụ Và Thiết Bị Sử Dụng Trong Tổng Hợp
Xem toàn bộ 186 trang tài liệu này.

(Nguồn: Cevik)
Nhận thấy các dẫn xuất benzimidazole ngưng tụ với oxadiazole có tiềm năng lớn trong ức chế tế bào ung thư, năm 2020, nhóm Cevik tiếp tục tổng hợp 15 dẫn xuất loại này với sự thay đổi quan trọng trên khung nền benzimidazole: các dẫn xuất oxadiazole được đưa vào vị trí C-6, trong khi đó vị trí C-2 là các nhóm thế phenyl khác nhau, các dẫn xuất này được đánh giá hoạt tính ức chế tế bào trên các dòng A549, MCF-7, C6 – tế bào u thần kinh đệm ở chuột, Hep G2, HeLa và NIH 3T3, kết quả cho thấy có 2 dẫn xuất (5a, 5n) có hoạt tính ức chế tốt hơn chứng dương doxorubicin trên dòng A549 (bảng 1.4 và 1.5). So sánh với năm 2019 cho thấy việc
thay đổi nhóm chức đã làm hoạt tính các dẫn xuất thu được cao hơn, cùng trên dòng A549 (năm 2019 có 4/18 dẫn xuất có IC50 < 100 µM, trong khi đó năm 2020 là 4/15 dẫn xuất). Ngoài ra, nghiên cứu còn chứng minh hợp chất 5a, 5b, 5d, 5e, 5k, 5l, 5n và 5o có cơ chế tác động ức chế, xen kẽ vào phức hợp DNA-topoisomerase I giống như Hoechst 33342 và camptothecin [43].
Bảng 1.4. Cấu trúc của các dẫn xuất benzimidazole- 1,3,4-oxadiazole
Hợp chất | R1 | R2 | Hợp chất | R1 | R2 |
5a | OH | CH3 | 5i | OCH3 |
|
5b | OH | C2H5 | 5j | OCH3 | |
5c | OH |
| 5k | OC2H5 | -CH3 |
5d | OH |
| 5l | OC2H5 | -C2H5 |
5e | OH | 5m | OC2H5 |
| |
5g | OCH3 | C2H5 | 5o | OC2H5 | |
5h | OCH3 |
|
Bảng 1.5. Hoạt tính gây độc tế bào của các dẫn xuất 5a-5o, doxorubicin và Hoechst 33342
IC50 (µM)
A549 | MCF-7 | C6 | Hep G2 | HeLa | NIH 3T3 | |
5a | 43,256 ± 1,785 | 5,704 ± 0,254 | 15,614 ± 0,615 | 5,675 ± 0,283 | 13,960 ± 0,65 | 39,105 ± 1,940 |
5b | ≥100 | ≥100 | ≥100 | ≥100 | 0,698 ± 0,032 | 944,360 ± 7,625 |
5c | ≥100 | ≥100 | ≥100 | 21,860 ± 0,991 | 20,285 ± 1,101 | 44,556 ± 0,221 |
Hợp chất
≥100 | 9,148 ± 0,391 | 38,93 ± 1,921 | ≥100 | ≥100 | 720,645 ± 5,032 | |
5e | ≥100 | 7,318 ± 0,352 | ≥100 | ≥100 | ≥100 | 54,026 ± 2,682 |
5f | ≥100 | ≥100 | ≥100 | ≥100 | ≥100 | - |
5g | ≥100 | ≥100 | ≥100 | ≥100 | ≥100 | - |
5h | ≥100 | ≥100 | ≥100 | ≥100 | ≥100 | - |
5i | ≥100 | ≥100 | ≥100 | ≥100 | ≥100 | - |
5j | ≥100 | ≥100 | ≥100 | ≥100 | ≥100 | - |
5k | 22,254 ± 1,054 | 38,705 ± 1,875 | 3,204 ± 0,152 | ≥100 | 11,167 ± 0,467 | 74,630 ± 3,631 |
5l | 31,017 ± 1,530 | ≥100 | ≥100 | ≥100 | 0,224 ± 0,011 | 113,451 ± 5,472 |
5m | ≥100 | ≥100 | 32,167 ± 1,552 | ≥100 | ≥100 | 52,264 ± 2,512 |
5n | 7,388 ± 0,325 | ≥100 | ≥100 | ≥100 | 0,205 ± 0,010 | 188,570 ± 8,728 |
5o | ≥100 | 6,442 ± 0,287 | 24,951 ± 1,237 | 59,369 ± 2,589 | ≥100 | 44,072 ± 2,104 |
Doxorubicin | 12,420 ± 0,521 | 10,525 ± 0,472 | 28,690 ±1,228 | 16,482 ± 0,804 | 14,280 ± 0,704 | 1110,80 ± 8,254 |
Hoechst 33342 | 0,422 ± 0,020 | 2,404 ± 0,118 | 1,051 ± 0,307 | 27,815 ± 1,190 | 0,306 ± 0,015 | 7,388 ± 0,269 |
Các vị trí trên vòng benzimidazole được biến đổi và đánh giá SAR là vị trí N- 1, C-2, C-5 và C-6, tuy nhiên cũng có các nghiên cứu đề cập đến việc thay đổi hydro ở vị trí N-1 bằng các nhóm thế khác nhau sẽ làm giảm hoạt tính kháng tế bào. Ngoài ra, như các phân tích ở trên cho thấy vị trí số 2 đóng vai trò quan trọng trong việc hình thành hoạt tính kháng tế bào ung thư trên dòng A549 và MDA-MB-231. Do đó trong nghiên cứu này tập trung vào các dẫn xuất benzimidazole chứa nhóm thế ở vị trí C-2, đặc biệt là các nhóm phenyl thế khác nhau, kết hợp với đó là thay đổi nhóm chức ở vị trí C-5 và C-6, có ảnh hưởng thế nào đến hoạt tính ức chế tế bào ung thư của các dẫn xuất thu được. Ngoài ra, các nhóm chức được lựa chọn trong nghiên cứu là các nhóm chức phổ biến có mặt trong các phân tử có hoạt tính sinh học (ether, amine bậc 3, các halogen, alcohol, phenol…) [44], kết hợp với điều kiện thực tế, các nhóm thế khác nhau như: OCH3, N(CH3)2, CF3, I, Cl, OH, NO2, O-CH2-Ph, CH3 đã được sử dụng để đưa vào các cấu trúc benzimidazole trong nghiên cứu này.
1.2.3. Một số phương pháp tổng hợp benzimidazole
1.2.3.1. Đi từ carboxylic acid
Phản ứng giữa o-phenylendiamine và mono acid tạo thành nhân benzimidazole với các nhóm thế khác nhau ở vị trí số 2. Phản ứng được tiến hành bằng các chất xúc tác khác nhau cho hiệu suất cao. Phản ứng được tiến hành với các mono acid trong môi trường nước ở nhiệt độ cao [45]. Phản ứng được tiến hành trong lò vi sóng với các chất xúc tác acid như polyphosphoric acid (PPA) [46], alumina- methanesulfonic
acid [47], hydrochloric acid [48],… Ngoài các mono acid, o-phenylendiamine còn phản ứng với dicarboxylic acid (sơ đồ 1.1).
![]()
Sơ đồ 1.1. Một số phản ứng ngưng tụ vòng benzimidazole giữa o-phenylendiamine và mono acid hoặc dicarboxylic acid
1.2.3.2. Phản ứng với aldehyde
Phản ứng ngưng tụ o-phenylendiamine với các aldehyde ở nhiệt độ phòng trong dung môi ethanol, sử dụng xúc tác là Co(OH)2 hoặc CoO(II). Hiệu suất phản ứng 80% - 94% [49]. Phản ứng ngưng tụ o-phenylendiamine và các aldehyde theo tỉ lệ 1:1,1 mol, với 5% mol In(OTf)3 được tiến hành ở nhiệt độ phòng khoảng 30 phút. Phản ứng cho hiệu suất cao khoảng 74% - 95%. Nghiên cứu còn chỉ ra trong các xúc tác Cu(OTf)2, La(OTf)3 , Lu(OTf)3 , Nd(OTf)3, Ce(OTf)3 và In(OTf)3, thì In(OTf)3 là chất xúc tác hiệu quả nhất trong việc chuyển đổi phản ứng [50]. Tổng hợp các dẫn xuất benzimidazole bằng o-phenylendiamine và các aldehyde trong dung môi methanol ở nhiệt độ phòng, thời gian khoảng 4h – 14h, phản ứng sử dụng chất xúc tác là nano Cu(OH)2 trên nền silica. Hiệu suất phản ứng 68% - 93% [51]. Ngoài ra còn sử dụng các dẫn xuất của o-phenylendiamine cho ngưng tụ với aldehyde với sự có mặt của Na2S2O5 trong dung hệ dung môi ethanol:nước (9:1) với sự hỗ trợ của vi sóng để tạo thành các dẫn xuất benzimidazole, với hiệu suất phản ứng 76 – 86% [52] (sơ đồ 1.2).
Sơ đồ 1.2. Các phản ứng ngưng tụ khung benzimidazole từ o-phenylendiamine với các aldehyde
1.2.3.3. Phản ứng với acid anhydride
Phản ứng giữa o-phenylendiamine và acid anhydride của một carboxylic acid tạo ra các dẫn xuất benzimidazole phụ thuộc vào các điều kiện sử dụng, nhưng thời gian phản ứng là yếu tố quyết định. Acid anhydride được sử dụng phổ biến là acetic anhydride. Ngoài ra hỗn hợp formic-acetic anhydride và benzoic anhydride, acetic anhydride-sodium acetate hoặc acetic acid cũng được sử dụng thành công. Khi đun hồi lưu o-phenylendiamine với acetic anhydride trong vài giờ sẽ chuyển thành 2- methylbenzimidazole [53]. o-Phenylendiamine phản ứng với acid anhydride của hai carboxylic acid như acid anhydride của một carboxylic acid. Ví dụ: o- phenylendiamine phản ứng succinic anhydride thành 𝛽-(2-benzimidazole)propionic acid [23] (sơ đồ 1.3).
![]()
Sơ đồ 1.3. Một số phản ứng đóng vòng benzimidazole từ o-phenylendiamine và dẫn xuất acid anhydride
1.2.3.4. Phản ứng với ester
Vào năm 2006, Yong-Mei Wang và cộng sự đã tổng hợp các dẫn xuất benzimidazole bằng o-phenylendiamine với các ortho-ester và Lewis acid (ZrCl4,
TiCl4, SnCl4.5H2O, HfCl4...) được khuấy trong dung môi ethanol ở nhiệt độ phòng, thời gian phản ứng khoảng 1h – 14h. Hiệu suất phản ứng từ 5% - 95% [54] (sơ đồ 1.4).
NH2
NH2
+ R1C(OR2)3
H
Lewis acid N
R1
EtOH, rt N
Sơ đồ 1.4. Tổng hợp dẫn xuất benzimidazole từ o-phenylendiamine với các ortho- ester
1.2.3.5. Phản ứng với acetyl chloride
Phản ứng giữa 3,4-diaminotoluene và acetyl chloride trong dung môi benzene tạo ra 2,5-dimethylbenzimidazole [53] (sơ đồ 1.5).
Sơ đồ 1.5. Tổng hợp dẫn xuất 2,5-dimethylbenzimidazole
1.3. Giới thiệu về indole
1.3.1. Đặc điểm chung
Indole hay còn có tên gọi khác là benzo[b]pyrrole, là một hợp chất hữu cơ dị vòng phẳng. Công thức cấu tạo bao gồm vòng benzene sáu cạnh gắn với vòng pyrrole năm cạnh chứa nitơ. Trong phân tử indole, cặp electron độc thân của nitơ tham gia vào hệ liên hợp của vòng thơm nên indole thể hiện tính base yếu [54].
Công thức phân tử: C8H7N
Công thức cấu tạo và quy tắc đánh số trên khung indole như sau:
1
7 H
6 8 N
2
5 9
4 3
Trong tự nhiên, indole tồn tại dưới dạng terpene indole alkaloid rất đa dạng, rất nhiều nhóm chất có cấu trúc indole (khoảng 2000 chất). Các hợp chất chứa khung indole rất phong phú và chúng thường sở hữu khung cấu trúc phức tạp với những hoạt tính sinh học riêng biệt như là nhóm corynanthe (ajmalicine, serpentine, yohimbine), nhóm iboga (catharanthine), nhóm aspidosperma (tabersonine, vindoline) và nhóm quinoline (camptothecin, quinin) [55]. Ajmalicine là một chất chống tăng huyết áp, được chiết từ cây dừa cạn (Catharanthus roseus) [56]. Khung indole còn hiện diện trong chất dẫn truyền thần kinh serotonin.
Ajmalicine Serotonin
Indole được tìm thấy trong một số thuốc điều trị ung thư đã thương mại hóa như Vincristine, Vinblastine. Ngoài ra khung indole còn hiện diện trong một số thuốc điều trị đau thấp khớp và kháng viêm indomethacin. Indomethacin còn có thể giảm đau, sưng, cứng khớp do viêm khớp, bệnh gout, viêm bao hoạt dịch, viêm gân, Thuốc này được biết đến như loại thuốc chống viêm khớp không steroid [57] (hình 1.4).
![]()
![]()
![]()
![]()
![]()
Hình 1.4. Một số thuốc thương mại có chứa khung indole
Ngoài ra còn có các loại thuốc thương mại khác có chứa khung indole như: Oxipertin – thuốc an thần; Iprindole – thuốc chống trầm cảm; Ondansentron – thuốc chống nôn mửa trong quá trình điều trị cho bệnh nhân ung thư do dùng thuốc điều trị ung thư (hoá trị), liệu pháp xạ trị, thuốc hoạt động bằng cách ngăn chặn một hợp chất