Hình 3.53. Ảnh SEM của các mẫu vật liệu rGO (a), MoS2 (b), 3%Mn-MoS2 (c), 3%Mn- MoS2/rGO (d) và MoS2/rGO (e)
Quan sát kết quả ở hình 3.53a có thể thấy, rGO có cấu trúc dạng lớp phẳng với độ dày gần 10 nm hình thành từ quá trình khử tách lớp GO về rGO với tác nhân khử là axit ascorbic kết hợp với nung trong môi trường N2 ở 600oC. Trong khi đó, hình 3.53b và 3.53c cho thấy giữa hai mẫu MoS2 và 3%Mn-MoS2 không có sự khác biệt rò nét, đều chung cấu trúc tấm tương tự nhưng dày đặc hơn và kết tụ lại với nhau, làm giảm khả năng tiếp xúc của các tâm hoạt tính với chất cần phản ứng, dẫn tới hoạt động kém hơn [219], [166]. Khi tạo compozit MoS2/rGO và Mn-MoS2/rGO (hình 3.53d và 3.53e), có thể thấy rò các vảy MoS2 và Mn-MoS2 được phân tán đều hơn trên rGO, làm giảm sự kết tụ tâm hoạt tính do rGO có diện tích bề mặt riêng lớn, giúp tăng các vị trí tâm hoạt tính xúc tác, cải thiện hoạt tính của vật liệu. Do đó, để cải thiện hiệu quả quang xúc tác của MoS2 thì tạo compozit với rGO là một giải pháp đúng đắn.
Để xem xét việc biến tính Mn vào vật liệu sẽ hình thành nên các kiểu liên kết và lai hóa thế nào, phổ Raman của mẫu 3%Mn-MoS2 và mẫu 3%Mn-MoS2/rGO được ghi lại và mô tả trên hình 3.54.
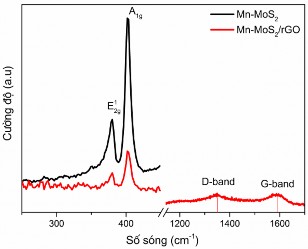
Hình 3.54. Phổ Raman của các mẫu vật liệu 3%Mn-MoS2 và 3%Mn-MoS2/rGO
Quan sát hình 3.54 có thể thấy, trong các mẫu biến tính bởi Mn đều xuất hiện các dao động của Mn-MoS2. Cường độ các pic tại các dao động A1g và E12g của pha hexagonal 2H-MoS2 trong mẫu compozit Mn-MoS2/rGO thấp hơn nhiều so với mẫu Mn-MoS2 không tạo compozit. Hiện tượng này là do đã có sự hình thành liên kết giữa Mn-MoS2 với rGO, làm giảm đi các liên kết đơn thuần của Mn-MoS2 như đã quan sát thấy.
Phổ EPR cũng được sử dụng để nghiên cứu sự thay đổi trong cấu trúc vật liệu khi tạo compozit với rGO và biến tính với Mn. Kết quả thể hiện trên hình 3.55.
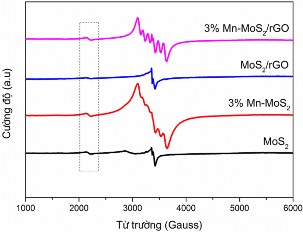
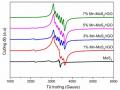
Hình 3.55. Phổ EPR của các mẫu vật liệu MoS2, 3%Mn-MoS2, MoS2/rGO và 3%Mn- MoS2/rGO
Hình 3.55 cho thấy phổ EPR của MoS2 và compozit MoS2/rGO có phần dao động ở vùng từ trường thấp rất nhỏ thể hiện được liên kết không có tính chất từ [181, 189]. Nhưng khi biến tính Mn vào mẫu MoS2 thì cường độ thể hiện rò nét
chứng tỏ vật liệu có tính chất từ. Bên cạnh đó, đường hyperfine của mẫu Mn-MoS2 chưa thể hiện rò được 6 pic của Mn, có thể do các tấm Mn-MoS2 kết tụ lại với nhau. Chỉ khi Mn-MoS2 tạo compozit với rGO, giá trị electron quay mới thể hiện rò nét 6 pic của Mn. Điều này cho phép khẳng định rằng Mn đã được biến tính vào trong các tinh thể và thay thế vị trí Mo trong mạng MoS2 [182, 192]. Khi đó, các tấm Mn- MoS2 phân tán đều trên mạng lưới rGO làm giảm được sự kết tụ, tăng các vị trí hoạt tính của vật liệu dẫn đến làm tăng hiệu quả quang xúc tác của vật liệu biến tính.
Mặt khác, dựa trên phổ EPR thì loại khuyết tật thể hiện trong các hạt nano của mẫu có thể được nghiên cứu theo hệ số g được tính bằng g = ![]() /BH [193]. Kết quả được thể hiện trong bảng 3.14.
/BH [193]. Kết quả được thể hiện trong bảng 3.14.
Bảng 3.14. Giá trị hệ số g của các mẫu MoS2, 3%Mn-MoS2, MoS2/rGO và 3%Mn- MoS2/rGO
Vùng từ trường (Gauss) | Hệ số g | |
MoS2 | 3300 - 3400 | 2,003 |
3%Mn-MoS2 | 2121 - 2235 | 3,084 |
3099 - 3618 | 2,000 | |
MoS2/rGO | 2121 - 2235 | 3,081 |
3354 - 3423 | 1,980 | |
3%Mn-MoS2/rGO | 2127 - 2235 | 3,080 |
3099 - 3633 | 1,995 |
Có thể bạn quan tâm!
-
 Phổ Epr Của Các Mẫu Compozit X%mn-Mos 2 /rgo (X = 1%mn, 3%mn, 5%mn Và 7%mn) Với Các Hàm Lượng Biến Tính Khác Nhau
Phổ Epr Của Các Mẫu Compozit X%mn-Mos 2 /rgo (X = 1%mn, 3%mn, 5%mn Và 7%mn) Với Các Hàm Lượng Biến Tính Khác Nhau -
 Phổ Eis Của Mos 2 (Am), Mos 2 /rgo (Cm) Và Mn-Mos 2 /rgo (Dm)
Phổ Eis Của Mos 2 (Am), Mos 2 /rgo (Cm) Và Mn-Mos 2 /rgo (Dm) -
 Ảnh Hưởng Của Ph Đến Quá Trình Quang Phân Hủy Rhb Trên Xúc Tác Mos 2 /rgo
Ảnh Hưởng Của Ph Đến Quá Trình Quang Phân Hủy Rhb Trên Xúc Tác Mos 2 /rgo -
 Phan Thi Thuy Trang , Truong Cong Duc, Truong Thanh Tam, Vo Vien, Nguyen Hong Lien, “Effect Of Mn 2+ Dopants On The Photocatalytic Efficiency Of Mos 2 ” , Vietnam Journal Of Catalysis And
Phan Thi Thuy Trang , Truong Cong Duc, Truong Thanh Tam, Vo Vien, Nguyen Hong Lien, “Effect Of Mn 2+ Dopants On The Photocatalytic Efficiency Of Mos 2 ” , Vietnam Journal Of Catalysis And -
 Nghiên cứu tổng hợp, đặc trưng xúc tác MoS2/rGO biến tính với Mn và ứng dụng cho quá trình quang phân hủy rhodamine B trong vùng ánh sáng khả kiến - 19
Nghiên cứu tổng hợp, đặc trưng xúc tác MoS2/rGO biến tính với Mn và ứng dụng cho quá trình quang phân hủy rhodamine B trong vùng ánh sáng khả kiến - 19 -
 Nghiên cứu tổng hợp, đặc trưng xúc tác MoS2/rGO biến tính với Mn và ứng dụng cho quá trình quang phân hủy rhodamine B trong vùng ánh sáng khả kiến - 20
Nghiên cứu tổng hợp, đặc trưng xúc tác MoS2/rGO biến tính với Mn và ứng dụng cho quá trình quang phân hủy rhodamine B trong vùng ánh sáng khả kiến - 20
Xem toàn bộ 192 trang tài liệu này.
Qua kết quả ở bảng 3.14 cho thấy các giá trị hệ số g của các mẫu compozit MoS2/rGO (g = 1,98) và mẫu biến tính 3%Mn-MoS2/rGO (g = 1,99) đều giảm so với mẫu MoS2 đơn chất (g = 2,003) và mẫu 3%Mn-MoS2 (g = 2,00). Điều này càng khẳng định hơn có sự tồn tại của Mn biến tính vào tinh thể MoS2.
Phổ UV-Vis DRS được sử dụng để nghiên cứu tính chất hấp thụ ánh sáng và dự đoán khả năng quang xúc tác của vật liệu. Kết quả phân tích các mẫu MoS2, 3%Mn-MoS2, MoS2/rGO và 3%Mn-MoS2/rGO được thể hiện trên hình 3.56.
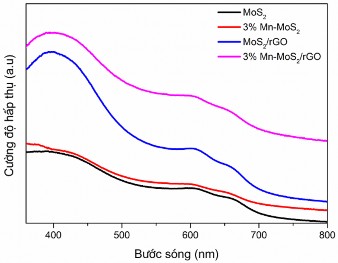
Hình 3.56. Phổ UV-Vis DRS của các mẫu vật liệu MoS2, 3%Mn-MoS2, MoS2/rGO và 3%Mn-MoS2/rGO
Kết quả cho thấy, các mẫu compozit hấp thụ ánh sáng mạnh hơn mẫu đơn chất MoS2 hoặc Mn-MoS2 là do khả năng hấp thụ mạnh ánh sáng của rGO [220]. Khi biến tính Mn vào mạng lưới MoS2/rGO, hiệu quả hấp thụ ánh sáng cao hơn so với khi không biến tính, có thể là do hiệu ứng plasma của các ion Mn đã giúp tăng cường hiệu quả hấp thụ ánh sáng [221].
Những phân tích trên đây chỉ ra rằng, khi tổ hợp MoS2 với rGO (vật liệu có diện tích bề mặt riêng lớn, khả năng hấp thụ tốt ánh sáng) và biến tính với kim loại Mn tạo compozit, hiệu ứng hiệp trợ giữa các chất này đã làm cải thiện độ phân tán các tâm hoạt tính, tăng hiệu quả hấp thụ ánh sáng, khả năng truyền điện tích, nên dự kiến sẽ dẫn đến tăng hiệu quả quang xúc tác của vật liệu.
3.6.2. Hoạt tính quang xúc tác của các tổ hợp vật liệu
Hoạt tính quang xúc tác của vật liệu MoS2, 3%Mn-MoS2, MoS2/rGO và 3%Mn-MoS2/rGO cho quá trình phân hủy RhB (nồng độ đầu 20 mg/L) trong vùng ánh sáng khả kiến (đèn compact 60W) được so sánh và thể hiện trên hình 3.57.
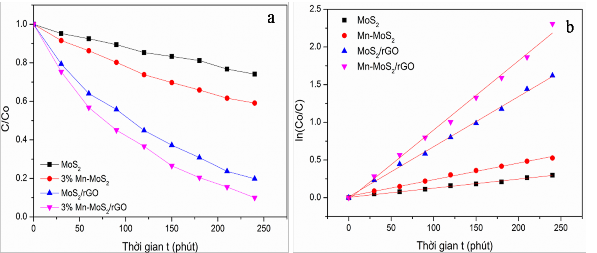
Hình 3.57. Sự phân hủy RhB (a) và mô hình động học Langmuir – Hinshelwood (b) của các mẫu vật liệu MoS2, 3%Mn-MoS2, MoS2/rGO và 3%Mn-MoS2/rGO
(Điều kiện: CRhB = 20 mg/L, m xúc tác = 0,1g, 400 ml dung dịch RhB, đèn 60W-220V, pH=6,04)
Kết quả hình 3.57a cho thấy, hiệu quả quang xúc tác của vật liệu tăng theo thứ tự MoS2 < 3%Mn-MoS2 < MoS2/rGO < 3%Mn-MoS2/rGO tương ứng với các giá trị độ chuyển hóa RhB là 25,89%; 40,9%; 80% và 90%. Điều này chỉ ra rằng, khi tiến hành biến tính Mn vào compozit MoS2/rGO đã làm tăng hiệu quả quang xúc tác một cách đáng kể do các ưu việt về mặt cấu trúc như đã phân tích ở trên.
Về mặt động học, kết quả thống kê các thông số động học phản ứng trên 4 mẫu vật liệu được đưa ra trong bảng 3.15.
Bảng 3.15. Dữ liệu của các mẫu vật liệu thu được từ mô hình động học Langmuir- Hinshelwood
kapp (phút-1) | Hệ số hồi quy R2 | |
MoS2 | 0,00121 | 0,993 |
3%Mn-MoS2 | 0,00221 | 0,994 |
MoS2/rGO | 0,00652 | 0,998 |
3%Mn-MoS2/rGO | 0,00919 | 0,993 |
Kết quả cho thấy, hằng số tốc độ của mẫu Mn-MoS2/rGO cao gấp gần 1,4 lần hằng số tốc độ của mẫu MoS2/rGO; 4,2 lần với mẫu Mn-MoS2 và 7,6 lần so với
mẫu đơn MoS2. Phản ứng quang xúc tác xảy ra trên cả 4 mẫu vật liệu đều tuyến tính theo mô hình động học Langmuir-Hinshelwood. Các kết quả thực nghiệm này chỉ ra rằng quá trình tạo compozit với rGO và biến tính với Mn đã giúp cải thiện đáng kể hiệu quả quang xúc tác của MoS2 ban đầu trong phản ứng phân hủy RhB dưới ánh sáng khả kiến. Ngoài các yếu tố về tăng diện tích bề mặt riêng, tăng độ phân tán tâm hoạt tính xúc tác, cải thiện tốc độ truyền điện tích, thì việc thay thế của Mn vào một số vị trí của Mo trong mạng lưới tinh thể MoS2 sẽ hình thành nên các vị trí khiếm khuyết về điện tích (do điện tích của ion Mn2+ và Mo4+ có sự khác biệt với nhau), hình thành thêm các tâm hoạt động trên bề mặt của xúc tác, dẫn tới tăng khả năng quang xúc tác của vật liệu.
3.7. Khả năng quang xúc tác của Mn-MoS2/rGO dưới các nguồn sáng khác nhau
Để xem xét khả năng làm việc của vật liệu Mn-MoS2/rGO, mẫu được thử nghiệm hoạt tính quang xúc tác cho phản ứng phân hủy RhB dưới các nguồn sáng khả kiến khác nhau, bao gồm đèn compact, đèn LED và ánh sáng mặt trời (ứng với cường độ chiếu sáng trung bình của ánh sáng mặt trời là 98,76 mW/cm2). Kết quả được thể hiện trên hình 3.58.
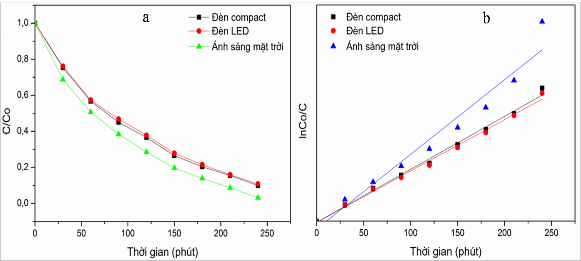
Hình 3.58. Hiệu suất quá trình phân hủy RhB (a) và mô hình động học Langmuir-
Hinshelwood (b) trên xúc tác 3%Mn-MoS2/rGO
(Điều kiện: CRhB = 20 mg/L, m xúc tác = 0,1g, 400 ml dung dịch RhB, pH=6,04)
Kết quả cho thấy, hiệu suất của quá trình phân hủy RhB trên xúc tác 3%Mn- MoS2/rGO dưới ánh sáng của đèn compact và đèn LED là gần tương đương với nhau, tương ứng 90% và 89,1%. Điều này chỉ ra rằng, khả năng tác động nhiệt đến phản ứng của đèn compact gần như không đáng kể, do đã được loại bỏ nhờ ổn nhiệt hệ phản ứng. Tuy nhiên, khi thực hiện phản ứng dưới tác dụng của ánh sáng mặt trời thì hiệu suất phân hủy RhB đạt 96,8%, cao hơn so với sử dụng đèn compact (90%). Điều này có thể được giải thích là do vật liệu Mn-MoS2/rGO có khả năng hấp thụ photon ánh sáng từ vùng tử ngoại đến vùng khả kiến thể hiện ở phổ UV-Vis DRS và sự có mặt của bức xạ UV trong ánh sáng mặt trời đã làm gia tăng khả năng xúc tác phân hủy RhB.
Áp dụng mô hình động học Langmuir-Hishelwood [6] đối với quá trình phân hủy RhB trên vật liệu xúc tác Mn-MoS2/rGO dưới cả 3 nguồn sáng đều cho thấy có sự tuyến tính rò rệt như thể hiện ở bảng 3.16.
Bảng 3.16. Dữ liệu từ mô hình động học Langmuir-Hinshelwood của mẫu 3%Mn- MoS2/rGO với sự ảnh hưởng của các đèn khác nhau
Hằng số tốc độ k (phút-1) | Hệ số tương quan (R2) | |
Đèn compact 60W | 0,00919 | 0,993 |
Đèn LED | 0,00891 | 0,994 |
Ánh sáng mặt trời | 0,01294 | 0,951 |
Bảng 3.16 cho thấy, tốc độ phân hủy RhB trên xúc tác Mn-MoS2/rGO khi được kích thích bằng ánh sáng mặt trời diễn ra nhanh hơn khoảng 1,4 lần so với khi chiếu sáng bằng đèn compact và đèn LED.
3.8. Độ bền hoạt tính xúc tác của vật liệu Mn-MoS2/rGO
Khả năng tái sử dụng của vật liệu 3%Mn-MoS2/rGO được khảo sát sau 5 lần phản ứng. Kết quả thể hiện ở hình 3.59 cho thấy, sau 5 lần phản ứng, vật liệu vẫn thể hiện hoạt tính xúc tác ở mức cao với hiệu suất phân hủy RhB đạt 86,5%. Điều này chỉ ra rằng, vật liệu Mn-MoS2/rGO đã tổng hợp có hoạt tính quang xúc tác tốt và bền trong việc xử lý chất màu khó phân hủy RhB trong môi trường nước dưới tác dụng bức xạ của vùng ánh sáng khả kiến.
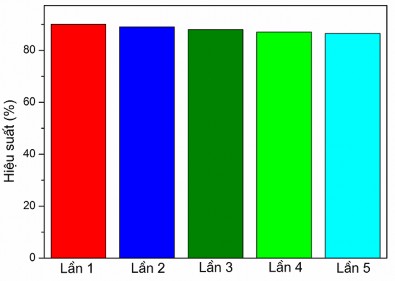
Hình 3.59. Độ bền hoạt tính của vật liệu Mn-MoS2/rGO cho quá trình quang xúc tác phân hủy RhB dưới tác dụng bức xạ vùng ánh sáng khả kiến
Kết quả này hứa hẹn khả năng ứng dụng của vật liệu Mn-MoS2/rGO trong thực tế xử lý nước thải chứa RhB, nước thải ngành công nghiệp dệt nhuộm, và mở ra hướng nghiên cứu mới áp dụng cho xử lý các chất hữu cơ khó phân hủy khác trong môi trường nước.