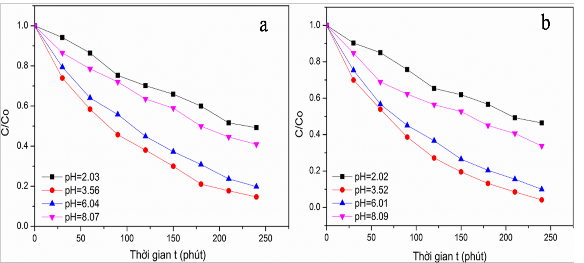
Hình 3.46. Ảnh hưởng của pH đến quá trình quang phân hủy RhB trên xúc tác MoS2/rGO
(a) và Mn-MoS2/rGO (b)
Bảng 3.12. Hiệu quả quang xúc tác của các vật liệu đến quá trình quang xúc tác phân hủy RhB dưới sự ảnh hưởng của pH
Hiệu suất phân hủy RhB trên xúc tác MoS2/rGO (%) | Hiệu suất phân hủy RhB trên xúc tác Mn-MoS2/rGO (%) | |
2,03 | 50,8 | 53,6 |
3,56 | 85,3 | 95,9 |
6,04 | 80 | 90,05 |
8,07 | 59,1 | 66,3 |
Có thể bạn quan tâm!
-
 Ảnh Sem Của Các Mẫu Mos 2 /rgo-140 O C (A), Mos 2 /rgo-160 O C (B), Mos 2 /rgo-180 O C (C) Và Mos 2 /rgo-200 O C (D)
Ảnh Sem Của Các Mẫu Mos 2 /rgo-140 O C (A), Mos 2 /rgo-160 O C (B), Mos 2 /rgo-180 O C (C) Và Mos 2 /rgo-200 O C (D) -
 Phổ Epr Của Các Mẫu Compozit X%mn-Mos 2 /rgo (X = 1%mn, 3%mn, 5%mn Và 7%mn) Với Các Hàm Lượng Biến Tính Khác Nhau
Phổ Epr Của Các Mẫu Compozit X%mn-Mos 2 /rgo (X = 1%mn, 3%mn, 5%mn Và 7%mn) Với Các Hàm Lượng Biến Tính Khác Nhau -
 Phổ Eis Của Mos 2 (Am), Mos 2 /rgo (Cm) Và Mn-Mos 2 /rgo (Dm)
Phổ Eis Của Mos 2 (Am), Mos 2 /rgo (Cm) Và Mn-Mos 2 /rgo (Dm) -
 Ảnh Sem Của Các Mẫu Vật Liệu Rgo (A), Mos 2 (B), 3%mn-Mos 2 (C), 3%mn- Mos 2 /rgo (D) Và Mos 2 /rgo (E)
Ảnh Sem Của Các Mẫu Vật Liệu Rgo (A), Mos 2 (B), 3%mn-Mos 2 (C), 3%mn- Mos 2 /rgo (D) Và Mos 2 /rgo (E) -
 Phan Thi Thuy Trang , Truong Cong Duc, Truong Thanh Tam, Vo Vien, Nguyen Hong Lien, “Effect Of Mn 2+ Dopants On The Photocatalytic Efficiency Of Mos 2 ” , Vietnam Journal Of Catalysis And
Phan Thi Thuy Trang , Truong Cong Duc, Truong Thanh Tam, Vo Vien, Nguyen Hong Lien, “Effect Of Mn 2+ Dopants On The Photocatalytic Efficiency Of Mos 2 ” , Vietnam Journal Of Catalysis And -
 Nghiên cứu tổng hợp, đặc trưng xúc tác MoS2/rGO biến tính với Mn và ứng dụng cho quá trình quang phân hủy rhodamine B trong vùng ánh sáng khả kiến - 19
Nghiên cứu tổng hợp, đặc trưng xúc tác MoS2/rGO biến tính với Mn và ứng dụng cho quá trình quang phân hủy rhodamine B trong vùng ánh sáng khả kiến - 19
Xem toàn bộ 192 trang tài liệu này.
Để giải thích hiện tượng này, ảnh hưởng của pH đến điện tích bề mặt của vật liệu hay điểm đẳng điện (pHpzc) của vật liệu MoS2/rGO và Mn-MoS2/rGO được xác định. Các dung dịch ban đầu được điều chỉnh pHi về các giá trị 2,03; 3,56; 6,04 và 8,07. Quá trình hấp phụ của vật liệu được tiến hành trong vòng 24 giờ. Dung dịch thu được đem lọc bỏ chất rắn và đo lại pHf. Đồ thị ![]() pHi = pHi – pHf cắt trục hoành
pHi = pHi – pHf cắt trục hoành
tại các giá trị có hoành độ chính xác là pHpzc. Kết quả được thể hiện trên hình 3.47.
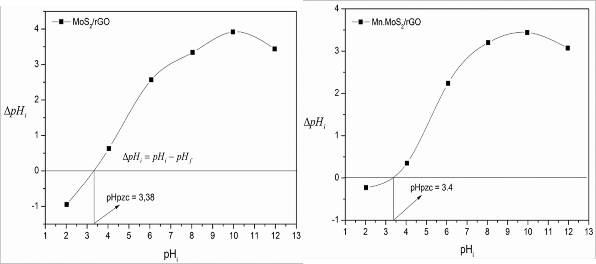
Hình 3.47. Đồ thị xác định điểm đẳng điện của vật liệu MoS2/rGO và Mn-MoS2/rGO
Kết quả ở hình 3.47 cho thấy điểm đẳng điện của các vật liệu MoS2/rGO là pHpzc = 3,38 và Mn-MoS2/rGO có pHpzc = 3,4. Điều này có nghĩa là khi pH < pHpzc thì các nhóm chức được proton hóa do đó làm tăng điện tích dương bề mặt xúc tác quang. Ngược lại khi pH > pHpzc thì bề mặt quang xúc tác tích điện âm. Do đó ở pH=3,56 (gần với pHpzc của vật liệu nhất) thì hiệu quả hấp phụ quang xúc tác của vật liệu tốt nhất như đã quan sát thấy.
Một yếu tố khác cũng có thể được sử dụng để giải thích ảnh hưởng của pH đến hiệu suất quá trình phân hủy RhB, đó là bản chất cấu trúc của chất màu. Phân tử chất màu RhB trong thực tế tồn tại ở hai trạng thái, đó là dạng cation và dạng ion lưỡng cực thể hiện ở hình 3.48 [209].
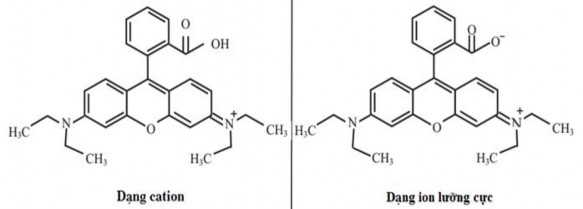
Hình 3.48. Hai dạng tồn tại của RhB trong dung dịch nước
Vì hằng số phân ly axit pKa của nhóm cacboxyl trong phân tử RhB có giá trị vào khoảng 3,7 [210] nên trong vùng pH < 3,7 thì RhB tồn tại dạng cation và pH >
3,7 thì RhB tồn tại dạng ion lưỡng cực. Do vậy, tại giá trị pH = 2,03 (pH < pHpzc) thì bề mặt vật liệu mang điện tích dương và bản thân RhB cũng ở dạng cation nên tồn tại một lực đẩy tĩnh điện giữa RhB và bề mặt của vật liệu làm cho sự hấp phụ của phân tử hữu cơ cation trên bề mặt xúc tác quang giảm dẫn đến hiệu suất phân hủy chất màu RhB của vật liệu giảm xuống chỉ còn 50,8% (vật liệu MoS2/rGO) và 53,6% (vật liệu Mn-MoS2/rGO). Qua vùng pH = 3,56 thì lúc này bề mặt của vật liệu tích điện âm (pH > pHpzc) do quá trình deproton hóa nhóm cacboxyl, trong khi đó RhB vẫn tồn tại ở dạng cation nên làm tăng khả năng hấp phụ các chất hữu cơ cation trên bề mặt của vật liệu làm hiệu quả quang xúc tác tăng cực đại lên 85,3% (vật liệu MoS2/rGO) và 95,9% (vật liệu Mn-MoS2/rGO).
Sau khi vượt qua pH= 3,56 và càng tiến về vùng trung tính, RhB tồn tại dạng chính là ion lưỡng cực nên dễ dẫn đến quá trình kết tụ các phân tử RhB hình thành dạng dime, do tương tác tĩnh điện giữa nhóm cacboxyl và nhóm xanhthen trong các phân tử monome. Tuy nhiên, pH tăng lên đồng nghĩa làm tăng các gốc hydroxyl
[211] nên quá trình này vẫn giữ cho hiệu suất quá trình quang phân hủy RhB vẫn khá cao. Đến pH=6,04, hiệu suất vẫn đạt khoảng 80,2% (trên vật liệu MoS2/rGO) và 90,05% (trên vật liệu Mn-MoS2/rGO), không chênh lệch nhiều so với ở ngưỡng pH=3,56. Nhưng đến khi chuyển hẳn sang môi trường bazơ (pH=8,07) thì hiệu quả phân hủy RhB giảm mạnh còn 59,1% (vật liệu MoS2/rGO) và 66,3% (vật liệu Mn- MoS2/rGO). Nguyên nhân của hiện tượng này là do khi pH càng tăng cao, môi trường càng có nhiều nhóm hydroxyl, gây ra sự cạnh tranh giữa các nhóm hydroxyl với các phân tử hữu cơ để hấp phụ trên bề mặt xúc tác làm giảm khả năng phân hủy các hợp chất hữu cơ. Mặt khác, trong quá trình này hình thành nhiều dime, dạng này khó bị oxi hóa hơn so với dạng monome làm giảm số lượng phân tử RhB hấp phụ trên các tâm hoạt động. Bên cạnh đó, bề mặt vật liệu tích điện âm nên tồn tại lực đẩy tĩnh điện giữa điện tích âm trên bề mặt chất hấp phụ và nhóm cacboxylat làm giảm mạnh khả năng hấp phụ của RhB trên vật liệu [210] làm cho hiệu quả quá trình quang xúc tác phân hủy RhB của vật liệu MoS2/rGO và Mn-MoS2/rGO càng giảm mạnh trong môi trường bazơ như đã quan sát thấy.
Từ các phân tích này, môi trường trung tính được lựa chọn cho các nghiên cứu tiếp theo về quá trình quang phân hủy RhB trên xúc tác trên cơ sở MoS2/rGO vì
hiệu quả xúc tác vẫn khá cao, không khác biệt nhiều so với ở môi trường axit (pH=3,56), mà lại tránh được vấn đề về ăn mòn khi đưa vào ứng dụng trong thực tế.
3.5.4. Ảnh hưởng của các chất dập tắt gốc tự do
Sự có mặt của các gốc tự do OH; O2-; h+ và e- cũng có những ảnh hưởng rất lớn đến hiệu suất của quá trình phân hủy quang xúc tác của vật liệu. Kết quả khảo sát khi bổ sung các chất dập tắt AO, BQ, TB, DMSO vào môi trường phản ứng phân hủy RhB được thể hiện trên hình 3.49 và bảng 3.13.
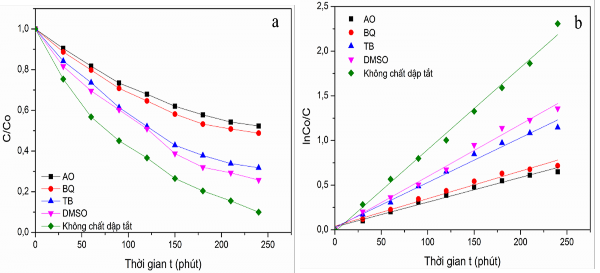
Hình 3.49. Hiệu suất quang xúc tác phân hủy RhB (a) và mô hình động học Langmuir-
Hinshelwood với các chất dập tắt của mẫu Mn-MoS2/rGO
(Điều kiện: CRhB = 20 mg/L, m xúc tác = 0,1g, 400 ml dung dịch RhB, đèn 60W-220V, pH=6,04)
Bảng 3.13. Hiệu suất quang phân hủy RhB và dữ liệu mô hình động học Langmuir - Hinshelwood với sự có mặt của các chất dập tắt của mẫu 3%Mn-MoS2/rGO.
AO | BQ | TB | DMSO | Không chất dập tắt | |
Hiệu suất (%) | 47,68 | 51,21 | 68,21 | 74,25 | 90,04 |
R2 | 0,983 | 0,978 | 0,987 | 0,990 | 0,993 |
k (phút-1) | 0,00277 | 0,00308 | 0,00501 | 0,00583 | 0,00919 |
Kết quả cho thấy, sự có mặt của chất bắt gốc tự do làm giảm đáng kể hiệu quả quang phân hủy RhB. Cụ thể, hiệu quả phân hủy RhB giảm từ 90,04% xuống
còn 74,25% khi có mặt DMSO, giảm nhiều hơn xuống 68,21% khi có mặt TB, và tiếp tục xuống 51,21% khi có mặt BQ. Nếu sử dụng chất dập tắt là AO, hiệu quả phân hủy RhB giảm còn một nửa (47,68%).
Trên cơ sở ảnh hưởng của các chất dập tắt này, cơ chế cho quá trình quang xúc tác phân hủy RhB trên xúc tác Mn-MoS2/rGO được đưa ra ở hình 3.50. Như đã đề cập ở mục khảo sát hoạt tính quang xúc tác của vật liệu MoS2/rGO (phần 3.3.2), có thể thấy rằng h+ và O2- đóng vai trò quan trọng hơn so với gốc OH và e- trong quá trình quang xúc tác phân hủy RhB.
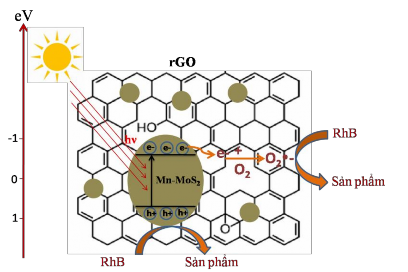
Hình 3.50. Mô hình cơ chế của quá trình quang xúc tác phân hủy RhB dưới vùng ánh sáng khả kiến của vật liệu 3%Mn-MoS2/rGO [110]
Theo mô hình cơ chế này, khi ánh sáng được hấp thụ bởi vật liệu xúc tác thì electron quang sinh từ vùng dẫn của Mn-MoS2 chuyển đến rGO. Sau đó, electron quang sinh sẽ phản ứng với phân tử O2 đã bị hấp phụ lên bề mặt của xúc tác để tạo thành gốc O2-. Những gốc O2- và các lỗ trống quang sinh (h+) phân hủy RhB. Trong quá trình này, rGO sẽ nhận và vận chuyển electron kích thích do cấu trúc liên hợp ![]() trong cấu trúc của vật liệu. Ngoài ra, Mn đóng vai trò như là chất nhận các
trong cấu trúc của vật liệu. Ngoài ra, Mn đóng vai trò như là chất nhận các
electron quang sinh từ MoS2 và vận chuyển electron làm hạn chế sự tái tổ hợp các
electron – lỗ trống quang sinh, dẫn đến tăng hiệu quả quang xúc tác của vật liệu. Quá trình quang xúc tác phân hủy RhB trên xúc tác Mn-MoS2/rGO có thể được mô tả bằng sơ đồ sau [110]:
Mn-MoS2/rGO + hν → Mn-MoS2(e- + h+)/rGO
Mn-MoS2(e- + h+)/rGO→ Mn-MoS2(h+)/rGO(e-) rGO(e-) + O2→ rGO + O2•-
Mn-MoS2(h+) + RhB → sản phẩm O2•- + RhB → sản phẩm
Ngoài mô hình cơ chế này, để hiểu rò hơn về tiến trình và sản phẩm của quá trình phân hủy RhB, dung dịch sau những khoảng thời gian phản ứng nhất định được phân tích xác định bằng phương pháp sắc ký lỏng ghép nối khối phổ (LC/MS). Trên cơ sở này, có thể đề xuất sự phân hủy của RhB trong điều kiện thí nghiệm thích hợp.
Từ phổ khối lượng có thể thấy, các sản phẩm phân hủy trung gian của RhB ứng với các giá trị m/z = 443, 399, 355, 311, 282 và 255. Con đường phân hủy của RhB bao gồm các quá trình: tách các nhóm etyl chứa N, sự phân cắt cấu trúc các hợp chất mang màu, sự mở vòng và sự khoáng hóa. Trong quá trình tách các nhóm etyl chứa N, các gốc ∙OH, O2•- và h+ sẽ tấn công cacbon trung tâm của phân tử RhB với mật độ điện tích âm cao [212],[213]. Dựa vào kết quả thu được và các công trình đã báo cáo trước đây [214],[215],[216], con đường phân hủy của RhB khi có mặt của xúc tác 3%Mn-MoS2/rGO được đề xuất trên hình 3.51.
Theo sơ đồ này, quá trình tách nhóm etyl chứa N và sự phân cắt cấu trúc các nhóm mang màu có thể xảy ra đồng thời. Sau đó, trong điều kiện môi trường phản ứng là hỗn hợp phức tạp với nhiều thành phần khác nhau, quá trình mở vòng diễn ra. Một số sản phẩm oxy hóa sơ cấp được tạo ra và bị phân hủy thêm thành các hợp chất có khối lượng nhỏ hơn. Theo các kết quả nghiên cứu của An và cộng sự [217], các hợp chất trung gian hình thành từ quá trình oxy hóa tiếp tục được khoáng hóa thành CO2, H2O, NO3- và NH4+.
N
O
N+
m/z = 443
OH
O
OH
O
O•
O
N
O
m/z = 399
N+
N
O
m/z = 399
N+
H N
2
O
m/z = 282
N+
H N
2
O
m/z = 282
N+
N+
O•
O
•
•
N+
N
O
m/z = 355
N+
N
O
m/z = 282
+
H
N 2
N
O
m/z = 282
+
H
N 2
N
COOH
O
m/z = 282
+
H
N 2
m/z = 355
•
N
O
m/z = 311
N+
HN COOH
O
+
NH2
m/z = 255
OH O
•
N O
m/z = 399
N
O
Quá trình tách nhóm alkyl chứa N, cacbonyl hóa, decacboxyl hóa và sự phân cắt các họp chất mang màu
Mở vòng
Các hợp chất có khối lượng phân tử nhỏ hơn
Quá trình khoáng hóa
CO2 + H2O + NO3- + NH4+
Hình 3.51. Con đường phân hủy của quá trình quang xúc tác phân hủy RhB trên xúc tác 3%Mn-MoS2/rGO dưới vùng ánh sáng khả kiến.
3.6. SO SÁNH ĐẶC TRƯNG CẤU TRÚC VÀ HOẠT TÍNH QUANG XÚC TÁC CỦA CÁC TỔ HỢP VẬT LIỆU
Để hiểu rò mức độ cải thiện hoạt tính quang xúc tác của vật liệu MoS2 qua các quá trình tạo compozit với rGO, biến tính với Mn, và chọn ra loại xúc tác thích hợp nhất cho quá trình quang phân hủy RhB, đặc trưng cấu trúc và hoạt tính xúc tác các tổ hợp MoS2, 3%Mn-MoS2, MoS2/rGO và 3%Mn-MoS2/rGO đã được so sánh.
3.6.1. Đặc trưng cấu trúc của các tổ hợp vật liệu
Đặc trưng cấu trúc thành phần pha bằng kỹ thuật XRD của các vật liệu MoS2, 3%Mn-MoS2, MoS2/rGO và 3%Mn-MoS2/rGO được thể hiện trên hình 3.52.
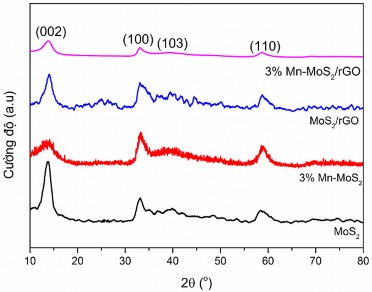
Hình 3.52. Giản đồ XRD của các mẫu vật liệu MoS2, 3%Mn-MoS2, MoS2/rGO và 3%Mn- MoS2/rGO
Kết quả ở hình 3.52 cho thấy các pic đặc trưng xuất hiện trong giản đồ nhiễu xạ của cả 4 loại vật liệu đều phù hợp với pha hexagonal của MoS2. Riêng các mẫu biến tính bằng Mn không thấy có pic nào đặc trưng thể hiện cho sự có mặt của nguyên tố này, chứng tỏ quá trình biến tính không làm thay đổi cấu trúc mạng lưới của MoS2. Mặt khác, mặt (002) của mẫu vật liệu khi biến tính Mn vào có cường độ thấp hơn và tù hơn so với mẫu MoS2 nguyên chất, cho thấy khoảng cách giữa các lớp được mở rộng khi tiến hành biến tính Mn vào MoS2 [218], dự đoán Mn đã được đưa vào thay thế một số vị trí của Mo trong các tinh thể của MoS2. Khi tổ hợp với rGO, cường độ của các pic đặc trưng cũng giảm là do có sự phân tán tốt của MoS2, Mn-MoS2 trên nền rGO.
Hình thái các mẫu vật liệu MoS2, 3%Mn-MoS2, MoS2/rGO và 3%Mn- MoS2/rGO được thể hiện qua ảnh SEM ở hình 3.53.