Bảng 3.1: Dữ liệu phổ 1H-NMR và 13C-NMR của quercetin bán tổng hợp và mẫu quercetin so sánh.
Quercetin (DMSO) 500 MHz | Quercetin so sánh 500 MHz [48] | |||
δC ppm | δH ppm (J,Hz) | δC ppm | δH ppm (J,Hz) | |
1 | - | - | ||
2 | 146.78 | - | 146.9 | - |
3 | 135.69 | - | 135.8 | - |
4 | 175.80 | - | 175.9 | - |
5 | 160.69 | - | 160.8 | - |
6 | 98.15 | 6.18 (1H, d, J = 2.0 Hz) | 98.2 | 6.18 (1H, d, J = 2.0 Hz) |
7 | 163.85 | - | 163.9 | |
8 | 93.32 | 6.40 (1H, d, J = 2.0 Hz) | 93.4 | 6.40 (1H, d, J = 2.0 Hz) |
9 | 156.11 | - | 156.2 | - |
10 | 102.98 | - | 103.1 | - |
1’ | 121.93 | - | 122.0 | - |
2’ | 115.04 | 7.67 (1H, d, J =2.5 Hz) | 115.1 | 7.67 (1H, d, J = 2.5 Hz) |
3’ | 145.02 | 6.89 (1H, d, J = 8.5 Hz) | 145.1 | 6.88 (1H, d, J = 8.5 Hz) |
4’ | 147.66 | - | 147.7 | - |
5’ | 115.57 | - | 115.7 | - |
6’ | 119.95 | 7.54(1H, dd, J = 7.5, 2.5Hz) | 120.0 | 7.54 (1H,dd, J = 7.5, 2.5Hz) |
Có thể bạn quan tâm!
-
 Tình Hình Nghiên Cứu Trong Nước Và Trên Thế Giới Về Phức Nano Của Β-Cyclodextrin.
Tình Hình Nghiên Cứu Trong Nước Và Trên Thế Giới Về Phức Nano Của Β-Cyclodextrin. -
 Rutin Thu Được Sau Tinh Chế Bằng Phương Pháp Acid-Base.
Rutin Thu Được Sau Tinh Chế Bằng Phương Pháp Acid-Base. -
 Khoảng Chuyển Dịch Hóa Học Các Dạng Carbon Chọn Lọc.
Khoảng Chuyển Dịch Hóa Học Các Dạng Carbon Chọn Lọc. -
![Phổ Hồng Ngoại Biến Đổi Fourier Của Quer (1), Hpβcd (2) Và Phức Hợp [Quer-Hpβcd] (3).](data:image/svg+xml,%3Csvg%20xmlns=%22http://www.w3.org/2000/svg%22%20viewBox=%220%200%2075%2075%22%3E%3C/svg%3E) Phổ Hồng Ngoại Biến Đổi Fourier Của Quer (1), Hpβcd (2) Và Phức Hợp [Quer-Hpβcd] (3).
Phổ Hồng Ngoại Biến Đổi Fourier Của Quer (1), Hpβcd (2) Và Phức Hợp [Quer-Hpβcd] (3). -
 Nghiên cứu tạo phức hợp bao của B-Cyclodextrin với một số Polyphenol định hướng ứng dụng trong y sinh - 9
Nghiên cứu tạo phức hợp bao của B-Cyclodextrin với một số Polyphenol định hướng ứng dụng trong y sinh - 9 -
 Nghiên cứu tạo phức hợp bao của B-Cyclodextrin với một số Polyphenol định hướng ứng dụng trong y sinh - 10
Nghiên cứu tạo phức hợp bao của B-Cyclodextrin với một số Polyphenol định hướng ứng dụng trong y sinh - 10
Xem toàn bộ 86 trang tài liệu này.
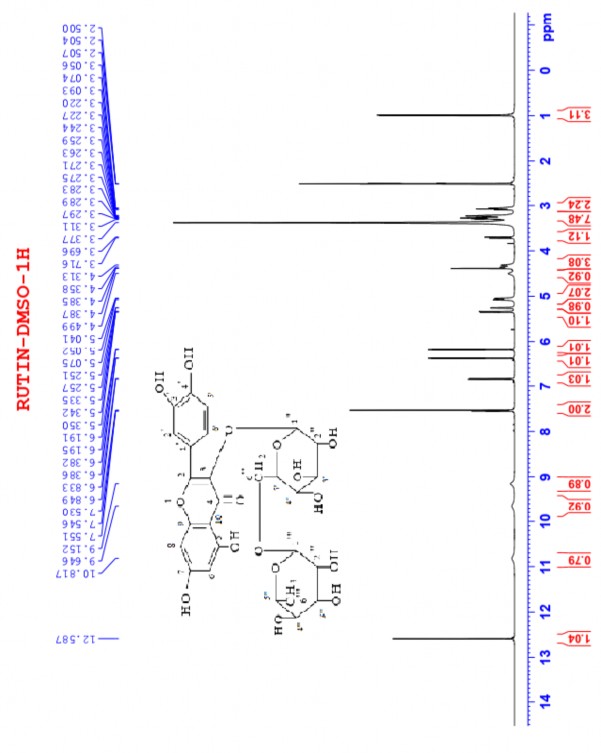
Hình 3.5: Phổ 1H-NMR của rutin.
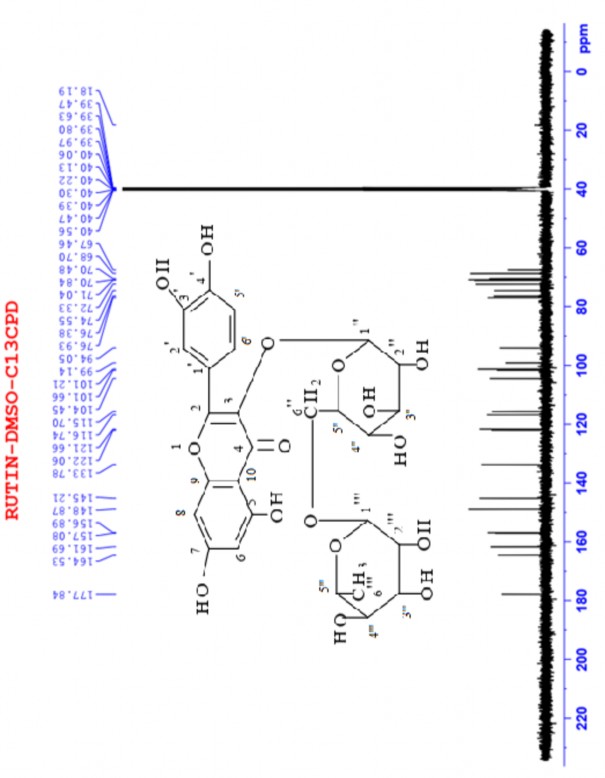
Hình 3.6: Phổ 13C-NMR của rutin.
Rutin được phân lập dưới dạng tinh thể màu vàng, nhiệt độ nóng chảy 214 - 215°C. Cấu trúc của rutin có thể được làm sáng tỏ bằng cách so sánh phổ của nó với phổ NMR của quercetin. Phổ 1H-NMR cho thấy tín hiệu của một vòng thơm chứa ba nhóm thế ở 7,55 (m, H-2', 6') và 6,84 (d, J = 8,0 Hz, H-5') và hai proton anomeric ở 5,34 (d, J = 7,5 Hz, glc H-1'') và 4,38 (d, J = 1,0 Hz, rham H- 1'''). Điều này được chứng minh rằng rutin có cùng loại aglycone như quercetin. Tuy nhiên, phổ 1H-NMR của mẫu rutin phân lập cho thấy sự hiện diện của tín hiệu proton của hai glycoside ở mức 3,71-3,05 (m, 12H của các gốc đường) và nhóm methyl ở 0,99 (3H, d, J = 6.0, rham-CH3). Phổ 13C-NMR của quercetin cho thấy tín hiệu của 27 nguyên tử cacbon, bao gồm 15 nguyên tử khung flavonoid và 12 nguyên tử của hai gốc đường của rutin (β-D-glucose: δC 101.3, 74.2, 76.5, 70.1, 76.0, 67.1 và α-L-
rhamnose: δC 104.0, 74.1, 71.9, 70.7, 70.5, 17.8). Việc so sánh dữ liệu phổ của của mẫu rutin phân lập với mẫu rutin so sánh khẳng định hợp chất phân lập được là rutin (quercetin-3-O- [α-L-rhamnopyranosyl-(1-6)-β-D glucopyranoside).
Bảng 3.2: Dữ liệu phổ 1H-NMR và 13C-NMR của rutin phân lập từ hoa hòe và mẫu rutin so sánh.
Rutin (DMSO) 500 MHz | Rutin so sánh 500 MHz [48] | |||
δC ppm | δH ppm (J,Hz) | δC ppm | δH ppm (J,Hz) | |
1 | - | - | ||
2 | 148.87 | - | 156.7 | - |
3 | 133.78 | - | 133.4 | - |
4 | 177.84 | - | 177.5 | - |
5 | 161.69 | - | 161.3 | - |
6 | 99.14 | 6.19 (1H, d, J = 2.0 Hz) | 98.8 | 6.19 (1H, d, J = 2.0 Hz) |
7 | 164.53 | - | 164.2 | |
8 | 94.05 | 6.38 (1H, d, J = 2.0 Hz) | 93.7 | 6.38 (1H, d, J = 2.0 Hz) |
9 | 156.89 | - | 156.5 | - |
10 | 101.66 | - | 104.0 | - |
1’ | 122.06 | - | 121.3 | - |
2’ | 115.70 | 7.55 (1H, d, J =2.5 Hz) | 115.3 | 7.54 (1H, d, J = 2.5 Hz) |
145.21 | 6.84 (1H, d, J = 8.5 Hz) | 144.8 | 6.84 (1H, d, J = 8.5 Hz) | |
4’ | 147.66 | - | 148.5 | - |
5’ | 115.70 | - | 116.4 | - |
6’ | 121.66 | 7.55(1H, dd, J = 7.5, 2.5Hz) | 121.7 | 7.54 (1H,dd, J = 7.5,2.5Hz) |
1’’ | 101.66 | 5.34 (1H, d, J = 7.0 Hz) | 101.3 | 5.34 (1H, d, J = 7.0 Hz) |
2’’ | 74.55 | 3,51 (1H, brs) | 74.2 | 3,51 (1H, brs) |
3’’ | 76.93 | 3,27 (1H, m) | 76.5 | 3,42 (1H, m) |
4’’ | 70.48 | 3,24 (1H, m) | 70.1 | 3,30 (1H, m) |
5’’ | 76.38 | 3,25 ( 1H, m) | 76.0 | 3,34 (1H, m) |
6’’ | 67.46 | 3,71 (1H, m) 3,69 (1H, m) | 67.1 | 3,84 (1H, m) 3,81 (1H, m) |
1’’’ | 99.14 | 4.39 (1H, brs) | 100.8 | 4.38 (1H, brs) |
2’’’ | 70.48 | 3,37 (dd, J1=1,5; J2= 5,0) | 70.5 | 3,65 (dd, J1=1,5; J2= 5,0) |
3’’’ | 70.84 | 3,31 (dd, J1= 3,5, J2= 13,0) | 70.7 | 3,55 (dd, J1= 3,5, J2= 13,0) |
4’’’ | 71.04 | 3,22 ( 1H, m) | 71.9 | 3,32 ( 1H, m) |
5’’’ | 68.70 | 3,29 (1H, m) | 68.3 | 3,47 (1H, m) |
6’’’ | 18.19 | 1.00 (3H, d, J = 6.0) | 17.8 | 1.0 3H, d, J = 6.0) |
3’
3.1.2. Kiểm nghiệm độ tinh sạch của rutin sau khi tinh chế

Hình 2.3: Các mẫu khảo sát tinh chế rutin bằng axit acetic (1: dung dịch rutin thô trong nước, rutin Đ/c : dung dịch rutin đối chứng trong nước)
Từ hình.. ta nhận thấy, màu sắc của các mẫu kết tủa rutin trong axit acetic ở nồng độ axit cao hơn (40-50%) giống màu sắc (vàng nhạt) của rutin sạch đối chứng. Ở nồng độ axit thấp hơn (10-20%), màu sắc kết tủa là màu trắng đục, có vẩn đen giống với rutin thô. Để khẳng định lại, thực hiện đo định tính xác định độ tinh sạch của rutin bằng phương pháp HPLC. Kết quả được trình bày trên hình…
Các mẫu rutin tinh chế bằng phương pháp axit-bazo được kết tủa trong axit acetic các nồng độ từ 10% đến 50% được kiểm độ tinh khiết bằng máy sắc ký lỏng hiệu năng cao (HPLC) số hiệu X500R-QTOF, hãng SCIEX.
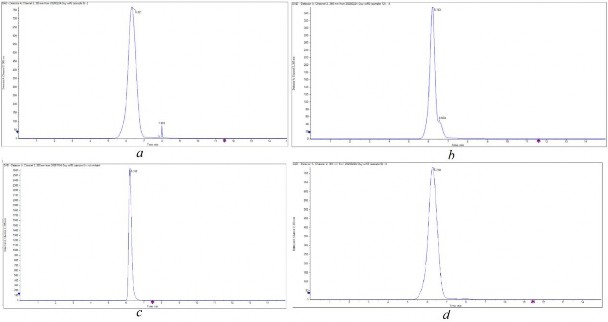
Hình 3.7: Phổ HPLC mẫu rutin tinh chế trong axit acetic (a: nồng độ axit acetic 20%; b: nồng độ axit acetic 30%; c: nồng độ axit acetic 40%; d: nồng độ axit acetic 50%).
Hình 3.7 thể hiện sắc ký đồ của các mẫu rutin. Trường hợp kết tủa rutin bằng axit acetic 20% (hình 3.7a) cho biết rutin sau tinh chế có độ tinh sạch 80.873% tính theo diện tích pic; ở nồng độ axit acetic 30% (hình 3.7b) cho biết rutin thu được có độ tinh khiết 91.115% tính theo diện tích pic. Đến sắc ký đồ hình 3.7c, rutin tinh chế bằng axit acetic nồng độ 40% cho độ tinh khiết 98.827% tính theo diện tích pic. Tuy nhiên, sắc ký đồ của mẫu rutin thu được từ quá trình kết tủa bằng axit acetic 50% (hình 3.7d) lại cho độ tinh khiết là 96.128% tính theo diện tích pic. Như vậy, nồng độ axit acetic 40% là nồng độ phù hợp nhất trong khoảng nghiên cứu để kết tủa rutin từ dung dịch rutin trong kiềm loãng.
HIỆU SUẤT TỔNG HỢP PHỨC CỦA β-CYCLODEXTRIN VỚI MỘT SỐ POLYPHENOL TRONG DUNG MÔI HỖN HỢP H2O-EtOH
Trong phương pháp đồng kết tủa, phân tử khách và phân tử chủ cần được hòa tan với nhau để tăng sự tiếp xúc. Cyclodextrin tan trong nước nhưng rutin và quercetin lại tan trong một số dung môi hữu cơ. Do đó, cần lựa chọn được dung môi thích hợp để cả cyclodextrin và các hoạt chất đều tan tốt, mặt khác lại dễ bay hơi để dễ dàng bị loại khỏi sản phẩm sau phản ứng. Bên cạnh đó, một số nghiên cứu trước đã chứng minh, khả năng tạo phức của các hợp chất hữu cơ với cyclodextrin tăng lên rò rệt khi cho thêm một lượng nhỏ nhất định dung môi hữu cơ vào nước [49]. Do đó, trong nghiên cứu này, dung môi hỗn hợp nước-cồn tuyệt đối được lựa chọn để điều chế các phức hợp.
Chúng tôi đã khảo sát hiệu suất phản ứng tổng hợp phức [RuTβCD] và [Quer- HPβCD] theo sự thay đổi hàm lượng ethanol trong dung môi hỗn hợp trong khoảng 0-50% (v/v). Các dung môi có hàm lượng ethanol lớn hơn 50% (v/v) không được khảo sát do độ tan của cyclodextrin trong ethanol rất kém [50]. Kết quả cụ thể được trình bày trong bảng 3.3.
Bảng 3.3: Hiệu suất tổng hợp phức cyclodextrin-polyphenol trong dung môi hỗn hợp EtOH-H2O.
0 | 10 | 15 | 20 | 25 | 30 | 40 | 50 | |
[RuT-βCD] | 25 | 73 | - | 56 | - | 50 | 46 | 41 |
[Quer-HPβCD] | 38 | 50 | 73 | 80 | 70 | 66 | - | 52 |
Từ bảng 3.3 ta nhận thấy, hiệu suất tổng hợp đối với cả hai loại phức hợp trong dung môi có chứa EtOH trong khoảng nghiên cứu đều lớn hơn giá trị tương ứng trong môi trường nước. Điều này có thể giải thích được bằng thuyết nhiệt động học
– solvat hóa [51]. Theo đó, sự có mặt của các phân tử ethanol là nguyên nhân chính làm giảm đi tính kị nước trong khoang rỗng của phân tử cyclodextrin, do đó gây nên sự khác biệt trong cấu trúc và nhiệt động lực học của dung môi hỗn hợp so với dung môi thuần, làm tăng lên khả năng cho phân tử khách “thâm nhập” vào bên trong khoang rỗng của phân tử “chủ”. Hiệu suất tổng hợp [RuT-βCD] và [Quer- HPβCD] đạt giá trị cực đại lần lượt bằng 73% và 80% trong những dung môi có
hàm lượng EtOH nhỏ (10-20%) có thể do sự tăng cường không gian ba chiều của các liên kết hydro khi bổ sung thêm dung môi hữu cơ vào nước [52]. Trong những dung môi có nồng độ EtOH lớn hơn 20% hiệu suất tổng hợp bị suy giảm, có thể là do độ tan của phức hợp trong môi trường hữu cơ tốt hơn làm cản trở lên quá trình thu hồi và do đó, giảm đi hiệu suất tổng hợp. Kết quả này cũng phù hợp với quan điểm mà tác giả Al-Nasiri và cộng sự đã đưa ra trong bài báo [53].
3.3.1 PHÂN TÍCH MỘT SỐ TÍNH CHẤT LÝ HÓA ĐẶC TRƯNG VÀ HÌNH THÁI CẤU TRÚC CỦA PHỨC HỢP β-CYCLODEXTRIN-POLYPHENOL
3.3.1 Kết quả phân tích phổ hồng ngoại
FTIR là một công cụ rất hữu ích để chứng minh phản ứng tạo phức dạng khách - chủ xảy ra bởi các dao động đặc trưng của phân tử "khách" sau phản ứng thường biến mất, bị dịch chuyển hoặc cường độ bị suy giảm [53,54].
2941
a
3431
2925
b
3425
1641
c
2929
3404
Maät đoä quang
1656
1598
1506
1455
1363
1294
1204
1062
1012
940
808
595
Hình 3.8 biểu diễn kết quả phân tích quang phổ hồng ngoại của rutin, β- cyclodextrin và phức hợp.
1652
1602
1506
1455
1363
1294
1417
1365
1331
1204
1158
1081
1031
1158
1081
1062
1031
940
857
754
709
1012
940
808
754
709
3500 3000 2500 2000 1500 1000 500
Soá soùng, cm-1
Hình 3.8: Phổ hồng ngoại của rutin (a), phức chất [RuT-βCD] (b) và βCD (c).




![Phổ Hồng Ngoại Biến Đổi Fourier Của Quer (1), Hpβcd (2) Và Phức Hợp [Quer-Hpβcd] (3).](https://tailieuthamkhao.com/uploads/2022/06/13/nghien-cuu-tao-phuc-hop-bao-cua-b-cyclodextrin-voi-mot-so-polyphenol-dinh-8-1-120x90.png)

