CHƯƠNG 2. NGUYÊN VẬT LIỆU VÀ PHƯƠNG PHÁP NGHIÊN CỨU
2.1. THIẾT BỊ VÀ DỤNG CỤ
2.1.1 Thiết bị
- Máy siêu âm (Saehan Sonic).
- Máy cất quay dung môi (SIBATA Model RE-10E-100).
- Máy khuấy từ gia nhiệt (Heating Magnetic Stirrer–VELP Scientifica).
- Máy đo phổ hồng ngoại biến đổi Fourier (Nicolet Nexus 670).
- Phổ kế cộng hưởng từ hạt nhân (AVANCE III-Bruker BioSpin- Viện Hóa học- Viện Hàn lâm Khoa học & Công nghệ Việt Nam).
- Máy đo nhiệt lượng kế vi phân (DSC, DSC204F1-NETZSCH-Germany).
- Kính hiển vi điện tử quét phát xạ trường (FE-SEM) số hiệu JSM-6510LV Jeol, Nhật Bản).
Có thể bạn quan tâm!
-
 Nghiên cứu tạo phức hợp bao của B-Cyclodextrin với một số Polyphenol định hướng ứng dụng trong y sinh - 2
Nghiên cứu tạo phức hợp bao của B-Cyclodextrin với một số Polyphenol định hướng ứng dụng trong y sinh - 2 -
 Các Phương Pháp Chiết Xuất Rutin Từ Hoa Hòe Và Điều Chế Quercetin
Các Phương Pháp Chiết Xuất Rutin Từ Hoa Hòe Và Điều Chế Quercetin -
 Tình Hình Nghiên Cứu Trong Nước Và Trên Thế Giới Về Phức Nano Của Β-Cyclodextrin.
Tình Hình Nghiên Cứu Trong Nước Và Trên Thế Giới Về Phức Nano Của Β-Cyclodextrin. -
 Khoảng Chuyển Dịch Hóa Học Các Dạng Carbon Chọn Lọc.
Khoảng Chuyển Dịch Hóa Học Các Dạng Carbon Chọn Lọc. -
 Dữ Liệu Phổ 1 H-Nmr Và 13 C-Nmr Của Quercetin Bán Tổng Hợp Và Mẫu Quercetin So Sánh.
Dữ Liệu Phổ 1 H-Nmr Và 13 C-Nmr Của Quercetin Bán Tổng Hợp Và Mẫu Quercetin So Sánh. -
![Phổ Hồng Ngoại Biến Đổi Fourier Của Quer (1), Hpβcd (2) Và Phức Hợp [Quer-Hpβcd] (3).](data:image/svg+xml,%3Csvg%20xmlns=%22http://www.w3.org/2000/svg%22%20viewBox=%220%200%2075%2075%22%3E%3C/svg%3E) Phổ Hồng Ngoại Biến Đổi Fourier Của Quer (1), Hpβcd (2) Và Phức Hợp [Quer-Hpβcd] (3).
Phổ Hồng Ngoại Biến Đổi Fourier Của Quer (1), Hpβcd (2) Và Phức Hợp [Quer-Hpβcd] (3).
Xem toàn bộ 86 trang tài liệu này.
- Tủ sấy thường, cân thường và cân vi lượng.
2.1.2 Dụng cụ
- Bình tam giác loại 50 mL, 100 mL, 250 mL.
- Bescher loại 50 mL, 100 mL, 250 mL.
- Ống hút, pipet, đũa thủy tinh, cá từ, lọ thủy tinh, chai đựng mẫu, ống đong 50 mL, 25 mL, 10 mL, 5 mL.
- Bình định mức 100 mL, 500 mL.
2.2. CHIẾT XUẤT, TINH CHẾ RUTIN TỪ HOA HÒE
Rutin được chiết xuất, tinh chế từ nụ hoa hòe theo sơ đồ sau:
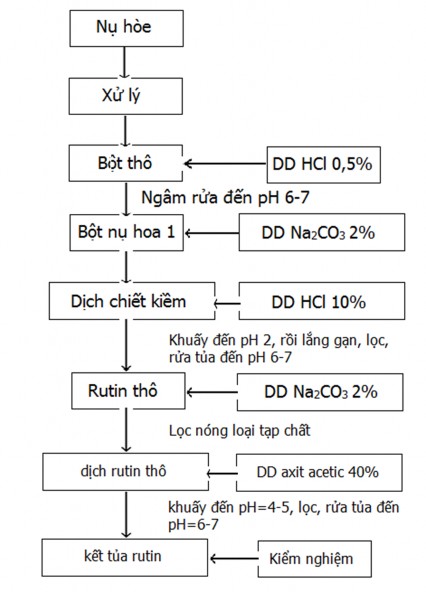
Hình 2.1: Sơ đồ chiết xuất, tinh chế từ nụ hoa hòe.
2.2.1 Phương pháp chiết xuất rutin
Hoa hòe sau khi thu hái được phơi khô trong bóng râm, sau đó sấy ở nhiệt độ 60-70oC đến khi khô hoàn toàn. Thực hiện chiết xuất rutin từ nụ hoa hòe bằng dung dịch kiềm Na2CO3 2%.
Phương pháp chiết xuất bằng dung dịch kiềm được thực hiện như sau: Rửa bằng HCl 0,5% rồi rửa bằng nước cho hết axit. Cho 100g hoa hòe đã giã dập vào 800 mL dung dịch Na2CO3 2%, đun sôi trong 30 phút. Đem lọc trên phễu Buchner thu dịch chiết; tiếp tục chiết thêm 1 lần với 500mL dung dịch Na2CO3 2%. Gộp hai
phần dịch chiết lại, dùng dung dịch HCl 10% điều chỉnh đến pH=2, để lạnh thấy xuất hiện kết tủa màu vàng. Lọc thu lấy kết tủa, sau đó rửa lại bằng nước cất đến khi pH=6-7. Sấy kết tủa thu được ở nhiệt độ 40-50oC trong 24h thu được sản phẩm thô.

Hình 2.2: Chiết xuất rutin trong Na2CO3 2%.
2.2.2 Tinh chế rutin
Sau khi thu được rutin thô từ các phương pháp chiết xuất rutin từ hoa hòe, tiến hành tinh chế trong các điều kiện và dung môi khác nhau dựa vào tính chất và độ tan của rutin. Hai phương pháp tinh chế được sử dụng trong nghiên cứu bao gồm: tinh chế rutin bằng cồn và tinh chế rutin bằng acid-base. Hiện nay, các nghiên cứu vẫn chủ yếu sử dụng axit HCl để kết tủa rutin trong dung dịch kiềm, tuy nhiên HCl có nhiều mặt hạn chế (độc hại, ăn mòn thiết bị…). Vì vậy, trong nghiên cứu này rutin được kết tủa bằng axit acetic để khắc phục những nhược điểm trên. Trong lĩnh vực dược phẩm, axit acetic là một trong số ít những axit được ưu tiên lựa chọn vì tính an toàn cho người trực tiếp sản xuất và người sử dụng.
Phương pháp tinh chế rutin bằng acid-bazo: Chuẩn bị 5 cốc thủy tinh chứa 100mL dung dịch Na2CO3 2%, đun đến sôi. Thêm từ từ rutin thô vào bình chứa
dung dịch Na2CO3 sôi đến khi đạt trạng thái bão hòa. Lọc các dung dịch qua phễu Buchner loại bỏ cặn và tạp chất, sau đó đun nóng ở 70oC. Chuẩn bị 5 cốc chứa dung dịch acid acetic ở các nồng độ 10%-20%-30%-40% và 50%, đun nóng đến 70oC. Thêm từ từ acid acetic các nồng độ vào lần lượt từng bình chứa dung dịch rutin đến khi đạt pH=4-5. Khuấy lắc mạnh đến khi xuất hiện tủa màu trắng đục. Để nguội dung dịch đến nhiệt độ phòng, lọc qua phễu Buchner thu kết tủa; rửa lại kết tủa bằng nước cất đến pH=6-7 thu được rutin sạch. Sấy khô ở nhiệt độ 40-45oC thu được sản phẩm.

Hình 2.2: Rutin thu được sau tinh chế bằng phương pháp acid-base.
2.3. BÁN TỔNG HỢP QUERCETIN
Sau khi thu được rutin tinh khiết, tiến hành bán tổng hợp quercetin bằng dung dịch HCl nồng độ thấp. Đây là phương pháp đơn giản, các điều kiện thực hiện không yêu cầu kỹ thuật cao; tuy nhiên thiết bị thực hiện cần có khả năng chống acid ăn mòn.
Phương pháp bán tổng hợp quercetin : chuẩn bị 10g rutin tinh cho vào bình cầu chứa 100ml dung dịch HCl có nồng độ 5%. Tiến hành đun sôi cách thủy các bình cầu, có hồi lưu dung môi. Sau 2h, rutin trong dung dịch HCl 5% đã chuyển
hóa toàn bộ thành quercetin, kiểm tra quá trình biến đổi bằng phương pháp sắc ký bản mỏng.
Phương pháp tinh chế quercetin: hòa tan quercetin thu được trong 50ml cồn 96o đun sôi, thêm từ từ 100 ml nước cất vào dung dịch đến khi xuất hiện kết tủa. Giữ bình ổn định ở điều kiện thường trong 1h đến khi nhiệt độ bình bằng nhiệt độ phòng. Lọc qua phễu lọc Buchner thu kết tủa màu vàng xanh, rửa tủa với nước cất lạnh thu được quercetin tinh.

Hình 2.4: Quercetin thu được sau tinh chế.
2.4. TỔNG HỢP PHỨC NANO CỦA Β-CYCLODEXTRIN VỚI RUTIN VÀ QUERCETIN
Dung dịch cyclodextrin được thêm vào các dung dịch chứa RuT và Quer, mỗi lần 10 mL và được khuấy bằng máy khuấy từ trong 24 giờ ở 25oC. Hỗn hợp dung dịch sau phản ứng được lưu giữ trong vòng 48h ở 4oC để tạo kết tủa màu vàng mịn. Kết tủa được rửa nhiều lần với DMSO và được đem đi đông khô trong vòng 48 giờ.
2.5. CÁC PHƯƠNG PHÁP NGHIÊN CỨU
2.5.1 Phương pháp phổ hồng ngoại biến đổi Fourier
Các phức hợp [RuT-βCD], [Quer-HPβCD] được phân tích cấu trúc bằng phổ hồng ngoại biến đổi Fourier (FTIR) trên máy Nicolet Nexus 670 bằng cách ép viên
với KBr. Các mẫu được quét phổ ở vùng 400 cm-1 – 4000 cm-1. Phổ FTIR được ghi dưới dạng đường cong phụ thuộc phần trăm truyền qua vào số sóng (1/λ) sau khi đã bù trừ phổ nền của không khí. Các hoạt chất và cyclodextrin cũng được phân tích đồng thời để đối chứng. Trong hỗn hợp với KBr, hàm lượng của các mẫu đều bằng 6% khối lượng.
2.5.2 Phương pháp sắc ký lớp mỏng TLC
Sắc ký lớp mỏng là kỹ thuật tách các chất được tiến hành khi cho pha động di chuyển qua pha tĩnh đã đặt sẵn hỗn hợp chất cần phân tích. Pha tĩnh là chất hấp phụ được lựa chọn tùy theo yêu cầu phân tích, được trải mỏng đồng nhất và được cố định trên các phiến kính hoặc kim loại. Pha động là một hệ dung môi đơn hoặc đa thành phần được trộn với nhau theo tỷ lệ nhất định tùy theo mục đích cụ thể. Trong quá trình di chuyển qua lớp hấp phụ, các cấu tử trong hỗn hợp mẫu thử được di chuyển trên lớp mỏng theo hướng pha động, với những tốc độ khác nhau. Kết quả, ta thu được một sắc ký đồ trên lớp mỏng.
Rf = ![]()
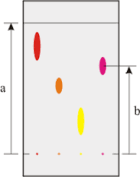
Hình 2.5: Cách tính giá trị Rf.
Đại lượng đặc trưng cho mức độ di chuyển của chất phân tích là hệ số di chuyển Rf được tính bằng tỷ lệ giữa khoảng dịch chuyển của chất thử và khoảng dịch chuyển của dung môi (Hình 2.5).
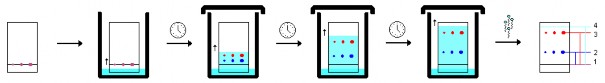
Các bước tiến hành định tính RuT và Quer bằng sắc ký lớp mỏng (Hình 2.6):
Chuẩn bị bản mỏng:Bản mỏng sử dụng trong nghiên cứu là bản mỏng tráng sẵn silica gel Merck 60 F254, kích thước 20×20 cm, dày 0,2 mm. Bản mỏng trước
khi dùng phải hoạt hóa trong tủ sấy và sấy ở 105-110°C trong một giờ. Dùng bút chì mềm kẻ bản mỏng. Vạch đường chấm chất phân tích (cách mép dưới của bản mỏng 1,2 cm), đường giới hạn di chuyển của dung môi (cách mép trên của bản mỏng 0,8 cm) và đánh dấu vị trí chấm chất (các vết chấm cách nhau 0,5 cm và cách hai bờ bên của bản mỏng ít nhất 1 cm).
Chấm chất phân tích lên bản mỏng:Dùng ống mao quản hoặc micropipet chấm dung dịch RuT và Quer lên các vị trí đã đánh dấu. Các vết chấm phải nhỏ, lượng chất phải đồng đều, không quá lớn dễ kéo vết hoặc chồng vết, cũng không quá nhỏ khó hiện vết bằng thuốc thử.
Triển khai sắc ký:Bình triển khai thường là bình thủy tinh, có nắp đậy kín và đáy phải bằng. Lót giấy lọc xung quanh thành trong của bình. Pha hệ dung môi với tỷ lệ thích hợp và vừa đủ, rót vào bình triển khai. Hệ dung môi triển khai đối với rutin: Ethyl acetate-methanol: 7-3, hệ dung môi triển khai đối với quercetin: hexane-ethanol: 4-6. Lắc rồi để giấy lọc thấm đều dung môi. Đặt bản mỏng gần như thẳng đứng với bình triển khai, các vết chấm phải ở trên bề mặt của lớp dung môi triển khai. Đậy kín bình và để yên ở nhiệt độ không đổi. Khi dung môi chạy đến đường giới hạn, lấy bản mỏng ra khỏi bình và sấy khô bản mỏng rồi hiện vết.
Hiện vết trên bản mỏng:Có thể hiện vết bằng cách soi UV (bước sóng 254 và 365 nm) hoặc phun thuốc thử (thuốc thử dùng trong nghiên cứu là Ce(SO4)2).
hương pháp phổ cộng hưởng từ hạt nhân 1H-NMR, 13C
Hình 2.6: Các bước tiến hành sắc ký bản mỏng.
2.5.3 P -NMR
Mẫu rutin và quercetin thu được từ quá trình chiết xuất và bán tổng hợp được xác định cấu trúc bằng phương pháp phổ cộng hưởng từ hạt nhân 1H-NMR và 13C-
NMR bằng phổ kế cộng hưởng từ hạt nhân AVANCE III, hãng Bruker BioSpin, Thụy Sĩ.
Phổ 1H-NMR cho biết môi trường hoá học của proton trong phân tử. Các proton có môi trường hoá học khác nhau sẽ có chuyển dịch hoá học khác nhau, thường nằm trong khoảng 0 – 14 ppm (Hình 2.7).
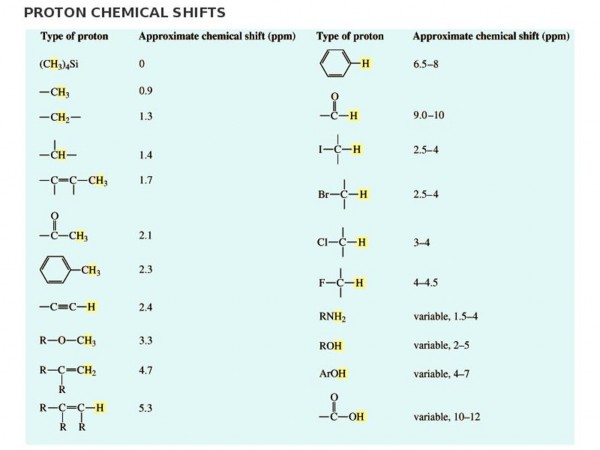
Hình 2.7: Khoảng chuyển dịch hóa học của một số proton.
Phổ 13C-NMR cung các cấp thông tin về môi trường hoá học của carbon. Độ chuyển dịch của carbon nằm trong khoảng 0 – 240 ppm (Hình 2.8). Đây là ưu điểm rất lớn của phổ 13C-NMR vì các tín hiệu phổ sẽ ít bị trùng lặp và đặc trưng đối với mỗi chất. Với kỹ thuật đo phổ hiện tại, phổ NMR của carbon là những vạch đơn, mỗi vạch ứng với 1 carbon (hơn 1 carbon nếu chúng có chung môi trường hoá học) của phân tử.



![Phổ Hồng Ngoại Biến Đổi Fourier Của Quer (1), Hpβcd (2) Và Phức Hợp [Quer-Hpβcd] (3).](https://tailieuthamkhao.com/uploads/2022/06/13/nghien-cuu-tao-phuc-hop-bao-cua-b-cyclodextrin-voi-mot-so-polyphenol-dinh-8-1-120x90.png)