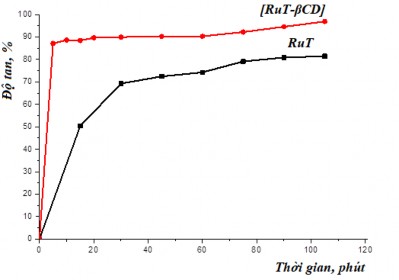
Hình 3.15: Phần trăm hòa tan của RuT và phức [RuT-βCD] theo thời gian trong môi trường pH 7,4.
Từ hình 3.15 có thể thấy, tại tất cả các thời điểm rút mẫu, phức có độ hòa tan tốt hơn rutin thuần. Ở phút thứ 5 sau khi hòa tan, độ tan của phức đã đạt được giá trị hơn 85% và đạt giá trị lớn nhất 97% trong khoảng thời gian nghiên cứu. Ngược lại, độ tan lớn nhất của rutin ở dạng tự do là 78% sau 110 phút. Như vậy, việc tạo phức nano với β-cyclocdextrin đã cải thiện rò rệt độ tan của rutin.
3.3.6. Kết quả xác định khả năng bắt gốc tự do DPPH của rutin và phức hợp [RuT-HPβCD]
Khả năng bắt gốc tự do DPPH của các mẫu ở các nồng độ khác nhau được trình bày trên hình 3.16.
Từ hình 3.16 ta nhận thấy, theo sự tăng dần nồng độ từ 0,5 µg/ml – 14
µg/ml, tỉ lệ % bắt gốc tự do DPPH của rutin và phức hợp tăng dần. Ở cùng một nồng độ, % khả năng bắt gốc tự do DPPH của phức hợp cao hơn rutin thuần. Với nồng độ 14 µg/ml, tỉ lệ % khả năng bắt gốc tự do của rutin và phức hợp lần lượt là 67% và 75%. Các phương trình hồi quy đơn giản thể hiện mối tương quan giữa tỉ lệ
% hoạt tính bắt gốc tự do DPPH và các nồng độ của dược chất được xây dựng dựa vào phần mềm Origin. Trên cơ sở đó, phương trình được chọn là phương trình có
hệ số tương quan và tương quan hiệu chỉnh cao nhất với độ tin cậy > 95%. Từ phương trình này ta xác định được giá trị IC50 của rutin và phức hợp là giá trị nồng độ của dược chất, mà tại đó % khả năng bắt gốc tự do DPPH đạt được là 50%. Kết quả được trình bày trong bảng 3.4.
[RuT-CD]
RuT
80
Hoaït tính choáng oxi hoùa, %
70
60
50
40
30
20
10
0 2 4 6 8 10 12 14
CRuT, g/ml
Hình 3.16: Đồ thị biểu diễn mối tương quan giữa % bắt gốc tự do DPPH của rutin và phức [RuT-HPβCD] theo giá trị nồng độ của rutin.
Bảng 3.5: Phương trình tương quan giữa % bắt gốc tự do DPPH và nồng độ dược chất của rutin và phức hợp và giá trị IC50 tương ứng.
Phương trình tương quan | Hệ số hồi quy | Giá trị IC50, µg/ml | |
RuT | y=3,2346+5,63x | 0,996 | 8,31 |
[RuT-HPβCD] | y=11,54+5,287x | 0,995 | 7,27 |
Có thể bạn quan tâm!
-
 Khoảng Chuyển Dịch Hóa Học Các Dạng Carbon Chọn Lọc.
Khoảng Chuyển Dịch Hóa Học Các Dạng Carbon Chọn Lọc. -
 Dữ Liệu Phổ 1 H-Nmr Và 13 C-Nmr Của Quercetin Bán Tổng Hợp Và Mẫu Quercetin So Sánh.
Dữ Liệu Phổ 1 H-Nmr Và 13 C-Nmr Của Quercetin Bán Tổng Hợp Và Mẫu Quercetin So Sánh. -
![Phổ Hồng Ngoại Biến Đổi Fourier Của Quer (1), Hpβcd (2) Và Phức Hợp [Quer-Hpβcd] (3).](data:image/svg+xml,%3Csvg%20xmlns=%22http://www.w3.org/2000/svg%22%20viewBox=%220%200%2075%2075%22%3E%3C/svg%3E) Phổ Hồng Ngoại Biến Đổi Fourier Của Quer (1), Hpβcd (2) Và Phức Hợp [Quer-Hpβcd] (3).
Phổ Hồng Ngoại Biến Đổi Fourier Của Quer (1), Hpβcd (2) Và Phức Hợp [Quer-Hpβcd] (3). -
 Nghiên cứu tạo phức hợp bao của B-Cyclodextrin với một số Polyphenol định hướng ứng dụng trong y sinh - 10
Nghiên cứu tạo phức hợp bao của B-Cyclodextrin với một số Polyphenol định hướng ứng dụng trong y sinh - 10
Xem toàn bộ 86 trang tài liệu này.
Từ bảng 3.5 ta nhận thấy sau khi tạo phức hoạt tính chống oxi hóa của rutin đã tăng lên rò rệt: giá trị IC50 đã giảm từ 8,31 xuống 7,27 µg/ml. Như vậy, việc tạo phức nano với cyclodextrin đã cho thấy những kết quả khả quan trong việc cải thiện độ tan và sinh khả dụng của dược chất.
CHƯƠNG 4. KẾT LUẬN VÀ KIẾN NGHỊ
4.1 KẾT LUẬN
-Trong nghiên cứu này, rutin được chiết xuất bằng dung dịch Na2CO3 2% và tinh chế bằng axit axetic ở các nồng độ khác nhau trong khoảng 10-50%, quercetin thu được từ rutin và tinh chế trong cồn 960. Kết quả phân tích sắc ký bản mỏng, phổ cộng hưởng từ hạt nhân và sắc ký lỏng hiệu năng cao cho thấy rutin thu được có dạng bột màu vàng, độ tinh khiết đạt được giá trị cực đại 98,83% khi tinh chế bằng axit axetic 40%; quercetin có dạng bột màu vàng xanh, độ sạch cao.
˗ Phức chất giữa rutin với β-cyclodextrin và quercetin với hydroxypropyl-β- cyclodextrin đã được tổng hợp thành công trong dung môi hỗn hợp nước-cồn tuyệt đối bằng phương pháp đồng kết tủa. Hiệu suất tổng hợp phức trong dung môi hỗn hợp tại tất cả các điểm nghiên cứu đều lớn hơn giá trị tương ứng trong môi trường nước. Giá trị hiệu suất đạt cực đại 73% và 80% trong dung môi có hàm lượng EtOH 15-20% v/v.
˗ Kết quả nghiên cứu đặc trưng phức chất bằng các phương pháp FTIR, UV- Vis, DLS, DSC và phân tích hình thái cấu trúc vật liệu FESEM cho thấy có sự dịch chuyển và suy giảm rất mạnh các dao động đặc trưng cho liên kết C=C, O-H và C- O-H trong phân tử rutin, chứng tỏ một phần phân tử rutin đã chui vào bên trong khoang rỗng của phân tử chất mang; đỉnh nội nhiệt của rutin trong phức đã giảm đi đáng kể cả về cường độ và nhiệt độ; kích thước hạt khá đồng đều với đường kính ~ 50-60 nm.
˗ Sự khác biệt chủ yếu trong quang phổ IR của phức [Quer-HPβCD] so với Quer thuần và HPβCD là: dải dao động hóa trị của liên kết O-H trong phức (3424 cm-1) mở rộng hơn so với dao động tương ứng trong HPβCD; các dao động hóa trị của liên kết carbonyl thơm đặc trưng trong quercetin chuyển sang vùng có số sóng
ngắn hơn 1646 cm-1 cùng với việc suy giảm cường độ rò rệt, chứng tỏ liên kết C=O đã tham gia vào việc tạo phức. Kết quả DSC cho thấy, Đỉnh nội nhiệt của Quer trong phức đã giảm đi rò rệt và gần như biến mất (1330C).
˗ Kết quả xây dựng giản đồ pha của quá trình hòa tan cho thấy, trong nước rutin và quer tạo phức với CD theo tỷ lệ stoichometric 1:1, độ tan của của các dược chất tăng lên đáng kể và phụ thuộc tuyến tính vào nồng độ của CD trong dung dịch.
˗ Độ tan của rutin và phức hợp theo thời gian đã được khảo sát. Tại tất cả các điểm rút mẫu, độ tan của phức đều cao hơn độ tan của rutin thuần.
˗ Khả năng bắt gốc tự do DPPH của phức hợp cao hơn của rutin thuần. Cụ thể, hoạt tính chống oxi hóa của rutin sau khi tạo phức đã tăng lên rò rệt: giá trị IC50 đã giảm từ 8,31 xuống 7,27 µg/ml.
4.2 KIẾN NGHỊ
Từ những kết quả nghiên cứu thu được chúng tôi nhận thấy:
˗ Việc sử dụng axit axetic để tinh chế rutin hoàn toàn có thể thay thế được axit HCl với độ tinh sạch lên đến >98%. Hơn nữa việc sử dụng axit axetic có ưu điểm an toàn với người lao động, không độc hại lại không gây tổn hao về thiết bị, máy móc, do đó cần nghiên cứu trên quy mô rộng hơn.
˗ Việc tăng độ tan của các hoạt chất không những do phức hợp tạo thành mà kích thước hạt cũng ảnh hưởng đáng kể. Do đó, việc tạo phức nano có kích thước ổn định, nhỏ hơn sẽ được quan tâm trong các nghiên cứu tiếp theo.
˗ Độ tan, khả năng bắt gốc tự do của quercetin và phức [Quer-HPβCD] cần được nghiên cứu.
TÀI LIỆU THAM KHẢO
1. Peng Z.F., Strackb D., Baumert A. et al, Antioxidant flavonoids from leaves of Polygonum hydropip L, Phytochem, 2003 (62): 219-504.
2. A. N. Panche, A. D. Diwan and S. R. Chandra, Flavonoids: an overview. Journal of Nutritional Science (2016), vol. 5, e47, page 1-15. doi:10.1017/jns.2016.41.
3. Satyendra et al, A review of quercetin: Antioxidant and anticancer properties, World Journal of Pharmacy and Pharmaceutical Sciences, Volumee 11, Issue 1, 146-160.
4. Ross JA, Kasum CM, Dietary flavonoids: bioavailability, metabolic effects, and safety, Annu Rev Nutr 2002;22:19-34.
5. Hollman PC, Bijsman MN, van Gameren Y, et al, The sugar moiety is a major determinant of the absorption of dietary flavonoid glycosides in man, Free Radic Res 1999;31:569-573.
6. Hosseinzadeh H, Nassiri-Asl M, Review of the protective effects of rutin on the metabolic function as an important dietary flavonoid, J Endocrinol Invest. 2014; 37: 783–788.
7. Salvamani S, Gunasekaran B, Shaharuddin NA, Ahmad SA, Shukor MY, Antiartherosclerotic effects of plant flavonoids, Biomed Res Int 2014. 2014: 480258.
8. Sultana B, Anwar F, Flavonols (Kaempeferol, quercetin, myricetin) contents of selected fruits, vegetables and medicinal plants, Food Chem. 2008; 108:879–84.
9. Lakhanpal P, Rai DK, Quercetin: A versatile flavonoid, Int J Med Update, 2007; 2:22–37.
10. Akan Z, Garip AI, Antioxidants may protect cancer cells from apoptosis signals and enhance cell viability, Asian Pac J Cancer Prev, 2013; 14:4611–4.
11. Vásquez-Garzón VR, Arellanes-Robledo J, García-Román R, Aparicio- Rautista DI, Villa-Treviđo S, Inhibition of reactive oxygen species and pre- neoplastic lesions by quercetin through an antioxidant defense mechanism, Free Radic Res. 2009; 43:128–37.
12. Johari J, Kianmehr A, Mustafa MR, Abubakar S, Zandi K, Antiviral activity of baicalein and quercetin against the Japanese encephalitis virus, Int J Mol Sci. 2012; 13:16785–95.
13. Cushnie TP, Lamb AJ, Antimicrobial activity of flavonoids. Int J Antimicrob Agents, 2005; 26:343–56.
14. Ramos FA, Takaishi Y, Shirotori M, Kawaguchi Y, Tsuchiya K, Shibata H, et al, Antibacterial and antioxidant activities of quercetin oxidation products from yellow onion (Allium cepa) skin, J Agric Food Chem. 2006; 54:3551–7.
15. Coles LS. Quercetin: A Review of Clinical Applications, Available
: http://www.chiro.org/nutrition/ABSTRACTS/Quercetin_A_Review.shtml.
16. P. Stanley Mainzen Prince, N. Kamalakkannan, Rutin improves glucose homeostasis in streptozotocin diabetic tissues by altering glycolytic and gluconeogenic enzymes, J. Biochem. Mol. Toxicol, 20 (2) (2006), pp. 96-102
17. N. Kamalakkannan, P.S. Prince, Antihyperglycaemic and antioxidant effect of rutin, a polyphenolic flavonoid, in streptozotocin-induced diabetic wistar rats, Basic Clin. Pharmacol. Toxicol., 98 (1) (2006), pp. 97-103
18. J. Nones, A.P. Costa, R.B. Leal, F.C. Gomes, A.G. Trentin, The flavonoids hesperidin and rutin promote neural crest cell survival, Cell Tissue Res., 350 (2) (2012), pp. 305-315
19. C.F. Gonçalves, M.C. Santos, M.G. Ginabreda, R.S. Fortunato, D.P. Carvalho, A.C. Freitas Ferreira, Flavonoid rutin increases thyroid iodide uptake in rats, PLoS One, 8 (9) (2013), p. e73908
20. Nguyễn Hoàng Hợp (2002). Nghiên cứu kỹ thuật chiết xuất rutin từ hoa hòe (Sophora japonica L. Fabaceae). Khóa luận tốt nghiệp dược sĩ. Đại học Dược Hà Nội.
21. Beatriz Gullon et al. Rutin: A review on extraction, identification and purification methods biological activities and approaches to enhance its bioavailability. Trends in Food Science & Technology 67 (2017) 220-235
22. Jinwoo Yang et al. Conversion of Rutin to Quercetin by Acid Treatment in Relation to Biological Activities. Prev Nutr Food Sci. 2019 Sep; 24(3): 313–320
23. A. Magnúsdóttir, M. Másson and T. Loftsson, J. Incl. Phenom. Macroc. Chem. 44, 213-218, 2002.
24. Del Valle EMM (2004), Cyclodextrins and their uses: a review, Process Biochem. 39: 1033-1046.
25. K. Miyake, H. Arima, F. Hirayama, M. Yamamoto, T. Horikawa, H. Sumiyoshi, S. Noda, K. Uekama, Improvement of solubility and oral bioavailability of rutin by complexation with 2-hydroxypropyl-beta-cyclodextrin, Pharm. Dev. Technol. 5(3) (2000) 399–407. DOI: 10.1081/pdt-100100556
26. S. Shuang, J. Pan, S. Guo, M. Cai, C. Liu, Fluorescence study on the inclusion complexes of rutin with β-cyclodextrin, hydroxypropyl-β-cyclodextrin and γ-cyclodextrin, Anal. Lett. 30(12) (1997) 2261–2270. DOI: 10.1080/00032719708001737
27. I.M. Savic, I.M. Savic-Gajic, V.D. Nikolic, B.L. Nikolic, B.C. Radovanovic, A. Milenkovic-Andjelkovic, Enhencemnet of solubility and photostability of rutin by complexation with β-cyclodextrin and (2-hydroxypropyl)- β-cyclodextrin, J. Incl. Phenom. Macrocycl. Chem. 86 (2016) 33–43. DOI 10.1007/s10847-016-0638-8
28. Azat Bilalov, Jonas Carlstedt et al, DNA with amphiphilic counterions: tuning colloidal DNA with cyclodextrin, Soft Matter, 2012, 8, 4988–4994
29. Sylvan G. Frank. Inclusion Compounds. Journal of Pharmaceutical sciences.Vol. 64, No. 10, October 1975. 1585-1604
30. Patil J.S. et al, Inclusion complex system; A novel technique to improve the solubility and bioavailability of poorly soluble drugs: A review, International Journal of Pharmaceutical Sciences Review and Research, Volume 2, Issue 2, May
– June 2010; Article 006, 29-34. ISSN 0976 – 044X
31. Nerome H., Machmudah S., Wahyudiono et al. Nanoparticle formation of lycopene/β-cyclodextrin inclusion complex using supercritical antisolvent precipitation. The Journal of Supercritical Fluids. 2013 (83): 97-103.
32. Khalid Q., Ahmad M., Minhas M. U. Synthesis of β-cyclodextrin hydrogel nanoparticles for improving the solubility of dexibuprofen; Characterization and Toxicity Evaluation. Drug Development and Industrial Pharmacy, 2017. DOI:10.1080/03639045.2017.1350703.
33. Coneac G., Gafiţanu E., Hădărugă N. G. et al. Quercetin and rutin/2- hydroxypropyl-β-cyclodextrin nanoparticles: obtaining, characterization and antioxidant activity. Journal of Agroalimentary Processes and Technologies. 2009 (15) (3): 441-448
34. Bùi Quang Thuật. Nghiên cứu công nghệ tạo hương liệu bột từ cyclodextrin, Tạp chí Khoa học và Công nghệ, 2010, 48, 67-69
35. Nguyễn Ngọc Sao Mai, Nguyễn Thanh Hải, Vò Thụy Cẩm Vy, Huỳnh Văn Hóa. Nghiên cứu điều chế và đánh giá phức hợp piroxicam-cyclodextrin. Tạp chí Dược học, 2009, 5, 19-23.
36. Tiêu Vĩnh Thuận, Phạm Đình Duy, Huỳnh Văn Hóa. Tối ưu hóa quy trình sản xuất viên nén chứa phức piroxicam-beta cyclodextrin bằng thiết kế thực nghiệm. Tạp chí Y học TP Hồ Chí Minh, 2010, 1, 169-173.
37. Phùng Đức Truyền, Nguyễn Phước Trường, Huỳnh Văn Hóa, Đặng Văn Tịnh. Nghiên cứu điều chế hệ phân tán rắn hydroxybutyl-beta-cyclodextrin làm tăng độ tan của rutin. Tạp chí Dược học, 2013, 442, 53, 23-27.


![Phổ Hồng Ngoại Biến Đổi Fourier Của Quer (1), Hpβcd (2) Và Phức Hợp [Quer-Hpβcd] (3).](https://tailieuthamkhao.com/uploads/2022/06/13/nghien-cuu-tao-phuc-hop-bao-cua-b-cyclodextrin-voi-mot-so-polyphenol-dinh-8-1-120x90.png)
