* Phẫu thuật sữa chữa toàn phần là mở rộng đường ra thất phải và đóng kín lỗ thông liên thất bằng miếng vá màng ngoài tim. Hai đường phẫu thuật chính là qua nhĩ phải/động mạch phổi và qua thất phải, có hay không sử dụng miếng vá mở rộng đường ra thất phải (transannular patch) và có thể sử dụng van động mạch phổi nhân tạo [25], [42].
* Chạy THNCT với máy SARNS 8000 (Terumo - Nhật) sử dụng bơm con lăn và bộ oxy hóa màng (Air/ Oxygen Mixer sê-ri 3500/ 3500 HL) của hãng Sechrist (Hoa Kỳ).
* Liều heparin trước khi đặt canule THNCT là 300 UI/kg (3 mg/kg), duy trì thời gian đông máu hoạt hóa (activated clotting time) > 400 giây.
* THNCT sử dụng dịch mồi gồm ringer lactat, canxi, dịch keo và / hoặc albumin, huyết tương tươi đông lạnh (FFP) và heparin liều trung bình 200 UI/kg để chạy mồi. Thể tích mồi tính theo trọng lượng: < 10 kg: 300 mL, từ 10 - < 20 kg: 500 mL, 20 - 40 kg: 800 mL và > 40 kg: 1000 mL. Tốc độ truyền ban đầu từ 2,00 - 2,40 L/m2/phút theo trọng lượng. Trường hợp trẻ nhỏ hoặc hematocrit thấp, bổ sung 1 - 2 đơn vị khối hồng cầu để duy trì hematocrit trong THNCT từ 25 - 30%.
* Hạ nhiệt sâu (< 27oC), trung bình (27 - 32oC) hoặc nhẹ (> 32oC) [198].
* Liệt tim bằng dung dịch liệt tim của hãng Mayne Pharma Pty Ltd, Úc.
* Hematocrit được duy trì > 25%. Trong quá trình chạy THNCT, nếu máu bị hòa loãng nhiều (hematocrit xuống thấp hơn nhiều dưới 25%) hoặc nghi do dung dịch liệt tim vào tuần hoàn ngoài cơ thể (cân bằng nước vào > ra), bệnh nhân được lọc máu một lần bằng bộ lọc máu để loại bớt dịch và các ion thừa.
* Sau khi ngừng THNCT, heparin được trung hòa bằng protamin sulfat với liều 1,3 mg/kg cân nặng.
* Các xét nghiệm theo dõi điều trị chống đông trong THNCT:
Trong phẫu thuật, theo dõi nồng độ heparin (chuẩn) máu bằng xét
nghiệm thời gian đông máu hoạt hóa tại phòng mổ với thời gian > 400 giây (nồng độ heparin 200 - 300 UI/kg).
Ngoài thời gian phẫu thuật, theo dõi heparin bằng thời gian thromboplastin từng phần hoạt hóa tại phòng xét nghiệm đông máu của Trung tâm Huyết học Truyền máu - Bệnh viện Trung ương Huế.
* Máu thu hồi từ máy có thể truyền lại cho bệnh nhân sau phẫu thuật.
- Điều trị và chăm sóc sau phẫu thuật
+ Điều trị sau phẫu thuật: sử dụng dịch truyền glucose 10%, kali clorua 10% (bù theo điện giải đồ), các dung dịch keo, FFP, kháng sinh cephalosporin thế hệ III, ranitidin, giảm đau bằng acetaminophen và diclofenac, furosemid nếu tiểu ít, ... Nếu bệnh nhân đau nhiều, kích thích có thể giảm đau gây ngủ bằng morphin phối hợp với mydazolam. Hỗ trợ tuần hoàn bằng các thuốc trợ tim mạch và / hoặc vận mạch: dopamine, dobutamine, epinephrine, norepinephrine, milrinone qua bơm tiêm điện nếu cung lượng tim thấp.
+ Chăm sóc và theo dõi sau phẫu thuật
* Theo dõi các dấu hiệu sinh tồn như mạch, nhiệt, huyết áp, lượng nước tiểu, ... qua monitoring hoặc được đo bởi điều dưỡng.
* Máu dẫn lưu ngực được đo hằng giờ sau phẫu thuật bởi điều dưỡng Khoa Hồi sức tim. Nếu chảy máu quá mức, rối loạn đông máu được xử lý:
†) Sử dụng protamin liều thấp từ 10 - 20 mg, điều chỉnh theo thời gian thromboplastin từng phần hoạt hóa, nhưng thường theo kinh nghiệm nên không thử lại xét nghiệm này.
†) Truyền 125 - 500 mL FFP nếu thời gian thời gian thromboplastin từng phần hoạt hóa > 50 giây (1,5 lần giá trị bình thường của Labo Huyết học).
†) Truyền huyết tương giàu tiểu cầu hoặc máu tươi toàn phần hoặc khối tiểu cầu khi 2 biện pháp trên không cải thiện hoặc khi tiểu cầu giảm thấp < 100 x 106 /L [113].
* Theo dõi diễn biến và các biến chứng sau phẫu thuật.
2.2.6.2. Quy trình xét nghiệm và thăm dò chức năng
- Mẫu nghiệm
+ Mẫu máu: trước phẫu thuật lấy máu ở tĩnh mạch, sau phẫu thuật lấy ở catheter động mạch (bỏ 5 mL đầu vì hòa loãng và có chứa heparin) bảo đảm đúng tiêu chuẩn xét nghiệm Huyết học, Hoá sinh và Miễn dịch.
+ Mẫu bệnh phẩm vi sinh: theo tiêu chuẩn xét nghiệm vi sinh.
- Xét nghiệm và thăm dò chức năng
Tất cả bệnh nhân được xét nghiệm và thăm dò chức năng với cùng một nhóm chuyên phục vụ phẫu thuật tim tại Bệnh viện Trung ương Huế.
Các xét nghiệm bao gồm xét nghiệm thường quy, xét nghiệm MD và các xét nghiệm bổ sung khác như cấy vi sinh vật, … Các xét nghiệm thường quy được thực hiện và trả kết quả sớm. Tuy nhiên, đối với xét nghiệm cytokine, mẫu huyết thanh thường được bảo quản đông lạnh sâu để xét nghiệm thành từng đợt.
2.2.7. Xử lý số liệu
- Số liệu thu thập được ghi vào bệnh án nghiên cứu theo mẫu thống nhất
(phụ lục 1), mã hóa và nhập bằng phần mềm Excel 2007.
- Xử lý số liệu bằng 3 phần mềm: SPSS 10.05 (Statistical Package for Social Science, SPSS Inc., Chicago, IL), Epi info 6.04 và Medcalc 10.4.8.
- Xử lý số liệu theo phương pháp thống kê y học:
+ Kết quả các biến định lượng được trình bày theo giá trị trung bình và độ lệch chuẩn (X ± SD) hoặc phân nhóm và trình bày theo tỉ lệ phần trăm như các biến định tính.
+ So sánh 2 số trung bình: sử dụng test "t" hoặc test t Student.
+ So sánh các tỉ lệ bằng test χ2, đọc kết quả bằng test chính xác của Fisher hoặc test hiệu chỉnh Yates.
+ Trường hợp không phân phối chuẩn như interleukin:
* Sử dụng thuật toán logarit đưa mẫu về phân phối chuẩn để kiểm định sự khác biệt thống kê và tính tương quan.
Ngoài ra, để kiểm định thêm sự khác biệt, sử dụng các test phi tham số:
* Số liệu interleukin được trình bày dưới dạng trung vị (median) và khoảng tứ phân vị 25% - 75%.
* Kiểm định sự khác biệt hai trung vị bằng phép kiểm định test Mann-Whitney (test U).
* Kiểm định sự khác biệt trong 1 nhóm: sử dụng test Wilcoxon.
+ Sự khác biệt có ý nghĩa thống kê khi p < 0,05.
+ Khảo sát mối tương quan giữa hai biến định lượng: sử dụng hệ số tương quan Pearson (r).
Mức độ tương quan giữa hai biến định lượng được đánh giá như sau:
* | r | > 0,7 : tương quan rất chặt chẽ
* 0,5 < | r | ≤ 0,7 : tương quan khá chặt chẽ
* 0,3 ≤ | r | ≤ 0,5 : tương quan mức độ vừa
* | r | < 0,3 : tương quan rất ít
* 0 < r < + 1 : tương quan thuận
* -1 < r < 0 : tương quan nghịch [17].
Tuy nhiên, do interleukin không phân phối chuẩn nên mối tương quan được tính bằng tương quan Spearman (rs).
+ Tìm yếu tố nguy cơ:
* Phân tích đơn biến (univariable test):
Sử dụng bảng 2 x 2 để tính toán yếu tố nguy cơ dựa vào các đặc tính của biến: có / không đối với biến định tính hoặc dựa vào ngưỡng cắt (cut-off points) của các biến định lượng. Tính tỷ suất chênh (OR), ý nghĩa thống kê với hai biến định tính với khoảng tin cậy (CI) 95%. Nếu OR < 1: biến phân tích có tính bảo vệ, trái lại nếu OR > 1: biến phân tích là yếu tố nguy cơ.
* Phân tích đa biến (multivariable test):
Qua phân tích đơn biến, chọn các biến số (các yếu tố nguy cơ trước, trong và sau phẫu thuật) có ý nghĩa thống kê (p < 0,05) và đưa vào phép hồi quy logistic để tìm tỷ suất chênh hiệu chỉnh (adjusted OR), nhằm xác định các yếu tố nguy cơ độc lập của một biến định tính.
+ Giá trị dự đoán SIRS, MODS, nhiễm trùng và tử vong của một số xét nghiệm như CRP, IL-6, IL-10, glucose, số lượng BC, BCTT và tế bào lympho hoặc điểm số SIRS và MODS cũng được tính toán.
Các giá trị bao gồm độ nhạy, độ đặc hiệu, giá trị dự đoán dương tính và âm tính của các tham số được tính toán để dự đoán kết quả và vẽ đường cong ROC (receiver - operating characteristics).
Diện tích dưới đường cong (areas under curves) có ý nghĩa trong giới hạn từ 0,5 - 1,0 với khoảng tinh cậy (CI) 95%. Diện tích dưới đường cong ROC càng gần 1 càng có ý nghĩa.
2.2.8. Vấn đề y đức trong nghiên cứu
Nghiên cứu này được sự chấp thuận của Hội đồng Y Đức và Hội đồng Khoa học Kỹ thuật - Bệnh viện Trung ương Huế.
- Đối với nhóm tiến cứu
Vào thời điểm bắt đầu tiến hành nghiên cứu, GC đã được sử dụng thường quy nên chúng tôi chỉ tiến hành thu thập mẫu nghiên cứu theo quy trình điều trị thường quy của cơ sở điều trị và không đặt ra vấn đề đồng thuận tham gia nghiên cứu (phụ lục 1).
- Đối với nhóm hồi cứu
Do bệnh nhân đã xuất viện nên việc nghiên cứu được chấp thuận bởi Hội đồng Y Đức và Hội đồng Khoa học Kỹ thuật - Bệnh viện Trung ương Huế và cũng không đặt ra vấn đề đồng thuận tham gia nghiên cứu.
CHƯƠNG 3
KẾT QUẢ NGHIÊN CỨU
3.1. ĐẶC ĐIỂM CHUNG CỦA MẪU NGHIÊN CỨU
3.1.1. Đặc điểm lâm sàng
Bảng 3.1. Đặc điểm chung trước phẫu thuật
GC (n = 63) | KGC (n = 81) | p | |
Nam (n, %) | 46 (73,0%) | 42 (51,9%) | 0,010 |
Nữ (n, %) | 17 (27,0%) | 39 (48,1%) | |
Tuổi (năm) | 7,08 ± 8,18 | 9,25 ± 7,08 | 0,091 |
Cân nặng (kg) | 15,85 ± 10,37 | 20,30 ± 12,57 | 0,025 |
Thiếu oxy (tím) (n, %) | 28 (44,4%) | 45 (55,6%) | 0,240 |
Thể nặng (n, %) | 7 (11,1%) | 16 (19,8%) | 0,226 |
Có thể bạn quan tâm!
-
 Thang Điểm Glasgow Đánh Giá Bệnh Nhân Hôn Mê
Thang Điểm Glasgow Đánh Giá Bệnh Nhân Hôn Mê -
 Các Dấu Hiệu Sống Và Các Biến Xét Nghiệm Theo Nhóm Tuổi
Các Dấu Hiệu Sống Và Các Biến Xét Nghiệm Theo Nhóm Tuổi -
 Nghiệm Pháp Miễn Dịch Hóa Phát Quang Định Lượng
Nghiệm Pháp Miễn Dịch Hóa Phát Quang Định Lượng -
 Sự Biến Đổi Interleukin-6, Interleukin-10 Và Mối Liên Quan Với Các Đặc Điểm Lâm Sàng Và Cận Lâm Sàng
Sự Biến Đổi Interleukin-6, Interleukin-10 Và Mối Liên Quan Với Các Đặc Điểm Lâm Sàng Và Cận Lâm Sàng -
 Tương Quan Của Il-6 Và Il-10 Sau Phẫu Thuật Ở Nhóm Tiến Cứu
Tương Quan Của Il-6 Và Il-10 Sau Phẫu Thuật Ở Nhóm Tiến Cứu -
 Tác Dụng Đối Với Một Số Điều Trị Sau Phẫu Thuật Liên Quan Đến Đáp Ứng Viêm Toàn Thân
Tác Dụng Đối Với Một Số Điều Trị Sau Phẫu Thuật Liên Quan Đến Đáp Ứng Viêm Toàn Thân
Xem toàn bộ 171 trang tài liệu này.
Nhận xét: nhóm GC có xu hướng nhỏ tuổi hơn nhóm KGC nên trọng lượng thấp hơn có ý nghĩa thống kê so với nhóm KGC (p < 0,05). Tỷ lệ nam cao hơn nữ có ý nghĩa thống kê trên toàn mẫu (p < 0,05).
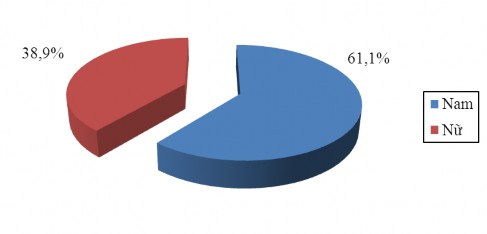
Biểu đồ 3.1. Tỷ lệ bệnh nhân tứ chứng Fallot theo giới Nhận xét: tỷ lệ nam cao hơn nữ có ý nghĩa thống kê (p < 0,05)
Bảng 3.2. Đặc điểm chung trong phẫu thuật
GC (n = 63) | KGC (n = 81) | p | |
Hạ nhiệt (0C) | 30,86 ± 1,90 | 29,30 ± 2,48 | < 0,001 |
THNCT (phút) | 131,37 ± 30,74 | 121,60 ± 22,77 | 0,030 |
Kẹp động mạch chủ (phút) | 80,68 ± 17,03 | 68,63 ± 17,24 | < 0,001 |
Thời gian phẫu thuật (phút) | 255,48 ± 39,41 | 246,91 ± 37,43 | 0,185 |
Đường phẫu thuật qua nhĩ phải/động mạch phổi (n, %) | 56 (88,9%) | 52 (64,2%) | 0,001 |
Đường phẫu thuật qua thất phải (n, %) | 7 (11,1%) | 29 (35,8%) | 0,001 |
Lọc máu (1 lần) (n, %) | 22 (34,9%) | 38 (46,9%) | 0,174 |
Nhận xét:
- Nhóm GC ít hạ nhiệt trong phẫu thuật hơn nhóm KGC nhưng có thời gian THNCT và thời gian kẹp động mạch chủ dài hơn nhóm KGC (p < 0,05).
- Nhóm GC được phẫu thuật qua đường nhĩ phải/ động mạch phổi nhiều hơn nhóm KGC và ngược lại, nhóm KGC được phẫu thuật qua đường thất phải nhiều hơn nhóm GC (p < 0,05).
3.1.2. Đặc điểm cận lâm sàng
Bảng 3.3. Phân suất tống máu thất trái trước và sau phẫu thuật
Ngày | GC (n = 63) | KGC (n = 81) | p | |
Phân suất tống máu thất trái (%) | N0 | 63,52 ± 2,48 | 64,02 ± 2,57 | 0,241 |
N1 | 62,49 ± 4,31 | 63,02 ± 5,09 | 0,512 |
Nhận xét:
Chức năng thất trái không khác biệt giữa 2 nhóm trước và sau phẫu thuật.
Bảng 3.4. Các biến số hồng cầu trước và sau phẫu thuật
Ngày | GC (n = 63) | KGC (n = 81) | p | |
Hồng cầu (x 1012/L) * | N0 | 5,96 ± 0,95 | 6,23 ± 1,21 | 0,145 |
N1 | 4,57 ± 0,69 | 4,91 ± 0,82 | 0,010 | |
Hemoglobin (g/dL) * | N0 | 15,64 ± 3,04 | 16,86 ± 3,38 | 0,026 |
N1 | 12,33 ± 1,83 | 13,63 ± 2,33 | < 0,001 | |
Hematocrit (%) * | N0 | 48,53 ± 9,09 | 51,70 ± 10,24 | 0,055 |
N1 | 37,94 ± 5,82 | 40,71 ± 6,94 | 0,012 |
*) So sánh N0 với N1 trong mỗi nhóm: p < 0,05
Nhận xét:
- Trước phẫu thuật (N0): nhóm KGC có xu hướng đa hồng cầu hơn nhóm GC.
- Sau phẫu thuật (N1): tất cả các biến số hồng cầu đều giảm rõ rệt so với trước phẫu thuật ở cả hai nhóm (p < 0,05). Tuy nhiên, nhóm GC có các biến số hồng cầu thấp hơn có ý nghĩa thống kê so với nhóm KGC (p < 0,05).






