CÁC PHƯƠNG PHÁP ĐỊNH LƯỢNG TRONG PHÂN TÍCH THỰC PHẨM 2
PHƯƠNG PHÁP LẤY MẪU TRONG PHÂN TÍCH THỰC PHẨM 13
CÁC KỸ THUẬT CHUẨN BỊ MẪU TRONG PHÂN TÍCH THỰC PHẨM. 25 CÁC PHƯƠNG PHÁP XÁC ĐỊNH HÀM LƯƠNG NƯỚC TRONG THỰC PHẨM 77
CÁC PHƯƠNG PHÁP XÁC ĐỊNH HÀM LƯỢNG PROTEIN TRONG THỰC PHẨM 93
PHƯƠNG PHÁP XÁC ĐỊNH GLUXIT TRONG THỰC PHẨM 119
CÁC PHƯƠNG PHÁP XÁC ĐỊNH LIPID 134
CÁC PHƯƠNG PHÁP ĐỊNH LƯỢNG TRONG PHÂN TÍCH THỰC PHẨM
1.1 VAI TRÒPHÂN TÍCH THỰC PHẨM
Việc kiểm nghiệm chất lượng thực phẩm nói riêng và và sản phẩm nói chungphục vụ cho rất nhiều mục đích, như là:
Có thể bạn quan tâm!
-
 Phân tích thực phẩm - Lê Nhất Tâm - 2
Phân tích thực phẩm - Lê Nhất Tâm - 2 -
 Những Điểm Lấy Mẫu Khi Mẫu Ở Dạng Lỏng
Những Điểm Lấy Mẫu Khi Mẫu Ở Dạng Lỏng -
 Kỹ Thuật Vô Cơ Hóa Ướt (Xử Lý Ướt)
Kỹ Thuật Vô Cơ Hóa Ướt (Xử Lý Ướt)
Xem toàn bộ 176 trang tài liệu này.
Đối với công tác kiểm tra, cấp giấy chứng nhận chất lượng thì việc kiểm nghiệm chất lượng để đưa đến quyết định chấp nhận lô hàng hoặc từ chối cấp chứng nhận cho lô hàng.
Trong sản xuất, quản lý chất lượng, nghiên cứu phát triển sản
phẩm: đánh giá chất lượng sản phẩm là để nhận biết mức chất
lượng của sản phẩm đạt được so với tiêu chuẩn qui định (về cảm quan, thành phẩm dinh dưỡng và vi sinh) nhằm điều chỉnh những sai
xót, tìm hiểu nguyên nhân gây ra, để thời đảm bảo chất lượng sản phẩm.
có biện pháp chấn chỉnh kịp
Kiểm nghiệm còn nhằm xác định chính xác chất lượng sản phẩm, trên cơ sở đó phân loại, xếp hạng sản phẩm đúng yêu cầu của từng mặt hàng.
Cung cấp số liệu về chất lượng thực phẩm phục vụ cho công tác quản lý nhà nước.
Người ta đã đưa ra nhiều phương pháp để đánh giá các khía cạnh
khác nhau về chất lượng sản phẩm. Một số phương pháp chỉ thích hợp cho mục đích này mà không thích hợp cho mục đích khác.
Tùy theo yêu cầu kiểm tra mà người ta chọn phương pháp thích hợp để đạt được độ tin cậy cao nhất. Các phương pháp kiểm nghiệm đã được áp dụng bao gồm: phương pháp cảm quan, phương pháp hoá học, phương pháp vi sinh vật.
1.2 CÁC PHƯƠNG PHÁP PHÂN TÍCH TRONG PHÂN TÍCH THỰC PHẨM
Phân tích thực phẩm phải xuất phát từ việc lựa chọn phương pháp phân tích. Vì thế, lựa chọn phương pháp là mắt xích đầu tiên trong quy trình phân tích, nó có ý nghĩa quan trọng.
Hiện nay, các phương pháp định lượng được sử dụng trong phân tích
được chia thành hai nhóm phương pháp đó là nhóm các phương pháp hóa học (gọi tắt là phương pháp hóa học) và nhóm các phương pháp hóa lý (gọi tắt là phương pháp hóa lý).
Những tiêu chí được sử gồm:
dụng để
lựa chọn phương pháp phân tích bao
Độ đúng của phương pháp
Độ chính xác của phương pháp
Tính chuyên biệt của phương pháp
Kích cỡ mẫu
Trang thiết bị
Tính kinh tế
Tính an toàn và độ độc hại
Tốc độ và tính cấp thiết của công việc
1.2.1 Phương pháp hóa học
Phương pháp hóa học còn được gọi là phương pháp cổ điển không chỉ vì nó là phương pháp dựa trên phản ứng hóa học để định lượng cấu tử mà đó
còn là nhóm những phương pháp được sử phương pháp hóa lý.
dụng sớm hơn so với những
Phương pháp hóa học lại được chia thành hai phương pháp nhỏ đó là
phương pháp khối lượng và phương pháp thể tích thông qua việc cân hay đo
chính xác khối lượng hay thể
tích cấu tử
hay thuốc thử
cần xác định.
Phương pháp hoá học được sử dùng để phân tích xác định hàm lượng lớn (đa lượng) của các chất, thông thường lớn hơn 0.05%
Phương pháp phân tích khối lượng: dựa vào việc cân sản phẩm tạo
thành sau quá trình thực hiện phản lượng cấu tử cần phân tích như:
Phương pháp bay hơi
Phương pháp kết tủa
ứng tạo kết tủa từ
đó xác định hàm
Phương pháp phân tích thể tích: Dựa vào việc đo chính xác thể tích
dung dịch thuốc thử có nồng độ phân tích bao gồm:
chính xác để
tính hàm lượng cấu tử
cần
Phương pháp chuẩn độ axit – bazo
Phương pháp chuẩn độoxy hóa – khử
Phương pháp chuẩn độ kết tủa
Phương pháp chuẩn độ phức chất
Cơ sở chung của phương pháp phân tích thể tích:
Dựa vào bản chất của phản ứng để xây dựng phương pháp
Sử dụng những lý thuyết liên quan để xây dựng phương pháp
Dùng định luật đương lượng làm cơ sở việc tính toán
Dùng chất chỉ thị màu để nhận biết điểm cuối
Các quá trình trong phương pháp thể tích chủ yếu là thao tác bằng tay và sự quan sát bằng mắt của người thực hiện nên sự mất mát xảy ra là tương đối lớn vì vậy để tránh sai số thì lượng phân tích thường lớn. Để xác định
điểm tương đương người ta dùng chất chỉ thị màu cho vào vì vậy, độ nhạy của phương pháp không cao.
1.2.2 Phương pháp hóa lý
Phương pháp hóa lý còn được gọi là phương pháp hiện đại. Phương
pháp này được sử dụng khi cần yêu cầu độ chính xác cao, yêu cầu tốc độ phân tích nhanh chống hoặc khi hàm lượng cấu tử cần phân tích nhỏ. Cơ sở của phương pháp dựa trên tính chất hóa lý của cấu tử để xác định chúng.
Phương pháp hóa lý được phân chia dựa trên tính chất được sử dụng để
xác định cấu tử đó là: phương pháp quang phổ, phương pháp điện, và
phương pháp sắc ký.
Trong giáo trình này, chúng tôi chỉ đề cập đến phương pháp quang phổ UV – Vis trong phân tích định lượng.
1.3 PHƯƠNG PHÁP QUANG PHỔ
Phương pháp quang phổ
là phương pháp hóa lý, dựa trên sự
tương tác
giữa bức xạ điện từ và vật chất (nguyên tử, phân tử). Khi có sự tương tác với vật chất, bức xạ điện từ sẽ hấp thụ hoặc phát xạ mà bức xạ được ứng dụng trong thiết bị quang phổ hấp thụ hay quang phổ bức xạ tương ứng.
Bức xạ
điện từ
bao gồm một dải các sóng điện từ
có bước sóng dao
động trong một khoảng rộng từ bước sóng rất nhỏ như tia gamma (λ = 1016
– 108m) đến bước sóng rất dài như
sóng radio (λ
= 100 – 108m). Bức xạ
điện từ là tổ hợp dao động của điện trường và từ trường vuông góc nhau, lan truyền trong không gian như sóng ngang. Do vậy mà bức xạ điện từ vừa có bản chất của sóng, lại vừa mang bản chất của hạt.
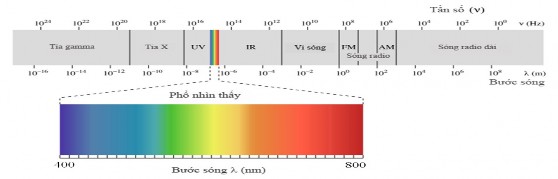
Hình 1.1. Bước sóng dải bức xạ điện từ
Năng lượng phân tử hay nguyên tử là tổng các dạngnăng lượng:
E = Eđt+Edđ+ Eq
Eđt: Năng lượng điện tử của phân tử
Edđ: Năng lượng do những dao động gây bởi tươngtác giữa các nguyên tử trong phân tử.
Eq: Năng lượng do sự quay của các phân tử chungquay trong trục nào đó của nó.
Ở điều kiện bình thường, các phân tử tồn tại ở trạng thái bền vững, có mức năng lượng thấp – trạng thái cơ bản Eo. Khi chiếu chùm bức xạ điện từ vào môi trường vật chất sẽ xảy ra hiện tượng hấp thu hoặc bức xạ năng lượng. Khi đó điện tử sẽ dịch chuyển lên trạng thái có năng lượng lớn hơn gọi là trạng thái kích thích.
Như
vậy khi xảy ra tương tác, năng lượng của phân tử sẽ
thay đổi
(ΔE≠0, với ΔE=E2E1).Nếu năng lượng phân tử thay đổi thì phân tử hấp thu (nếu ΔE>0) hoặc bức xạ năng lượng (nếu ΔE<0). Mỗi phân tử chỉ hấp thu hay phát xạ chọn lọc các bức xạ điện từ có tần số hay bước sóng nhất định. Là đây chính là cơ sở của phương pháp quang phổ nói chung.
Các dạng chuyển dịch điện tử: ![]() ,
, ![]() ,
,![]() ,
, ![]()
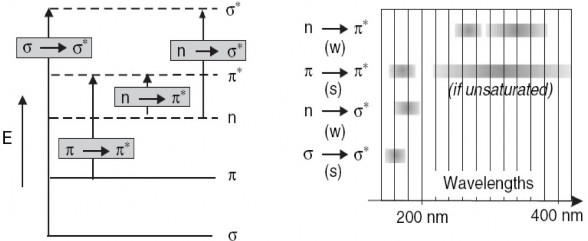
Hình 1.2 Các dạng chuyển mức điện tử
Chuyển mức ![]()
Sự chuyển vị của electron trong liên kết σ của các hợp chấthữu cơ từ
orbital liên kết σ lên phản liên kết σ*.Sự chuyển vị này đòi hỏi năng lượng khá lớn, vìvậy quá trình chuyển vị nằm trong vùng tử ngoại xa. Đó là vùng có bước sóng ngắn, năng lượng lớn.
Chuyển mức n → σ*
Sự chuyển vị
của các điện tử từ
obital n lên cácorbital
σ* trong các
nguyên tử như O, N, S. Chuyển mức này xảy ra ở vùng phổ tử ngoại gần có năng lượng khônglớn. Sự dịch chuyển này dao động ở 180nm với alcol còn vớidẫn xuất halogen của nó là 190nm. Đối với các aminlà 220nm. Cụ thể: Ete có λmax= 190nm (ε =2000), Metanol có λmax= 183nm (ε =50), Etylamin có λmax= 210 nm (ε =800).
Chuyển mức n→ π*
Điện tử từ orbital không liên kết n lên orbital phản liênkết π*.Đây là quá trình thường xảy ra trong phân tử có một nguyêntử chứa điện tử không liên
kết như ở
những phân tử
chứanhóm chức cacbonyl (C=O) và bước sóng
hấp thu 270nm 295nm. Bản chất của các dung môi có ảnh hưởng đến
bước sónghấp thu vì nó tác động đến liên kết trong phân tử.
Chuyển mức π→π*
Các hợp chất đồng phân với etylen chứa liên kết đôi trongphân tử có khả năng hấp thu mạnh trong vùng bướcsóng 170nm. Vị trí hấp thu phụ thuộc
vào sự
hiện diện của nhóm thế
vídụ
etylen có λmax= 165nm (ε
=16000).
Những hợp chất không màu thường có phổ hấp thu trongvùng cận tử ngoại. Khi chúng hấp thu bức xạ thì chúng sẽchuyển tới trạng thái thông qua cơ
chế
chonhận điện tử.Lúc này điện tử
từ orbital cho điện tử
sẽ chuyển
lênorbital nhận điện tử tạo thành những ion hay có sự phâncực trong phân tử.
Chuyển mứcd→d
Sự chuyển mức xảy ra
ở các orbital d, nhất là ở
các kimloại vùng
chuyển tiếp. Các phối tử có cặp điện tử tự do tham gia lai hóa vớinhững
orbital này chuyển điện tử
vào các orbital này gâyra sự
chuyển mức.Màu
tạo ra của các phức làm cho phức có khả năng hấpthu những bước sóng ở
vùng khả kiến.
Những yếu tố ảnh hưởng đến sự chuyển mức: sự liên hợp, dung môi, pH...
Ảnh hưởng của dung môi Bước sóng hấp thu và cường độ
hấp thu của các hợpchất chịu
ảnh
hưởng của dung môi.Sự tác động của những dung môi khác nhau lên
cácphân tử làm thay đổi mức năng lượng giửa các trạng tháikích thích và cơ