61. Liu D. F., Zhang Y. and Yang C. D. (2010), Method for extracting and separating monotropein from radix morindae officinalis, China.
62. The Metabolomics Innovation Centre, monotropein, https://hmdb.ca/metabolites/HMDB0035608
63. The Metabolomics Innovation Centre (TMIC), nystose, https://hmdb.ca/metabolites/HMDB0039176
64. MedchemExpress (2020), Nystose, Medchem Express, USA, https://www.medchemexpress.com.
65. Merck - Sigma Aldrich (2020), Monotropein, Merck - Sigma Aldrich, https://www.sigmaaldrich.com.
66. Merck - Sigma Aldrich (2020), Nystose, Merck - Sigma Aldrich, https://www.sigmaaldrich.com.
67. Nair R. R. et al (2012), "Molecular distinction of two closely resembling Morinda species using rbcL and matK loci for quality management of Indian herbal medicines", Plant Genetic Resources, 11(1), pp. 90-93.
68. National Center for Biotechnology Information, https://www.ncbi.nlm.nih.gov.
69. Neuhaus H., Link G. (1987), "The chloroplast tRNALys(UUU) gene from mustard (Sinapis alba) contains a class II intron potentially coding for a maturase-related polypeptide", Curr Genet, 11(4), pp. 251-257.
70. Poczai P., Hyvonen J. (2010), "Nuclear ribosomal spacer regions in plant phylogenetics: problems and prospects", Mol Biol Rep, 37(4), pp. 1897-1912.
Có thể bạn quan tâm!
-
 Thẩm Định Phương Pháp Định Tính Nystose Trong Dược Liệu Bằng Tlc
Thẩm Định Phương Pháp Định Tính Nystose Trong Dược Liệu Bằng Tlc -
 Nhân Bản Đoạn Gen, Giải Trình Tự Gen Và Định Danh Ba Kích
Nhân Bản Đoạn Gen, Giải Trình Tự Gen Và Định Danh Ba Kích -
 Nghiên cứu nâng cấp tiêu chuẩn dược liệu rễ Ba kích Radix Morindae officinalis của Việt Nam - 18
Nghiên cứu nâng cấp tiêu chuẩn dược liệu rễ Ba kích Radix Morindae officinalis của Việt Nam - 18 -
 Kết Quả Chồng Phổ Và Đánh Giá Độ Tinh Khiết Pic Monotropein
Kết Quả Chồng Phổ Và Đánh Giá Độ Tinh Khiết Pic Monotropein -
 Sắc Ký Đồ Dung Dịch Chuẩn Nystose (Định Lượng Trong Dược Liệu Ba Kích)
Sắc Ký Đồ Dung Dịch Chuẩn Nystose (Định Lượng Trong Dược Liệu Ba Kích) -
 So Sánh Kết Quả Phân Tích Của 2 Phòng Thí Nghiệm Thiết Lập Chất Chuẩn Monotropein
So Sánh Kết Quả Phân Tích Của 2 Phòng Thí Nghiệm Thiết Lập Chất Chuẩn Monotropein
Xem toàn bộ 226 trang tài liệu này.
71. Raven P.H. (2011), Biology, Vol. ninth edition, McGraw-Hill Connect Biology.
72. Roberfroid M. B. (2007), "Inulin-Type Fructans: Functional Food Ingredients", The Journal of Nutrition, 137(11), pp. 2493S-2502S.
73. Singh D.R. et al (2012), "Diversity of Morinda citrifolia L. in Andaman and Nicobar Islands (India) assessed through morphological and DNA markers", African Journal of Biotechnology, 11(86).
74. Singh D.R. et al (2011), "Genetic diversity of Morinda officinalis by RAPD and ISSR markers", Indian Journal of Biotechnology, 10.
75. Soltis P.S., Soltis D.E. and Doyle J.J. (1998), Molecular systematics of plants II: DNA sequencing, Kluwer Academic Publishers, Boston.
76. Štorchová H., OlsonM. S. (2007), "The architecture of the chloroplast psbA- trnH non-coding region in angiosperms", Plant Systematics and Evolution, 268(1-4), pp. 235-256.
77. Taberlet P. et al. (2007), "Power and limitations of the chloroplast trnL (UAA) intron for plant DNA barcoding", Nucleic Acids Res, 35(3), pp. e14.
78. Tamura K. et al (2013), "MEGA6: Molecular Evolutionary Genetics Analysis version 6.0", Mol. Biol. Evol., 30(12), pp. 2725-2729.
79. Takhtajan A. (2009), Flowering Plants, Springer, New York.
80. The United States Pharmacopoeial Convention (2017), The United States Pharmacopoeia 40, Vol. 40, USA.
81. Timmermans J. et al (1993), “NMR spectroscopy of nystose”, Carbohydrate Research, 243 (2), pp. 379-384.
82. TRC-Canada (2020), Nystose, TRC-Canada, Canada, https://www.trc- canada.com.
83. Vijayan K., Tsou C. H. (2010), "DNA barcoding in plants: taxonomy in a new perspective", Current Science, 99(11), pp. 1530-1541.
84. White T. J. et al (1990), "Ampli cation and direct sequencing of fungal ribosomal RNA genes for phylogenetics", PCR Protocols: a guide to methods and applications, Academic Press, New York, USA, pp. 315-322.
85. WHO Expert committee (2006), General guidelines for the establishment, maintenance and distribution of chemical reference substances, Specifications for Pharmaceutical Preparations, Geneva.
86. WHO Expert committee (2017), “WHO guidelines for selecting marker substances of herbal origin for quality control of herbal medicines”, WHO Technical Report Series, No. 1003, pp. 76.
87. William J. Murphy (2008), "Phylogenomics", Methods in molecular biology, Humana Press.
88. Wolfe K. H. (1991), "Protein-coding genes in chloroplast DNA: compilation of nucleotide sequences, data base entries and rates of molecular evolution", in Vasil, K., Cell Culture and Somatic Cell Genetics of Plants, Academic Press, San Diego, pp. 467-482.
89. Wu Y. B. et al (2009), "Antiosteoporotic activity of anthraquinones from Morinda officinalis on osteoblasts and osteoclasts", Molecules, 14(1), pp. 573- 583.
90. Xu J. et al (2007), “Determination of monotropein in Radix Morindae from different processed products by HPLC” (Abstract), Zhong Yao Cai, Jan, 30(1), pp. 20-22.
91. Yoshikawa M. et al (1995), "Chemical constituents of Chinese natural medicine, morindae radix, the dried roots of morinda officinalis How: structures of morindolide and morofficinaloside", Chem. Pharm. Bull. (Tokyo), 43(9), pp. 1462-1465.
92. Zhang H. L. et al (2009), "Structural characterization and anti-fatigue activity of polysaccharides from the roots of Morinda officinalis", International Journal of Biological Macromolecules, 44(3), pp. 257-261.
93. Zhang H. L. et al (2010), “Chemical Constituents from the Roots of Morinda officinalis”, Chinese Journal of Natural Medicines, 8(2), pp.192-195.
94. Zhang J. H. et al (2018), "Morinda officinalis How - A comprehensive review of traditional uses, phytochemistry and pharmacology", Journal of Ethnopharmacol, 213, pp. 230-255.
95. Zhang Z. et al (2000), "Antidepressant effect of the ethanolic extracts of the roots of Morinda officinalis in rats and mice" (Abstract), Z. Hongguo Pharmaceutical Journal, 35(11), pp.739-741.
96. Zhang Z. et al (2016), “Monotropein isolated from the roots of Morinda officinalis increases osteoblastic bone formation and prevents bone loss in ovariectomized mice”, Fitoterapia, 110, pp.166–172.
97. Zhu M. Y. et al (2011), "Extraction of polysaccharides from Morinda officinalis by response surface methodology and effect of the polysaccharides on bone-related genes", Carbohydrate Polymers, 85(1), pp. 23-28.
98. Zhu Z. et al (2019), "Morinda Officinalis Polysaccharides Attenuate Varicocele-Induced Spermatogenic Impairment through the Modulation of Angiogenesis and Relative Factors", Evidence-based complementary and alternative medicine: eCAM, 2019, pp. 8453635-8453635.
DANH MỤC PHỤ LỤC
PHỤ LỤC 1: SẮC KÝ ĐỒ ĐẠI DIỆN CỦA PHƯƠNG PHÁP ĐỊNH TÍNH, ĐỊNH LƯỢNG MONOTROPEIN ..................................................................................PL-1 PHỤ LỤC 2: SẮC KÝ ĐỒ ĐẠI DIỆN CỦA PHƯƠNG PHÁP ĐỊNH TÍNH, ĐỊNH LƯỢNG NYSTOSE............................................................................................PL-10 PHỤ LỤC 3: BỘ DỮ LIỆU CHUẨN XÁC ĐỊNH CẤU TRÚC VÀ ĐỊNH DANH MONOTROPEIN................................................................................................PL-15 PHỤ LỤC 4: BỘ DỮ LIỆU CHUẨN XÁC ĐỊNH CẤU TRÚC VÀ ĐỊNH DANH NYSTOSE...........................................................................................................PL-17 PHỤ LỤC 5: KẾT QUẢ KIỂM TRA ĐỘ ẨM BẰNG TGA .............................PL-20 PHỤ LỤC 6: SẮC KÝ ĐỒ THIẾT LẬP CHẤT CHUẨN MONOTROPEIN...PL-21 PHỤ LỤC 7: SO SÁNH KẾT QUẢ PHÂN TÍCH CỦA 2 PHÒNG THÍ NGHIỆM THIẾT LẬP CHẤT CHUẨN MONOTROPEIN ...............................................PL-25 PHỤ LỤC 8: CHỨNG CHỈ PHÂN TÍCH CHẤT CHUẨN DƯỢC ĐIỂN VIỆT NAM MONOTROPEIN .....................................................................................PL-26 PHỤ LỤC 9: SẮC KÝ ĐỒ CỦA NGHIÊN CỨU ĐỘ ỔN ĐỊNH CHẤT CHUẨN MONOTROPEIN (0119.C005.01) .....................................................................PL-28 PHỤ LỤC 10: CHỨNG CHỈ PHÂN TÍCH CHẤT CHUẨN SIGMA MONOTROPEIN................................................................................................PL-36 PHỤ LỤC 11: QUY TRÌNH THIẾT LẬP CHẤT CHUẨN MONOTROPEIN PL-37 PHỤ LỤC 12: SẮC KÝ ĐỒ THIẾT LẬP CHẤT CHUẨN NYSTOSE ............PL-42 PHỤ LỤC 13. SO SÁNH KẾT QUẢ PHÂN TÍCH CỦA 2 PHÒNG THÍ NGHIỆM THIẾT LẬP CHẤT CHUẨN NYSTOSE ..........................................................PL-46 PHỤ LỤC 14: CHỨNG CHỈ PHÂN TÍCH CHẤT CHUẨN DƯỢC ĐIỂN VIỆT NAM NYSTOSE ................................................................................................PL-47 PHỤ LỤC 15: SẮC KÝ ĐỒ CỦA NGHIÊN CỨU ĐỘ ỔN ĐỊNH CHẤT CHUẨN NYSTOSE (0119.C006.01) ................................................................................PL-49 PHỤ LỤC 16: CHỨNG CHỈ PHÂN TÍCH CHẤT CHUẨN SIGMA NYSTOSE..53 PHỤ LỤC 17: QUY TRÌNH THIẾT LẬP CHẤT CHUẨN NYSTOSE ...........PL-54 PHỤ LỤC 18: KẾT QUẢ KIỂM TRA DƯỢC LIỆU RỄ BA KÍCH THEO DƯỢC ĐIỂN VIỆT NAM V ...........................................................................................PL-59 PHỤ LỤC 19: KẾT QUẢ ĐỊNH LƯỢNG MONOTROPEIN TRONG MỘT SỐ DƯỢC LIỆU BA KÍCH......................................................................................PL-73
PHỤ LỤC 1: SẮC KÝ ĐỒ ĐẠI DIỆN CỦA PHƯƠNG PHÁP ĐỊNH TÍNH,
ĐỊNH LƯỢNG MONOTROPEIN
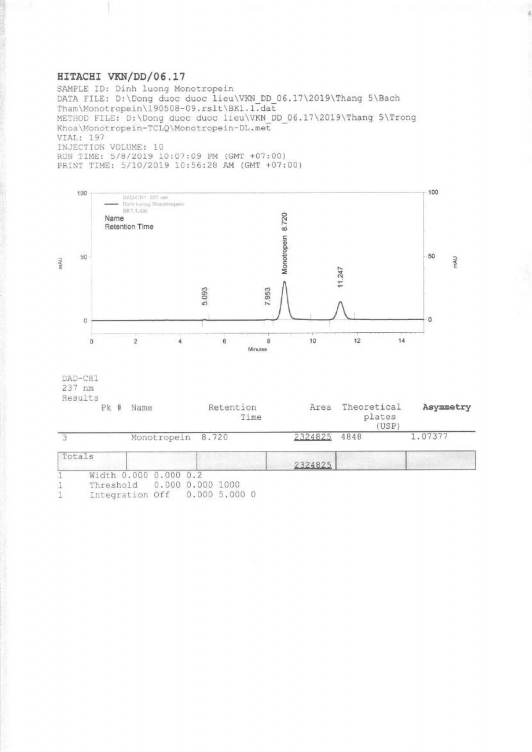
1. Dung dịch chuẩn monotropein (định lượng trong nguyên liệu)

2. Sắc ký đồ dung dịch thử monotropein (định lượng trong nguyên liệu)
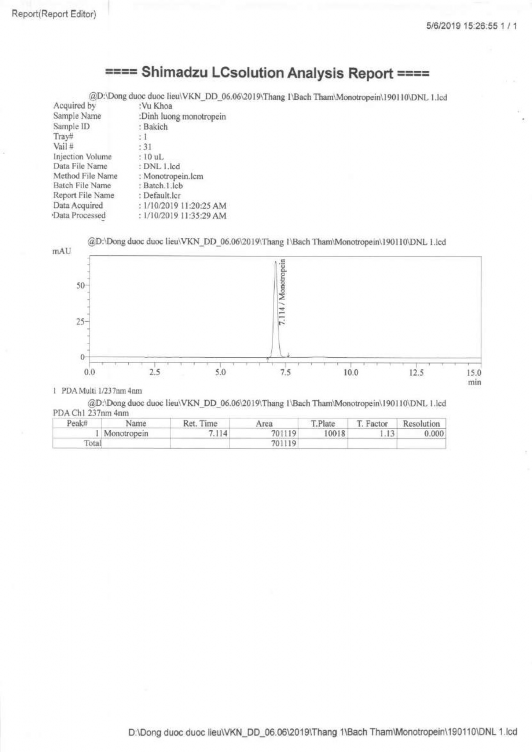
3. Dung dịch chuẩn monotropein (định lượng trong dược liệu Ba kích)
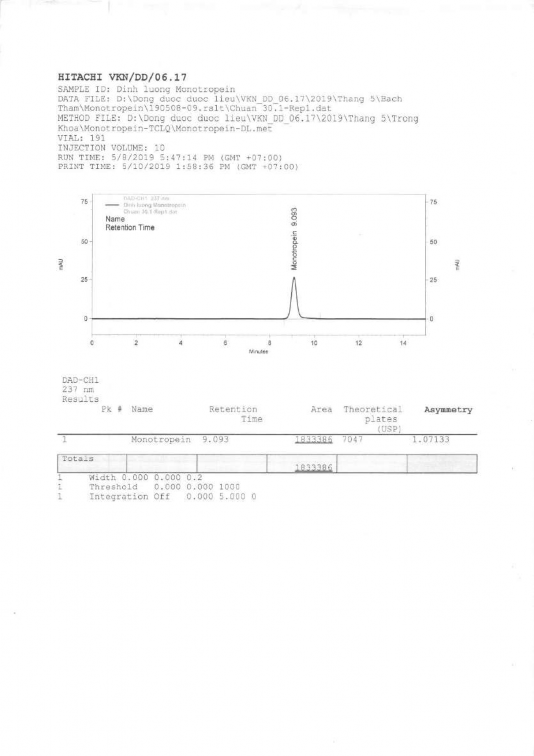
4. Sắc ký đồ dung dịch thử monotropein (định lượng trong dược liệu Ba kích)