có trách nhiệm ở một mức độ cho dư vị đắng này, mặc dù vai trò của rebaudiosid A là ít hơn đáng kể so với các steviosid (Phillips, 1987).
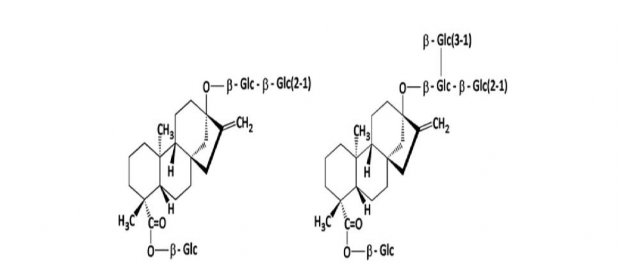
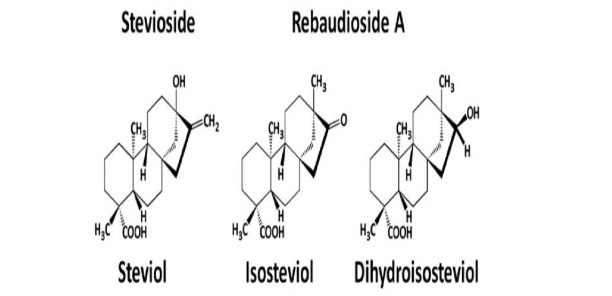
Hình2.3 Công thức hóa học của steviosid, thành phần chính được tìm thấy trong lá của cây Cỏ Ngọtvà một số thành phần khác có liên quan.
![]()
![]()
![]()
![]()
![]()
![]()
Bảng 2.3 Cấu trúc của các dẫn xuất steviosid và các hợp chất liên quan của cây Cỏ Ngọt và độ ngọt so với đường sucrose (Cramer et al., 1986 ), (Geuns, 2003)
Chuỗi R1 | Chuỗi R2 | Độ ngọt so với sucrose | ||||
Stevioside | β - Glc | β-Glc-β-Glc (2 | 1) | 300 | ||
Steviolbioside | H | β - Glc - β - Glc (2 | 1) | 100-125 | ||
Rebaudioside A | β - Glc | β - Glc - β - Glc (2 β - Glc – (3 1) | 1) | 250-50 | ||
Rebaudioside B | H | β - Glc - β - Glc (2 β - Glc – (3 1) | 1) | 300-350 | ||
Rebaudioside C | β - Glc | β - Glc - α - Rha (2 β - Glc – (3 1) | 1) | 50-120 | ||
Rebaudioside D | β - Glc - β - Glc (2 | 1) | β - Glc - β - Glc (2 β - Glc – (3 1) | 1) | 250-450 | |
Rebaudioside E | β - Glc - β - Glc (2 | 1) | β - Glc - β - Glc (2 | 1) | 150-300 | |
Dulcoside A | β - Glc | β - Glc - α - Rha (2 | 1) | 50-120 | ||
Có thể bạn quan tâm!
-
 Nghiên cứu chiết xuất và tinh sạch steviosid và rebaudiosid A từ cây Cỏ Ngọt Stevia rebaudiana làm chất tạo ngọt trong thực phẩm và dược phẩm - 1
Nghiên cứu chiết xuất và tinh sạch steviosid và rebaudiosid A từ cây Cỏ Ngọt Stevia rebaudiana làm chất tạo ngọt trong thực phẩm và dược phẩm - 1 -
 Nghiên cứu chiết xuất và tinh sạch steviosid và rebaudiosid A từ cây Cỏ Ngọt Stevia rebaudiana làm chất tạo ngọt trong thực phẩm và dược phẩm - 2
Nghiên cứu chiết xuất và tinh sạch steviosid và rebaudiosid A từ cây Cỏ Ngọt Stevia rebaudiana làm chất tạo ngọt trong thực phẩm và dược phẩm - 2 -
 Thí Nghiệm 1: Khảo Sát Tỷ Lệ Chiết Giữa Nước Và Nguyên Liệu Trong Quá
Thí Nghiệm 1: Khảo Sát Tỷ Lệ Chiết Giữa Nước Và Nguyên Liệu Trong Quá -
 Kết Quả Khảo Sát Tỷ Lệ Chiết Giữa Nước Và Nguyên Liệu Trong Quá Trình Ly Trích Hỗn Hợp Glycosid Thô.
Kết Quả Khảo Sát Tỷ Lệ Chiết Giữa Nước Và Nguyên Liệu Trong Quá Trình Ly Trích Hỗn Hợp Glycosid Thô. -
 Kết Quả Phân Lập Và Tinh Sạch Steviosid
Kết Quả Phân Lập Và Tinh Sạch Steviosid
Xem toàn bộ 73 trang tài liệu này.
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
2.4 Hoạt tính sinh học
Quá trình sử dụng hai thành phần chính của cây Cỏ Ngọt là steviosid và rebaudiosid A uống bằng đường miệng để kiểm tra độc tính thì được chấp nhận không độc trong quá trình sử dụng (Medon et al., 1982), (Toyoda et al., 1997). Sử dụng steviol glycosid với liều cao cho vào miệng của chuột và nuốt vào bụng cho thấy trọng lượng cơ thể của chuột giảm (Curry et al., 2008), nhưng không có bằng chứng mạnh mẽ về độc tính (Carakostas et al., 2008),
(Hagiwara et al.,1984), nghiên cứu tác dụng gây ung thư của steviosid trên
bàng quang thấy rằng không có tiền ung thư hoặc ung thư.
Dịch chiết cũng như các chất tách được từ Cỏ Ngọt có tác dụng mạnh trong việc điều khiển quá trình chuyển hoá glucose và insulin trong cơ thế. Theo Chen et al., 2005, khi sử dụng steviosid với liều 0,5 mg/kg sẽ làm giảm lượng đường glucose trong máu đồng thời hạn chế sự kháng insulin ở chuột bị tiểu đường. Tác giả Ferreira cũng chỉ ra rằng dịch chiết nước Cỏ Ngọt (20 mg/kg/ngày) cũng có tác dụng làm ức chế quá trình chuyến hoá glucose trong gan trên chuột thí nghiệm (Arayjo et al.,2006). Trước đó vào năm 1986, Curi đã thử nghiệm tác dụng của dịch chiết nước Cỏ Ngọt trên một nhóm người tình nguyện. Kết quả cho thấy với dịch chiết 5 g lá dùng liên tục trong 3 ngày, hàm lượng đường glucose trong huyết tương giảm rò rệt (Curi et al.,1986). Các nghiên cứu này mở ra khả năng ứng dụng Cỏ Ngọt trong việc chữa trị bệnh tiểu đường và các bệnh liên quan đến sự chuyển hoá glucose. Ngoài ra, cùng với tác dụng giảm đường huyết, steviosid còn có tác dụng hạ huyết áp trên lô chuột bị tiểu đường (Xiao et al., 2003).
Tác dụng chống ung thư và chống viêm của Cỏ Ngọt cũng được nghiên cứu chi tiết trên mô hình chuột thí nghiệm gây u bằng 12-0- tetradecanoylphorbol-13-acetate (TPA). Các hợp chất tách được từ cây này gồm steviosid, rebaudiosid A và C, và dulcosid A ức chế mạnh quá trình gây viêm đồng thời hỗn hợp các hợp chất này ngăn ngừa tốt sự hình thành ung thư da trên chuột với liều 1,0 và 0,1 mg/con (Yasukawa et al.,2002).
Hợp chất steviosid còn được sử dụng trong trị liệu chữa tiêu chảy hiệu quả. Khởi nguồn từ kết quả nghiên cứu tác dụng kháng khuẩn và kháng virút của dịch chiết nóng cây Cỏ Ngọt cho thấy tác dụng diệt mạnh chủng E. coli là nguyên nhân gây ra bệnh ỉa chảy (Tomita et al.,2002). Các nghiên cứu tiếp sau đó khẳng định tác dụng và khả năng ứng dụng rất cao của Cỏ Ngọt cũng
như nhóm chất steviosid trong việc chữa trị ỉa chảy (Pariwat et al.,2008),(Shiozaki et al.,2006),(Takahashi et al.,2001).
Ngoài các hợp chất đitecpen, trong cây Cỏ Ngọt còn chứa nhóm chất phenol và flavonoit. Tác giả Ghanta đã định lượng được hàm lượng nhóm chất này trong dịch chiết etyl axetat là tương đương 0,86 mg axit galic và 0,83 mg quercetin trên 1 mg. Bằng phân tích LC-MS và phổ NMR, nhóm tác giả đó nhận dạng được sự có mặt của quercetin-3-O-arabinoside, quercitrin, apigenin, apigenin-4-O-glucoside, luteolin, and kaempferol-3-O-rhamnoside. Dịch chiết metanol và etyl axetat cho thấy có khả năng diệt các gốc tự do bằng phương pháp thử DPPH và lipid peroxidation. Nghiên cứu này chứng tỏ cây Cỏ Ngọt còn là một dược liệu thiên nhiên chống oxy hoá hiệu quả (Ghanta et al., 2007).
2.5 Các phương pháp chiết mẫu thực vật
Sau khi tiến hành thu hái và làm khô mẫu, tuỳ thuộc vào đối tượng chất có trong mẫu khác nhau (chất phân cực, chất không phân cực, chất có độ phân cực trung bình...) mà ta chọn dung môi và hệ dung môi khác nhau.
2.5.1 Chọn dung môi chiết
Thông thường các chất chuyển hoá thứ cấp trong cây có độ phân cực khác nhau. Tuy nhiên những thành phần tan trong nước ít khi được quan tâm. Dung môi dùng trong quá trình chiết cần phải được lựa chọn rất cẩn thận. Điều kiện của dung môi là phải hoà tan được những chất chuyển hoá thứ cấp đang nghiên cứu, dễ dàng được loại bỏ, có tính trơ (không phản ứng với chất nghiên cứu), không độc, không dễ bốc cháy.
Những dung môi này nên được chưng cất để thu được dạng sạch trước khi sử dụng. Nếu chúng có lẫn các chất khác thì có thể ảnh hưởng đến hiệu quả và chất lượng của quá trình chiết. Thường có một số chất dẻo lẫn trong
dung môi như các diankyl phtalat, tri-n-butyl-axetylcitrar và tributylphosphat. Những chất này có thể lẫn với dung môi trong quá trình sản xuất hoặc trong khâu bảo quản như trong các thùng chứa hoặc các nút đậy bằng nhựa.
Metanol và chloroform thường chứa dioctylphtalat [di-(2- etylhexyl) phtalat hoặc bis-2-etylhexyl-phtalat]. Chất này sẽ làm sai lệch kết quả phân lập trong các quá trình nghiên cứu hoá thực vật, thể hiện hoạt tính trong thử nghiệm sinh học và có thể làm bẩn dịch chiết của cây. Chloroform, metylen clorit và metanol là những dung môi thường được lựa chọn trong quá trình chiết sơ bộ một phần của cây như: lá, thân, rễ, củ, quả, hoa...
Những tạp chất của chloroform như CH2C12, CH2ClBr có thể phản ứng với một vài hợp chất như các ancaloit tạo muối bậc 4 và những sản phẩm khác. Tương tự như vậy sự có mặt của lượng nhỏ axit clohiđric (HCl) cũng có thể gây ra sự phân huỷ, sự khử nước hay sự đồng phân hoá với các hợp chất khác. Vì chloroform có thể gây tổn thương cho gan và thận nên nó cần được thao tác khéo léo, cẩn thận ở nơi thoáng và phải đeo mặt nạ phòng độc. Metylen clorit ít độc hơn và dễ bay hơi hơn chloroform.
Metanol và etanol 80% là những dung môi phân cực hơn các hiđrocacbon thế clo. Người ta cho rằng các dung môi thuộc nhóm rượu sẽ thấm tốt hơn lên màng tế bào nên quá trình chiết với các dung môi này sẽ thu được lượng lớn các thành phần trong tế bào.Trái lại, khả năng phân cực của chlorofrom thấp hơn, nó có thể rửa giải các chất nằm ngoài tế bào. Các etanol hoà tan phần lớn các chất chuyển hoá phân cực cùng với các hợp chất phân cực trung bình và thấp. Vì vậy khi chiết bằng etanol thì các chất này cũng bị hoà tan đồng thời. Thông thường dung môi etanol trong nước có những đặc tính tốt nhất cho quá trình chiết sơ bộ.
Tuy nhiên cũng có một vài sản phẩm mới được tạo thành khi dùng metanol trong suốt quá trình chiết (Goad et al.,1997). Thí dụ trechlonolid A
thu được từ Trechonaetes aciniata được chuyển thành trechonolid B bằng quá trình phân huỷ 1-hydroxytropacocain cũng xảy ra khi erythroxylum novogranatense được chiết trong metanol nóng. Người ta thường ít sử dụng nước để thu được dịch chiết thô từ cây mà thay vào đó là dùng dung dịch nước của metanol.
Dietyl ete hiếm khi được dùng cho các quá trình chiết thực vật vì nó rất dễ bay hơi, bốc cháy và rất độc, đồng thời nó có xu hướng tạo thành peroxit dễ nổ, peroxit của dietyl ete dễ gây phản ứng oxi hoá với những họp chất không có khả năng tạo cholesterol như các carotenoid. Tiếp đến là axeton cũng có thế tạo thành axetonit nếu 1,2-cis-diol có mặt trong môi trường axit. Quá trình chiết dưới điều kiện axit hoặc bazơ thường được dùng với quá trình phân tách đặc trưng, cũng có khi xử lý các dịch chiết bằng axit-bazơ có thể tạo thành những sản phẩm mong muốn. Sự hiểu biết về những đặc tính của những chất chuyển hoá thứ cấp trong cây được chiết sẽ rất quan trọng để từ đó lựa chọn dung môi thích hợp cho quá trình chiết tránh được sự phân huỷ chất bởi dung môi và quá trình tạo thành chất mong muốn. Sau khi chiết dung
môi được cất ra bằng máy cô quay ở nhiệt độ không quá 30-40ỏC, với một
hoá chất chịu nhiệt có thể thực hiện ở nhiệt độ cao hơn.
2.5.2 Quá trình chiết
Hầu hết quá trình chiết đơn giản được phân loại như sau:
- Chiết ngâm.
- Chiết sử dụng một loại thiết bị là bình chiết soxhlet.
- Chiết sắc với dung môi nước.
- Chiết lôi cuốn theo hơi nước.
Chiết ngâm là một trong những phương pháp được sử dụng rộng rãi nhất trong quá trình chiết thực vật bởi nó không đòi hỏi nhiều công sức và thời
gian. Thiết bị sử dụng là một bình thuỷ tinh với một cái khoá ở dưới đáy để điều chỉnh tốc độ chảy thích hợp cho quá trình tách rửa dung môi, dung môi có thể nóng hoặc lạnh nhưng nóng sẽ đạt hiệu quả chiết cao hơn. Trước đây, máy chiết ngâm đòi hỏi phải làm bằng kim loại nhưng hiện nay có thể dùng bình thuỷ tinh.
Thông thường quá trình chiết ngâm không được sử dụng như phương pháp chiết liên tục bởi mẫu được ngâm với dung môi trong máy chiết khoảng 24 giờ rồi chất chiết được lấy ra. Thông thường quá trình chiết một mẫu chỉ thực hiện qua 3 lần dung môi vì khi đó cặn chiết sẽ không còn chứa những chất giá trị nữa. Sự kết thúc quá trình chiết được xác định bằng một vài cách khác nhau.
Như vậy tuỳ thuộc vào mục đích cần chiết lấy chất gì để lựa chọn dung môi cho thích hợp và thực hiện quy trình chiết hợp lý nhằm đạt hiệu quả cao. Ngoài ra, có thể dựa vào mối quan hệ của dung môi và chất tan của các lớp chất mà ta có thể tách thô một số lớp chất ngay trong quá trình chiết.
CHƯƠNG III NGUYÊN LIỆU VÀ PHƯƠNG PHÁP NGHIÊN CỨU
3.1 Nguyên liệu nghiên cứu
3.1.1 Nguyên liệu thí nghiệm
Nguyên liệu dùng để chiết xuất các đối tượng nghiên cứu của đề tài: lá cây Cỏ Ngọt dùng để chiết xuất steviosid và rebaudiosid A. Cỏ Ngọt thuộc họ cúc được mua tại nhà thuốc Minh Phát, 73B Hải Thượng Lãng Ông, phường 10, quận 5, Thành phố Hồ Chí Minh.
3.1.2 Hóa chất, chất chuẩn
- Metanol (99,99%), (Merck KGaA, 64271 Darmstadt, Đức)
- Acetonitrile (99,9 %), (Merck KGaA, 64271 Darmstadt, Đức)
- Etanol (99,9%), (Merck KGaA, 64271 Darmstadt, Đức)
- Steviosid hydrate (98%), (Sigma – Aldrich)
- Rebaudiosid A (96%),(Sigma – Aldrich)
- Amberlite FPC23 H (Sigma – Aldrich)
- Amberlite FPA51 (Sigma – Aldrich)
- Amberlite FPA98Cl (Sigma – Aldrich)
- Ca(OH)2(96%), (Merck KGaA, 64271 Darmstadt, Đức)
- FeCl3 (98%)(Merck KGaA, 64271 Darmstadt, Đức)
- Nước khử ion
3.1.3 Thiết bị và dụng cụ
- Sắc ký lỏng cao áp (HPLC, 20A, Shimadzu, Nhật)
- Thiết bị lọc nước khử ion (TKA, Thermo Fisher scientific, Mỹ)
- Thiết bị đun cách thuỷ (Thermo Haake V15, Mỹ)
- Cân phân tích (Sartorius, MC 210S, Đức)





