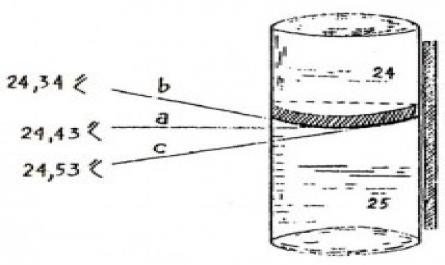
6.3. Hiệu chỉnh dung tích của pipet Đo nhiệt độ của nước cất, lấy đầy pipet tới vạch ngấn, sau đó lại bỏ nước đó ra chén đã cân trước. Đậy nắp chén cân lại rồi đem cân trên cân phân tích. Làm lại thí nghiệm ít nhất hai lần ...
Bài 3 Phương pháp định lượng thể tích mục tiêu 1. Trình bày được nội dung của phương pháp phân tích thể tích. Nêu được cách xác định điểm tương đương. 2. Kể tên được bốn loại phương pháp chuẩn độ chính và ba kỹ thuật ...
2. Những động tác cơ bản của phương pháp Phân tích khối lưỵng 2.1. Hòa tan Nếu mẫu phân tích ở dạng dung dịch không cần giai đoạn này. Mẫu phân tích rắn cần phải tìm cách chuyển nó vào dung dịch rồi dùng thuốc thử thích hợp để ...
Bài 1 đại cương về hóa phân tích định lượng mục tiêu 1. Trình bày được vị trí, đối tượng của môn học. 2. Nêu được các phương pháp phân tích định lượng, nguyên tắc chung của các phương pháp hóa học dùng trong phân tích định ...
Tđa: carbonat các cation không phải kim loại kiềm (bỏ đi hoặc để tìm các cation) Nước ly tâm (nước soda): Chứa anion nhóm I + Cation kim loại kiềm và NH 4 + + HNO 3 2N + AgNO 3 Sơ đồ 6. Sơ đồ thực hành phân tích các anion nhóm I: Cl , Br , I ...
2.3. Hòa tan kết tủa T 1 bằng HNO 3 10%, đun sôi, dung dịch sau đó chia ra làm 4 phần để tìm Fe 2+ , Fe 3+ , Bi 3+ , Mn 2+ bằng các phản ứng đặc trưng: 3 6 2+ * Tìm Fe 2+ : Cho vào thuốc thử K [Fe(CN) ], nếu có kết tủa màu xanh Tua bin (Fe 3 [Fe(CN) 6 ]) ...
1.2. Những dụng cụ thường dùng để tiến hành các phản ứng è ng nghiệm: Dùng để làm các phản ứng l − ỵng nhá è ng nghiệm th − ờng và ống nghiệm có chia vạch (hình 10) Giá ống nghiệm (hình 11) Cốc có mỏ: Dùng để pha chế, ...
4. Nhận xét kết quả Sau khi có kết quả phân tích, cần phải nhận xét lại nó lần cuối cùng, chẳng hạn ở các khía cạnh: 4 3 Các ion tìm thấy có thực sự cùng tồn tại với nhau trong dung dịch gốc hay không. Ví dụ: không thể cùng có ...
Với Na 2 S 2 O 3 trong môi trưêng acid: + 3- 3Na 2 S 2 O 3 + 6H + 2AsO 3 = As 2 S 3 vàng + 3Na 2 SO 4 + 3H 2 O 3 3 3 vàng Với Ag + trong môi trưêng trung tÝnh: 3Ag + + AsO 3- = Ag AsO 3- 3- - + Với nưíc I 2 trong môi trưêng trung tÝnh: AsO 3 + I 2 + H 2 O = ...
Sơ đồ 4*: Sơ đồ lý thuyết phân tích cation nhóm V: Hg 2+ , Cu 2+ và nhóm VI: NH 4 + , Na + , K + Dung dịch phân tích: Hg 2+ , Cu 2+ , NH 4+ , Na + , K + t Tìm NH4+: Bằng NaOH đặc Bằng TT Nessler t Tìm Na+: Bằng TT Streng t Tìm K+: Bằng TT Garola Dung dịch ...
2.7. Với KSCN 3 đỏ máu Fe 3+ + 3KSCN = Fe(SCN) + 3K + Fe(SCN) 3 + 3KSCN = K 3 [Fe(SCN) 6 ] tan màu đỏ mỏu 2.8. Với K 3 [Fe(CN) 6 ] 3 6 3 6 2 xanh tua bin 3Fe 2+ + 2K [Fe(CN) ] = Fe [Fe(CN) ] + 6K + 2.9. Với K 4 [Fe(CN) 6 ] 4 6 4 6 3 xanh phỉ 4Fe 3+ + 3K [Fe(CN) ] = Fe ...
Bài 5 cation nhãm III: Al 3+ , Zn 2+ Mục tiêu 1. Trình bày và giải thích được phản ứng của thuốc thử nhóm với các cation nhóm III. 2. Viết được một số phản ứng đặc trưng của các cation nhóm III. 3. Giải thích được các bước phân tích ...
Trang 1877, Trang 1878, Trang 1879, Trang 1880, Trang 1881, Trang 1882, Trang 1883, Trang 1884, Trang 1885, Trang 1886,