Không những tính axit của zeolit tăng lên mà đường kính trung bình của mao quản cũng tăng, bởi vì kích thước của nguyên tử H nhỏ hơn kích thước của nguyên tử Na. * Có rất nhiều yếu tố ảnh hưởng đến vận tốc và tỷ số trao đổi ...
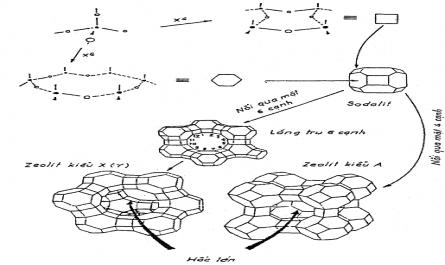
Công thức tổng quát của các zeolit được biểu diễn như sau: Me x/n (AlO 2 ) x (SiO 2 ) y .z H 2 O Trong đó: x, y, z là các hệ số tương ứng n là hóa trị của cation bù trừ (Na + , K + , Ca 2+ ) Công thức cấu tạo của các zeolit: OO O O O O O O . . . Al ...
Ví dụ : điều chế Ni/Al 2 O 3 Cho kiềm vào dung dịch Al(NO 3 ) 3 và Ni(NO 3 ) 2 . Kết tủa thu được bao gồm 2 hydroxyt được tạo thành. Sau khi rửa, sấy ta nhận được một hỗn hợp Al 2 O 3 và NiO. Khử dưới dòng H 2 ở 300 o C ta được Ni/Al 2 O 3 ...
(1) r f . g . V L . cos k ⎛ P ⎞ R . T . ln ⎜ ⎜ P ⎟ ⎟ ⎝ S ⎠ khp Trong đó: f: thừa số phụ thuộc hình dáng của màng Để đơn giản, phương pháp BJH giả thiết rằng màng bán cầu nên f = 2 g: sức căng bề mặt của chất lỏng ...
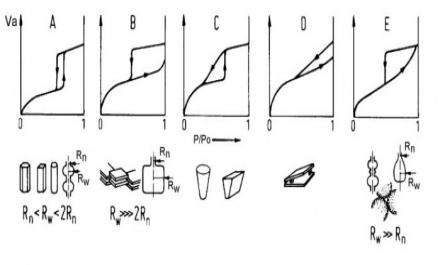
X Mao quản trung bình, hình trụ Mao quản trung bình, hình lớp, hình chai Mao quản trung bình, hình trụ Mao quản trung bình, hình khe Mao quản trung bình Các phương trình hấp phụ đẳng nhiệt : Các phương trình hấp phụ đẳng nhiệt có thể tất cả ...
+ với xúc tác là oxyt kim loại (Cr 2 O 3 , V 2 O 5 .) ở nhiệt độ 500 o C, phản ứng xảy ra theo hướng sau: C 6 H 12 3 CH 4 + 3 C CH 4 5 C 1 2 C C 4 3 CH 4 6 CH 4 - 4, 5, 6: là những trung tâm hoạt động có nhiệm vụ làm cắt đứt mối nối C-C tạo ...
Ở điều kiện cân bằng: k h . P H 2 .(1 - H ) 2 = k n . H 2 1 ⎛ k ⎞ 1/ 2 ⎛ 1 ⎞ 1/ 2 K . P H ⎜ n ⎟ ⎜ ⎟ k . P ⎜ ⎟ H ⎝ h H 2 ⎠ H K . P 1 / 2 H H 2 1 K . P 1/ 2 H H 2 ⎜ ⎟ ⎝ H H 2 ⎠ Trường hợp ...
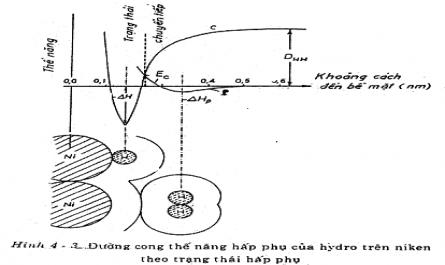
CHƯƠNG IV : THUYẾT HẤP PHỤ Mặc dù có nhiều công trình nghiên cứu về xúc tác, ảnh hưởng của xúc tác đến tốc độ và hướng phản ứng, cho đến nay vẫn chưa có một lý thuyết chung về hiện tượng xúc tác. Có lẽ không thể xây dựng ...
Xúc tác không bền nhiệt có khi làm thay đổi cả bản chất xúc tác, xúc tác dễ bị nóng cục bộ dẫn đến bị vón cục (tức các phân tử nhỏ kết hợp với nhau thành những phần tử lớn), bề mặt xúc tác giảm dẫn đến hoạt tính xúc ...
Giai đoạn I : chất phản ứng khuếch tán đến bề mặt xúc tác Giai đoạn II : hấp phụ lý học và hóa học Giai đoạn III : khuếch tán thành phẩm ra môi trường (cách phân chia này không rõ ràng lắm) Cách 2: Chia làm 5 giai đoạn I V II III IV l ...
Nhận xét: v c tỷ lệ với lực bazơ, nếu muốn tăng vận tốc phản ứng thì phải dùng xúc tác có lực bazơ mạnh Trường hợp III: giai đoạn (3) chậm, giai đoạn (1), (2) nhanh - + Khi đó: v c = v 3 = k 3 . [P 2 ].[BH ] Nhờ giai đoạn (2) nhanh nên ...
v c = k 3 K. C A n . C H+ . C Xo K. C A n . C H+ = k 3 . C Xo v c = f(C Xo ) Nhận xét: tốc độ phản ứng chung không phụ thuộc môi trường, không phụ thuộc nồng độ chất phản ứng mà chỉ phụ thuộc nồng độ của xúc tác trong trường hợp ...
Trang 5551, Trang 5552, Trang 5553, Trang 5554, Trang 5555, Trang 5556, Trang 5557, Trang 5558, Trang 5559, Trang 5560,