VIỆN HÀN LÂM KHOA HỌC VÀ CÔNG NGHỆ VIỆT NAM |
Có thể bạn quan tâm!
-
 Nghiên cứu xây dựng tiêu chuẩn chất lượng vi rút Beijing-1 để ứng dụng sản xuất vắc xin viêm não Nhật Bản bất hoạt trên tế bào Vero tại Việt Nam - 2
Nghiên cứu xây dựng tiêu chuẩn chất lượng vi rút Beijing-1 để ứng dụng sản xuất vắc xin viêm não Nhật Bản bất hoạt trên tế bào Vero tại Việt Nam - 2 -
 Dịch Tễ Học Phân Tử Của Vi Rút Viêm Não Nhật Bản
Dịch Tễ Học Phân Tử Của Vi Rút Viêm Não Nhật Bản -
 Sự Phát Triển Của Vắc Xin Viêm Não Nhật Bản Trên Tế Bào
Sự Phát Triển Của Vắc Xin Viêm Não Nhật Bản Trên Tế Bào
Xem toàn bộ 178 trang tài liệu này.

HỌC VIỆN KHOA HỌC VÀ CÔNG NGHỆ
-----------------------------
NGUYỄN THỊ LÝ
NGHIÊN CỨU XÂY DỰNG TIÊU CHUẨN
CHẤT LƯỢNG VI RÚT BEIJING-1 ĐỂ ỨNG DỤNG SẢN XUẤT VẮC XIN VIÊM NÃO NHẬT BẢN BẤT HOẠT TRÊN TẾ BÀO VERO TẠI VIỆT NAM
LUẬN ÁN TIẾN SĨ SINH HỌC
Hà Nội, 2022
VIỆN HÀN LÂM KHOA HỌC VÀ CÔNG NGHỆ VIỆT NAM |
BỘ GIÁO DỤC VÀ ĐÀO TẠO
HỌC VIỆN KHOA HỌC VÀ CÔNG NGHỆ
-----------------------------
NGUYỄN THỊ LÝ
NGHIÊN CỨU XÂY DỰNG TIÊU CHUẨN
CHẤT LƯỢNG VI RÚT BEIJING-1 ĐỂ ỨNG DỤNG SẢN XUẤT VẮC XIN VIÊM NÃO NHẬT BẢN BẤT HOẠT TRÊN TẾ BÀO VERO TẠI VIỆT NAM
Chuyên ngành: Vi sinh vật học Mã số: 9 42 01 07
LUẬN ÁN TIẾN SĨ SINH HỌC
NGƯỜI HƯỚNG DẪN KHOA HỌC:
1. GS. TS. Huỳnh Thị Phương Liên
2. PGS.TS. Đinh Duy Kháng
Hà Nội, 2022
LỜI CẢM ƠN
Với tất cả sự kính trọng, lòng biết ơn sâu sắc, tôi xin gửi lời cảm ơn tới:
Tôi xin trân trọng cảm ơn tới Ban lãnh đạo Viện Công nghệ sinh học và Học viện Khoa học và Công nghệ, Viện Hàn lâm Khoa học và Công nghệ Việt Nam đã hỗ trợ tôi rất nhiều trong suốt quá trình làm nghiên cứu sinh tại Viện.
Tôi xin trân trọng cảm ơn tới các thầy cô, anh chị Cơ sở đào tạo là Viện Công nghệ sinh học và Học viện Khoa học và Công nghệ, Viện Hàn lâm Khoa học và Công nghệ Việt Nam đã nhiệt tình giảng dạy, hướng dẫn và giúp đỡ tôi rất nhiều trong suốt quá trình làm nghiên cứu sinh tại Viện.
Tôi xin trân trọng cảm ơn Ban Lãnh đạo Viện Kiểm định Quốc gia Vắc xin và Sinh phẩm Y tế, TS. Đoàn Hữu Thiển đã tạo điều kiện cho tôi thực hiện nghiên cứu và tham gia khóa đào tạo này;
Tôi xin tỏ lòng biết ơn sâu sắc tới GS. TS. Huỳnh Thị Phương Liên, PGS.TS. Đinh Duy Kháng, những người thầy đã tận tình hướng dẫn tôi trong suốt quá trình học tập, nghiên cứu và viết luận án;
Tôi xin chân thành cảm ơn đồng nghiệp tại Khoa Kiểm định vắc xin Vi rút, Viện Kiểm định Quốc gia Vắc xin và Sinh phẩm Y tế đã tạo điều kiện hỗ trợ và giúp đỡ tôi trong suốt quá trình học tập;
Đặc biệt, tôi xin bày tỏ lòng biết ơn tới gia đình tôi, nơi đã cho tôi thêm sức mạnh vượt qua những khó khăn trong suốt quá trình học tập và nghiên cứu.
Nghiên cứu sinh
Nguyễn Thị Lý
i
LỜI CAM ĐOAN
Tôi xin cam đoan đây là công trình nghiên cứu do chính tôi thực hiện.
Các số liệu, kết quả nghiên cứu trong luận án là trung thực. Các số liệu này chưa được ai công bố trong bất kỳ công trình nghiên cứu khoa học nào khác
Nghiên cứu sinh
Nguyễn Thị Lý
ii
MỤC LỤC
LỜI CẢM ƠN i
LỜI CAM ĐOAN ii
MỤC LỤC iii
DANH MỤC CHỮ VIẾT TẮT vi
DANH MỤC CÁC BẢNG viii
DANH MỤC CÁC HÌNH VẼ, ĐỒ THỊ x
MỞ ĐẦU 1
CHƯƠNG 1: TỔNG QUAN NGHIÊN CỨU 4
1.1. Vi rút Viêm não Nhật Bản 4
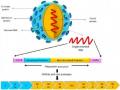
1.1.1. Đặc điểm cấu trúc 4
1.1.2. Kháng nguyên và các yếu tố độc lực của vi rút 4
1.1.3. Sự nhân lên của vi rút trên tế bào 7
1.1.4. Dịch tễ học phân tử của vi rút Viêm não Nhật Bản 8
1.2. Vắc xin Viêm não Nhật Bản 9
1.2.1. Lịch sử phát triển vắc xin VNNB 9
1.2.2. Sự phát triển của vắc xin Viêm não Nhật Bản trên tế bào 13
1.2.3. Các biến thể di truyền và kháng nguyên trong vi rút VNNB và việc tiêm phòng[34] 15
1.2.4. Đánh giá chất lượng an toàn và tính sinh miễn dịch của vắc xin 16
1.3. Chủng vi rút sản xuất vắc xin Viên não Nhật Bản 20
1.3.1. Chủng vi rút Nakayama-NIH 20
1.3.2. Chủng vi rút Beijing-1 20
1.3.3. Chủng SA14-14-2 22
1.3.4. Chủng Beijing-3 24
1.3.5. Dòng tế bào nuôi cấy (nhân) vi rút 26
1.4. Các khuyến cáo của TCYTTG cho sản xuất và kiểm định chủng sản xuất vắc xin VNNB bất hoạt[22] 27
1.4.1. Yêu cầu chung trong sản xuất vắc xin VNNB bất hoạt 27
1.4.2. Yêu cầu đối với nguồn nguyên liệu đầu vào: 28
1.5. Tóm tắt quy trình thiết lập ngân hàng chủng (Beijing-1) để sản xuất vắc xin viêm não Nhật Bản bất hoạt trên tế bào Vero tại Việt Nam 31
iii
CHƯƠNG 2: ĐỐI TƯỢNG, VẬT LIỆU VÀ PHƯƠNG PHÁP NGHIÊN CỨU 35
2.1. Đối tượng nghiên cứu 35
2.2. Vật liệu nghiên cứu 36
2.2.1. Sinh phẩm, hóa chất, thiết bị 36
2.2.2. Động vật thí nghiệm 38
2.3. Thiết kế nghiên cứu 38
2.4. Biến số và nội dung nghiên cứu 39
2.5. Phương pháp nghiên cứu (chi tiết xem phụ lục 5) 41
2.5.1. Kiểm định vi rút ngoại lai 41
2.5.2. Kiểm định vô khuẩn 42
2.5.3. Nhận dạng 42
2.5.4. Đánh giá ổn định di truyền 42
2.5.5. Hiệu giá vi rút 45
2.5.6. Thử nghiệm công hiệu của vắc xin 47
2.5.7. An toàn chung 48
2.5.8. An toàn đặc hiệu 49
2.5.9. Chất gây sốt 49
2.5.10. Hàm lượng Thimerosal 50
2.5.11. Hàm lượng Formaldehyde 50
2.5.12. Hàm lượng DNA tồn dư 50
2.5.13. Hàm lượng protein tổng số 52
2.5.14. pH 52
2.5.15. Cảm quan 52
2.6. Xử lý và phân tích số liệu 53
CHƯƠNG 3: KẾT QUẢ VÀ BÀN LUẬN 54
3.1. Kết quả nghiên cứu 54
3.1.1. Tính ổn định về hiệu giá và di truyền của chủng Beijing-1 54
3.1.2. Tính an toàn và sinh miễn dịch bảo vệ của chủng trên các lô vắc xin thành phẩm sản xuất từ chủng BV-WSV-0310 ở quy mô phòng thí nghiệm 66
3.1.3. Xây dựng tiêu chuẩn chất lượng của chủng sử dụng để sản xuất vắc xin VNNB bất hoạt trên tế bào Vero tại Việt Nam 72
3.2. Bàn luận 74
iv
3.2.1. Tính ổn định về hiệu giá, di truyền của chủng vi rút Viêm não Nhật Bản sau sản xuất và điều kiện bảo quản 74
3.2.2. Sự tương đồng kháng nguyên của chủng sản xuất vắc xin VNNB so với các chủng Viêm não Nhật bản lưu hành tại Việt Nam 81
3.2.3. Tính an toàn và tính sinh miễn dịch của JECEVAX sản xuất từ chủng BV- WSV-0310 ở quy mô phòng thí nghiệm 88
3.2.4. Xây dựng tiêu chuẩn chất lượng của chủng để sản xuất vắc xin VNNB bất hoạt trên tế bào Vero (JECEVAX) 93
KẾT LUẬN VÀ KIẾN NGHỊ 103
DANH MỤC CÁC CÔNG TRÌNH CỦA TÁC GIẢ 105
TÀI LIỆU THAM KHẢO 106
PHỤ LỤC
v
DANH MỤC CHỮ VIẾT TẮT
AE Adverse events (biến cố bất lợi)
BYT Bộ Y tế
BHK-21 Baby Hamster Kidney – 21 (Tế bào thận chuột Hamter sơ sinh)
BR209 Beijing reference (Vắc xin mẫu chuẩn Beijing-1) CF Complement Fixation (Cố định bổ thể)
CPE Cytopathic effect (hiệu quả gây độc/hủy hoại trên tế bào)
CV Challenge virus (vi rút thử thách)
E Envelope protein (Protein vỏ)
FTM Fluid Thioglycollate Medium (môi trường nuôi cấy vi khuẩn)
HA Haemagglutinin Assay (thử nghiệm ngưng kết hồng cầu)
HI Haemagglutinin inhibition (ức chế ngưng kết hồng cầu)
HT Huyết thanh
HLKN Hàm lượng kháng nguyên
HGKTTH Hiệu giá kháng thể trung hòa
IC51 Vắc xin VNNB trên tế bào vero của Intercell – Áo JEVAX Vắc xin VNNB bất hoạt sản xuất từ não chuột tại Việt
Nam
JECEVAX Vắc xin VNNB bất hoạt sản xuất trên tế bào vero tại Việt Nam
JE-MB Vắc xin VNNB sản xuất trên não chuột của Nhật Bản KT Kháng thể
MRC5 Tế bào phôi phổi bào thai người
NICVB Viện Kiểm định Quốc gia vắc xin và sinh phẩm Y tế (National Institute for Control of Vaccines and Biologicals).
NS Non structural Protein (Protein không cấu trúc)
NSX Nhà sản xuất
vi