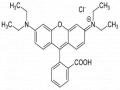
của ánh sáng đơn sắc ban đầu, được gọi là hiệu ứng Raman. Sự thay đổi này sẽ cung cấp các thông tin về các dao động và chuyển động quay của vật liệu.
Phổ Raman cho phép khẳng định sự khuyết tật trên bề mặt của vật liệu. Thông thường trong phổ Raman thường xuất hiện 2 pic cơ bản với cường độ cao là pic D (Disorder - Độ mất trật tự), pic G (Graphite). Khi tỷ lệ cường độ pic D và pic G (ID/IG) càng lớn, thể hiện độ khuyết tật trên bề mặt vật liệu càng cao.
* Thực nghiệm:
Phổ Raman của các mẫu trong luận án được phân tích trên máy Xplora plus (hãng Horiba) tại viện Khoa học Vật liệu - Viện Hàn lâm Khoa học và Công nghệ Việt Nam.
2.3.11. Phương pháp cộng hưởng thuận từ điện tử (EPR)
* Nguyên tắc:
Cộng hưởng thuận từ điện tử (Electron Paramagnetic Resonance - EPR) hoặc cộng hưởng spin điện tử (Electron Spin Resonance - ESR) là phương pháp để nghiên cứu các vật liệu có chứa các điện tử tự do, chưa ghép cặp. Nguyên lý của EPR tương tự với cộng hưởng từ hạt nhân (NMR) chỉ với điểm khác là thay vì kích thích các spin của hạt nhân nguyên tử (như trong NMR) thì sẽ kích thích các spin điện tử. Phổ EPR đặc biệt hữu ích nghiên cứu các phức kim loại hoặc gốc tự do.
Khi chưa có từ trường ngoài, các trạng thái của nguyên tử có J xác định (nguyên tử có momen từ MJ) có cùng năng lượng Eo nào đó. Mức năng lượng Eo khi đó có sự suy biến theo số lượng tử mJ (độ suy biến bằng 2J + 1). Trong từ trường B, nguyên tử có momen MJ có năng lượng phụ:
E = -MJB.Bo = -ge.µB.mJ.Bo (2.12)
trong đó: ge là hệ số Landé, µB là magneton Bohr và Bo là cường độ từ trường.
Có thể bạn quan tâm!
-
![Mô Hình Tổng Hợp Vật Liệu Mos 2 /gr Bằng Phương Pháp Vi Sóng [95]](data:image/svg+xml,%3Csvg%20xmlns=%22http://www.w3.org/2000/svg%22%20viewBox=%220%200%2075%2075%22%3E%3C/svg%3E) Mô Hình Tổng Hợp Vật Liệu Mos 2 /gr Bằng Phương Pháp Vi Sóng [95]
Mô Hình Tổng Hợp Vật Liệu Mos 2 /gr Bằng Phương Pháp Vi Sóng [95] -
 Ứng Dụng Làm Xúc Tác Quang Trong Xử Lý Chất Màu Của Mos 2
Ứng Dụng Làm Xúc Tác Quang Trong Xử Lý Chất Màu Của Mos 2 -
 Phương Pháp Hiển Vi Điện Tử Truyền Qua (Tem) Và Kính Hiển Vi Điện Tử Truyền Qua Phân Giải Cao (Hr-Tem)
Phương Pháp Hiển Vi Điện Tử Truyền Qua (Tem) Và Kính Hiển Vi Điện Tử Truyền Qua Phân Giải Cao (Hr-Tem) -
 Ảnh Tem Và Hrtem Của Rgo Ở Nhiệt Độ Nung 200 O C (A), 400 O C(B) Và 600 O C(C)
Ảnh Tem Và Hrtem Của Rgo Ở Nhiệt Độ Nung 200 O C (A), 400 O C(B) Và 600 O C(C) -
 Đường Đẳng Nhiệt Hấp Phụ-Giải Hấp Phụ N 2 Ở 77K (Bet) (A) Và Đường Phân Bố Kích Thước Mao Quản Của Các Mẫu Vật Liệu Mos 2 (B)
Đường Đẳng Nhiệt Hấp Phụ-Giải Hấp Phụ N 2 Ở 77K (Bet) (A) Và Đường Phân Bố Kích Thước Mao Quản Của Các Mẫu Vật Liệu Mos 2 (B) -
 Đường Đẳng Nhiệt Hấp Phụ-Giải Hấp Phụ (A) Và Đường Phân Bố Kích Thước Mao Quản (B) Của Các Mẫu Vật Liệu Mos 2 /rgo(180 O C-X) Với X =2/1, 4/1
Đường Đẳng Nhiệt Hấp Phụ-Giải Hấp Phụ (A) Và Đường Phân Bố Kích Thước Mao Quản (B) Của Các Mẫu Vật Liệu Mos 2 /rgo(180 O C-X) Với X =2/1, 4/1
Xem toàn bộ 192 trang tài liệu này.
Tương tác hyperfine là tương tác giữa momen từ của một electron với momen từ hạt nhân. Momen từ hạt nhân trong từ trường có (2I + 1) định hướng được phép. Từ trường liên quan đến momen từ hạt nhân có thể cộng thêm hoặc trừ đi từ trường ngoài tác dụng lên hệ spin electron.
* Thực nghiệm: Mẫu vật liệu đo trên máy Bruker tại Trường Đại học Bách Khoa Hà Nội.
2.3.12. Phương pháp phổ tổng trở điện hóa (EIS)
* Nguyên tắc:
Khi đưa một tín hiệu điện thế xoay chiều hình sin có biên độ nhỏ Eo, tần số góc ω = 2πf vào một hệ điện hóa, trong mạch sẽ xuất hiện một dòng điện phản hồi hình sin có biên độ Io cùng tần số góc ω nhưng lệch pha một góc θ so với thế đặt vào.
E = Eo sinωt (2.13)
I = Io sin (ωt + θ) (2.14) Theo định luật Ohm có thể định nghĩa tổng trở Z như sau:
(2.15)
Z(ω) là một vectơ có modun và góc lệch pha θ.Z(ω) là một hàm phức:
![]() (2.16)
(2.16)
![]() (2.17)
(2.17)
![]()
(2.18)
với θ = ![]() );
); ![]() (Z’) là phần thực của tổng trở,
(Z’) là phần thực của tổng trở, ![]() (Z”) là phần ảo của tổng trở.
(Z”) là phần ảo của tổng trở.
Khảo sát đặc tính tần số Z = Z(ω) sẽ cho phép xác định các đại lượng ![]() , Zr, Zi và góc lệch pha
, Zr, Zi và góc lệch pha ![]() . Các kết quả nhận được thường được biểu diễn dưới dạng phổ: dạng
. Các kết quả nhận được thường được biểu diễn dưới dạng phổ: dạng ![]() , dạng Bode
, dạng Bode ![]() hay
hay ![]() hoặc
hoặc ![]() , với Y’ = Re(1/Z) =
, với Y’ = Re(1/Z) = ![]() 2; Y” = Im(1/Z) =
2; Y” = Im(1/Z) =![]() .
.
Bất kì một hệ điện hóa nào cũng có thể biểu diễn bằng một sơ đồ mạch tương đương gồm có các điện trở và các tụ điện. Bằng cách quét tần số một cách liên tục từ giá trị cao đến thấp trong một khoảng rộng với thế một chiều cố định, đường phổ trở kháng phức (Z” với Z’) thực nghiệm sẽ được xử lý và mô phỏng bằng một mạch điện tương đương mà mỗi phần tử của mạch sẽ đại diện cho một tính chất điện của
hệ điện phân. Giá trị của các phần tử mô phỏng sẽ được các phần mềm xử lý, tính toán đưa ra. Do chỉ đưa vào hệ một tín hiệu nhỏ tuần hoàn hình sin nên luôn được giữ ở trạng thái cân bằng.
* Thực nghiệm:
Các mẫu vật liệu được đo trên máy Autolab 86590 tại Trường Đại học Bách Khoa Hà Nội.
2.3.13. Phương pháp ICP-OES (Inductively Coupled Plasma-Optical Emission Spectroscopy)
* Nguyên tắc
ICP-OES là một phương pháp đo phổ phát xạ quang học, kĩ thuật phân tích dùng để phát hiện các nguyên tố hóa học.
Khi năng lượng plasma được cung cấp cho một mẫu phân tích từ bên ngoài, các phần tử thành phần (nguyên tử) được kích thích. Khi các nguyên tử bị kích thích trở lại vị trí năng lượng thấp, các tia phát xạ (tia quang phổ) được giải phóng và đo được các tia phát xạ ứng với bước sóng photon. Loại phần tử được xác định dựa trên vị trí của các tia photon và nội dung của mỗi phần tử được xác định dựa trên cường độ của các tia. Để tạo ra plasma, đầu tiên, khí argon được cung cấp cho cuộn dây của ngọn lửa và dòng điện tần số cao được đưa vào cuộn dây làm việc ở đầu của ống mỏ hàn. Sử dụng trường điện từ do dòng điện tần số cao tạo ra trong ống đuốc, khí argon bị ion hóa và plasma được tạo ra. Plasma này có mật độ và nhiệt độ điện tử cao (10000K) và năng lượng này được sử dụng trong quá trình phát xạ kích thích của mẫu. Các mẫu dung dịch được đưa vào plasma ở trạng thái nguyên tử hóa qua ống hẹp ở trung tâm của ống đèn khò.
* Thực nghiệm
Mẫu được tiến hành đo trên máy ICP - OES iCAP 7000SERIES Thermo Fisher Scient ở Hàn Quốc.
2.4. Đánh giá hoạt tính quang xúc tác của vật liệu
2.4.1. Xác định điểm đẳng điện của vật liệu
Điểm đẳng điện của vật liệu [127] được xác định như sau: cho vào 6 bình tam giác (dung tích 100 ml) 25 ml dung dịch NaCl 0,1M có giá trị pH ban đầu (pHi)
đã được điều chỉnh nằm trong khoảng từ 2 đến 12 bằng dung dịch HCl 0,1M hoặc NaOH 0,1M. Giá trị pH của dung dịch được đo trên máy HANA HI2011.
Tiếp theo cho vào mỗi bình tam giác trên 0,05g vật liệu MoS2/rGO đậy kín và khuấy trên máy khuấy từ trong 24 giờ. Sau đó, để lắng và lọc lấy dung dịch, đo lại các giá trị pH gọi là pHf. Đồ thị biểu diễn mối quan hệ sự khác nhau giữa các giá trị pH ban đầu và sau cùng ![]() pH = pHf - pHi) theo pHi là đường cong cắt trục hoành tại
pH = pHf - pHi) theo pHi là đường cong cắt trục hoành tại ![]() pH = 0 cho ta giá trị pH đẳng điện (pHpzc).
pH = 0 cho ta giá trị pH đẳng điện (pHpzc).
Tiến hành tương tự để xác định điểm đẳng điện của vật liệu Mn-MoS2/rGO.
2.4.2. Đánh giá khả năng hấp phụ RhB của vật liệu
Khả năng hấp phụ RhB của vật liệu được xác định theo quy trình sau:
Chuẩn bị 6 cốc dung tích 100 ml, cho vào mỗi cốc 5 mg xúc tác compozit MoS2/rGO với 20 ml dung dịch chất màu (RhB). Khuấy các hỗn hợp trong bóng tối để tránh khả năng phản ứng quang xúc tác xảy ra khi nghiên cứu khả năng hấp phụ của vật liệu. Thời gian khuấy của các cốc lần lượt là 30 phút, 60 phút, 90 phút, 120 phút, 180 phút và 240 phút. Sau khi ly tâm để loại bỏ chất hấp phụ, các mẫu dung dịch được đo quang trên máy quang phổ CE - 2011 để xác định nồng độ của RhB. Lượng chất màu RhB hấp phụ lên compozit MoS2/rGO tại thời điểm t được xác định theo công thức [105]:
![]() (2.19)
(2.19)
Trong đó: Co là nồng độ ban đầu của dung dịch chất màu RhB (mg/l); Ct là nồng độ của chất màu tại thời điểm t (mg/l); V là thể tích của dung dịch RhB; và m là khối lượng của compozit MoS2/rGO sử dụng cho quá trình hấp phụ.
2.4.3. Đánh giá khả năng hoạt tính quang xúc tác của vật liệu
Hoạt tính quang xúc tác của vật liệu cho phản ứng phân hủy RhB được xác định như mô tả trên hình 2.7. Cho 0,1g xúc tác vào trong 400 ml dung dịch chất màu RhB với nồng độ 20 mg/l dưới điều kiện khuấy từ ở nhiệt độ phòng. Dung dịch được khuấy trong bóng tối với thời gian 120 phút để đạt cân bằng hấp phụ - nhả hấp phụ của chất màu RhB trên bề mặt của vật liệu.
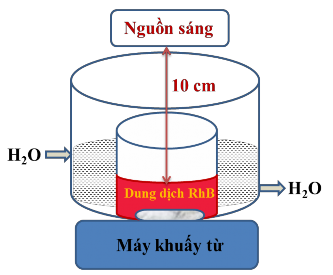
Hình 2.7. Sơ đồ thí nghiệm khảo sát hoạt tính xúc tác quang của vật liệu
Chiếu sáng hệ phản ứng bằng đèn compact. Cứ sau 30 phút phản ứng, 4 ml dung dịch được lấy ra, ly tâm để tách xúc tác và phân tích xác định nồng độ RhB trong dung dịch bằng máy đo quang phổ ở bước sóng 553 nm.
2.4.4. Động học phản ứng quang xúc tác của vật liệu
Phản ứng phân hủy xúc tác dị thể thường tuân theo mô hình động học Langmuir-Hishelwood [128]. Theo mô hình này, tốc độ phản ứng xúc tác dị thể (r) tỉ lệ với phần diện tích bề mặt bị che phủ bởi chất phản ứng () theo phương trình:
r = k = k
KC
(2.20)
1 + KC
Trong đó, C là nồng độ chất phản ứng, k là hằng số tốc độ phản ứng, K là hằng số cân bằng hấp phụ của chất phản ứng trên bề mặt xúc tác. Đối với các dung dịch loãng thì giá trị C thường rất bé (C < 10-3 mol/L) nên KC << 1 và phương trình có dạng:
r = k = kKC = k’C = -dC/dt. (2.21) Vì vậy, phương trình động học được áp dụng là:
ln(Co/Ct) = k’t (2.22)
Trong đó, Co và Ct là nồng độ chất phản ứng tại thời điểm t = 0 và t 0 tương ứng; k’ là hằng số tốc độ phản ứng.
2.4.5. Xác định sản phẩm trung gian trong quá trình phân hủy RhB
Để xác định các sản phẩm trung gian hình thành trong quá trình phân hủy RhB, phương pháp sắc ký lỏng khối phổ (LC/MS) được sử dụng. Mẫu dung dịch sau những khoảng thời gian phản ứng nhất định được rút ra từ môi trường phản ứng và chuyển đi phân tích LC/MS.
Nguyên tắc của phương pháp: Dung môi từ hệ thống bơm kết hợp với mẫu phân tích được đưa qua cột sắc ký dưới dạng dung dịch. Các chất phân tích được phân bố liên tục giữa pha động và pha tĩnh tạo ra sự phân tách cân bằng khi di chuyển xuống cột. Đĩa chứa các hợp chất đã tách này rửa giải khỏi cột ở các thời điểm khác nhau, đi vào bề mặt phân cách nơi dung môi được bay hơi và các hợp chất này bị ion hóa và sau đó di chuyển vào bộ phận phân tích phổ khối. Thấu kính điện thu chùm ion tích điện và đưa vào máy phân tích khối lượng. Chúng được quét bằng dòng điện trực tiếp/tần số vô tuyến (dc/RF) được áp vào xen kẽ trên đường di chuyển của các ion. Vì thế tín hiệu các ion có giá trị m/z được lựa chọn đưa vào máy dò và kích hoạt tín hiệu. Tín hiệu này kết hợp trong máy tính với thông tin điều khiển mà nó đang gửi đến khối phổ kế để tạo ra một mảng ba chiều cường độ tín hiệu theo thời gian so với thông tin m/z để lưu trữ và xử lý [129].
* Thực nghiệm:
Trong luận án này, các chất trung gian xuất hiện trong quá trình phân hủy RhB được phân tích xác định trên hệ LC/MS D-Trap-SL Agilent 1100 tại Viện Hóa học- Viện Hàn lâm Khoa học và Công nghệ Việt Nam.
2.4.6. Đánh giá khả năng tái sử dụng của vật liệu
Quá trình thực nghiệm đánh giá khả năng tái sử dụng và tuổi thọ của các chất xúc tác: vật liệu sau khi tham gia xúc tác được ly tâm giữ lại phần rắn, rửa lại nhiều lần bằng rượu etylic và sau đó rửa lại bằng nước cất. Mẫu được sấy khô ở 60oC qua đêm và tái sử dụng làm xúc tác trở lại. Lặp lại quy trình như vậy 5 lần để khảo sát khả năng tái sử dụng của vật liệu cũng như qua đó đánh giá được độ bền hay tuổi thọ của các chất xúc tác.
CHƯƠNG 3. KẾT QUẢ VÀ THẢO LUẬN
3.1. Kết quả tổng hợp vật liệu GO và rGO
3.1.1. Sự hình thành vật liệu GO
Để biết được mức độ oxi hóa graphit, sự thay đổi cấu trúc tinh thể của vật liệu thì kỹ thuật XRD được sử dụng để xác định khoảng cách giữa các lớp cũng như cấu trúc tinh thể của vật liệu GO. Kết quả thể hiện trên hình 3.1.
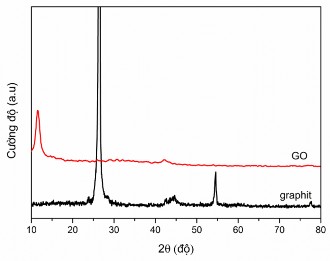
Hình 3.1. Giản đồ XRD của mẫu vật liệu graphit và GO
Từ hình 3.1 có thể thấy, với mẫu graphit, pic nhiễu xạ đặc trưng cho mặt
(002) của graphit xuất hiện tại 2θ = 26,5o tương ứng với khoảng cách các lớp là 0,335 nm, có cường độ rất mạnh. Ngoài ra, các mặt (101) và (004) trong mạng graphit được hình thành do quá trình oxi hóa không hoàn toàn, cũng được quan sát thấy tương ứng với các pic xuất hiện tại 2θ = 42,31º và 2θ = 54,6º [130]. Với mẫu GO, pic nhiễu xạ xuất hiện tại 2θ = 11,8o tương ứng với mặt (002) thể hiện cho sự hình thành của GO sau quá trình oxi hóa. Sự thay đổi này là do có sự tương tác giữa các vùng kị nước và các nhóm chức có chứa oxi phân tán ở các cạnh của cấu trúc vòng benzen trong GO, phù hợp với kết quả thực nghiệm của Zakaria và cộng sự [131]. Trong quá trình oxi hóa, các nhóm chức chứa oxi như epoxi, cacbonyl, hydroxyl được hình thành do sự bẻ gãy liên kết C-C trong mạng lưới graphit. Những nhóm chức này đóng vai trò hỗ trợ cho quá trình tách lớp của các lớp graphit, chèn vào các lớp graphit và làm thay đổi trật tự của các lớp trong mạng lưới graphit. Nếu các lớp sắp xếp một cách có trật tự thì các nhóm chức này làm gia tăng
khoảng cách giữa các lớp [132]. Do vậy, có sự giãn khoảng cách lớn giữa các tấm graphit trong quá trình oxi hóa làm cho pic nhiễu xạ dịch chuyển sang góc có giá trị bé hơn và rộng hơn là 11o so với pic nhiễu xạ ban đầu chưa thực hiện quá trình oxi hóa của graphit là 26,5o.
Cơ chế của quá trình oxi hóa graphit tạo GO được thực hiện qua ba bước khác nhau. Bước đầu tiên, chuyển graphit thành hợp chất trung gian đầu tiên bằng cách dùng axit sunfuric xen kẽ vào các tấm graphit được gọi là H2SO4-GIC (the sulfuric acid graphite intercalation compound). Tốc độ hình thành GIC phụ thuộc vào môi trường điện hóa của quá trình tổng hợp. Bước thứ hai là tiến hành biến đổi GIC thành dạng oxi hóa của graphit gọi là PGO (pristine graphite oxide) dạng hợp chất trung gian thứ hai. Bước thứ ba là tạo thành sản phẩm GO bằng phản ứng của PGO với nước [133].
Như vậy, các kết quả đặc trưng XRD trên đây đã khẳng định được rằng graphit đã bị oxi hóa tạo thành GO theo phương pháp Hummers.
3.1.2. Ảnh hưởng của nhiệt độ nung đến quá trình hình thành rGO
Một trong những yếu tố ảnh hưởng đến quá trình tổng hợp rGO là nhiệt độ nung để khử GO về rGO. Do vậy, trong luận án này quá trình nung khử GO về rGO được khảo sát trong vùng từ 200oC-600oC. Kết quả được thể hiện rò nét trên giản đồ nhiễu xạ tia X ở hình 3.2.
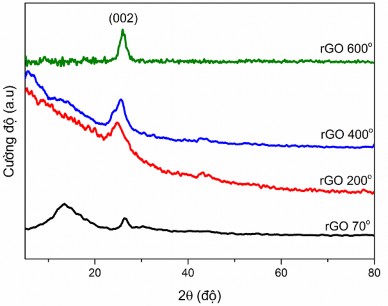
Hình 3.2. Giản đồ XRD của các mẫu rGO ở các nhiệt độ nung khác nhau

![Mô Hình Tổng Hợp Vật Liệu Mos 2 /gr Bằng Phương Pháp Vi Sóng [95]](https://tailieuthamkhao.com/uploads/2022/07/14/nghien-cuu-tong-hop-dac-trung-xuc-tac-mos2-rgo-bien-tinh-voi-mn-va-ung-dung-6-1-120x90.jpg)