2.2. Tổng hợp RNA
Sự tổng hợp ARN là quá trình chuyển thông tin di truyền từ ADN sang phân tử ARN. Quá trình tổng hợp này dựa trên nguyên tắc giống như sự tái bản ADN:
o Chiều tổng hợp từ 5’- 3’.
o Năng lượng do ATP cung cấp.
Tuy nhiên cũng có một số điểm khác:
- Khuôn ADN được bảo tồn hoàn toàn trong quá trình tổng hợp ARN.
- ARN polymerase không có hoạt tính nuclease.
- Quá trình tổng hợp không cần có sự tham gia của đoạn mồi.
Các enzym tham gia
- ARN polymerase phụ thuộc ARN (replicase): xúc tác tự nhân đôi ARN của virut trong tế bào chủ.
- ARN polymerase phụ thuộc AND: xúc tác phản ứng tổng hợp ARN từ các nucleosid triphosphat bằng cách kéo dài chuỗi ARN theo phản ứngL
(NMP)n + NTP (NMP)n+1 + Ppi
ARN kéo dài
Các giai đoạn của quá trình tổng hợp ARN
- Giai đoạn mở đầu: ARN polymerase liên kết với promoter trên ADN ở vị trí - 35 tạo thành phức hợp đóng. Sau đó ARN polymerase di chuyển đến vị trí 10 tạo thành phức hợp mở. Một vùng xoắn kép khoảng 17 cặp base được tháo xoắn. ARN polymerase xúc tác sự tổng hợp với sự tham gia của GTP hoặc ATP. Đoạn ngắn ARN mới được tổng hợp (~ 12 nucleotid) được xoắn kép tạm thời với ADN.
- Giai đoạn kéo dài chuỗi: Phân tử ARN polymerase di chuyển dần theo chiều dài sợi ADN đã được tháo xoắn để lộ vùng khuôn sẽ được ghép bổ sung. Như vậy, chuỗi ARN được kéo dài theo chiều 5-3 với sự tham gia của yếu tố kéo dài. Sau khi đã làm khuôn thì đoạn ADN được xoắn trở lại ngay lập tức.
- Giai đoạn kết thúc: Sau khi tổng hợp được các U, đoạn ARN trước đó có thể tự bổ sung thành đoạn kép đôi gấp khúc như kẹp (nhờ yếu tố kết thúc). Đoạn ARN này chứa nucleoyid có tính chất bổ sung tạo thành cặp đôi xoắn kép. ARN ngừng tổng hợp, ARN polymerase giải phóng khỏi ADN, được dephosphoryl hóa để có thể bắt đầu một chu kỳ sao chép mới.
CÂU HỎI LƯỢNG GIÁ
1. Base nitơ trong thành phần acid nucleic dẫn xuất từ nhân:
A. Purin, Pyridin
B. Purin, Pyrol
C. Pyrimidin, Imidazol
D. Pyrimidin, Purin
2. Base nitơ dẫn xuất từ pyrimidin:
A. Uracil, Cytosin, Thymin
B. Thymin, Uracil, Guanin
C. Uracil, guanin, Hypoxanthin
D. Cytosin, Guanin, Adenin
3. Base nitơ dẫn xuất từ purin:
A. Adenin, Guanin, Cytosin
B. Guanin, Hypoxanthin , Thymin
C. Hypoxanthin, Metylhypoxanthin, Uracil
D. Guanin, Adenin, Hypoxanthin
4. Công thức sau có tên:
NH2
N N
N NH
A. Guanin
B. Adenin
C. Cytosin
D. Hypoxanthin
5. Công thức sau có tên:
N
NH2
HO N
A.Cytosin
B. Thymin
C. Hypoxanthin
D. Adenin
6. Thành phần hóa học chính của ADN:
A. Guanin, Adenin, Cytosin, Uracil, .D ribose, H3PO4
B. Adenin, Guanin, Uracil, Thymin, .D deoxyribose, H3PO4
C. Guanin, Adenin, Cytosin, Thymin, .D deoxyribose, H3PO4
D. Guanin, Adenin, Uracil, Thymin, .D deoxyribose, H3PO4
7. Thành phần hóa học chính của ARN :
A. Guanin, Adenin, Cytosin, Thymin, .D deoxyribose, H3PO4
B. Guanin, Adenin, Cytosin, Thymin, .D ribose
C. Guanin, Adenin, Cytosin, Thymin, .D ribose
D. Uracil, Thymin, Adenin, Hypoxanthin, .D deoxyribose, H3PO4
8. Thành phần hóa học chính của acid nucleic :
1. Pentose, H3PO4 , Base nitơ
2. Deoxyribose, H3PO4 , Base dẫn xuất từ purin
3. Ribose, H3PO4 , Base dẫn xuất từ pyrimidin
4. Ribose, H3PO4 , Base dẫn xuất từ pyridin
5. Deoxyribose, H3PO4 , Base dẫn xuất từ pyrol
A. 1, 2, 4 B. 1, 2, 3 C. 2, 4, 5 D. 1, 4, 5
9. Các nucleosid sau gồm :
1. Adenin nối với Ribose bởi liên kết glucosid
2. Uracil nối với Hexose bởi liên kết glucosid
3. Guanin nối với Deoxyribose bởi liên kết glucosid
4. Thymin nối với Deoxyribose bởi liên kết glucosid
5. Cytosin nối với Ribinose bởi liên kết peptid
A. 1,2,3 B. 1,3,5 C. 2,3,4 D. 1,3,4
10. Thành phần nucleotid gồm :
1. Nucleotid, Pentose, H3PO4
2. Base nitơ, Pentose, H3PO4
3. Adenosin, Deoxyribose, H3PO4
4. Nucleosid, H3PO4
5. Nucleosid, Ribose, H3PO4
A. 1, 2 B. 3, 4 C. 4, 5 D. 2, 3
Chương 7: HÓA HỌC VÀ CHUYỂN HÓA PROTID
Mục tiêu
1. Trình bày được định nghĩa, cấu tạo, tính chất chung của acid amin, peptid.
2. Trình bày được định nghĩa, cấu trúc và tính chất của protein
3. Trình bày được chức năng của protein.
4. Trình bày được sự thoái hóa chung của acid amin.
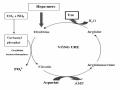
5. Trình bày được chu trình urê
PHẦN 1. HÓA HỌC PROTID
1. ĐẠI CƯƠNG
1.1. Định nghĩa
Protid là những hợp chất hữu cơ trong thành phần cấu tạo gồm bốn nguyên tố chính: C, H, O, N. Ngoài ra còn có các nguyên tố khác như: P, Fe, S, Cu, v.v..
1.2. Vai trò
- Là thành phần cấu tạo nhân và nguyên sinh chất của tế bào
- Tham gia điều khiển hoạt động sinh lý của cơ thể (insulin, corticoid).
- Xúc tác các phản ứng chuyển hóa của cơ thể (lipase, urease…).
- Tham gia vào các quá trình bảo vệ cơ thể (các kháng thể).
- Tham gia vận chyển và phân bố oxy khắp cơ thể (hemoglobin).
- Cung cấp năng lượng.
1.3. Phân loại protid
Thuật ngữ protid dùng để chỉ ba loại: acid amin, peptid và protein.
- Acid amin: Đơn vị cấu tạo nên protein.
- Peptid: Gồm từ hai đến hàng chục acid amin nối với nhau bằng liên kết peptid có phân tử lượng < 6000 dalton.
- Protein gồm hàng trăm hàng ngàn acid amin nối với nhau. Tạo thành một hoặc nhiều chuỗi polypeptid.
2. ACID AMIN
2.1. Cấu tạo
Acid amin là những chất hữu cơ trong phân tử vừa có chứa nhóm amin (-NH2) vừa có chứa nhóm carboxyl (-COOH), cùng gắn vào vị trí carbon nên các được gọi là acid
amin, một số khác có nhóm amin không gắn vào carbon , ví dụ …alanin.
Công thức chung: R-CH-COOH
NH2
Trừ prolin, còn tất cả các acid amin có cấu tạo chung như trên và chỉ khác nhau ở gốc R. Thành phần gốc R đơn giản nhất là H, hoặc là gốc hydrocarbon, hoặc còn có thêm nhóm chức -SH, -OH, -NH2, -COOH.
Acid amin là đơn vị cấu tạo của protein. Có khoảng 300 acid amin hiện diện trong tự nhiên nhưng chỉ có 20 acid amin tham gia cấu trúc protein.
Bảng 7.1. 20 acid amin tham gia vào cấu trúc protein
Tên acid amin gọi theo danh pháp hoá học | Tên viết tắt | Ký hiệu | Khối lượng (MW) | |
Glycin | Acid α-aminoacetic | Gly | G | 75 |
Alanin | Acid α-aminopropionic | Ala | A | 89 |
Prolin | Acid α-pyrolydilcarboxylic | Pro | P | 115 |
Valin | Acid α-aminoisovaleric | Val | V | 117 |
Leucin | Acid α-aminoisocaproic | Leu | L | 131 |
Isoleucin | Acid α-amino-β-metylvaleric | Ile | I | 131 |
Methionin | Acid α-amino-β-etylthiobutyric | Met | M | 149 |
Phenylalanin | A. α-amino-β-phenylpropionic | Phe | F | 165 |
Tyrosin | A. α-amino-β- hydroxyphenylpropionic | Tyr | Y | 181 |
Tryptophan | Acid α-amino-β-indolylpropionic | Trp | W | 204 |
Serin | Acid α-amino-β-hydoxypropionic | Ser | S | 105 |
Threonin | Acid α-amino-β-hydroxybutiric | Thr | T | 119 |
Cystein | Acid α-amino-β-thiopropionic | Cys | C | 121 |
Aspargin | Amid của aspartate | Asn | B | 132 |
Glutamin | Amid của glutamate | Gln | Q | 146 |
Lysin | Acid α, ε diaminocaproic | Lys | K | 146 |
Histidin | Acid α-amino-β-imidazolpropionic | His | H | 155 |
Arginin | Acid α-amino-δ-guanidinvaleric | Arg | R | 174 |
Aspartat | Acid α-aminosuccinic | Asp | D | 133 |
Glutamat | α-aminoglutarate | Glu | E | 147 |
Có thể bạn quan tâm!
-
 Giáo trình Hóa sinh Dùng cho sinh viên Cao đẳng Dược - Đại học Tây Đô - 7
Giáo trình Hóa sinh Dùng cho sinh viên Cao đẳng Dược - Đại học Tây Đô - 7 -
 Các Con Đường Thoái Hóa Tiếp Tục Của Acetyl Coa A). Oxy Hóa Ở Chu Trình Krebs
Các Con Đường Thoái Hóa Tiếp Tục Của Acetyl Coa A). Oxy Hóa Ở Chu Trình Krebs -
 Giáo trình Hóa sinh Dùng cho sinh viên Cao đẳng Dược - Đại học Tây Đô - 9
Giáo trình Hóa sinh Dùng cho sinh viên Cao đẳng Dược - Đại học Tây Đô - 9 -
 Các Peptid Thường Gặp Trong Thiên Nhiên
Các Peptid Thường Gặp Trong Thiên Nhiên -
 Sự Thủy Phân Protid Ngoại Sinh (Sự Tiêu Hóa Protid)
Sự Thủy Phân Protid Ngoại Sinh (Sự Tiêu Hóa Protid) -
 Thành Phần Hóa Học Của Mật Gồm: Sắc Tố Mật, Muối Mật, Cholesterol.
Thành Phần Hóa Học Của Mật Gồm: Sắc Tố Mật, Muối Mật, Cholesterol.
Xem toàn bộ 122 trang tài liệu này.
Các acid amin được hình thành bằng nhiều con đường khác nhau. Tuy nhiên trong cơ thể người và động vật không tổng hợp được tất cả các loại đó mà phải đưa từ ngoài vào qua thức ăn. Những acid amin phải đưa từ ngoài vào được gọi là các acid amin không thể thay thế. Người ta biết được có khoảng 8-10 loại acid amin không thể thay thế bao gồm: Met, Val, Leu, Ile, Thr, Phe, Trp, Lys, Arg và His và ngày nay người ta còn xem Cys cũng là một acid amin không thể thay thế.
2.2. Phân loại acid amin
Các acid amin được phân loại theo nhiều kiểu khác nhau, mỗi kiểu phân loại đều có ý nghĩa và mục đích riêng. Tuy nhiên, đều dựa trên cấu tạo hoá học hoặc một số tính chất của gốc R.
Hiện nay cách phân loại các acid amin được sử dụng nhiều nhất là dựa vào gốc R và được chia làm 5 nhóm:
a) Nhóm I: Gồm 7 acid amin có R không phân cực, kỵ nước, đó là: glycin, alanin, prolin, valin, leucin, isoleucin và methionin.
b) Nhóm II: Gồm 3 acid amin có gốc R chứa nhân thơm, đó là phenylalanin, tyrosin và tryptophan.
c) Nhóm III: Gồm 5 acid amin có gốc R phân cực, không tích điện, đó là serin, theonin, cystein, aspargin và glutamin.
d) Nhóm IV: 3 acid amin có R tích điện dương: lysin, histidin và arginin, trong phân tử chứa nhiều nhóm amin.
e) Nhóm V: Gồm 2 acid amin có gốc R tích điện âm, đó là aspartat và glutamat, trong phân tử chứa hai hóm carboxyl.
Hình 7.1. Công thức cấu tạo của các acid amin nhóm I (a), II (b)
Hình 7.2. Công thức cấu tạo của các acid amin nhóm III
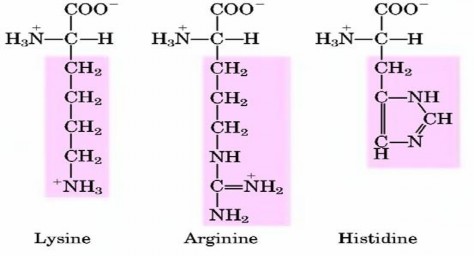
Hình 7.3. Công thức cấu tạo các acid amin nhóm IV
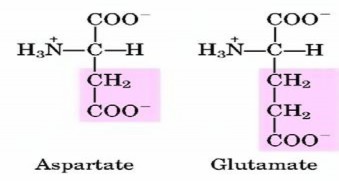
Hình 7.4. Công thức cấu tạo của các acid amin nhóm V
2.3. Tính chất của acid amin
2.3.1. Tính chất lý học
Acid amin dễ tan trong dung môi phân cực (nước, ethanol), không tan trong dung môi không phân cực (benzen, ether). Các acid amin thường có vị ngọt kiểu đường, muối natri của acid glutamic có vị ngọt kiểu đạm (được dùng làm chất gia vị).
2.3.2. Tính chất lưỡng tính
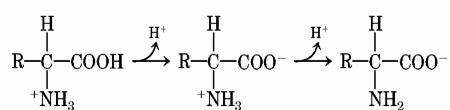
Trong phân tử acid amin có nhóm carboxyl -COOH nên có khả năng nhường proton (H+) thể hiện tính acid, mặt khác có nhóm amin –NH2 nên có khả năng nhận proton nên thể hiện tính base. Vì vậy acid amin có tính chất lưỡng tính.
Trong môi trường acid, acid amin ở dạng cation (tích điện dương), nếu tăng dần pH thì acid amin lần lượt nhường proton thứ nhất chuyển qua dạng lưỡng cực (trung hoà về điện), và tiếp tục tăng pH acid amin sẽ nhường proton thứ hai chuyển thành dạng anion (tích điện âm). Vì vậy người ta coi nó như một di-acid.
Các acid amin đều có nhóm –NH2 và -COOH liên kết với Cα, vì vậy chúng có những tính chất hoá học chung. Mặt khác các acid amin khác nhau bởi gốc R, vì vậy chúng có những phản ứng riêng biệt.
a). Phản ứng do gốc R
Do gốc R mang những nhóm hóa học khác nhau nên có thể dùng để xác định từng acid amin riêng rẽ nhờ các phản ứng đặc trưng của nó, như phản ứng oxy hoá khử (do nhóm -SH của cystein), tạo muối (do nhóm -COOH hay -NH2 của glutamat hay lysine), tạo este do nhóm -OH của tyrosin v.v...
b). Phản ứng do cả 2 nhóm α-carboxyl -COOH và α-amin
Phản ứng Ninhydrin
Tất cả các acid amin trong phân tử protein đều phản ứng với hợp chất ninhydrin tạo thành phức chất màu xanh tím, riêng imino acid như proline tạo thành màu vàng.
Phản ứng này được ứng dụng rộng rãi trong sắc ký, điện di … để xác định các acid amin định tính, định lượng).
Phản ứng tạo lên kiết peptid
Đây là phản ứng quan trọng nhất của các acid amin, xảy ra giữa nhóm α-amin của acid amin này với nhóm α-carboxyl của acid amin khác, tạo nên liên kết peptid và giải phóng một phân tử nước.