tribenzilamoni [(C6H5CH2)3NH+] thành hợp chất không mang điện tích được chiết bằng xilen.
- Kiểu 2: dung môi hữu cơ đóng vai trò rất quan trọng. Việc hình thành hợp chất bị chiết phụ thuộc vào sự có mặt của các anion thí dụ halogenua, thioxyanat, nitrat, cũng như các hợp chất hữu cơ chứa oxi, thí dụ ancol, ete, xeton, hay các ete phức tạp.
Ví dụ: Phức FeCl4- được chiết bởi ete đietyl từ dung dịch HCl ở dạng sau:
[(C2H5)2O: H+FeCl4[(C2H5)2O]-].
Nguyên tử oxi của phân tử dung môi phối trí với ion kim loại nên còn gọi hệ này là hệ oxoni. Dung môi hữu cơ tham gia vào thành phần hợp chất bị chiết.
- Kiểu 3: Ion kim loại kết hợp với các hợp chất hữu cơ có khối lượng phân tử lớn được hòa tan trong dung môi hữu cơ. Thí dụ: Chiết uran, molipđen bằng các amin có khối lượng phân tử lớn được hòa tan trong kerosin.
Câu 8:Các yếu tố ảnh hưởng đến việc hình thành dạng phức vòng càng? HDTL: Các yếu tố sau đây ảnh hưởng đến việc hình thành phức:
- Độ bazơ của nhóm chức.
- Độ âm điện của các nguyên tử tham gia liên kết.
Có thể bạn quan tâm!
-
 Đường Chuẩn Xác Định Hàm Lượng Na Trong Mẫu Cây Sồi.
Đường Chuẩn Xác Định Hàm Lượng Na Trong Mẫu Cây Sồi. -
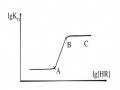
 Tách Sắc Kí Do Michael Txvet Thực Hiện, Các Hợp Phần A, B, C Có Thể Được Quan Sát Theo Trắc Diện Khoảng Cách (A) Và Trắc Diện Thời Gian (B).
Tách Sắc Kí Do Michael Txvet Thực Hiện, Các Hợp Phần A, B, C Có Thể Được Quan Sát Theo Trắc Diện Khoảng Cách (A) Và Trắc Diện Thời Gian (B). -
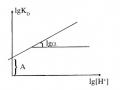
 Đường Cong Đặc Trưng Về Sự Phụ Thuộc Phần Trăm Chiết Vào Ph
Đường Cong Đặc Trưng Về Sự Phụ Thuộc Phần Trăm Chiết Vào Ph -
 Hiệu Quả Của Số Lần Chiết D = 2; V Nc = 100 Ml;
Hiệu Quả Của Số Lần Chiết D = 2; V Nc = 100 Ml; -
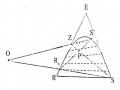
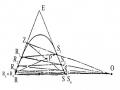
 Đường Binodan Và Đường Conot Đối Với Hệ 3 Cấu Tử Nước (R) - Axeton (E) - Clo Benzen (S).
Đường Binodan Và Đường Conot Đối Với Hệ 3 Cấu Tử Nước (R) - Axeton (E) - Clo Benzen (S). -
 Xây dựng hệ thống câu hỏi và bài tập một số chương trong phân tích lí hoá - 19
Xây dựng hệ thống câu hỏi và bài tập một số chương trong phân tích lí hoá - 19
Xem toàn bộ 167 trang tài liệu này.
- Kích thước vòng tạo thành.
Giữa độ bazơ của phối tử và tính ổn định của phức có quan hệ gắn bó với nhau.
Ví dụ: axetyl axeton (pKa = 9,7) tạo phức vòng càng với ion kim loại bền vững hơn phức hình thành giữa ion kim loại với thiophen cacbonyl trifloro axeton (pKa = 6,2) vì axyl axeton có tính bazơ mạnh hơn.
Độ âm điện của nguyên tử tạo lên liên kết với ion kim loại và độ bền phức vòng càng lớn có quan hệ tương phản. Phối tử chứa nguyên tử có độ âm điện càng kém thì phức hình thành càng bền.
Thí dụ: Điphenyl thio cacbazon tạo phức vòng càng bền hơn phức có phối tử hữu cơ chứa oxi điphenyl cacbazon.
Một yếu tố gây ảnh hưởng đến độ bền phức là kích thước của vòng tạo thành.
Ví dụ: Phức có vòng 5 cạnh và phức có vòng 6 cạnh đều là những phức bền.
Câu 9:Cân bằng trong hệ chiết vòng càng được xác định như thế nào? HDTL: Để chiết các ion kim loại, người ta phải sử dụng các thuốc thử có khả năng tạo phức vòng càng, có tính axit yếu, ví dụ cuferon, đithizon, thường được hoà tan trong dung môi hữu cơ. Nếu ta kí hiệu thuốc thử tạo phức vòng càng HR và được hoà tan trong các dung môi hữu cơ. Nó có khả năng tạo phức vòng càng với các ion kim loại. Các phản ứng xảy ra như sau:
1. Phân li thuốc thử:
HR H+ + R- Ki =
[H ][ R ] [HR]
(9.1)
2. Tạo phức vòng càng:
Mn+ + R- MR (n -1)+ K1 =
[M
[MR (n1)] [M n]
(9.2)
MR+
+ R- MR
K = [MR]n
n-1 n
= K1.K2… Kn
n
n1
][R]
3. Các phản ứng tạo phức với phối tử lạ: Mn+ + OH- = M(OH)(n-1)+
Mn+ + X- MX(n-1)+
X-: Cl-, NO , SO 2, ...
3 4
Sự phân bố của thuốc thử và phức vòng càng giữa hai dung môi.
4. Sự phân bố bản thân thuốc thử:
DR =
[HR]hc (9.3)
[HR]
5. Sự phân bố phức vòng càng: DMR =
[MRn ]hc [MRn ]
(9.4)
D =
[M n1 ]
[MRn ]
[MR (n1)] [MRn ]
...
[MRn ]hc [MRn ]
i
(M (OH ) )(ni )(MX
i j
[MRn ]
(nj )
)
j
Câu 10:Thế nào là quá trình giải chiết? Cho ví dụ? HDTL:
Giải chiết là quá trình ngược lại quá trình chiết, có nghĩa tách các nguyên tố cần chiết khỏi pha hữu cơ, để có thể xác định chúng bằng các phương pháp thích hợp. Nhờ quá trình giải chiết, người ta có thể tiếp tục tách triệt để nguyên tố cản trở khỏi nguyên tố cần xác định.
Ví dụ: Một hỗn hợp gồm 2 nguyên tố X và Y, đem chiết bằng dung môi hữu cơ có hệ số phân bố khác nhau. Giả sử nguyên tố X được chiết với hệ số phân bố 1000, còn nguyên tố Y được chiết với hệ số phân bố nhỏ hơn: 0,01. Khi chiết 2 nguyên tố trong cùng điều kiện thì trong pha hữu cơ có 99% lượng nguyên tố X và khoảng 1% lượng nguyên tố Y. Như vậy, chiết không được hoàn toàn. Nhưng nếu chúng ta trộn pha hữu cơ đó với thể tích pha nước như lần trước, nhưng trong pha này không có chứa nguyên tố X và Y, thì sau lần giải chiết này pha hữu cơ sẽ có 99,8% lượng ban đầu của nguyên tố X và chỉ có 0,01 % lượng ban đầu nguyên tố Y. Như vậy, nhờ giải chiết thực tế đã tách được khá hoàn toàn X khỏi Y. Khi tiến hành giải chiết, người ta dùng nước có thành phần (chất tạo phức, pH) khác với thành phần pha nước dùng để chiết.
Thí dụ: Khi chiết Pb2+, Cu2+, Fe2+ dưới dạng đietyl đithio cacbamat trong pha
nước pH = 4 11. Sau đó giải chiết các nguyên tố khỏi pha hữu cơ bằng các dung dịch nước khác nhau.
Thí dụ : Dung dịch HCl 0,4M thì giải chiết được Zn, HCl 4M thì giải chiết được Pb, còn Fe, Cu vẫn ở lại trong pha hữu cơ.
Câu 11: Phương pháp chiết lỏng - lỏng là gì? Giữa chiết và chưng cất có một điểm giống nhau là gì?
HDTL:
+ Chiết lỏng - lỏng hay còn gọi là chiết dung môi, là một phương pháp tách dựa vào sự phân bố khác nhau của những chất cần tách giữa hai pha lỏng không trộn lẫn. Bởi không thể thu được chất sạch chỉ qua 1 lần đạt cân bằng nên người ta tăng hiệu quả tách bằng cách, chiết ngược dòng trong cột hoặc thực hiện tách qua nhiều bậc nối tiếp nhau…
+ Giữa chiết và chưng cất có một điểm giống nhau là ở cả hai phương pháp cần tách phân bố với lượng khác nhau trong cả hai pha. Có điều trong chưng cất khi pha thứ hai (pha hơi) chứa một thành phần của pha lỏng ban đầu thì ở phương pháp chiết để tạo ra pha thứ hai (pha lỏng) người ta phải đưa chất vào, đó là đưa dung môi vào. Chất này tham dự vào cân bằng chất của phương pháp và xác định sự đặc trưng của phương pháp tách thông qua quan hệ của nó với chất cần tách. Trong phương pháp chiết, điều này thể hiện đơn giản nhất trong hệ 3 cấu tử.
Câu 12: Đặc tính chung của phương pháp chiết cấu tử đa lượng? HDTL:
- Phép cô đặc của vết vi lượng bằng cách chiết cấu tử đa lượng dựa trên khả năng tiến hành phép chiết này một cách chọn lọc (các nguyên tố vi lượng cần phải còn lại một cách định lượng trong pha nước).
- Cấu tử đa lượng cần phải được hoàn toàn loại trừ từ pha nước, tuy nhiên việc tuân theo điều kiện này trong một số trường hợp, đặc biệt trong các phép xác định hóa quang phổ thì không nhất thiết. Ngoài ra phần còn lại của nguyên tố đa lượng có khi được dùng để làm chất mang.
- Phép chiết các nguyên tố đa lượng có thể dùng tốt để cô đặc, về nguyên tắc chỉ được áp dụng khi mà mẫu cần phân tích có thành phần tương đối đơn giản về các cấu tử đa lượng.
- Việc tách chất cơ bản không làm nhiễm bẩn pha nước, do vậy cần làm việc một cách hợp lí với một số lượng nhỏ nhất và một lượng có thể nhỏ nhất của các thuốc thử và với các thuốc thử dễ dàng nhận được ở dạng sạch.
- Ví dụ: Việc chiết các axit phức kim loại halogenua như HGaCl4, HFeCl4, HInBr4 và các axit phức khác chỉ cần dùng một dung môi có chứa oxi với dung lượng chiết lớn sẽ thuận lợi hơn so với việc chiết các hợp chất nội phức. Các hợp chất nội phức khó hòa tan trong dung môi hữu cơ.
Ngoài ra, để chiết chúng cần một số lớn các thuốc thử, đặc biệt là các thuốc thử chelat, dung môi hữu cơ và các thuốc thử để điều chỉnh pH.
- Hiệu quả của cô đặc chiết dựa trên sự chiết cấu tử đa lượng ở một mức độ đáng kể phụ thuộc vào việc giải quyết nhiều vấn đề lí thuyết chung. Thuộc nhóm các vấn đề này, trước hết phải kể đến vấn đề ảnh hưởng của cấu tử đa lượng lên chiết của các cấu tử vi lượng (ảnh hưởng tương hỗ của các nguyên tố lên việc chiết) và ảnh hưởng của nồng độ nguyên tố đa lượng lên hệ số phân bố của nó.
Câu 13:Hãy nêu các phương pháp cô đặc?
HDTL: Để cô đặc chiết, người ta dùng chủ yếu các phương pháp chiết sau trong các hệ lỏng - lỏng:
1. Chiết chu kỳ trong đó chất được chiết được chuyển từ một pha vào một pha khác khi có sự lắc hai pha.
2. Chiết liên tục trong đó dung môi chiết đi qua dung dịch phân tích liên tục.
3. Chiết ngược dòng, trong số đó có chiết ngược dòng tuần hoàn.
4. Sắc kí chiết.
Câu 14:Hãy cho biết phương trình Van Deemter có ý nghĩa như thế nào? HDTL:
Từ lí thuyết đĩa, có thể xác định được các đại lượng đặc trưng quan trọng là n (số đĩa lí thuyết) và h (độ cao của một đĩa lí thuyết) nhưng không
cho biết ảnh hưởng của các điều kiện làm việc (nhiệt độ, áp suất, tốc độ dòng…) đến các đại lượng nói trên. Chỉ sau khi có sự hỗ trợ của lí thuyết động học, đặc biệt là với sự ra đời của phương trình Van Deemter, thì mọi ảnh của các thông số thực nghiệm lên các đại lượng nói trên mới được làm sáng tỏ. Phương trình Van Deemter được biểu diễn như sau: h = 2 dp +
2D
8k d 2
G+
i f .u
i
f
u 2 (1 k ) 2 D
Trong đó: u : tốc độ trung bình của dòng khí mang.
: độ không đồng nhất của chất nhồi cột.
dp : đường kính trung bình của hạt chất mang.
: hệ số Labyrinth về đường đi của khí trong cột. DG: hệ số khuếch tán phân tử trong pha khí .
DF : hệ số khuếch tán phân tử trong pha lỏng.
ki : hệ số dung lượng.
df : độ dày của lớp phim pha tĩnh trên chất mang.
Phương trình Van Deemter thu gọn có thể được diễn đạt như sau:
Trong đó:
h = A +
B + C u
u
A: đại diện cho sự khuếch tán tán xạ (còn gọi là khuếch tán Eddy), cho những thông tin về đường đi khác nhau của khí do chất nhồi cột quyết định.
B: đại diện cho những chỉ dẫn về sự khuếch tán phân tử trong pha khí.
C: biểu thị trở kháng của cột trong quá trình chuyển khối trong pha động cũng như trong pha tĩnh.
Câu 15:Đặc tính chung của phương pháp chiết - huỳnh quang là gì? HDTL:
- Các phương pháp phân tích dựa trên sự chiết các hợp chất nội phức và việc đo huỳnh quang trong dịch chiết về độ phổ biến và ý nghĩa thì kém hơn các phương pháp chiết - trắc quang. Tuy nhiên, đặc điểm quan trọng và ưu việt của chúng so với các phương pháp chiết - trắc quang là độ nhạy cao hơn.
- Số lớn nhất các phương pháp chiết - huỳnh quang trong đó có dùng các hợp chất nội phức được nghiên cứu cho Al va Ga. Người ta cũng biết các phương pháp đối với Inđi, các nguyên tố đất hiếm và một số nguyên tố khác.
- Các phương pháp chiết - huỳnh quang có một số ưu điểm so với các phương pháp huỳnh quang trong pha nước, các ưu điểm, ở một mức độ đáng kể tương tự các ưu điểm đã lưu ý đối với các phương pháp chiết trắc quang.
- Không ít phương pháp chiết - huỳnh quang đảm bảo có độ nhạy cao của phép xác định. Ví dụ, độ nhạy của phép xác định chiết - huỳnh quang của Ga đối với lumogalion 3,5 lần cao hơn độ nhạy của phép xác định trong dung dịch nước.
- Cường độ huỳnh quang tăng khi chiết các hợp chất này của Ga với các thuốc thử tương tự. Khi chiết phức của Zn với 8 - (n - tozilamino) - quinolin thì cường độ huỳnh quang cũng tăng lên.
- Sự tăng độ chọn lọc của phép xác định có thể được đảm bảo bằng cách phân chia chiết bình thường các nguyên tố cần xác định và cản trở.
- Cũng như trong tất cả các phương pháp dựa trên sự chiết các hợp chất nội phức, ảnh hưởng của dung môi trong các phép xác định chiết - huỳnh quang luôn luôn phải tính đến. Trước hết điều này có liên quan đến việc chọn dung môi theo quan điểm chiết được hoàn toàn nguyên tố.
Câu 16:Làm thế nào để có thể tìm được diện tích dưới pic? HDTL:
Phần lớn các máy sắc kí hiện nay đã được trang bị máy tích phân điện tử. Tuy nhiên nếu không có máy tích phân thì có 2 phương pháp gần đúng có
thể áp dụng rất tốt và cho kết quả chỉ khác vài phần trăm so với diện tích thực.
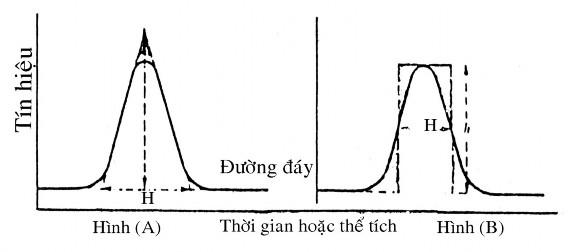
Hình 4.5 (A): Pic được làm gần đúng bằng một tam giác. Hình 4.5 (B): Pic được làm gần đúng bằng một hình chữ nhật.
Trong cả 2 phương pháp, người ta đều giả thiết rằng phần diện tích pic bị bỏ qua sẽ bằng một diện tích hình học nằm bên ngoài pic. Phương pháp hình chữ nhật của hình 4.5 (B) đúng hơn và được dùng nhiều hơn phương pháp tam giác. Rõ ràng cả hai phương pháp đều đòi hỏi pic có bề ngang vừa phải để cho giá trị diện tích đáng tin cậy. Phương pháp tích phân điện tử có thể cho được những giá trị diện tích đáng tin cậy. Phương pháp tích phân điện tử có thể cho được những giá trị diện tích đúng lặp lại tốt hơn 1 % còn các phương pháp tính diện tích gần đúng thường lặp lại từ 3 đến 4%...
Hình 4.5
Đo diện tích của pic: (A): diện tích pic = diện tích tam giác =
1 a.W.
2
(B): diện tích pic = diện tích hình chữ nhật = h.W1/2 W1/2 :Chiều ngang của pic ở nửa độ cao.
Khi chiều ngang pic quá bé nhà phân tích có thể dựa vào việc đo chiều cao pic. Chiều cao pic sẽ tỉ lệ thuận với diện tích pic (và do đó sẽ tỉ lệ với lượng chất phân tích) nếu mọi biến số đều được giám sát chặt chẽ. Tuy vậy chỉ một thay đổi nhỏ trong vận tốc chảy, vận tốc phun mẫu hoặc nhiệt độ đã có gây