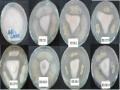
Thí nghiệm 3.2: Tuyển chọn chủng vi sinh vật vùng rễ có khả năng kháng nấm Fusarium trên cây hồ tiêu con trong điều kiện vườn ươm
- Chuẩn bị nguồn bệnh cho lây bệnh nhân tạo: Chủng nấm Fusarium oxysporum nuôi cấy trên môi trường PGA trong 5 ngày, ở 28oC. Chuyển sợi nấm sang bình tam giác chứa 50 ml môi trường Potato Glucose lỏng, nuôi trên máy lắc với tốc độ 150 vòng/ phút trong 2 ngày ở 28oC. Mật độ bào tử được điều chỉnh đạt 108CFU/ml được coi là dịch gốc.
- Phương pháp bố trí thí nghiệm: gồm 8 nghiệm thức (2 nghiệm thức đối chứng và 6 nghiệm thức sử dụng vi khuẩn), được bố trí với 3 lần lặp lại. Ngâm hom trong 10 ml dịch vi khuẩn với mật độ108CFU/ml, thời gian 30 phút trước khi giâm hom. Giâm hai hom/bầu. Mỗi nghiệm thức 15 bầu. Chăm sóc cây hồ tiêu theo đúng quy trình chăm sóc cây trong vườn ươm của Bộ Nông nghiệp và Phát triển Nông thôn (Số 730/QĐ- BNN-TT). Sau khi tiêu đạt 5 lá thật, loại bỏ những cây không đủ số lá, 1 cây con/bầu, chiều cao đồng đều, tiến hành lây bệnh nhân tạo. Các nghiệm thức RB.CJ4, RB.CJ12, RB.CJ27, RB.CJ41, RB.DC16, RB.EK2 và ĐC1 được lây bệnh nhân tạo với nấm Fusarium oxysporum, sau 15 ngày bổ sung các chủng vi khuẩn với mật độ đã chuẩn bị lần lượt là RB.CJ4, RB.CJ12, RB.CJ27, RB.CJ41, RB.DC16, RB.EK2. Nghiệm
thức ĐC 2: Không lây nhiễm nấm bệnh và không bổ sung vi khuẩn.
* Phương pháp lây bệnh nhân tạo: Thí nghiệm lây bệnh nhân tạo được tiến hành trong nhà lưới, thí nghiệm được bố trí theo kiểu khối đầy đủ ngẫu nhiên (RCBD). Tổng số cây thí nghiệm: 8 nghiệm thức x 15 cây/ nghiệm thức x 3 lần nhắc lại = 360 cây.
Bảng 2.2. Sơ đồ bố trí thí nghiệm tuyển chọn chủng vi sinh vật vùng rễ có khả năng kháng nấm Fusarium trên cây hồ tiêu con trong điều kiện vườn ươm
1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | |
I | ĐC 1 | RB.CJ 4 | RB.EK 2 | RB.CJ 12 | RB.DC16 | RB.CJ 27 | ĐC 2 | RB.CJ 41 |
CÁCH LY | ||||||||
II | RB.CJ 12 | ĐC 2 | RB.DC16 | ĐC 1 | RB.CJ 41 | RB.CJ 4 | RB.CJ 27 | RB.EK 2 |
CÁCH LY | ||||||||
III | RB.CJ 41 | RB.DC16 | ĐC 2 | RB.CJ 27 | RB.CJ 12 | RB.EK 2 | RB.CJ 4 | ĐC 1 |
Có thể bạn quan tâm!
-
 Các Giải Pháp Tổng Hợp Để Kiểm Soát Dịch Bệnh Trên Cây Hồ Tiêu Và Sản Xuất Bền Vững
Các Giải Pháp Tổng Hợp Để Kiểm Soát Dịch Bệnh Trên Cây Hồ Tiêu Và Sản Xuất Bền Vững -
 Tình Hình Nghiên Cứu Về Vi Sinh Vật Vùng Rễ Trên Cây Hồ Tiêu
Tình Hình Nghiên Cứu Về Vi Sinh Vật Vùng Rễ Trên Cây Hồ Tiêu -
 Phương Pháp Tuyển Chọn Các Chủng Vi Khuẩn Phân Lập Từ Vùng Rễ Cây Hồ Tiêu Tại Tây Nguyên, Định Danh Các Chủng Có Tiềm Năng Kháng Phytophthora, Fusarium
Phương Pháp Tuyển Chọn Các Chủng Vi Khuẩn Phân Lập Từ Vùng Rễ Cây Hồ Tiêu Tại Tây Nguyên, Định Danh Các Chủng Có Tiềm Năng Kháng Phytophthora, Fusarium -
 Chương Trình Pha Động Trên Cột C18
Chương Trình Pha Động Trên Cột C18 -
 Quy Trình Phân Tách Các Hợp Chất Vk01, Vk02, Vk03 Và Vk05
Quy Trình Phân Tách Các Hợp Chất Vk01, Vk02, Vk03 Và Vk05 -
 Hiệu Quả Kháng Phytophthora Capsici Trên Đoạn Thân Hồ Tiêu
Hiệu Quả Kháng Phytophthora Capsici Trên Đoạn Thân Hồ Tiêu
Xem toàn bộ 224 trang tài liệu này.

Bổ sung 10ml dịch bào tử nấm Fusarium oxysporum (Mật độ 108CFU/ml) vào mỗi bầu hồ tiêu. Sau 15 ngày, bổ sung 10ml dịch khuẩn gốc đã chuẩn bị vào mỗi bầu hồ tiêu.
Chỉ tiêu theo dõi sau 4 tháng lây nhiễm nấm bệnh
+ Số lá/cây, diện tích lá (mm2), chiều cao cây hồ tiêu (cm), đường kính cây hồ tiêu (mm), khối lượng cây tươi (g), khối lượng cây khô (g), khối lượng rễ tươi (g), khối lượng rễ khô (g), số rễ hồ tiêu, chiều dài rễ (cm), hàm lượng diệp lục tố (chlorophyll) và carotenoid được phân tích bằng phương pháp quang phổ được thực hiện theo phương pháp của Yoshida và cộng sự (1976) [124].
+ Số rễ bệnh để đánh giá tỷ lệ rễ bệnh:
Tỉ lệ bệnh (%) =Tổng số rễ bị bệnh/ tổng số rễ điều tra) x100
+ Mật độ Fusarium sp. trong đất: Mẫu đất sau 120 ngày lây nhiễm với nấm Fusarium sp. được gửi phân tích tại Viện Công nghệ Sinh học và Môi trường, Trường Đại học Tây Nguyên. Phương pháp pha loãng dung dịch đất được sử dụng để phân lập, xác định mật độ các loài nấm bệnh trong đất. Sử dụng môi trường PPA có bổ sung kháng sinh để phân lập nấm Fusarium spp. Thành phần 1lít môi trường PPA bao gồm: 20 g Agar, 15 g Peptone, 1g KH2PO4, 0,5 g MgSO4.7H2O, 1 g Terrachlor (PCNB 75%), 1g Streptomycin sulfate, 0,12 g Neomycinsulfate. Cân Agar, Peptone, KH2PO4, MgSO4.7H2O và Terrachlor theo tỷ lệ rồi thêm nước cất thành 1 lít hỗn hợp. Điều chỉnh pH = 6. Khuấy đều, hấp ở 121oCtrong 20 phút, để nguội xuống 55oC, bổ sung 20 ml nước cất tiệt trùng đã hòa tan 1 g Streptomycin sulfate và 12 ml nước cất tiệt trùng đã hòa tan 0,12 g Neomycin sulfate vào môi trường, khuấy đều rồi đổ môi trường ra đĩa petri.
1. Đất mang về phòng thí nghiệm, trải mỏng trên khay sạch để phơi khô tự nhiên ở điều kiện phòng trong 24 - 48 giờ, tùy độ ẩm đất. Mỗi mẫu đất được làm tơi, trộn đều và phơi trên mỗi khay riêng. Sau đó, dùng chày và cối sứ tiệt trùng để nghiền sơ đất, sàng qua rây có đường kính lỗ rây 710 μm và trộn đều.
2. Cho 10g mẫu đất vào một lọ có chứa 90mL WA 0.01% đã hấp tiệt trùng, tạo dung dịch có độ pha loãng 10-1.
3. Đổ 10mL dung dịch sang lọ thứ hai chứa 90mL WA 0.01% tạo dung dịch có độ pha loãng 10-2 và lắc đều để đảm bảo đất được phân tán đều trong dung dịch. Lặp lại bước này để có dung dịch với độ pha loãng 10-3.
4. Phân tán đều 1mL dung dịch đất trên bề mặt môi trường thạch trên đĩa Petri đường kính 90mm: (1) Chuẩn bị các đĩa môi trường thạch và để khô trong vài ngày;
(2) Dùng pipette cẩn thận hút 1mL dung dịch đất cho vào một phía ở rìa của đĩa môi
trường; (3) Cầm đĩa hơi nghiêng từ mép có dung dịch và lắc nhẹ vuông góc với chiều dốc để dung dịch ướt đều trên bề mặt đĩa.
5. Đặt các đĩa thạch ở điều kiện nhiệt độ phòng trong 5-7 ngày cho đến khi các tản nấm phát triển.
Nấm được định danh dựa vào khoá phân loại bằng hình thái của Seifert (1996), Leslie và Summerell (2006) và Tatiana Gagkaeva (2008) [127-129]. Số lượng những đơn vị tạo tản nấm (Colony-Forming Units - CFU) trong mỗi gram đất được tính như sau: Độ pha loãng × số tản nấm trung bình của loài nấm trên các đĩa phân lập = CFU/g đất.
Thí nghiệm 3.3:Tuyển chọn chủng vi sinh vật vùng rễ có khả năng tuyến trùng trên cây hồ tiêu con trong điều kiện vườn ươm
*Phương pháp chung
- Chuẩn bị vườn ươm: vườn ươm được che lưới phía trên và xung quanh, nhiệt độ từ 25-30oC, độ ẩm từ 70 -80 %, cường độ ánh sáng 50-500 µmol m2/s-1(đo từ 8h-16h).
- Chuẩn bị đất trồng hồ tiêu: Đất ươm hồ tiêu phải chọn đất tốt, không lấy đất ở những vùng trồng cây đã bị tuyến trùng, nấm bệnh gây hại. Đất được đập nhỏ, tạo lớp mỏng phơi nắng 1 ngày trước khi vào bịch. Thành phần đất trồng trong bịch theo tỷ lệ đất: cát: phân chuồng là 2:1:1. Phối trộn, ẩm độ 60 – 70%. Đóng bịch: 1 kg/ bịch. Hấp khử trùng: 90 – 950 C, 1giờ, để nguội, ươm trồng hồ tiêu.
- Chuẩn bị bầu ươm hồ tiêu: Bầu ươm kích thước: 13 x 22cm; có 8 lỗ thoát nước ở nửa dưới bầu phân bố thành 2 hàng, hàng dưới cách đáy bầu khoảng 2 cm.
+ Chuẩn bị dịch vi khuẩn: Các chủng vi khuẩn được nuôi cấy trên môi trường LB Agar trong 24 giờ, sau đó chuyển vào bình 200ml chứa môi trường LB, nuôi cấy lắc với tốc độ 150 vòng/ phút trong 2 ngày ở 25 oC. Tế bào vi khuẩn được điều chỉnh ở mật độ 108 CFU /ml được coi là dịch khuẩn gốc.
- Chuẩn bị hom giống hồ tiêu: Theo Tiêu chuẩn cơ sở về cây giống hồ tiêu (TCCS 07: 2012/BP). Chọn dây lươn giống hồ tiêu Vĩnh Linh. Đối với hom dây lươn chọn những dây lươn bánh tẻ, cắt thành các hom giống, mỗi hom 2 đốt. Dây lươn không sâu bệnh, được lấy ở các vườn tiêu 4 tuổi không có triệu chứng bệnh. Hom được cắt hết lá khi đem ươm, cắt hom vào buổi sáng, khi trời mát.
- Phương pháp bố trí thí nghiệm: Thí nghiệm gồm 8 nghiệm thức (2 nghiệm thức đối chứng và 6 nghiệm thức sử dụng vi khuẩn vùng rễ), được bố trí với 3 lần lặp lại.
Ngâm hom trong 10 ml dịch vi khuẩn với mật độ108CFU/ml, thời gian 30 phút trước khi giâm hom. Tiến hành giâm hai hom/bầu. Mỗi nghiệm thức 15 bầu. Chăm sóc cây hồ tiêu theo đúng quy trình chăm sóc cây trong vườn ươm của Bộ Nông Nghiệp và Phát Triển Nông Thôn (quyết định số 730/QĐ-BNN-TT). Sau khi cây hồ tiêu đạt 5 lá thật, loại bỏ những cây không đủ số lá, 1 cây con/bầu, chiều cao đồng đều, tiến hành lây bệnh nhân tạo. Các nghiệm thức RB.BH11, RB.EK2, RB.CJ4, RB.CS30, RB.DS33, RB.EK7,
ĐC1 được chủng nhiễm tuyến trùng Meloidogyne sp., sau 15 ngày bổ sung các chủng vi khuẩn với mật độ đã chuẩn bị lần lượt là RB.BH11, RB.EK2, RB.CJ4, RB.CS30, RB.DS33, RB.EK7. Nghiệm thức ĐC 2: Không chủng nhiễm tuyến trùng và không bổ sung vi khuẩn.
- Phương pháp lây bệnh nhân tạo: Thí nghiệm lây bệnh nhân tạo được tiến hành trong nhà lưới, thí nghiệm được bố trí theo kiểu khối đầy đủ ngẫu nhiên (RCBD). Tổng số cây thí nghiệm: 8 nghiệm thức x 10 cây/ công thức x 3 lần nhắc lại = 240 cây.
Bảng 2.3. Sơ đồ bố trí thí nghiệm tuyển chọn chủng vi sinh vật vùng rễ có khả năng kháng tuyến trùng Meloidogyne sp. trên cây hồ tiêu con trong điều kiện vườn ươm
1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | |
I | RB.EK2 | RB.CJ4 | RB.BH11 | RB.EK7 | ĐC1 | RB.CS30 | RB.DS33 | ĐC2 |
CÁCH LY | ||||||||
II | ĐC1 | RB.CS30 | RB.DS33 | RB.EK2 | ĐC2 | RB.EK7 | RB.CJ4 | RB.BH11 |
CÁCH LY | ||||||||
III | ĐC2 | RB.EK7 | RB.CJ4 | RB.CS30 | RB.BH11 | RB.DS33 | RB.EK2 | ĐC 1 |
Chủng nhiễm tuyến trùng 3 lần, mỗi lần cách nhau 5 ngày vào mỗi bầu hồ tiêu. Lượng tuyến trùng chủng nhiễm mỗi đợt: 350 J2/lần/bầu. Theo dõi 4 tháng sau khi chủng nhiễm tuyến trùng các chỉ tiêu sau:
- Các chỉ tiêu sinh trưởng: Số lá/cây, diện tích lá (mm2), chiều cao cây hồ tiêu (cm), đường kính cây hồ tiêu (mm), khối lượng cây tươi (g), khối lượng cây khô (g), khối lượng rễ tươi (g), khối lượng rễ khô (g), số rễ hồ tiêu, chiều dài rễ (cm), hàm lượng diệp lục tố (chlorophyll) và carotenoid được phân tích bằng phương pháp quang phổ được thực hiện theo phương pháp của Yoshida và cộng sự (1976) [124].
+ Số u sưng: đếm tất cả số u sưng có trên rễ
+ Tỷ lệ rễ u sưng (%) = (Tổng số rễ u sưng/ Tổng số rễ điều tra) x100
+ Mật độ tuyến trùng trong đất (con/50g đất): Tuyến trùng trong đất được lọc bằng phương pháp lọc Berman có cải tiến của Southey (1986) [130]. Cân 50 g đất
cho vào rây có đường kính 10 cm, bên trong rây đặt một mảnh vải lọc không cho đất và tàn dư thực vật rơi xuống đĩa petri. Đặt rây vào đĩa petri và cho nước vào, giữ mực nước cho ngập 1/2 chiều cao rây. Tuyến trùng di chuyển qua màng lọc và rớt xuống đĩa petri. Thời gian lọc là 24 giờ ở điều kiện nhiệt độ phòng. Thu lấy dịch lọc và dùng kính hiển vi để xác định thành phần và mật độ tuyến trùng.
+ Tuyến trùng trong rễ (con/5g rễ): tuyến trùng trong rễ được ly trích bằng phương pháp lọc qua rây. Mẫu rễ sau khi thu thập, rửa sạch đất dưới vòi nước mạnh, để ráo nước, cắt thành từng đoạn khoảng 0,5cm. Trộn đều mẫu, cân 5g rễ cho vào máy xay sinh tố chứa 100 ml nước, xay ba lần, mỗi lần 10 giây, sau mỗi lần xay nghỉ 10 giây. Hỗn hợp sau đó được chuyển sang rây lọc đường kính 10 cm và để ở điều kiện phòng 24 giờ- 48 giờ, tuyến trùng di chuyển qua màng lọc và rớt xuống đĩa. Khi đã đủ thời gian, bỏ rây ra khỏi đĩa, dùng bình tia xịt xung quanh và đáy đĩa để đảm bảo tuyến trùng không bị sót lại ở những vị trí này. Dịch lọc tuyến trùng bên trong đĩa được chuyển sang cốc đong thủy tinh dung tích 100 ml. Xác định mật độ tuyến trùng trong dịch lọc bằng kính hiển vi soi nổi.
Thí nghiệm 4: Định danh các chủng có tiềm năng kháng Phytophthora, Fusarium, kháng tuyến trùng Meloidogyne gây bệnh rễ ở cây hồ tiêu
*Thời gian nghiên cứu: nghiên cứu được thực hiện từ tháng 03/2019 – 04/2019
* Đối tượng nghiên cứu: chủng RB.DS29 kháng Phytophthora capsici, chủng RB.CJ41 kháng nấm Fusarium oxysporum và chủng RB.EK7 kháng tuyến trùng Meloidogyne sp. đã được tuyển chọn từ thí nghiệm 3.
* Phương pháp định danh truyền thống dựa trên hệ thống phân loại Bergey: được thực hiện thông qua các thử nghiệm bao gồm đặc điểm khuẩn lạc, đặc điểm hình thái tế bào, nhuộm Gram, một số thử nghiệm sinh hóa như: catalase, thử nghiệm khả năng lên men một số loại đường như glucose, arabinose, malnitose, xylose, thử nghiệm citrate, nitrate, arginine, indol, thử nghiệm tính di động, thử nghiệm ONPG và thử nghiệm VP, MR.
+ Mô tả các đặc điểm hình thái khuẩn lạc của các chủng vi khuẩn và làm tiêu bản tế bào để xem trên kính hiển vi. Các khuẩn lạc được quan sát bằng mắt thường và bằng kính hiển vi soi nổi 20X, 40X nhằm mô tả các đặc điểm của khuẩn lạc bao gồm: hình dạng, màu sắc, bề mặt, mép, mặt cắt ngang, cấu trúc hạt. Tiêu bản tế bào nhuộm gram được quan sát ở kính hiển vi quang học 10X, 40X và 100X.
+ Thử nghiệm catalase nhằm phát hiện enzyme catalase của vi sinh vật, catalase thủy phân hydrogen peroxide (H2O2) thành H2O và O2.
+ Thử nghiệm tính di động dựa vào sự quán sát khả năng tăng trưởng và di động của vi sinh vật trong môi trường thạch mềm chứa 0.5 % agar.
+ Thử nghiệm lên men một số loại đường nhằm thử nghiệm khả năng sử dụng các nguồn carbonhydrate của các vi sinh vật. VSV sử dụng nguồn đường trong môi trường phenolred broth base có bổ sung 0.5 – 1% đường cần thử nghiệm tạo acid làm giảm pH của môi trường nuôi cấy và làm thay màu chất chỉ thị phenol red
+ Thử nghiệm nitrate nhằm xác định khả năng khử nitrate thành nitrite hoặc sinh hơi nitrogen tự do của vi sinh vật.
+ Thử nghiệm citrate nhằm xác định khả năng sử dụng citrate như nguồn cacbon duy nhất. VSV sử dụng citrate, sinh khí CO2 làm kiềm hóa môi trường.
+ Thử nghiệm ONPG nhằm xác định khả năng sử dụng lactose để tổng hợp hai enzyme là β- galactosidase (Vai trò xúc tác thủy phân lactose) và permase (vai trò vận chuyển lactose vào bên trong tế bào). ONPG (D- galactopyranoside) được sử dụng làm cơ chất để xác định khả năng tổng hợp enzyme β- galactosidase của vi khuẩn. Quá trình thủy phân cơ chất phóng thích o-nitrophenol có màu vàng.
+ Thử nghiệm VP (Voges – Proskauer) được thực hiện nhằm phát hiện nhóm vi sinh vật tạo sản phẩm trung tính acetoin (acetylmethylcarbinol, AMC) trong quá trình lên men glucose.
+ Thử nghiệm Indol nhằm phát hiện khả năng sinh indol nhờ hệ enzyme tryptophanase của vi sinh vật.
* Phương pháp định danh sinh học phân tử: Quy trình giải trình tự gen được thực hiện như sau:
+ Tách chiết bộ gen vi khuẩn theo quy trình của Qiagen: (1)Thu sinh khối dịch nuôi cấy ở 8.000 vòng/phút, trong 5 phút; (2) Huyền phù sinh khối với 54% TE và 25 μl lysozyme nồng độ 5 mg/ml và ủ ở 37 oC, 30 phút; (3) Bổ sung 30 μl SDS 10% và 3 μl protein K 20 mg/ml, đảo đều và ủ 1 giờ, 37 oC; (4) Bổ sung 800 μl chloroform, lắc mạnh, ly tâm 12.000 vòng/phút trong 5 phút, thu dịch nổi; (5) Bổ sung phenol (bằng thể tích dịch nổi thu được), vortex, ly tâm, thu dịch nổi; (6) Bổ sung Phenol: Chloroform (bằng thể tích dịch thu được), vortex, ly tâm, thu dịch nổi (thực hiện 2 lần); (7) Bổ sung Chloroform bằng thể tích dịch nổi thu được, vortex, ly tâm thu dịch
trong (thực hiện 2 lần); (8) Thêm 10 μl RNase (20 μg/ul), ủ 30 phút ở nhiệt độ phòng;
(9) Bổ sung 0,7 lần thể tích Isopropanol, ly tâm 12.000 vòng/phút trong 5 phút, thu tủa; (10) Rửa tủa bằng 500 μl ethanol 70 % và bảo quản ở -20 oC.
+ Khuếch đại trình tự 16S rRNA: Sử dụng cặp mồi 27F (5’- AGAGTTTGATCMTGGCTCAG-3’), mồi ngược: 1492R (5’-
TACGGYTACCTTGTTACGACTT-3’) để khuếch đại vùng 16S rDNA của vi khuẩn với khuôn là DNA bộ gen đã tách chiết ở trên [131]. Thành phần của phản ứng PCR thu gen với thể tích 100 µl bao gồm Buffer có Mg2+ (1X), dNTP (200 µM), mồi xuôi (0,25 pmo), mồi ngược (0,25 pmo), sợi khuôn (300 - 500 ng), enzyme Pfu (2u). Chu trình nhiệt được thực hiện gồm 1 chu kỳ: 95C, 5 phút; 30 chu kỳ: 95C, 30 giây; 55C, 30 giây ; 72C, 1,5 phút; 3 chu kỳ: 72C, 5 phút; Bảo quản ở 4C.
+ Tinh chế sản phẩm PCR: Sản phẩm khuếch đại được tinh chế bằng bộ kít QIAquick PCR Purification. Quy trình thực hiện như sau: Hỗn hợp sản phẩm PCR được cho vào một eppendorf 1,5 ml; Bổ sung buffer PB với tỷ lệ 5:1 (v/v) so với thể tích sản phẩm PCR, trộn đều; Chuyển dung dịch vào cột tinh chế. Ly tâm 9000 vòng/phút trong 30 – 60 giây, đổ bỏ dịch sau khi qua cột; Bổ sung 750 µl buffer PE vào cột để rửa. Ly tâm 9000 vòng/phút trong 30 – 60 giây, đổ bỏ phần dịch sau khi qua cột; Ly tâm lại 9000 vòng/phút trong 1 phút để loại bỏ hoàn toàn buffer PE; Chuyển cột sang một eppendorf 1,5 ml mới; Bổ sung 30 – 50 µl Buffer EB (10mM Tris-HCl, pH 8,5) hay Mili Q vào chính giữa cột, ủ 1 phút ở nhiệt độ phòng; Ly tâm 9000 vòng/phút trong 2 phút, thu phần dịch chứa gen; Bảo quản ở nhiệt độ -20oC.
+ Giải trình tự 16S rDNA: Sản phẩm khuếch đại sau khi tinh chế được gửi giải trình tự tại công ty Macrogen (Hàn Quốc) với cặp mồi 27F và 1492R. Kết quả giải trình tự được xử lý bằng phần mềm BioEdit. Các trình tự nucleotide hoàn chỉnh được so sánh với ngân hàng dữ liệu gen của NCBI bằng công cụ BLAST.
+ Phương pháp xây dựng cây phát sinh loài: Cây phát sinh loài được xây dựng bằng phần mềm MEGA version 6.0.
2.2.2. Nghiên cứu đặc tính và xác định hoạt chất kháng Phytophthora/Fusarium, tuyến trùng Meloidogyne của các chủng vi khuẩn tiềm năng được tuyển chọnThí nghiệm 5:Nghiên cứu điều kiện nhân sinh khối của các chủng vi khuẩn vùng rễ tuyển chọn
*Thời gian và địa điểm nghiên cứu: Nghiên cứu được thực hiện từ tháng 4/2019- 07/2019 tại phòng Công nghệ Vi sinh, Viện CNSH&MT và phòng Công nghệ vi sinh, Bộ môn Sinh học, trường ĐH Tây Nguyên
*Đối tượng nghiên cứu: chủng RB.DS29 kháng Phytophthora capsici, chủng RB.CJ41 kháng nấm Fusarium oxysporum và chủng RB.EK7 kháng tuyến trùng Meloidogyne sp. đã được định danh tại thí nghiệm 4.
* Phương pháp nghiên cứu điều kiện nhân nuôi được thực hiện với các yếu tố một cách tuần tự bao gồm môi trường, pH, thời gian, nhiệt độ, tốc độ lắc. Kết quả nghiên cứu của yếu tố trước được sử dụng trong nghiên cứu yếu tố tiếp theo.
Môi trường nuôi cấy
+ Chuẩn bị giống cấp 1: Cấy chủng vi khuẩn tuyển chọn từ ống giống vào bình tam giác có chứa 50ml môi trường LB lỏng (đã hấp khử trùng ở 121oC trong 15 phút). Nuôi vi khuẩn trên máy lắc với tốc độ 150 vòng/phút, thời gian 24 giờ, điều chỉnh để đạt mật độ 108 CFU/ml.
Bảng 2.4. Thành phần của môi trường nuôi cấy vi khuẩn
Glucose | Cao nấm men | Cao thịt | Pepton | KH2PO4 | (NH4)2SO4 | MnCl2. 4H2O | MgSO4. 7H2O | |
M1 (g/l) | 2 | 5 | 5 | - | 6 | 4 | - | - |
M2 (g/l) | 2 | 5 | - | 3 | 6 | 4 | 0,5 | - |
M3 (g/l) | 2 | 5 | - | - | - | - | 0,5 | 0,5 |
M4 (g/l) | 1 | 2,5 | 2,5 | 1,5 | 3 | 2 | 0,25 | 0,25 |
M5 (g/l) | 2 | - | 5 | 3 | 6 | - | 0,5 | 0,5 |
M6 (g/l) | 2 | - | 5 | 3 | - | 4 | - | 0,5 |
+ Đối với chủng RB.DS29 kháng nấm P.capsici: Chuyển 1ml giống cấp 1 với mật độ 108 CFU/ml vào các bình tam giác có chứa sẵn 50ml các môi trường khác nhau bao gồm TSB, NB, LB, PEP và pepton cải biên [132]. Chủng vi khuẩn được nuôi trên máy lắc với tốc độ 150 vòng/phút, thời gian 24 giờ. Thí nghiệm được bố trí theo kiểu đầy đủ ngẫu nhiên với 3 lần lặp lại.
+ Đối với chủng RB.CJ41 kháng nấm F. oxysporum và chủng RB.EK7 kháng tuyến trùng: Chuyển 1ml giống cấp 1 với mật độ 108 CFU/ml vào các bình tam giác