Ngày 1 và 2: từ 1 đến 2 giọt mỗi 30 phút trong khi tỉnh táo và khoảng 4 và 6 giờ khi nghỉ ngơi.
Ngày 3 đến 7: từ 1 đến 2 giọt mỗi giờ khi thức.
Ngày 7 đến 9 thông qua điều trị: từ 1 – 2 giọt 4 lần một ngày (www.drugs.com).
2.2. ĐẠI CƯƠNG VỀ GEL IN SITU
2.2.1. Khái niệm
Gel được định nghĩa là một hệ bán rắn trong đó sự chuyển động của môi trường phân tán bị giới hạn bởi mạng không gian ba chiều với nhiều liên kết vật lý hay hoá học hoặc cả hai liên kết này của các tác nhân tạo gel được solvate hoá (Clyder M. O. et al., 2007). Gel bôi da và niêm mạc là những chế phẩm thể chất mềm, sử dụng tá dược tạo gel thích hợp. Tác nhân tạo gel bao gồm các nhóm như protein, polysaccharid, polymer bán tổng hợp, polymer tổng hợp, các chất vô cơ và một số chất diện hoạt (Kiểm nghiệm thuốc, 2011; Bào chế và sinh dược học tập 2, 2010).
Bảng 2.2. Phân loại chất tạo gel
Ví dụ | |
Protein | Collagen, gelatin |
Polysaccharid | Agar, K – Carrageenan, gôm tragacan, tinh bột, acid hyaluronic, pectin, gôm guar |
Polymer bán tổng hợp | Carboxymethyl cellulose, hydroxypropyl cellulose, hydroxypropylmethyl cellulose, methylcellulose |
Polymer tổng hợp | Carbomer, poloxamer, polyacrylamid, polyvinyl alcol |
Chất vô cơ | Nhôm hydroxyd, bentonit, laponit |
Có thể bạn quan tâm!
-
 Nghiên cứu xây dựng công thức điều chế thuốc nhỏ mắt gel in situ chứa 0,3 % ofloxacin - 1
Nghiên cứu xây dựng công thức điều chế thuốc nhỏ mắt gel in situ chứa 0,3 % ofloxacin - 1 -
 Nghiên cứu xây dựng công thức điều chế thuốc nhỏ mắt gel in situ chứa 0,3 % ofloxacin - 2
Nghiên cứu xây dựng công thức điều chế thuốc nhỏ mắt gel in situ chứa 0,3 % ofloxacin - 2 -
 Chỉ Định, Chống Chỉ Định, Tác Dụng Không Mong Muốn
Chỉ Định, Chống Chỉ Định, Tác Dụng Không Mong Muốn -
 Xây Dựng Công Thức Cơ Bản Gel In Situ Chứa 0,3 % Ofloxacin
Xây Dựng Công Thức Cơ Bản Gel In Situ Chứa 0,3 % Ofloxacin -
 Nghiên cứu xây dựng công thức điều chế thuốc nhỏ mắt gel in situ chứa 0,3 % ofloxacin - 6
Nghiên cứu xây dựng công thức điều chế thuốc nhỏ mắt gel in situ chứa 0,3 % ofloxacin - 6 -
 Nghiên cứu xây dựng công thức điều chế thuốc nhỏ mắt gel in situ chứa 0,3 % ofloxacin - 7
Nghiên cứu xây dựng công thức điều chế thuốc nhỏ mắt gel in situ chứa 0,3 % ofloxacin - 7
Xem toàn bộ 63 trang tài liệu này.
Dựa theo cấu trúc, gel được phân loại thành gel một pha và gel hai pha (Clyder M. O. et al., 2007).
Gel một pha: là một thể thống nhất, không có giới hạn rò ràng giữa môi trường và đại phân tử phân tán. Ví dụ: gel carbomer, gel alginat.
Gel hai pha: là một hệ có chứa các tiểu phân tạo gel phân tán. Ví dụ như gel nhôm hydroxyl.
Dựa theo môi trường, gel được phân loại thành gel thân dầu và gel thân nước (Dược điển VN IV; Kiểm nghiệm thuốc, 2011).
Gel thân dầu (oleogel): trong thành phần sử dụng tá dược tạo gel, bao gồm dầu parafin phối hợp với tá dược thân dầu khác, có thêm keo silic, xà phòng nhôm hoặc xà phòng kẽm.
Gel thân nước (hydrogel): thành phần bao gồm nước, glycerin, propylen glycol, có thêm các tá dược tạo gel như polysacarid (tinh bột, tinh bột biến tính, acid alginic và natri alginat), dẫn chất cellulose, polymer của acid acrylic (carbomer, carbomer copolymer, carbomer interpolymer, methyl acrylat) và các chất vô cơ (magnesi – nhôm silicat).
2.2.2. Ưu nhược điểm của gel
Với mục tiêu điều trị tại chỗ, gel tiếp xúc trực tiếp với tác nhân gây bệnh và đưa dược chất đến đích tác động trên da gần như hoàn toàn. Do đó, hiệu quả trị liệu cao và hầu như không có hay ít có tác dụng phụ toàn thân. Hơn nữa, quy trình điều chế gel đơn giản, chế phẩm ổn định, cảm quan tốt. Tuy nhiên, sự hấp thu hoạt chất từ gel còn phụ thuộc vào nhiều yếu tố và thay đổi nhiều giữa các cá thể hay trong cùng một cá thể. Sự hấp thu thuốc qua da rất kém, chỉ có các dược chất có hoạt lực mạnh với liều điều trị không quá 2 mg/ngày, không gây kích ứng với da, có đặc tính phù hợp cho sự hấp thu qua da mới có thể bào chế ở dạng gel. Ngoài ra, do hiệu suất hấp thu không cao, sau khi sử dụng vẫn còn một lượng lớn dược chất trong dạng thuốc, gây phí phạm dược chất, có thể có vấn đề về sự an toàn và ô nhiễm môi trường (Sinh dược học và các hệ thống trị liệu mới, 2007).
2.2.3. Phương pháp điều chế
Tùy theo hoạt chất và tá dược mà có phương pháp điều chế gel sau đây:
Phương pháp hòa tan: khi dược chất dễ tan trong tá dược, hỗn hợp tá dược hoặc trong một dung môi trơ đồng tan với tá dược. Ta có gel kiểu dung dịch. Nếu tá dược thân dầu, ta có thể đun chảy (nếu tá dược dạng rắn) rồi phối hợp thành hỗn hợp đồng nhất bằng cách khuấy trộn. Sau đó thêm hoạt chất vào. Nếu tá dược thân nước ta thường ngâm cho trương nở rồi cho hoạt chất vào.
Phương pháp trộn đều đơn giản: áp dụng khi dược chất rắn không hòa tan trong tá dược hoặc trong trường hợp dược chất cần gây tác dụng tại chỗ hay cần hạn chế sự hấp thu hay khi các thành phần dược chất rắn có tương kỵ khi hòa tan. Đây là gel dạng hỗn dịch.
Phương pháp trộn đều nhũ hóa: áp dụng khi dược chất lỏng không đồng tan với tá dược, hoặc dược chất rắn mềm không đồng tan với tá dược nhưng lại dễ tan trong dung môi trơ phân cực, hoặc trường hợp dược chất rắn chỉ phát huy tác dụng dưới dạng dung dịch nước. Đây là dạng gel nhũ tương (Sinh dược học và các hệ thống trị liệu mới, 2007).
2.2.4. Gel in situ
Trong vài năm qua, một lượng lớn các nghiên cứu và báo cáo về các hệ thống tạo gel in situ (in situ – forming gel) đã được công bố. Sự hình thành của gel in situ có thể được định nghĩa là sự chuyển từ dạng lỏng sang dạng rắn hay bán rắn dưới ảnh hưởng của các tác nhân như nhiệt độ, pH hoặc ion. Dung dịch poly (N – isopropyl acrylamid) và poloxamer có sự chuyển pha sol – gel khi thay đổi nhiệt độ. Trong khi poly (methacrylic acid) và chitosan tạo gel dựa trên sự thay đổi pH (Clyder M. O. et al., 2007; Nirmal H. B. et al., 2010).
Hai điều kiện tiên quyết trong một hệ in situ gel đó là độ nhớt và khả năng tạo gel. Độ nhớt nên là tối ưu sao cho dễ dàng nhỏ thuốc vào mắt ở dạng lỏng và gel hóa nhanh chóng (kích hoạt nhờ việc tăng pH từ 6,0 lên 7,4). Ngoài ra, gel hình thành tại chỗ nên được bảo toàn tính nguyên vẹn của nó mà không bị hòa tan hay bị xói mòn trong một khoảng thời gian dài thích hợp.
Phân loại
Cơ chế tạo gel của dung dịch in situ gel được quyết định bởi loại polymer được sử dụng, mỗi loại polymer tạo gel dưới tác động của các yếu tố nhất định, được chia thành 3 nhóm như trong bảng 2.2 (Nirmal H. B. et al., 2010; Rajoria G. and Gupta A., 2012).
Bảng 2.3. Phân loại tác nhân tạo gel in situ
Polymer tạo gel | |
Nhiệt độ | Pluronics, tetronics, xyloglucans, hydroxypropylmethyl cellulose (HPMC) |
pH | Chitosan, cellulose acetate phtalat (CAP), Carbopol, polymethacrylic acid (PMMA), polyethylen glycol (PEG) |
Tương tác ion | Gelrite, gellan, acid hyaluronic, alginat. |
2.2.4.1. Hệ gel in situ nhạy cảm với nhiệt
Cơ chế
Sự chuyển thể sol – gel xảy ra chủ yếu do khả năng hoà tan khác nhau ở những nhiệt độ khác nhau của các polymer tạo gel. Ở nhiệt độ thấp hơn nhiệt độ bắt đầu xảy ra sự chuyển thể sol – gel, liên kết hydro giữa các nhóm ưa nước ở trên bề mặt polymer và phân tử nước làm tăng sự hoà tan của các chuỗi polymer và hệ tồn tại ở dạng dung dịch. Khi nhiệt độ cao hơn, các liên kết hydro bị phá vỡ, tương tác polymer
– polymer và nước – nước chiếm ưu thế hơn, do các đại phân tử hoà tan bị khử nước đột ngột và chuyển sang cấu trúc kỵ nước hơn, dung dịch chuyển thành dạng gel (Rajoria G. and Gupta A., 2012).
Nhiệt độ tăng
Dung dịch copolomer
Micellization
Sự hình thành gel
Hình 2.2. Cơ chế tạo gel hệ nhảy cảm với nhiệt (Rajoria G. and Gupta A., 2012)
Một số polymer thường dùng: poloxamer, xyloglucan …
2.2.4.2. Hệ tạo gel in situ do thay đổi pH
Cơ chế
Các polymer nhạy cảm với pH chuyển từ dạng dung dịch sang dạng gel do pH làm thay đổi mức độ ion hóa và độ tan trong nước của chúng. Tất cả các polymer nhạy cảm với pH đều có các nhóm ion (acid hay base) có thể cho hoặc nhận điện tử khi pH môi trường thay đổi. Khi pH môi trường tăng, sự trương nở của các polymer tăng lên nếu trong phân tử polymer có các nhóm có tính acid yếu, và giảm đi khi có các nhóm có tính base yếu (Rajoria G. and Gupta A., 2012).
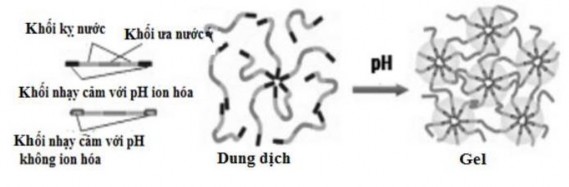
Hình 2.3. Cơ chế tạo gel của hệ nhạy cảm pH (Rajoria G. and Gupta A., 2012)
Một số polymer thường dung: chitosan, carbopol …
Carbopol 940 (acid acrylic – PAA)
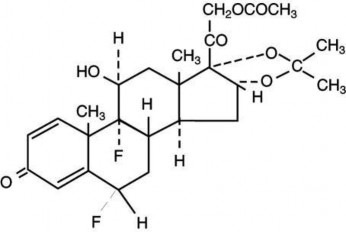
Hình 2.4. Cấu tạo của carbopol 940
Carbopol là những sản phẩm trùng hiệp cao phân tử của acid acrylic, dạng bột trắng, không tan hoặc rất ít tan trong nước nhưng trương nở trong nước tạo những thể gel có pH acid (dịch treo 1 % của các chất này có pH khoảng 3) và không sánh. Là chất tạo gel, có vai trò chuyển dung dịch thuốc ban đầu thành gel khi pH tăng lên. Nồng độ carbopol với vai trò tác nhân tạo gel thường được sử dụng từ 0,5 – 2 %. Khi carbopol trương nở hoàn toàn là lúc gel đạt đến độ nhớt cao nhất (Bào chế và sinh dược học tập 2, 2010; Kỹ thuật bào chế và sinh dược học các dạng thuốc tập 2, 2014).
Carbopol cũng có thể tạo gel với các dung môi ethanol, glycerin, propylen glycol. Carbopol tương kỵ với phenol, polymer dạng cation, acid mạnh và chất điện giải mạnh. Mỗi carbopol khác nhau về cấu trúc hóa học, mức độ liên kết, loại và lượng dung môi còn tồn dư ảnh hưởng đến mức độ và tốc độ phân tán, khả năng trương nở, thể chất và cấu trúc gel điển hình là độ nhớt. Ngoài ra, tùy theo dạng thuốc, tùy theo đường dùng mà lựa chọn loại carbopol thích hợp (Nirmal H. B. et al., 2010).
Ngoài vai trò tạo gel, carbopol còn được sử dụng như một tá dược hỗ trợ, cải thiện các tính chất của gel (Kỹ thuật bào chế và sinh dược học các dạng thuốc tập 2, 2014).
2.2.4.3. Hệ tạo gel in situ do ion hoá
Cơ chế
Hệ tạo gel do ion hóa bị kích hoạt bởi sự có mặt của các ion có trong dịch nước mắt như Na+, Ca2+, Mg2+. Các polymer được sử dụng là các polymer anion, như: natri alginat, gelrite, tamarind, gellan. Sự tạo gel xảy ra do tương tác ion giữa các ion của polymer và các ion hóa trị 2 của nước mắt. Khi các polymer anion tiếp xúc với các cation, chúng chuyển sang dạng gel có độ nhớt cao (Rajoria G. and Gupta A., 2012).
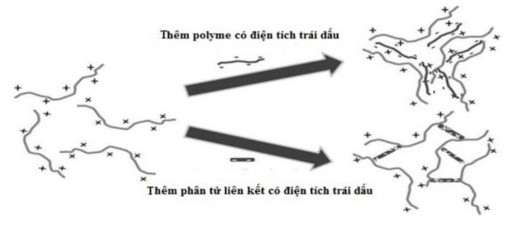
Hình 2.5. Cơ chế tạo gel do ion hoá (Rajoria G. and Gupta A., 2012)
Một số polymer thường dung: alginat, gellan, …
2.2.4.4. Các tá dược hỗ trợ
Hydroxypropyl methylcellulose (HPMC)
HPMC là một dẫn xuất của cellulose, có màu trắng hoặc trắng kem, dễ tan trong nước lạnh tạo thành một dung dịch keo nhớt, thực tế không tan trong nước nóng. Khi tăng nhiệt độ, dung dịch HPMC chuyển thành dạng gel ở nồng độ thấp (1 – 10 %). Nhiệt độ chuyển tiếp sol – gel 75 – 90 . Nhiệt độ này có thể hạ xuống bằng hóa chất hay thay đổi vật lý. Bằng cách giảm số nhóm hydroxypropyl thay thế trên phân tử HPMC, nhiệt độ chuyển tiếp có thể giảm xuống 40 . HPMC được sử dụng rộng rãi trong các công thức gel như là tác nhân làm tăng độ nhớt, cải thiện độ bám dính, điều chỉnh sự phóng thích hoạt chất … (Kulkarni A. P. et al., 2012; Raymond C. R. et al., 2009).
2.2.4.5. Các chỉ tiêu đánh giá gel in situ tạo bởi thay đổi pH
Gel in situ theo pH đặc trưng bởi tính chất tạo gel thuận nghịch theo pH. Bên cạnh pH tạo gel, gel in situ còn được đánh giá qua các chỉ tiêu khác như: độ trong, độ nhớt, khả năng chảy lỏng, lực bám dính, khả năng phóng thích hoạt chất, độ ổn định của gel … (Nirmal H. B. et al., 2010).
Dưới đây trình bày một số phương pháp của một số tác giả đánh giá các tính chất của gel in situ:
Khả năng tạo gel
Trong nghiên cứu của Nagaich U. và ctv (2015), khả năng tạo gel được xác định bằng cách nhỏ 1 giọt của DIG vào 1 ống nghiệm có chứa 2 mL nước mắt nhân tạo vừa được chuẩn bị ở nhiệt độ 37 °C. Trực quan đánh giá sự hình thành gel.
Khả năng chảy lỏng
Preetha J. P. và ctv (2010) đã xác định khả năng chảy lỏng theo phương pháp sau: hút 2 mL DIG cho vào một ống nghiệm, úp ngược ống nghiệm. Ghi nhận thời gian DIG chảy đến miệng ống.
Độ nhớt
Reddy J. và Ahmed M. năm 2013, đã xác định độ nhớt bằng cách sử dụng nhớt kế Brookfield. Cho chế phẩm được đổ vào một adaptor nhỏ của máy và vận tốc góc tăng dần từ 0,5 đến 50 rpm.
Độ ổn định
Kulkarni A. P. và ctv (2012), đã nghiên cứu độ ổn định của DIG bằng cách cho DIG được đựng trong lọ kín, bảo quản ở 5 1 . Theo dòi độ ổn định của gel trong 15, 30, 45 ngày.
Lực bám dính niêm mạc
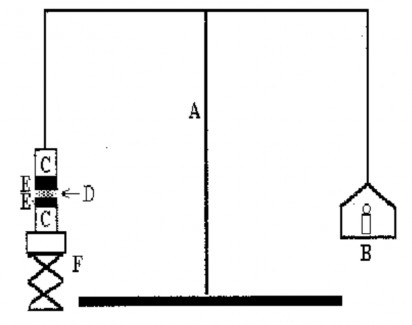
Hình 2.6. Mô hình thử kết dính sinh học gel in situ
A: trục cân bằng
B: nơi để cốc thuỷ tinh hứng nước từ buret hoặc quả cân C: vật cố định niêm mạc
D: mẫu
E: niêm mạc ruột heo được gắn vào C
Ramadan E. (2010) và ctv đã tiến hành xác định lực bám dính niêm mạc như sau: dùng niêm mạc ruột heo rửa sạch, ngâm trong nước bọt nhân tạo ở 37 . Cố định 2 miếng niêm mạc vào bề mặt C. Cho vào giữa 2C 0,2 mL gel. Nâng nhẹ B để 2C tiếp xúc vào nhau, tác động lên gel một lực dàn mỏng trong 30 giây, lần lượt cho các quả cân có khối lượng 50 g, 55 g, 60 g, 65 g … Ghi nhận khối lượng đầu tiên làm 2 miếng niêm mạc tách ra.
Lực bám dính niêm mạc được tính bằng công thức: BS = m/S. Trong đó: BS: lực bám dính niêm mạc (g/cm2)
m: khối lượng thêm vào làm mất bám dính S: diện tích tiếp xúc (S = 3,14 cm2)
Khả năng phóng thích hoạt chất
Khả năng phóng thích hoạt chất in vitro được xác định bằng phương pháp khuếch tán qua gel hay qua màng. Trong phương pháp khuếch tán qua gel, khả năng phóng