d. Nghiên cứu ảnh hưởng của biên độ xung
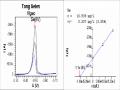
Biên độ xung được nghiên cứu trong khoảng 0,01V ÷ 0,1V. Kết quả ghi đo được trình bày trong bảng 3.22 và hình 3.20.
Bảng 3.22: Kết quả ghi đo nghiên cứu chọn biên độ xung tối ưu.
1 | 2 | 3 | 4 | 5 | |
Biên độ xung (V) | 0,01 | 0,03 | 0,05 | 0,08 | 0,10 |
Ip (nA) | 7,3 | 44,0 | 93,1 | 200,0 | 248,0 |
Có thể bạn quan tâm!
-
 Nghiên Cứu Tính Chất Điện Hóa Của Selen Trên Hmde
Nghiên Cứu Tính Chất Điện Hóa Của Selen Trên Hmde -
![Sự Phụ Thuộc Của I P Vào Tốc Độ Quét Thế [Se(Iv)] = 2Ppb, Nền Hcl 0,1M, E Dep = -0,3V, T Dep = 90S [Se-Cyst] = 25Ppb, Nền Hcl 0,1M, E Dep = -0,2V, T Dep = 90S](data:image/svg+xml,%3Csvg%20xmlns=%22http://www.w3.org/2000/svg%22%20viewBox=%220%200%2075%2075%22%3E%3C/svg%3E) Sự Phụ Thuộc Của I P Vào Tốc Độ Quét Thế [Se(Iv)] = 2Ppb, Nền Hcl 0,1M, E Dep = -0,3V, T Dep = 90S [Se-Cyst] = 25Ppb, Nền Hcl 0,1M, E Dep = -0,2V, T Dep = 90S
Sự Phụ Thuộc Của I P Vào Tốc Độ Quét Thế [Se(Iv)] = 2Ppb, Nền Hcl 0,1M, E Dep = -0,3V, T Dep = 90S [Se-Cyst] = 25Ppb, Nền Hcl 0,1M, E Dep = -0,2V, T Dep = 90S -
 Kết Quả Ghi Đo Nghiên Cứu Chọn Thời Gian Đuổi Ôxy Tối Ưu
Kết Quả Ghi Đo Nghiên Cứu Chọn Thời Gian Đuổi Ôxy Tối Ưu -
 Sự Phụ Thuộc Của I P Vào Nồng Độ Các Ion Zn(Ii), As(V)
Sự Phụ Thuộc Của I P Vào Nồng Độ Các Ion Zn(Ii), As(V) -
 Đường Dpcsv Và Đường Chuẩn Của Se(Iv) Vùng Nồng Độ (0,8 ÷ 10) Ppb
Đường Dpcsv Và Đường Chuẩn Của Se(Iv) Vùng Nồng Độ (0,8 ÷ 10) Ppb -
 Kết Quả Nghiên Cứu Ảnh Hưởng Của Nồng Độ Hcl
Kết Quả Nghiên Cứu Ảnh Hưởng Của Nồng Độ Hcl
Xem toàn bộ 165 trang tài liệu này.

0,05V
Hình 3.20: Đường DPCSV của DMDSe nghiên cứu biên độ xung
[DMDSe] = 5ppb, nền HCl 0,06M+LiClO4 0,2M+CH2Cl2/C2H5OH (1/1),
Edep = -0,08V, tdep = 60s, tốc độ quét 0,01V/s
Nhận xét:
Ip tăng khi biên độ xung tăng, tuy nhiên khi biên độ xung cao (từ 0,08 trở lên) pic có hiện tượng biến dạng, không cân đối. Từ kết quả đó, chúng tôi chọn biên độ xung tối ưu cho phép phân tích DMDSe là 0,05V.
e. Nghiên cứu thời gian đặt xung
Chúng tôi tiến hành nghiên cứu thời gian đặt xung trong khoảng 0,01s ÷ 0,06s và thu được kết quả ở bảng 3.23 và hình 3.21.
Bảng 3.23: Kết quả ghi đo nghiên cứu thời gian đặt xung
1 | 2 | 3 | 4 | 5 | |
t(s) | 0,01 | 0,02 | 0,03 | 0,04 | 0,06 |
Ip (nA) | 153,0 | 94,9 | 66,7 | 52,4 | 34,7 |
1
2 (0,02s)
Hình 3.21: Đường DPCSVcủa DMDSe nghiên cứu thời gian đặt xung
[DMDSe] = 5ppb, nền HCl 0,06M+LiClO4 0,2M+CH2Cl2/C2H5OH (1/1),
Edep = -0,08V, tdep = 60s, tốc độ quét 0,01V/s, biên độ xung 0,05V
Nhận xét:
Khi thời gian đặt xung nhỏ thì Ip cao, tuy vậy chân pic lại cao (pic 1). Nếu thời gian đặt xung tăng lên thì Ip giảm nhưng pic thu được cân đối, chân pic thấp (pic 2). Nếu tiếp tục tăng thời gian đặt xung thì Ip lại giảm. Từ kết quả đó, chúng tôi chọn thời gian đặt xung là 0,02s (pic 2).
f. Nghiên cứu tốc độ khuấy dung dịch
Để nghiên cứu tốc độ khuấy dung dịch, chúng tôi tiến hành thí nghiệm ở các tốc độ khuấy khác nhau từ 400 ÷ 2800 vòng/phút. Kết quả chỉ ra ở bảng 3.24 và hình 3.22.
Bảng 3.24: Kết quả ghi đo nghiên cứu tốc độ khuấy dung dịch
1 | 2 | 3 | 4 | 5 | 6 | |
V (vòng/phút) | 400 | 800 | 1200 | 2000 | 2400 | 2800 |
Ip (nA) | 55,8 | 79,4 | 94,9 | 116,0 | 117,0 | 125,0 |
2000v/ph
Hình 3.22: Đường DPCSV của DMDSe nghiên cứu tốc độ khuấy dung dịch
[DMDSe] = 5ppb, nền HCl 0,06M+LiClO4 0,2M+CH2Cl2/C2H5OH (1/1),
Edep = -0,08V, tdep = 60s, tốc độ quét 0,01V/s, biên độ xung 0,05V, thời gian đặt xung 0,02s
Nhận xét:
Khi tăng tốc độ khuấy trộn dung dịch thì Ip càng cao nhưng chân pic cũng nâng lên. Để đảm bảo tính ổn định và chính xác của phép ghi đo, pic thu được cân đối, chúng tôi chọn tốc độ khuấy là 2000 vòng/phút.
g. Nghiên cứu kích thước giọt thủy ngân
Chúng tôi thay đổi cỡ giọt thủy ngân từ 1 ÷ 7 để nghiên cứu ảnh hưởng của cỡ giọt thủy ngân đến cường độ pic Ip. Kết quả nghiên cứu thể hiện ở bảng 3.25 và hình 3.23.
Bảng 3.25: Kết quả ghi đo nghiên cứu chọn kích thước giọt thủy ngân tối ưu
1 | 2 | 3 | 4 | 5 | 6 | 7 | |
Cỡ giọt | 1 | 2 | 3 | 4 | 5 | 6 | 7 |
Ip (nA) | 49,7 | 80,1 | 103,0 | 125,0 | 146,0 | 162,0 | 185,0 |
4
Hình 3.23: Đường DPCSV của DMDSe nghiên cứu kích thước giọt thủy ngân
[DMDSe] = 5ppb, nền HCl 0,06M+LiClO4 0,2M+CH2Cl2/C2H5OH (1/1),
Edep = -0,08V, tdep = 60s, tốc độ quét 0,01V/s, biên độ xung 0,05V, thời gian đặt xung 0,02s, tốc độ khuấy 2000v/ph
Kết quả nghiên cứu cho thấy: khi tăng kích thước giọt thủy ngân thì Ip tăng. Tuy nhiên, khi kích thước giọt lớn, chân pic bị nâng lên và cỡ giọt lớn cũng làm giọt dễ bị rơi trong quá trình ghi đo. Vì vậy, để phù hợp, chúng tôi lựa chọn kích thước giọt là 4 trong các phép ghi đo sau này.
h. Nghiên cứu thời gian cân bằng (thời gian nghỉ)
Thời gian cân bằng được nghiên cứu từ 2 ÷ 25s. Kết quả được trình bày trong bảng 3.26 và hình 3.24.
Bảng 3.26: Kết quả ghi đo nghiên cứu chọn thời gian cân bằng tối ưu
1 | 2 | 3 | 4 | 5 | 6 | |
t (s) | 2 | 5 | 10 | 15 | 20 | 25 |
Ip (nA) | 108 | 120 | 125 | 128 | 118 | 113 |
15s
Hình 3.24: Đường DPCSV của DMDSe nghiên cứu thời gian cân bằng
[DMDSe] = 5ppb, nền HCl 0,06M+LiClO4 0,2M+CH2Cl2/C2H5OH (1/1),
Edep = -0,08V, tdep = 60s, tốc độ quét 0,01V/s, biên độ xung 0,05V, thời gian đặt xung 0,02s, tốc độ khuấy 2000v/ph, cỡ giọt 4
Từ kết quả nghiên cứu cho thấy, khi thời gian cân bằng tăng thì Ip tăng dần và ổn định từ 5s trở đi, đến 15s thì đạt cực đại, sau đó lại giảm dần. Chính vì vậy, chúng tôi chọn thời gian cân bằng là 15s cho các thí nghiệm tiếp theo.
i. Nghiên cứu thời gian đuổi khí ôxy (thời gian sục khí N2)
Để nghiên cứu ảnh hưởng của thời gian sục khí tới phép ghi đo DMDSe, chúng tôi thay đổi thời gian sục khí từ 0 ÷ 300s. Kết quả thu được ở bảng 3.27 và hình 3.25.
Bảng 3.27: Kết quả ghi đo nghiên cứu thời gian đuổi khí ôxy
1 | 2 | 3 | 4 | 5 | 6 | 7 | |
t (s) | 0 | 50 | 100 | 150 | 200 | 250 | 300 |
Ip (nA) | Nhiễu | 116 | 118 | 125 | 128 | 125 | 125 |
200s
Hình 3.25: Đường DPCSV của DMDSe nghiên cứu thời gian đuổi ôxy
[DMDSe] = 5ppb, nền HCl 0,06M+LiClO4 0,2M+CH2Cl2/C2H5OH (1/1),
Edep = -0,08V, tdep = 60s, tốc độ quét 0,01V/s, biên độ xung 0,05V, thời gian đặt xung 0,02s, tốc độ khuấy 2000v/ph, cỡ giọt 4, tnghỉ =15s
Kết quả nghiên cứu thu được cho thấy, khi không đuổi ôxy thì pic bị nhiễu, khi thời gian đuổi ôxy ít, Ip thấp. Nếu tăng thời gian đuổi ôxy thì Ip tăng và ổn định từ 100s trở đi. Ip đạt giá trị cao nhất tại 200s và pic cân đối. Do đó, chúng tôi chọn thời gian đuổi ôxy là 200s cho các thí nghiệm tiếp theo.
Tóm lại: Sau quá trình nghiên cứu, chúng tôi rút ra điều kiện tối ưu cho phép phân tích DMDSe được trình bày trong bảng 3.28.
Bảng 3.28: Điều kiện tối ưu phân tích DMDSe
HMDE | Thế điện phân làm giàu | -0,08V | ||
Chế độ ghi đo | DP | Thời gian điện phân làm giàu | 60s÷120s | |
Kích thước giọt thủy ngân | 4 | Thời gian cân bằng | 15s | |
Tốc độ khuấy (vòng/phút) | 2000 | Biên độ xung | 0,05V | |
Thời gian sục khí N2 | 200s | Thời gian đặt xung | 0,02s | |
Nền | HCl | 0,06M | Tốc độ quét thế | 0,01V/s |
LiClO4 | 0,2M | Khoảng thế quét | (-0,17÷-0,40)V | |
CH2Cl2+C2H5OH | 1/1 (v/v) | |||
3.3. NGHIÊN CỨU ẢNH HƯỞNG CỦA CÁC CHẤT CẢN TRỞ ĐẾN PHÉP GHI ĐO CÁC DẠNG SELEN
Trong mẫu thực tế luôn tồn tại một số ion, đặc biệt là cation kim loại, các cation này ở một nồng độ nào đó có thể ảnh hưởng tới phép ghi đo. Chúng có thể làm tăng hoặc giảm chiều cao của pic. Mặt khác, chúng có thể thể hiện tính chất điện hóa trong điều kiện ta tiến hành phép phân tích. Cụ thể là: tham gia vào quá trình điện phân làm giàu tạo hỗn hống với thủy ngân hay kết tủa đồng thời với các kim loại khác tạo dung dịch rắn hoặc hợp chất gian kim loại. Điều này ảnh hưởng đến khả năng phát hiện các chất cần phân tích. Đồng thời, trong đối tượng mẫu mà chúng tôi nghiên cứu là hải sản, ngoài sự tồn tại của các ion cần phải kể đến chất béo và protein là những chất có hàm lượng lớn trong các mẫu động vật. Khi ngâm chiết mẫu, những chất này cũng bị chiết ra một phần và có thể ảnh hưởng đến nền ghi đo mẫu, làm giảm độ dẫn điện của nền điện li, dẫn đến pic của chất cần xác định bị nhiễu hoặc bị giảm chiều cao. Vì vậy, cần nghiên cứu sự ảnh hưởng của các ion và các chất này để có biện pháp loại trừ thích hợp, đảm bảo độ đúng, độ chính xác của phép ghi đo.
Chúng tôi tiến hành nghiên cứu ảnh hưởng của một số ion có thế đỉnh Ep gần với Ep của các dạng selen hoặc có khả năng tạo hợp chất gian kim với selen hoặc có mặt nhiều trong các mẫu môi trường và sinh học, đồng thời nghiên cứu ảnh hưởng của chất béo (đại diện cho loại hợp chất ít và không tan cũng như kém điện li trong pha nước nhưng đễ tan trong dung môi hữu cơ) đến phép ghi đo các dạng selen.
3.3.1. Nghiên cứu ảnh hưởng của các chất cản trở đến phép ghi đo Se(IV)
3.3.1.1. Ảnh hưởng của một số ion đến phép ghi đo Se(IV)
Hút 20µl dung dịch Se(IV) 1000ppb cho vào bình định mức 10ml, thêm 1ml HCl 1M, thêm các ion Cu(II), Pb(II), Zn(II), Cd(II), As(V) và Fe(III) vào với các nồng độ khác nhau và định mức bằng nước cất siêu sạch tới vạch. Tiến hành ghi đo các đường DPCSV theo các điều kiện tối ưu đưa ra trong bảng 3.14 với thời gian điện phân 90s. Kết quả nghiên cứu được trình bày trong bảng 3.29 và các hình 3.26, 3.27.
Bảng 3.29: Kết quả nghiên cứu ảnh hưởng của Cu(II), Pb(II) Cd(II), Fe(III), Zn(II), As(V) đến Ip của Se(IV)
1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 | ||
Nồng độ ion thêm (ppb) | 0 | 2 | 5 | 7,5 | 10 | 15 | 30 | 50 | 75 | 100 | |
Ip (nA) | Cu(II) | 25,4 | 25,4 | 26,3 | 30,0 | 32,2 | 33,3 | 33,4 | 37,9 | 39,5 | 39,7 |
Pb(II) | 25,9 | 25,7 | 24,5 | 23,6 | 22,8 | 20,9 | 21,0 | 20,0 | 15,8 | 13,2 | |
Cd(II) | 25,0 | 24,9 | 25,9 | 22,9 | 20,1 | 18,4 | 15,4 | 10,4 | 8,1 | 6,4 | |
Fe(III) | 25,4 | 23,5 | 22,0 | 20,9 | 20,7 | 20,6 | 19,9 | 19,7 | 19,8 | 18,8 | |
Nồng độ ion thêm (ppb) | 0 | 5 | 10 | 15 | 30 | 50 | 100 | 150 | 200 | ||
Ip (nA) | Zn(II) | 25,3 | 26,6 | 25,7 | 25,9 | 25,9 | 25,8 | 25,2 | 24,7 | 24,5 | |
As(V) | 25,7 | 26,5 | 24,6 | 23,2 | 22,0 | 21,3 | 20,1 | 20,3 | 20,2 | ||
45
40
35
30
25
20
15
10
5
0
0
20
40
60
ppb
80
100 120
Ah của Cu(II) Ah của Pb(II)
Ah của Cd(II)
Ah của Fe(III)
I (nA)
Hình 3.26: Sự phụ thuộc của Ip vào nồng độ các ion Cu(II), Pb(II), Cd(II) và Fe(III)


![Sự Phụ Thuộc Của I P Vào Tốc Độ Quét Thế [Se(Iv)] = 2Ppb, Nền Hcl 0,1M, E Dep = -0,3V, T Dep = 90S [Se-Cyst] = 25Ppb, Nền Hcl 0,1M, E Dep = -0,2V, T Dep = 90S](https://tailieuthamkhao.com/uploads/2022/09/13/nghien-cuu-xac-dinh-mot-so-dang-selen-trong-hai-san-bang-phuong-phap-von-ampe-6-1-120x90.gif)