1.3.8. Bệnh tích của gia cầm mắc c gi cầm
1.3.8.1. Bệnh tích đại th
Bệnh tích đại thể các loài khác nhau có biểu hiện khác nhau. Đối với gà, bệnh tích thường gặp là mào, tích sưng to, tím tái phù quanh mí mắt. Thể nhẹ, bệnh tích các xoang trong cơ thể đặc trưng b i viêm ca ta, lắng đọng fibrin. Xuất huyết dưới da ống chân hoặc kẽ ngón chân thành vệt đỏ rất rõ. Xuất huyết điểm trên bề mặt niêm mạc và tương mạc nội tạng. Xuất huyết hầu hết toàn bộ đường tiêu hóa, đặc biệt thấy rõ manh tràng và dạ dày tuyến. Túi fabricius xung huyết và xuất huyết. Nói chung, các bệnh tích rất giống với bệnh tích của bệnh Newcastle (Lê Văn Năm, 2004; Alexander, 200 ). Các biến đổi bệnh lý đại thể của bệnh cúm gia cầm trên ngan và và vịt cơ bản cũng giống trên gà. Tuy nhiên tần suất biến đổi tập trung chủ yếu phổi, túi khí, tim, buồng trứng, xương lồng ngực và đường ruột (Lê Văn Năm, 2004).
1.3.8.2. Bệnh tích i th
Bệnh tích vi thể chủ yếu là xung huyết, xuất huyết, thâm nhiễm bạch cầu đơn nhân não và một số cơ quan khác. ạch quản của các cơ quan như mào, tích, gan, lách, phổi, thận, cơ tim, cơ vân, não và một số cơ quan khác bị giãn rộng và thâm nhiễm tế bào xung quanh mạch quản (Beard, 1998).
1.4. Chẩn đo n bệnh
1.4.1. Chẩn đo n dự ào dịch tễ học
Căn cứ vào các yếu tố dịch tễ như bệnh lây lan nhanh, gia cầm mọi lựa tuôi, nhiều loại gia cầm mắc bệnh, tỷ lệ chết cao lên tới 100% số gia cầm mắc bệnh, những vùng có ổ dịch cũ, những nơi gia cầm chưa được tiêm phòng vacxin cúm hoặc tiêm phòng chưa đủ thời gian đáp ứng miễn dịch, hoặc đã tiêm phòng nhưng qua khảo sát hiệu giá kháng thể bảo hộ chỉ đạt mức thấp.
1.4.2. Chẩn đo n dự ào t iệ chứng à bệnh tích
Căn cứ vào các triệu chứng lâm sàng và bệnh tích để chẩn đoán. Lưu ý các đặc điểm chính như gia cầm bệnh chảy nhiều nước mắt, viêm xoang mũi, mào, tích tím tái, phù đầu và mí mắt, lông cổ dựng ngược, ỉa chảy và có triệu chứng thần kinh, da chân vùng không lông xuất huyết.
Căn cứ những bệnh tích điển hỉnh như phổi, gan, thận lách sưng to. Xuất huyết mỡ vành tim, ruột viêm cata, xuất huyết. Xuất huyết dạ dày cơ, dạ dày tuyến giống bệnh Newcastle. Túi fabricius xuất huyết điểm, lỗ huyệt xuất huyết...Alexander, 200 ; Baigent và c Cauley, 2001). Trong trường hợp gia cầm chết cấp tính thì biểu hiện bệnh tích thường không điển hình.
1.4.3. Chẩn đo n phòng thí nghiệ
Chẩn đoán virus học: nuôi cấy, phân lập virus trên trứng gà có phôi ấp 9- 10 ngày hoặc trên môi trường tế bào xơ phôi gà hoặc tế bào thận chó DCK. Giám định virus trong dịch nuôi cấy b ng các phản ứng HA, HI.
Chẩn đoán và giám định virus b ng kỹ thuật Real time RT-PC : cho phép xác định virus với lượng rất nhỏ. Khẳng định chắc chắn subtyp H và N1 căn cứ vào primer và probe được thiết kế đặc hiệu. Hiện nay kỹ thuật này đã được ứng d ng rộng rãi và thường quy Việt Nam, cũng như nhiều nước trên thế giới.
Chẩn đoán huyết thanh học: dùng phản ứng HI để phát hiện và xác định hiệu giá kháng thể trong huyết thanh gia cầm chưa tiêm phòng. Ngoài ra có thể dùng phản ứng ELISA để phát hiện kháng thể.
1.5. V cxin phòng bệnh c gi cầm
Các chủng virus cường độc A/H5N1 sau 1996, qua thời gian tiến hóa, có xu hướng biến đổi nội gen nh m tăng tính gây bệnh, và thay đổi thành phần nội gen kháng nguyên làm mất tương quan miễn dịch giữa chúng và các chủng vacxin được tạo ra. Do vậy, vấn đề này phải được hết sức chú ý trong chiến lược kiến tạo vacxin, cũng như sử d ng vacxin được tạo ra (Horimoto và Kawaoka, 1994) Trong tự nhiên, “lệch kháng nguyên” và “glycosyl hóa” là các hiện tượng xảy ra liên t c theo thời gian, còn “trộn kháng nguyên” tái tổ hợp subtype Hemagglutinin (HA) và Neuraminidase (NA) thường định kỳ xảy ra giữa các loài mắc nh m tạo nên các biến thể virus cúm mới mà hệ miễn dịch của cơ thể vật chủ không có khả năng nhận dạng đáp ứng và kịp hình thành miễn dịch. H5N1 sử d ng th thể sialic xâm nhập tế bào (Xu và cs, 1999).
Đối với bệnh truyền nhiễm, vacxin được coi là biện pháp có tính chiến lược, nh m ngăn chặn lây lan, tạo bảo hộ miễn dịch (Subbarao và Luke, 200 ). Kháng thể đặc hiệu có thể được cơ thể sinh ra do kích thích của kháng nguyên
trong vacxin, và đó là các kháng thể kháng HA, NA, A và nhiều loại hình khác của virus đương nhiễm, góp phần vô hiệu hóa virus cúm đúng đối tượng khi chúng xâm nhập vào. Có nhiều loại kháng thể, nhưng trước hết chỉ kháng thể kháng HA(H ) có vai trò tiên quyết quan trọng trong quá trình trung hòa virus cho bảo hộ miễn dịch. Các vacxin phòng bệnh hiện nay dựa trên cơ s hai loại chính: vacxin truyền thống và vacxin thế hệ mới (Subbarao và Joseph, 200 ; Capua và Alexander, 2008).
Vacxin truyền thống: bao gồm vacxin vô hoạt đồng chủng và dị chủng. Vacxin vô hoạt đồng chủng (homologous vacxin), đó là các loại vacxin được sản xuất chứa cùng những chủng virus cúm gà giống như chủng gây bệnh trên thực địa (Swayne, 1999). Vacxin vô hoạt dị chủng (heterologous vacxin) là vacxin sử d ng các chủng virus có kháng nguyên HA giống chủng virus trên thực địa, nhưng có kháng nguyên NA dị chủng.
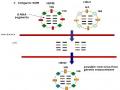
Vacxin thế hệ mới hay vacxin công nghệ gen: là loại vacxin được sản xuất dựa trên sử d ng kỹ thuật gen loại bỏ các vùng “gen độc” đang được nghiên cứu và đưa vào sử d ng phổ biến, bao gồm:
- Vacxin tái tổ hợp có vector dẫn truyền: sử d ng virus đậu gia cầm làm vector tái tổ hợp song song gen H và N1 phòng chống virus type A/H5N1 (Pfeiffer và cs, 2010). Ví d , hãng erial của Pháp sản xuất vacxin TrovacAIV- H5 lấy nguồn gen H5 từ chủng A/Turkey/Ireland/83 (H5N2), sử d ng được cho gia cầm lúc 1 ngày tuổi.
- Vacxin dưới nhóm chứa protein kháng nguyên NA, HA tái tổ hợp và tách chiết làm vacxin (Perkin và Swayne, 2002; Pfeiffer và cs, 2009).
- Vacxin tái tổ hợp có vector dẫn truyền: sử d ng adenovirus hoặc virus Newcastle hoặc virus đậu chim làm vector dẫn truyền, lắp ghép gen kháng nguyên H vào hệ gen của adenovirus, tạo nên virus tái tổ hợp làm vacxin phòng chống virus cúm A/H5N1 (Hoelscher và cs, 2006; Gao và cs, 2006; Qiao và cs, 2006).
- Vacxin DNA: sản phẩm DNA plasmid tái tổ hợp chứa gen HA, NA, NP,
2 đơn lẻ hoặc đa gen (Kilpatrick và cs, 2006, Kaewcharoen và cs, 200 ).
- Vacxin nhược độc virus cúm nhân tạo: được sản xuất b ng kỹ thuật di truyền ngược (reverse genetics), đó là việc lắp ghép virus cúm nhân tạo chứa đầy đủ hệ gen, trong đó các gen kháng nguyên H có vùng "độc" đã được biến đổi b ng kỹ thuật gen (Liu và cs., 2003; Swayne và Suarez, 2000). Trung Quốc cũng là nước sản xuất nhiều giống virus vacxin chống cúm, ví d , vacxin vô hoạt nhũ dầu đơn chủng lấy nguồn gen H và N2 từ chủng A/Turkey/England/N- 28/73(H5N2), loại subtype H N2 có độc lực yếu; hay giống vacxin vô hoạt nhũ dầu đơn chủng lấy nguồn gen H và N1 từ chủng A/Goose/Guangdong/1996(H5N1), loại có độc lực yếu (Swayne và Suarez, 2000; Pfeiffer và cs, 2010). Các loại vacxin này đã được nhập và sử d ng tại Việt Nam từ năm 2006 (Tô Long Thành, 2006).
1.5.1. Tình hình ử dụng vacxin c gi cầ t ên thế giới
Số lượng vacxin đã được sử d ng trên thực địa chưa được thông báo c thể, nhưng có một số nguồn thông tin cho r ng exico đã sử d ng 1 tỷ 300 triệu liều virus vô hoạt và 8 0 triệu liều vacxin tái tổ hợp đậu gà trong chương trình sử d ng vacxin chống bệnh cúm từ đầu tháng 1 199 và đã thanh toán được bệnh cúm gia cầm thể độc lực cao do virus H N2 và tháng 6 199 , mặc dù virus H N2 chủng độc lực thấp vẫn lưu hành. Indonexia cũng sử d ng vacxin AI H vô hoạt. Từ năm 199 , Pakistan cũng sử d ng vacxin phòng cúm cả ổ dịch H7N3 thể độc lực cao. Các vacxin vô hoạt chế từ chủng virus H9N2 độc lực thấp đã và đang được sử d ng một số nước châu Á, vùng Cận Đông và Đông Âu. Gần đây, vacxin vô hoạt nhũ dầu H đã được dùng cho các vùng nguy cơ cao phía Bắc Italia và tại một công ty nuôi gà con một ngày tuổi Mỹ.
Trung Quốc là nước sử d ng nhiều vacxin cúm nhất. Trung Quốc đã có bản tường trình về kết quả của các loại vacxin đang được sử d ng tại nước này, bao gồm:
- Vacxin vô hoạt chủng H5, N-28: được phê chuẩn từ tháng 12 2003 và được sử d ng rộng rãi Trung Quốc trong các ổ dịch cúm gia cầm thể độc lực cao vào đầu năm 2004.
Bảng1.3. M t s loại vacxin phòng c gi cầ H5N1 đ ng được sử dụng t ên thế giới (FAO/EMPRESS/2009)
Chủng virus sử dụng | Subtype | Loại vacxin | Nước sản xuất) | |
1 | A/Chicken/Mexico/232/94/CPA | A H N2, độc lực thấp | Vô hoạt nhũ dầu | Mexico |
2 | A/TY/California/20902/2002 | A H N2, độc lực thấp | Vô hoạt nhũ dầu | Mỹ |
3 | A/Turkey/England/N-28/73 | A H N2, độc lực thấp | Vô hoạt nhũ dầu | Trung Quốc, Indonesia |
4 | A/Turkey/ Minnesota/3689-1551/81 | A/H5N2 | Vô hoạt nhũ dầu | Đức |
5 | A/duck/Potsdam/1402/86 | A H N2, độc lực thấp | Vô hoạt nhũ dầu | Hà Lan |
6 | A/Turkey/Wisconsin/68 | A H N9, độc lực thấp | Vô hoạt nhũ dầu | Mỹ; Italia |
7 | A/chicken/Italy/22A/98 | A H N9, độc lực thấp | Vô hoạt nhũ dầu | Mỹ; Italia |
8 | A/duck/Potsdam/2243/84 | A H N6, độc lực thấp | Vô hoạt nhũ dầu | Hà Lan |
9 | A/Goose/Guangdong/1996 | A H N1, độc lực cao | Vô hoạt nhũ dầu | Trung Quốc |
10 | A/Ck/Legok/2003 | A H N1, độc lực cao | Vô hoạt nhũ dầu | Indonesia |
11 | A/Ck/Mansehra/2006 | A H N1, độc lực cao | Vô hoạt nhũ dầu | Pakistan |
12 | rg-A/ck/VN/C58/04 mang gen N3 từ chủng A/Duck/Germany/1215/73 (H2N3) và 6 nội gen của chủng PR8 | A/H5N3 RG | Di truyền ngược, nhũ dầu | Mỹ |
13 | A/Goose/Guangdong/1996 (Re-1), và 6 nội gen của chủng PR8 | A/H5N1 RG | Di truyền ngược, nhũ dầu | Trung Quốc |
14 | BHG/QH/05 (Re-3) và 6 nội gen của chủng PR8 | A/H5N1 RG | Di truyền ngược, nhũ dầu | Trung Quốc |
15 | DK/AH/06 (Re- ) và 6 nội gen của chủng PR8 | A/H5N1 RG | Di truyền ngược, nhũ dầu | Trung Quốc |
16 | CK/SX/06 (Re-4) và 6 nội gen của chủng PR8 | A/H5N1 RG | Di truyền ngược, nhũ dầu | Trung Quốc |
17 | Vacxin virus đậu với cDNA của gen H và N1 lấy từ chủng A/Goose/Guangdong/1996 | A H phái sinh từ H N1 độc lực cao | Tái tổ hợp sống, đông khô | Trung Quốc |
18 | Vacxin Newcastle sống (LaSota) và gen H của chủng A/Barheadedgoose/Qinghai/3/2005 | A H N1, độc lực cao | Newcastle tái tổ hơp sống mang gen H , đông khô | Trung Quốc |
19 | Virus đậu với cDNA của gen H5 lấy từ chủng from A/Turkey/ Ireland/83 | A H phái sinh từ H N8 độc lực thấp | Tái tổ hợp, đông khô, tiêm dưới da | Mỹ |
Có thể bạn quan tâm!
-
 M Ph Ng Cấ T C Kh Ng Ng Yên H E L Tinin À Neuraminidase (Www.aht.org.uk)
M Ph Ng Cấ T C Kh Ng Ng Yên H E L Tinin À Neuraminidase (Www.aht.org.uk) -
 Đặc Đi Tiến Hó À Hình Thành Genotype Củ I C Gi Cầ Gi I Đoạn 1996-2008
Đặc Đi Tiến Hó À Hình Thành Genotype Củ I C Gi Cầ Gi I Đoạn 1996-2008 -
 C C Genotype Củ I C Gi Cầ A/h5N1 Đ C Lực Cao (Li À C , 2007)
C C Genotype Củ I C Gi Cầ A/h5N1 Đ C Lực Cao (Li À C , 2007) -
 Bảng Tổng Hợp Liệ Tính To N Theo Phương Ph P Reed-Muench
Bảng Tổng Hợp Liệ Tính To N Theo Phương Ph P Reed-Muench -
 Ch Ẩn Bị Ix (Hỗn Hợp Phản Ứng Rt- Cr Giải T Ình Tự Gen
Ch Ẩn Bị Ix (Hỗn Hợp Phản Ứng Rt- Cr Giải T Ình Tự Gen -
 Cây Phả Hệ Dự Chuỗi Nucleotide Gen H5 Củ Những I C A/h5N1 Cl De 7 (Được Lập Bằng Phương Ph P Phân Tích Neighbor-
Cây Phả Hệ Dự Chuỗi Nucleotide Gen H5 Củ Những I C A/h5N1 Cl De 7 (Được Lập Bằng Phương Ph P Phân Tích Neighbor-
Xem toàn bộ 162 trang tài liệu này.

- Vacxin vô hoạt virus cúm sản xuất theo công nghệ di truyền ngược (subtype H5N1, chủng Re-1 thuộc clade 0): được phê chuẩn tháng 1 200 . Vacxin được đánh giá là rất có hiệu quả trong tạo miễn dịch chống cúm với hiệu giá kháng thể cao và thời gian bảo hộ dài hơn. Bên cạnh việc sử d ng vacxin Re-
1, Trung Quốc còn sử d ng một số loại vacxin khác được sản xuất theo cùng công nghệ là vacxin Re-3, vacxin Re-4 và vacxin Re-5. Bốn loại vacxin sản xuất theo công nghệ di truyền ngược được sản xuất từ 4 chủng virus cúm gia cầm khác nhau: Vacxin Re-1 sử d ng gen H và N1 của virus A/Goose/GD/1/96 (clade 0); Vacxin Re-3 sử d ng gen H và N1 của virus A/bar-headed goose/Qinghai/3/2005 (clade 2.2); Vacxin Re-4 sử d ng gen H và N1 của virus A chicken Shanxi 2 2006 (clade ); và Vacxin Re-5 sử d ng gen H và N1 của virus A/duck/Anhui/1/2006 (clade 2.3.4).
Theo Báo cáo về kinh nghiệm sử d ng vacxin cúm gia cầm của Trung Quốc (Chen, 2009) từ năm 2004 đến năm 2008, Trung Quốc đã sử d ng 22,64 tỷ liều vacxin Re-1, 1,26 tỷ liều vacxin Re-4 và 4,4 tỷ liều vacxin Re-5.
- Vacxin sống virus đậu tái tổ hợp phòng cúm gia cầm H : được phê chuẩn tháng 1 200 và được nhiều nước sử d ng như Trung Quốc, Mexico... sử d ng loại vacxin này có thể phân biệt được miễn dịch do tiêm phòng vacxin hay bị nhiễm tự nhiên.
1.5.2. Tình hình ử sụng vacxin c gi cầm tại Việt Nam
Từ tháng 200 , “Dự án sử d ng vacxin nh m khống chế và thanh toán bệnh cúm gia cầm” đã triển khai tại Việt Nam. Nước ta đã tiến hành tiêm phòng thử nghiệm các loại vacxin cúm gia cầm ngoại nhập trên địa bàn tỉnh Nam Định và Tiền Giang. Sau đó đã triển khai tiêm phòng trên địa bàn cả nước và thực hiện liên t c qua các năm. ỗi năm có 2 đợt tiêm phòng vào tháng 4- và tháng 9-10, trước thời điểm dịch cúm gia cầm có nguy cơ bùng phát cao nhất. Một số loại vacxin được sử d ng Việt Nam như:
- Vacxin nhũ dầu vô hoạt H5N2 (Trung Quốc): là loại vacxin dị chủng bất hoạt, sử d ng chủng virus A/Turkey/England/N28/73 (H5N2).
- Vacxin di truyền ngược vô hoạt dạng nhũ dầu H5N1 (Trung Quốc): là loại vacxin đồng chủng bất hoạt (Re-1) sử d ng chủng virus A Goose Guangdong 1 96 và ( e-5) sử d ng chủng A/Duck/Anhui/2006. Trong đó vacxin Re-1 đã được sử d ng từ năm 200 , còn vacxin Re-5 mới được đưa
vào sử d ng từ năm 2011 thay cho vacxin Re-1 vì công ty Trung Quốc sản xuất và cung cấp loại vacxin Re-1 ngừng sản xuất loại vacxin Re-1.
Bảng 1.4. Kết quả tiê phòng vacxin c gi cầ chương t ình q c gia
(tổng hợp từ báo cáo của Cục Th y qua các nă 2005-2010)
S liề vacxin tiê cho gà (t iệ | S liề vacxin tiê cho ịt (t iệ | Tổng liề VX cho gà à ịt (t iệ | |
2005 | 166,40 | 78,10 | 244,5 |
2006 – Đợt 1 | 100,60 | 35,40 | 136 |
2006 – Đợt 2 | 91,30 | 47,33 | 138,6 |
2007 – Đợt 1 | 101,20 | 89,30 | 190,5 |
2007 – Đợt 2 | 90,46 | 65,97 | 156,43 |
2008 – Đợt 1 | 84,32 | 66,42 | 150,74 |
2008 – Đợt 2 | 61,73 | 55,53 | 117,26 |
2009 – Đợt 1 | 84,86 | 67,62 | 152,48 |
2009 – Đợt 2 | 79,07 | 91,49 | 170,56 |
2010 – Đợt 1 | 89,85 | 50,77 | 140,62 |
2010 – Đợt 2 | 29,72 | 42,54 | 72,26 |
- Vacxin Nobilis Influenza H (Hà Lan): đây là loại vacxin dị chủng, sử d ng chủng virus A/chicken/Mexico/232/94/CPA (H5N2).
- Vacxin Trovac AIV H5 (vacxin đậu-cúm dạng sống, đông khô): là vacxin chứa virus đậu gà sống làm vectơ có mang gen virus cúm gia cầm chủng A, sử d ng chủng A/Turkey/Ireland 13 8 83. Tuy nhiên vacxin này hiện nay không được sử d ng nữa do không hiệu quả điều kiện Việt Nam, và nhiều đàn gà sử d ng vacxin này không có hiệu quả bảo hộ chống lại virus A/H5N1 Việt Nam (Báo cáo của Trung tâm Chẩn đoán Thú y Trung ương)
CHƯƠNG 2
N I DUNG – NGUYÊN LIỆU – HƯƠNG HÁ NGHIÊN CỨU
2.1. N i dung
2.1.1. hân lập à gi định i c gi cầm A/H5N1 từ c c dịch ngo y ổ nhớp
- Xác định virus cúm gia cầm A H N1 b ng phương pháp ealtime T- PCR (RRT-PCR)
- Phân lập virus trên phôi trứng gà 9-10 ngày tuổi đối với các mẫu xét nghiệm dương tính cúm A/H5N1.
- Giám định virus phân lập được b ng phản ứng HA, HI và RRT-PCR.
2.1.2. X c định đặc tính di t yền học của virus c A/H5N1 clade 7
Mối quan hệ về di truyền của virus A/H5N1 clade 7 với các virus A/H5N1 khác thông qua phân tích cây phả hệ của gen HA, NA và .
2.1.3. X c định m t s đặc tính inh học của i c A/H5N1 clade 7
- Tính thích ứng trên phôi gà
- Tính thích ứng trên tế bào xơ phôi gà
- Xác định độc lực của virus cúm A/H5N1 clade trên một số động vật thí nghiệm (gà, vịt và ngan).
- Một số biến đổi bệnh lý cơ bản của gà mắc virus cúm A/H5N1 clade 7.
2.1.4. X c định đặc tính kh ng ng yên (tính tương đồng kh ng ng yên
- Mối quan hệ về kháng nguyên học của virus A/H5N1 clade 7 với các virus A/H5N1 khác thông qua phản ứng huyết thanh học chéo của virus cúm gia cầm A H N1 clade và kháng nguyên, huyết thanh chuẩn của một số chủng virus cúm A/H5N1 thuộc một số clade khác.
2.1.5. X c định hiệu lực của vacxin H5N1 Re-1
- Hiệu lực của vacxin cúm gia cầm Re-1 Việt Nam đối với virus cúm gia cầm A/H5N1 clade 7 trên gà.
2.2. Đị đi à phạm vi nghiên cứ
- Nơi thu thập mẫu vùng biên giới Lạng Sơn