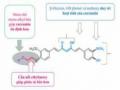
Như vậy, kết hợp thực nghiệm đã chứng minh sự có mặt đầy đủ 2 nhóm -OH phenol trên cấu trúc curcumin là yếu tố chính gây nên tác dụng chống oxy hóa các dẫn chất. Nguyên nhân có thể là do, DPPH là một gốc oxy hóa tự do có mặt trong tế bào, khi có mặt chất chống oxy hóa, nó sẽ bị khử thành DPPH-H, và nhóm chức đóng vai trò chủ đạo về hoạt tính chống oxy hóa trong cấu trúc curcumin chính là nhóm β-diceton, liên kết đôi C=C của cầu nối heptadien và đặc biệt là nhóm -OH phenol, trong đó, proton của -OH phenol dễ cho đi nhất tạo gốc tự do phenoxy bền hơn gốc oxy hóa tự do ban đầu nhờ có cân bằng cộng hưởng qua cấu trúc ceton - enol [84]. Chính vì vậy, khi 1 hoặc 2 nhóm -OH này bị thế thì hoạt tính chống oxy hóa đều giảm và dẫn chất thế 1 nhóm -OH phenol sẽ làm giảm tác dụng ít hơn các dẫn chất thế 2 nhóm -OH phenol.
Về hoạt tính chống viêm, thực tế chứng minh, chỉ cần 1 nhóm -OH phenol và các thành phần khác (nhóm methoxy, β-dicetonheptadien) là duy trì được hoạt tính này. Đáng chú ý là, trong một số trường hợp khi thêm nhóm thế vào cấu trúc (hydroxyethylsuccinyl và nhóm phosphat) đã làm tăng cường hoạt tính chống viêm so với curcumin (PH9 và PH11). Điều này cǜng được chứng minh khi trong một dãy các dẫn chất thế hai nhóm -OH phenol, dẫn chất diester (PH14, PH15) làm giảm hoạt tính chống viêm so với curcumin không đáng kể. Mặt khác, trong thử nghiệm này, phép thử ức chế sinh NO được tiến hành song song với phép thử độ sống sót của tế bào, kết quả chỉ ra, với cùng nồng độ thử (20-30 µg/ mL) thì các dẫn chất đều không gây chết tết bào (tỷ lệ khoảng 100% tế bào còn sống sót), tỷ lệ này cao hơn curcumin. Chứng tỏ các dẫn chất có độc tính thấp hơn curcumin và thử nghiệm này loại bỏ được các hiện tượng gây dương tính giả.
Về hoạt tính gây độc tế bào ung thư: Do tác dụng tác động lên việc loại bỏ tế bào ung thư của curcumin có thể theo nhiều cơ chế khác nhau nên việc thế các nhóm -OH phenol có thể làm tăng hoặc giảm tác dụng này của các dẫn chất [147]. Thực nghiệm chứng minh, trên một số dòng ung thư (Hela, HepG2) việc thế 1 hay 2 nhóm -OH phenol đều làm tăng khả năng gây độc tế bào ung thư của các dẫn chất so với curcumin ban đầu, trong đó, các dẫn chất thế 1 nhóm thể hiện tác dụng tốt, vượt trội hơn so với dẫn chất thế 2 lần (Bảng 4.3). Còn trên hai dòng ung thư thử nghiệm khác (K562 và MCF-7), dẫn chất thế 1 nhóm -OH thể hiện tác dụng tốt hơn dẫn chất thế 2 nhóm -OH phenol. Đặc biệt, khi thế 1 nhóm ester succinyl (PH9) hoặc gluraryl (PH8) thể hiện tốt tác dụng gây độc tế bào trên tất cả các dòng đã thử và tốt hơn curcumin ban đầu.
4.4. BÀN LUẬN VỀ DẪN CHẤT TIỀM NĂNG MONO-O-(2- (SUCCINYLOXY)ETHYL)CURCUMIN (PH9)
Dẫn chất PH9 được chúng tôi lựa chọn là dẫn chất tiềm năng trong luận án có cơ sở thực nghiệm về độ tan đã được cải thiện và hoạt tính sinh học in vitro tốt hơn cả so với các dẫn chất đã tổng hợp, đồng thời phù hợp với các dự đoán của docking và đặc tính giống thuốc. PH9 là dẫn chất thế một vị trí -OH phenol của curcumin, nên có những ưu điểm như đã phân tích ở Mục 4.3: còn một OH phenol tự do, còn 2 nhóm methoxy ở các nhân thơm và giữ được cầu nối β-dicetonheptadien. Cấu trúc này có khả năng duy trì được những hoạt tính sinh học của curcumin ban đầu, đồng thời có thể ổn định hơn và chuyển hóa chậm hơn curcumin như một số tài liệu đã phân tích [22], [43], [48], [157]. Với thời gian có hạn, trong khuôn khổ luận án chúng tôi bước đầu thực hiện những nghiên cứu sâu hơn về xây dựng quy trình tổng hợp dẫn chất này, đánh giá một số đặc tính chất lượng (cấu trúc phổ hai chiều, định lượng, độ ẩm, tro toàn phần…); đánh giá một số đặc tính sinh dược học (độ tan và hệ số phân bố n-octanol/ nước); đánh giá hoạt tính kháng viêm và độc tính cấp trên chuột của dẫn chất.
4.4.1. Bàn luận về xây dựng quy trình tổng hợp dẫn chất tiềm năng PH9
4.4.1.1. Bàn luận về xây dựng quy trình tổng hợp dẫn chất trung gian PH6 từ curcumin
Từ kết quả thăm dò hoạt tính cho thấy, PH6 là mắt xích trung gian quan trọng theo hướng nghiên cứu cải thiện độ tan của curcumin. Phân tử này có 1 nhóm hydroxyethyl là cầu nối tốt để gắn các nhóm thân nước khác. Thực nghiệm cho thấy, khi gắn trực tiếp anhydrid diacid vào OH phenol của curcumin để tạo môn ester (succinyl và glutaryl), thì phản ứng có xảy ra, song không hoàn toàn, sản phẩm rất dễ thủy phân khi xử lý phản ứng với acid loãng (để loại base xúc tác). Trong khi đó, các sản phẩm ester qua cầu nối hydroxyethyl thì ổn định hơn. Điểm khó khăn nhất trong phản ứng hydroxyethyl hóa tạo PH6 là kiểm soát tính chọn lọc của phản ứng do hiện tượng polyalkyl hóa. Các điều kiện đã được chúng tôi khảo sát để tối ưu quy trình về các yếu tố: tác nhân alkyl hóa (2-bromoethanol), tỷ lệ mol 2-bromoethanol : curcumin, dung môi, thời gian, nhiệt độ phản ứng, cách thức nạp liệu và phương pháp tinh chế.
Về mặt lý thuyết, có thể sử dụng tỷ lệ mol 2-bromoethanol : curcumin = 1 : 1 để thu được chọn lọc PH6. Tuy nhiên, kết quả thực nghiệm chỉ ra, ở điều kiện này chỉ có một lượng rất nhỏ curcumin phản ứng, và cần thiết phải tăng lượng tác nhân
so với lý thuyết. Sau khảo sát, chúng tôi đã lựa chọn được tỷ lệ thích hợp 2- bromoethanol : curcumin = 2 : 1. Nhiệt độ có ảnh hưởng lớn đến tốc độ của phản ứng alkyl hóa. Kết quả khảo sát chỉ ra, ở nhiệt độ 55 °C (là nhiệt độ sôi của aceton), phản ứng xảy ra nhanh nhất, hạn chế được sự phân hủy của curcumin trong tiến trình alkyl hóa. Ở nhiệt độ phòng, phản ứng alkyl hóa hầu như không xảy ra. Khi thay thế dung môi aceton bằng acetonitril nhằm nâng cao nhiệt độ (tốc độ) phản ứng, song acetonitril cho hiệu suất thấp hơn nhiều so với aceton. Kali carbonat là chất bổ trợ (additive) giúp chuyển curcumin thành dạng muối phenolat (ArO-K+), có khả năng phản ứng với 2-bromoethanol tốt hơn so với curcumin ban đầu. Nồng độ tác nhân (lượng 2-bromoethanol/tổng thể tích dung môi) có ảnh hưởng đến sự chọn lọc của phản ứng. Ở nồng độ cao (không thực hiện pha loãng tác nhân), phản ứng tạo ra nhiều tạp polyalkyl hóa. Ở nồng độ loãng hơn, phản ứng có xu hướng tạo ra ít tạp hơn, hiệu suất PH6 cao hơn, đặc biệt khi nâng cấp quy mô. Bằng cách điều chỉnh cách thức nạp liệu (pha loãng tác nhân alkyl hóa trong aceton và cho dần vào khối phản ứng) chúng tôi đã hạn chế được các sản phẩm phụ và duy trì sự ổn định của phản ứng. Nồng độ tác nhân phù hợp được lựa chọn là 3,60 mL 2- bromoethanol/ 600 mL aceton (ở quy mô 5 g/mẻ).
Có thể bạn quan tâm!
-
 Cấu Trúc Ph3 Và Các Giá Trị Tín Hiệu Proton, Carbon Trong Phân Tử Trên Phổ Nmr
Cấu Trúc Ph3 Và Các Giá Trị Tín Hiệu Proton, Carbon Trong Phân Tử Trên Phổ Nmr -
 Bảng Kết Quả Phân Tích Phổ 1H-Nmr, 13C-Nmr Và Dept Của Ph9
Bảng Kết Quả Phân Tích Phổ 1H-Nmr, 13C-Nmr Và Dept Của Ph9 -
 Cấu Trúc Ph12 Và Các Giá Trị Tín Hiệu Proton, Carbon Trong Phân Tử Trên Phổ Nmr
Cấu Trúc Ph12 Và Các Giá Trị Tín Hiệu Proton, Carbon Trong Phân Tử Trên Phổ Nmr -
 Nghiên cứu bán tổng hợp một số dẫn chất curcumin nhằm cải thiện độ tan trong nước hướng ứng dụng trong dược phẩm - 24
Nghiên cứu bán tổng hợp một số dẫn chất curcumin nhằm cải thiện độ tan trong nước hướng ứng dụng trong dược phẩm - 24 -
 Nghiên cứu bán tổng hợp một số dẫn chất curcumin nhằm cải thiện độ tan trong nước hướng ứng dụng trong dược phẩm - 25
Nghiên cứu bán tổng hợp một số dẫn chất curcumin nhằm cải thiện độ tan trong nước hướng ứng dụng trong dược phẩm - 25 -
 Phổ Phổ Esi-Ms-Negative Của Sản Phẩm Thủy Phân Ph1,
Phổ Phổ Esi-Ms-Negative Của Sản Phẩm Thủy Phân Ph1,
Xem toàn bộ 442 trang tài liệu này.
Tinh chế PH6 bằng sắc ký cột (dựa theo tác giả Changtam, 2010 [33]) cho sản phẩm có độ tinh khiết cao, song thời gian dài, sử dụng một lượng lớn dung môi, cần được kiểm soát chặt về độc hại và an toàn. Dựa vào sự khác biệt về cấu trúc của PH6 và các tạp còn lại trong hỗn hợp phản ứng (curcumin, PH7, PH6c, PH6d
- Hình 4.3), chúng tôi đã thử nghiệm thành công phương pháp chiết kết hợp chuyển đổi pH để tinh chế PH6 từ hỗn hợp này. Bằng thực nghiệm, chúng tôi xác định được 2 giá trị pH quan trọng để tách chất là pH 10 và pH 12. Phân tử curcumin có 2 nhóm -OH phenol có thể tan tốt trong nước ở pH ≥ 10, phân tử PH6 có 1 nhóm

-OH phenol tan tốt trong nước ở pH 12, các chất còn lại (PH7, PH6c, PH6d) đã bị khóa cả 2 nhóm -OH phenol bằng các nhóm 2-hydroxyethyl nên khó tan trong kiềm hơn và có khả năng phân bố trong dung môi hữu cơ (dicloromethan). Trên cơ sở đó, khi kiềm hóa hỗn hợp phản ứng đến pH 12, thì curcumin và PH6 chuyển thành dạng muối natri phenolat, tan trong pha nước; các tạp PH7, PH6c, PH6d tan được trong pha hữu cơ và bị tách loại. Tiếp tục acid hóa pha nước về pH 10 thì trong pha nước chỉ còn natri curcuminat, trong khi PH6 được giải phóng và tan vào pha dicloromethan. Từ đó, thu được PH6 thô chứa một lượng nhỏ các tạp chất
trên. Khảo sát một số dung môi để kết tinh, nhận thấy sản phẩm được kết tinh trong methanol tạo tinh thể hình kim, loại được hoàn toàn các tạp còn lại sau chiết.
4.4.1.2. Bàn luận về xây dựng quy trình tổng hợp dẫn chất tiềm năng PH9 từ PH6
Do cấu trúc PH6 có nhóm β-diceton và nhóm CH2 linh động nên dễ tạo dạng hỗ biến tạo –OH enol, có khả năng tham gia acyl hóa. Vì vậy, sản phẩm thu được ngoài PH9, còn có thể có tạp acyl hóa xảy ra trên nhóm enol này và –OH phenol còn lại. Vì vậy, cần phải kiểm soát chặt chẽ các thông số thời gian, nhiệt độ, tỷ lệ mol anhydrid succinic : PH6 để thu được lượng sản phẩm PH9 là nhiều nhất và hạn chế tạo ra tạp. Phản ứng cần được tiến hành trong điều kiện khan nước để tránh thủy phân tác nhân anhydrid succinic cǜng như đảm bảo độ ổn định của phản ứng. Khi nâng cấp lên quy mô 2 g và 20 g, chúng tôi nhận thấy hiệu suất phản ứng có giảm. Điều này có thể là do ester đã bị thủy phân (bởi HCl 1M khi xử lý loại pyridin) nhiều hơn ở quy mô 20 g/mẻ. Do vậy, khi nâng cấp quy mô, để loại pyridin, chúng tôi đã sử dụng dung dịch CuSO4 bão hòa thay cho dung dịch HCl 1M và thu được hiệu quả tốt hơn. CuSO4 có tính acid yếu hơn dung dịch HCl 1M, tạo phức với pyridin tan trong nước, làm giảm khả năng thủy phân liên kết ester.
Ngoài ra, chúng tôi đã tìm được là methanol làm dung môi kết tủa chọn lọc sản phẩm, loại đi được một số tạp khác có trong dịch chiết dicloromethan.
4.4.2. Bàn luận về các đặc tính sinh dược học của dẫn chất PH9
4.4.2.1. Bàn luận về phương pháp xác định độ tan các dẫn chất
Thực tế, có nhiều phương pháp để xác định độ tan, trong đó để xác định độ tan chính xác cho những chất rất ít tan. Có thể sử dụng phương pháp sắc ký lỏng hiệu năng cao (HPLC) với độ nhạy nanogam và có chất chuẩn đối chiếu; hoặc phương pháp quang phổ UV-VIS, đo độ hấp thụ của dung dịch ở bước sóng xác định (đã biết có chuẩn hoặc quét phổ), sau đó tính độ tan bão hòa của chất tan dựa vào độ hấp thụ riêng của chất (nếu có) hoặc so với chuẩn. Tuy nhiên, trong luận án, các dẫn chất tổng hợp từ curcumin đều là các dẫn chất mới, không có chất chuẩn để đối chiếu so sánh. Mặt khác, trong thử nghiệm này, chúng tôi chỉ xác định sơ bộ độ tan trong nước của các dẫn chất để có được những kết quả bước đầu. Chính vì vậy, chúng tôi đã xác định độ tan gián tiếp bằng phương pháp cân, tại nhiệt độ phòng và áp suất khí quyển, dựa trên tài liệu [182] và hướng dẫn trong Dược điển Việt Nam V [4]. Phương pháp này có ưu điểm: dễ thực hiện và có thể áp dụng với nhiều chất khác nhau. Tuy nhiên, nhược điểm của phương pháp là có thể gặp sai
số do lượng chất rắn thu được sau khi cô dung môi có thể chứa nhiều chất khác lẫn trong môi trường. Mặt khác, cân phân tích sử dụng có độ nhạy ±0,1 mg, chính vì vậy, với các dẫn chất ít tan thì số liệu có thể bị ảnh hưởng.
4.4.2.2. Bàn luận về độ tan in vitro của curcumin và dẫn chất PH9
Về kết quả đánh giá độ tan của curcumin và PH9 trong các môi trường pH khác nhau, nhận thấy:
Curcumin thực tế không tan trong nước và các môi trường pH khác nhau. Lượng curcumin hòa tan trong các môi trường này rất nhỏ, gần như bằng 0. Cụ thể, khối lượng cân được của curcumin tại môi trường nước và các môi trường pH khác nhau, (xem Bảng 3.8 và Bảng 3.34) đều trong khoảng <0,1mg coi như nằm dưới giới hạn xác định của cân (<0,1 mg).
Dẫn chất PH9 có độ tan cải thiện đáng kể so với curcumin. Tại pH 1,2; 4,5; nước cất tuy vẫn thuộc nhóm khó tan, nhưng độ tan của PH9 đã cải thiện hơn rất nhiều lần so với curcumin trong cùng một điều kiện thử. Tại pH 6,8 và pH 7,4 PH9 thuộc nhóm chất hơi tan.
4.4.2.3. Bàn luận về hệ số phân bố dầu nước
Do dẫn chất PH9 là một dẫn chất mới hoàn toàn, chưa xuất hiện trong bất kǶ tài liệu tham khảo nào. Vì vậy, dẫn chất này không có chuẩn để so sánh và chưa có phương pháp định lượng. Do đó, có thể tham khảo một số phương pháp dùng để định lượng curcumin trong các TLTK để có thể phân tích được hỗn hợp curcumin và PH9. Hệ số phân bố dầu nước được xác định là tỷ lệ chất có trong pha nước và pha dầu (n-octanol) ở trạng thái cân bằng nên có thể sử dụng phương pháp so sánh diện tích pic để tính toán.
Về kết quả hệ số log DpH của curcumin: Curcumin gần như không tan trong nước và các môi trường pH khác nhau. Do đó, bằng thực nghiệm phân tán curcumin từ pha nước sang pha dầu không xác định được giá trị hệ số phân bố của curcumin. Giá trị log P của curcumin tham khảo được thông qua các phần mềm dự đoán là 2,56 [170], tính toán theo ALOGPS là 3,62, theo ChemAxon là 4,12 [15]. Các giá trị này cho thấy curcumin thuộc nhóm thân dầu hơn.
Về kết quả hệ số log DpH của PH9: PH9 thể hiện độ tan tốt hơn nhiều so với curcumin tại các môi trường pH khác nhau, đặc biệt là tại môi trường pH 6,8 và 7,4. Tại môi trường pH thấp, lượng PH9 phân tán nhiều sang pha dầu hơn. Khi pH càng cao, thì phân tử PH9 tồn tại nhiều ở dạng ion trong nước, do đó lượng PH9 phân tán sang pha dầu sẽ ít hơn.
Như vậy, PH9 thể hiện tính thấm tốt trong điều kiện đã thử nghiệm. Giá trị log DpH thực tế của PH9 là thấp hơn nhiều so với curcumin và tiến dần về giá trị 0. Giá trị này cho thấy, PH9 thân cả dầu và nước, có khả năng thấm tốt qua màng phospholipid, phù hợp với bào chế dạng uống hoặc các dạng bôi viêm tại chỗ [9], [11].
4.4.3. Bàn luận về hoạt tính chống viêm và độc tính cấp trên chuột của dẫn chất tiềm năng PH9
4.4.3.1. Về hoạt tính chống viêm của dẫn chất PH9 trên chuột
Dẫn chất PH9 thể hiện tiềm năng trong nhiều hoạt tính sinh học: kháng viêm và gây độc tế bào ung thư trên nhiều dòng tế bào. Do giới hạn về thời gian và kinh phí trong khuôn khổ luận án, nên bước đầu chúng tôi tiến hành thử nghiệm hoạt tính kháng viêm trên chuột theo đường ngoài da để chứng minh tác dụng của chất tiềm năng trên cơ thể sống. Từ đó, làm cơ sở cho những thử nghiệm sau này.
Dẫn chất PH9 đã thể hiện được hoạt tính kháng viêm trên chuột theo đường bôi trên tai. Trong thử nghiệm này, tai chuột được gây viêm và bôi các dung dịch chứa: PH9, curcumin hoặc đối chứng dương. Mẫu PH9 ở liều 2 mg/20 µL/tai đã thể hiện hoạt tính kháng viêm tốt tại chỗ viêm theo hai thời điểm đo là 30 phút và 60 phút, (P<0,05). Ngược lại, với cùng mức liều như vậy, curcumin không thể hiện hoạt tính (P>0,05). Kết quả này có thể là do, khi bề mặt da bị viêm dẫn tới cấu trúc da thay đổi, những dẫn chất có tính thấm tốt ở cả pha nước và pha dầu sẽ dễ xâm nhập vào tổ chức viêm tại chỗ gây tác dụng giảm viêm; PH9 có logP thực tế là 0,542 thể hiện tốt cả khả năng thân nước cǜng như thân dầu nên thể hiện tác dụng tốt. Curcumin có thiên hướng thân dầu hơn, nên khó thấm vào tổ chức viêm, từ đó không thể hiện tác dụng kháng viêm ở liều đã thử.
4.4.3.2. Về độc tính cấp của dẫn chất PH9
Dựa trên các kết quả về đánh giá độc tính cấp của dẫn chất PH9 trên chuột, nhận thấy, sau khi uống mẫu thử nghiệm PH9 với mức liều 10000 mg/kg thể trọng, không có con chuột nào bị chết, không quan sát thấy hiện tượng bất thường về thần kinh hay hiện tượng tiêu chảy ở các chuột thí nghiệm. Điều này cho thấy mẫu thử nghiệm PH9 là an toàn không gây độc tính cấp với liều thử cao nhất là 10000 mg/kg thể trọng. Mẫu PH9 thuộc nhóm không gây độc cấp tính theo đường uống thử nghiệm trên chuột nhắt trắng với mức liều tối đa 10000 mg/kg thể trọng. Điều này chứng tỏ, mẫu PH9 vẫn giữ được độ an toàn với cơ thể sống giống curcumin.
Như vậy, PH9 là dẫn chất mới hoàn toàn của curcumin, có độ tan cải thiện hơn và tính thấm tốt hơn curcumin. Bên cạnh đó, PH9 thể hiện là một hoạt chất tiềm năng có thể ứng dụng trong dược phẩm; dẫn chất này không gây độc tính cấp trên chuột, có tác dụng kháng viêm, chống oxy hóa và gây độc tế bào ung thư in vitro; đặc biệt, khi thử nghiệm hoạt tính chống viêm trên tai chuột, PH9 đã thể hiện hoạt tính tốt vượt trội so với curcumin.
KẾT LUẬN
KẾT LUẬN VÀ KIẾN NGHỊ
1. Đã bán tổng hợp được 14 dẫn chất mục tiêu (chứa các nhóm chức thân nước: - COOH, -COONa, -SO3Na, -OH alcol, -OPO(OH)2, -OPO(ONa)2, -OSO3Na và -NH2) có độ tan trong nước được cải thiện so với curcumin và thăm dò tác dụng sinh học của các dẫn chất mới tổng hợp được. Trong đó:
+ Đã khẳng định được cấu trúc các dẫn chất qua các phương pháp phân tích phổ hồng ngoại, phổ khối lượng và phổ cộng hưởng từ hạt nhân. 12/14 dẫn chất mới hoàn toàn, chưa được công bố trong các tài liệu tham khảo được.
+ Đã sơ bộ đánh giá được độ tan của các dẫn chất bán tổng hợp. Tất cả các chất đều có độ tan trong nước tốt hơn curcumin ban đầu.
+ Đã đánh giá được các hoạt tính sinh học in vitro của các dẫn chất mới tổng hợp được. Về tác dụng chống oxy hóa, đã chỉ ra dẫn chất PH9 thể hiện hoạt tính mạnh hơn cả so với các dẫn chất còn lại, tuy nhiên đều kém hơn curcumin. Về tác dụng chống viêm, đã tìm ra hai dẫn chất PH9 và PH11 thể hiện hoạt tính tốt nhất trong các dẫn chất, tốt hơn curcumin tương ứng gấp 1,32 lần và 4,69 lần. Đối với hoạt tính gây độc tế bào ung thư, đã thu được hai dẫn chất PH8 và PH9 thể hiện tác dụng mạnh nhất trong các dẫn chất và mạnh hơn curcumin trên tất cả các dòng tế bào đã thử (Hela, HepG2, K562, MCF7).
2. Đã lựa chọn và xây dựng được quy trình tổng hợp dẫn chất tiềm năng (mono-O- (2-(succinyloxy)ethyl)curcumin, PH9), trong đó:
+ Đã khảo sát các phản ứng, tìm ra các thông số xây dựng quy trình tổng hợp dẫn chất tiềm năng PH9 ở quy mô 20 g/mẻ đạt hiệu suất 72,83% từ dẫn chất PH6 (được tổng hợp từ curcumin đạt hiệu suất 42,96% ở quy mô 25 g/mẻ).
+ Đã phân tích được cấu trúc phổ 2 chiều và đánh giá được độ tinh khiết của dẫn chất
PH9 (hàm lượng đạt 96,38%, HPLC).
+ Đã xác định được độ tan (tại pH 6,8 và 7,4 PH9 thuộc nhóm chất hơi tan) và hệ số phân bố dầu/nước của PH9 trong các môi trường pH (log DpH = 0,542; 0,820; 0,239 và
-0,543 lần lượt trong nước cất, pH 4,5; 6,8 và 7,4). Dẫn chất PH9 đã cải thiện được cả độ tan và tính thấm so với curcumin ở tất cả các môi trường thử nghiệm.
3. Đã đánh giá được hoạt tính chống viêm in vivo và độc tính cấp của dẫn chất tiềm
năng PH9.