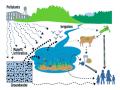
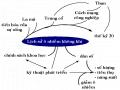
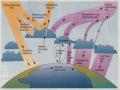
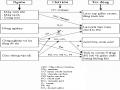
Trên thế giới có khoảng 60 triệu tấn chất hữu cơ tổng hợp như nhiên liệu, chất dẻo, chất màu, thuốc trừ sâu, chất phụ gia, nói chung là rất độc và khá bền hoặc các hợp chất sinh học đặc biệt là các hydrocacbon thơm.
![]()
Hóa chất bảo vệ thực vật
Các chất bảo vệ thực vật (pesticides) hiện có hơn 10.000 loại chất khác nhau bao gồm thuốc trừ sâu (insecticides), thuốc diệt cỏ (herbicides), diệt nấm (fungicides), diệt chuột và các loài thú gặm nhấm (edenticides), diệt ký sinh trùng (nemalocides) ... và các loại phân bón hữu cơ khác. Nói chung, các chất bảo vệ thực vật, kích thích sinh học đều rất độc. Cũng có một số loại độc, độc vừa hoặc ít độc. Người ta thường phân loại theo thành phần hóa học gồm halogen, phospho, cacbonat, chlorophenocyanid ...
![]()
Chất tẩy rửa
Các chất tẩy rửa (detergents) gồm các dạng thành phần:
![]()
Các chất hoạt động bề mặt, có hoạt tính bề mặt cao, hòa tan tốt, sức căng bề mặt nhỏ, tạo ra nhũ tương, huyền phù với các chất bẩn (tách ra từ nguyên liệu giặt).
![]()
Các chất phụ gia, bổ sung cho chất tẩy rửa chính, tạo môi trường kiềm theo ý muốn cho hoạt động bề mặt.
![]()
Dầu mỏ
Dầu mỏ được chế biến thành nhiều loại sản phẩm dạng khí, dạng lỏng và thể rắn. Dạng khí và dạng lỏng như khí đốt, xăng, dầu hôi, nhớt ... được thải ra môi trường từ các hoạt động sản xuất, giao thông, sinh hoạt gia đình, thường được lọc lắng khi rơi vãi ra đất, nước thải.
![]()
Các chất hữu cơ tổng hợp khác
Số lượng và chủng loại vô cùng nhiều, đều là những chất tiêu thụ oxy vì chúng không bền, có khuynh hướng oxy hóa thành các dạng đơn giản hơn, sẽ lấy oxy hòa tan trong nước để oxy hóa làm giảm độ hòa tan của oxy trong nước (DO). Hàm lượng oxy hòa tan này là chỉ tiêu quan trọng để kiểm soát chất lượng nước.
Khi nhu cầu oxy hóa hóa học (COD) và nhu cầu oxy hóa sinh học (BOD) tăng thì DO giảm và nước trở nên bị ô nhiễm.
![]()
1.2.Các hợp chất dạng vô cơ
![]()
Các loại phân bón vô cơ
Thành phần chủ yếu là C, H, O2 và N, P, K dưới dạng hợp chất vô cơ và hữu cơ cùng với yếu tố vi sinh vật. Một phần khá lớn các phân bón trôi theo nước, bốc hơi, chuyển hóa hoặc thấm xuống đất và tồn lưu trong đất. Sử dụng quá thừa phân bón vô cơ sẽ gây ra hiện tượng phú dưỡng (eutrophysation) trong nước bề mặt, tạo điều kiện phát triển các loại rong, rêu , tảo .v.v… làm mất cân bằng sinh thái do thiếu DO và tăng cao BOD.
![]()
Các khoáng acid
Nước thải từ sản xuất công nghiệp, trôi theo dòng nước thải vào nước làm gia tăng độ acid, giảm độ pH của nước.
![]()
Các chất lắng: mưa lũ, xói mòn đất, trôi theo nước rồi lắng lại có thể làm tăng vài trăm lần mức ô nhiễm thông thường của nước sinh hoạt.
![]()
Các kim loại hàm lượng "vết": Có một số kim loại (như Hg, Arsen, Thalium …) với hàm lượng rất nhỏ cũng gây độc hại cho sự sống của sinh vật được thải vào nước chủ yếu từ các nguồn sản xuất và giao thông.
![]()
Chất phóng xạ
Một số dạng phóng xạ tự nhiên được tìm thấy phổ biến là Radi và K40 từ khoáng chất lọt qua thấm lọc vào nguồn nước sinh hoạt. Một số chất phóng xạ lọt ra từ các nhà máy điện nguyên tử, sản xuất vũ khí hạt nhân.
![]()
1.3.Các vi sinh vật gây bệnh
Nước thải sinh hoạt chứa khá nhiều vi sinh vật gây bệnh, đặc trưng là các dạng Coliformes, tiêu biểu là Escheria Coli gây bệnh đường ruột.
![]() 1.4.Rác
1.4.Rác
Rác tuôn ra biển (mỗi năm khoảng 6,5 triệu tấn). Plastic là loại khó phân hủy nhất, nó có thể tồn tại hơn 50 năm trong môi trường biển, hiện đang có xu hướng tăng lên.
% rác thải là plastic | |
Dọc bờ biển Địa Trung Hải Thái Bình Dương | >70% >80% |
Có thể bạn quan tâm!
-
 Số Loài Động Vật Và Thực Vật Có Nguy Cơ Bị Tuyệt Chủng
Số Loài Động Vật Và Thực Vật Có Nguy Cơ Bị Tuyệt Chủng -
 Diện Tích Đất Nông Nghiệp Và Đất Rừng So Với Diện Tích Đất Tự Nhiên Năm 1994 Chia Theo Vùng
Diện Tích Đất Nông Nghiệp Và Đất Rừng So Với Diện Tích Đất Tự Nhiên Năm 1994 Chia Theo Vùng -
 Dự Trữ Than Đá Ở Một Số Nước Trên Thế Giới
Dự Trữ Than Đá Ở Một Số Nước Trên Thế Giới -
 Nguồn Gốc Và Tác Hại Của Các Loại Khí Trong Khí Quyển
Nguồn Gốc Và Tác Hại Của Các Loại Khí Trong Khí Quyển -
 Biện Pháp Phòng Ngừa Hoặc Làm Giảm Hiện Tượng Mưa Acid
Biện Pháp Phòng Ngừa Hoặc Làm Giảm Hiện Tượng Mưa Acid -
 Mật Độ Bụi Lơ Lửng Trong Không Khí Ở Một Số Thành Phố Của Việt Nam (1996)
Mật Độ Bụi Lơ Lửng Trong Không Khí Ở Một Số Thành Phố Của Việt Nam (1996)
Xem toàn bộ 207 trang tài liệu này.

2.Một số hậu quả
![]()
Cơ thể con người bị nhiễm giun sán, nhiễm độc, ảnh hưởng đến sức khỏe. Gây một số bệnh thường gặp như: tả, thương hàn, kiết, giun sán, viêm gan siêu vi …
![]()
Gây hiện tượng phú dưỡng hóa, ảnh hưởng đến sức khỏe của người dân và năng suất hải sản.
![]()
Trong các mẫu cá, tôm, cua ở Vịnh Jacarta (Indonesia), Pb >4%, Hg >38%, cadmium >76%. Ở Nhật, Úc, Trung Quốc, Hàn Quốc, Thổ Nhĩ Kỳ … có nồng độ acid, thủy ngân, chì trong nước vượt quá tiêu chuẩn cho phép. Ở Malaysia, nước thải từ các nhà máy dầu cọ và cao su, từ các nhà máy khác và các khu dân cư đã làm 42 con sông coi như chết.
![]()
Ô nhiễm nước ngầm: Ở Châu Mỹ Latinh, các chất độc hại từ các bãi thải thâm nhập vào nước ngầm cứ 15 năm tăng gấp đôi. Tại thành phố của các nước phát triển nước ngầm bị bẩn do thiếu hệ thống xử lý và quản lý kém các hố rác tự hoại.
![]()
Các loại "tảo đỏ” phát triển mạnh ở vùng cửa sông, dọc bờ biển Bắc Carolina và ở bờ biển phía Nam bán đảo Scandinave. Hoa của tảo đỏ tiết ra những độc tố ảnh hưởng tới thực phẩm biển. Năm 1987, ngộ độc do thực phẩm có độc tố tảo đỏ đã giết chết 26 người Guatamala. Ở Việt Nam, tại vùng biển phía bắc Bình Thuận, từ huyện Tuy Phong trở ra, đang phải đối đầu với nạn “Thủy triều đỏ”.
![]()
Dầu hỏa bao phủ trên mặt nước làm cản trở khả năng quang hợp, cản trở sự trao đổi oxy, làm chết cá, chim (do ăn cá có dầu).
![]()
Ở cảng dọc biển Thái lan hàng năm có khoảng 50.000 chim biển chết do ngộ độc dầu.
![]()
Ở Anh Quốc: 250.000 chim biển, dọc bờ biển Đại Tây Dương có
400.000 con.
![]()
Bơi lội ở vùng biển bị ô nhiễm hữu cơ thì bị rối loạn tiêu hóa, viêm tai, viêm đường hô hấp, nguy cơ tăng bệnh viêm gan siêu vi và dịch tả.
3.Các thông số xác định ô nhiễm nước
Dựa vào tiêu chuẩn quốc gia TCVN hoặc các tiêu chuẩn quốc tế người ta quy định cho các loại nước những tiêu chuẩn, các thông số cần giám sát (loại A và B).
![]()
Nước nguồn phải giám sát các thông số như độ pH, độ trong, độ cứng, màu, độ đục, hàm lượng oxy hòa tan, Fe, Mn và kim loại nặng….
![]()
Nước qua sử dụng phải giám sát: độ pH, độ kiềm, độ acid, COD, BOD, N, P, S, các hóa chất, dầu mỡ và kim loại nặng….
Các tiêu chuẩn cũng được quy định theo hai loại nước nói trên.
![]() 3.1.pH
3.1.pH
Nước trung tính có pH = 7; nếu pH < 7 là có tính acid, pH > 7 – tính kiềm. Nước ngầm thường có pH = 4-5; nước thải có pH dao động nhiều, đặc biệt trong các quá trình keo tụ, khử trùng, khử sắt, làm mềm nước, chống ăn mòn. pH là chỉ tiêu rất cần thiết cho phép xác định phương pháp xử lý nước thích hợp.
Độ acid tự nhiên là do CO2 hoặc acid vô cơ gây ra, có thể ăn mòn kim loại. CO2 là do hấp thụ từ không khí hoặc từ hoạt động oxy hóa sinh học các chất hữu cơ. Acid vô cơ thường có trong nước ngầm khi chảy qua các vùng mỏ hoặc các lớp khoáng chất, thường thấy dưới dạng hợp chất lưu huỳnh.
2- -
Độ kiềm tự nhiên là do 3 nhóm ion OH-, CO3 và HCO3 tạo nên. Một số muối như borat, silicat làm tăng độ kiềm. Vài acid hữu cơ khá bền với chất oxy hóa sinh học như humix; các muối của chúng gây tăng độ kiềm; tiêu thụ CO2 làm tăng độ pH. Độ kiềm cao gây ảnh hưởng xấu đến đời sống vi sinh vật. Nói chung cần giám sát độ kiềm để có biện pháp làm mềm nước hoặc tạo dung dịch đệm.
![]()
3.2.Độ cứng
Thường có hai loại là nước cứng và nước mềm.
Nước cứng không tạo bọt xà bông, dễ kết tủa do các ion hóa trị 2 như Ca++, Mg++ hoặc Fe++, Mn++, Zn++. Thường chủ yếu do Ca++ và Mg++. Giám sát độ cứng qua hàm lượng CaCO3 quy đổi. Nước mềm có CaCO3 < 50 mg/l. Nhìn chung nước cứng không độc hại nhưng ảnh hưởng không tốt đến sinh hoạt và công nghiệp vì không có bọt, giặt lâu sạch, hấp thụ Ca, Mg làm cho vải mau mục, dòn hoặc tạo thành màng cứng trên thành ống, nồi hơi ... dễ gây nổ.
![]()
3.3.Độ đục
Độ đục là do các hạt rắn lơ lửng, các chất hữu cơ phân rã hoặc do động thực vật chết gây nên. Độ đục làm giảm khả năng truyền ánh sáng vào nước, giảm quang hợp và đặc biệt giảm tính thẩm mỹ. Các hạt rắn có thể mang theo vi sinh vật và mầm bệnh.
Giám sát độ đục thông qua hàm lượng SiO2 trong 1 lít nước. Đơn vị độ đục là 1 mg SiO2/lít nước.
![]()
3.4.Độ màu
Nước tự nhiên không có màu; độ màu là do các chất như mùn, vụn chất hữu cơ (xác thực vật phân hủy), các hạt lơ lửng vô cơ, các tanin, acid humic phân hủy, thường có nguồn gốc từ nước thải công nghiệp đặc biệt là giấy, bông, nhuộm ... hoặc do Fe, có màu nâu đặc trưng.
Người ta phân biệt màu thực và màu biểu kiến. Màu thực là do các dạng hữu cơ, thực vật dạng keo, khó xử lý ví dụ mùn humic có màu vàng; thủy sinh, rong tảo có màu xanh. Màu biểu kiến là do các hạt rắn vô cơ có màu, xử lý đơn giản hơn.
Nước thải công nghiệp thường có màu hỗn hợp vừa thực, vừa màu biểu kiến. Đôi khi nước có màu không gây độc hại đáng kể cho sinh vật nhưng làm giảm vẻ thẩm mỹ hoặc làm giảm phẩm chất trong chế biến thực phẩm, công nghiệp nhuộm ...
![]()
3.5.Hàm lượng chất rắn
Các chất rắn bao gồm các chất vô cơ hòa tan (các muối) hoặc không hòa tan (đất đá dạng huyền phù) và các chất hữu cơ như vi sinh vật (kể cả động vật nguyên sinh và tảo), các chất hữu cơ tổng hợp (phân bón, chất thải).
Người ta thường giám sát hàm lượng chất rắn qua các thông số sau:
![]()
Tổng chất rắn (TS) là trọng lượng khô (mg/l) của phần còn lại sau khi bay hơi 1 lít nước, sấy khô ở 103oC.
![]()
Chất rắn lơ lửng (SS) là trọng lượng khô phần rắn còn lại trên giấy lọc sợi thủy tinh 1 lít nước, sấy khô ở 103-105oC.
![]()
Chất rắn hòa tan (DS) là hiệu số (TS – SS) = DS.
![]()
3.6.Hàm lượng oxy hòa tan (DO – Dissolved Oxygen)
Tất cả các sinh vật hiếu khí đều cần O2 cho hô hấp. Động vật trên cạn sử dụng O2 của không khí (khoảng 21% trong khí quyển), động vật dưới nước sử dụng O2 hòa tan (trung bình 4 mg/l); O2 hòa tan có nhiều hơn trên phần nước mặt, hoặc ở vùng có thực vật xanh. Hàm lượng O2 hòa tan phụ thuộc vào áp suất riêng phần O2 trong không khí; vào nhiệt độ nước và quang hợp, vào hàm lượng muối trong nước. O2 hòa tan giảm là dấu hiệu ô nhiễm nước. Khi hàm lượng O2 hòa tan gần bằng 0 thì nước ô nhiễm nặng. Nước sạch thì O2 bão hòa.
toC = 0oC; p = 1 atm thì DO # 14,6 mg/l toC = 20oC; p = 1 atm thì DO # 9,2 mg/l toC = 35oC; p = 1 atm thì DO # 7 mg/l
![]() 3.7.Nhu cầu oxy hóa sinh hóa (BOD – Biochemical Oxygen Demand)
3.7.Nhu cầu oxy hóa sinh hóa (BOD – Biochemical Oxygen Demand)
Đó là lượng O2 cần thiết để vi sinh vật thực hiện quá trình oxy hóa sinh hóa các chất hữu cơ bị phân hủy. Đơn vị là mg O2/l. Chỉ số BOD cao thì ô nhiễm nặng.
![]()
Nước sạch thì BOD < 2 mg O2/l
![]()
Nước thải sinh hoạt thường có BOD # 80-240 mg O2/l
Thông thường phải có thời gian dài khoảng 20 ngày thì 80-90% lượng chất hữu cơ mới bị oxy hóa hết. Người ta quy ước để 5 ngày vì vậy gọi là BOD5.
![]() 3.8.Nhu cầu oxy hóa hóa học (COD – Chemical Oxygen Demand)
3.8.Nhu cầu oxy hóa hóa học (COD – Chemical Oxygen Demand)
Đó là lượng oxy cần thiết cho quá trình oxy hóa hóa học các chất hữu cơ tạo thành CO2 và nước. Vì BOD không tính đến các chất hữu cơ bền vững vốn không bị oxy hóa sinh hóa, còn COD thì có tác dụng với mọi chất hữu cơ, nên COD được coi là đặc trưng hơn trong giám sát ô nhiễm nước. Nước thải ô nhiễm có tỉ lệ BOD/COD là 0,7 - 0,5.
![]()
3.9.Hàm lượng các chất
![]()
Sulfat SO42- ảnh hưởng đến sự tạo thành H2S gây mùi khó chịu, rất độc cho cá; gây cặn cứng ở thành nồi hơi, nồi nấu nước, làm mòn kim loại, gây bệnh tiêu chảy.
![]()
Nitơ và hợp chất nitơ: Chủ yếu bắt nguồn từ quá trình phân hủy chất hữu cơ do vi sinh vật. Nitrit – NO2 là giai đoạn trung gian trong quá trình đạm hóa. Nitrat – NO3 là giai đoạn oxy hóa cao nhất cũng là giai đoạn sau cùng của oxy hóa sinh học.
![]()
Phosphat PO43-: Đó là nguồn dinh dưỡng giúp sinh vật và hệ sinh thái nước phát triển. Nhưng nếu nhiều quá sẽ sinh ra thiếu O2 tạo nên hiện tượng thối rữa.
![]()
Các kim loại và kim loại nặng: Các kim loại thường được lưu ý giám sát bởi tính độc hại và tác động gây ô nhiễm của chúng như: đồng, sắt, mangan, kẽm, chì, crom, nhôm, thủy ngân.
4.Thành phần nước thải của một số nhà máy Bảng 2. Đặc điểm nước thải của một số nhà máy lớn ở Hà Nội
TÊN NHÀ MÁY | LƯỢN G XẢ m3/ngày | BOD5 mg/l | COD mg/l | CÁC CHẤT BẨN ĐẶC TRƯNG | ĐIỂM XẢ | |
1. | Da Thụy Khê | 1.300 | 350 | 675 | Crom, tananh, sulfur | Mương Thụy Khê |
2. | Bia Hà Nội | 3.000 | 150 | 290 | Cặn bia | Mương Đại |
Yên | ||||||
3. | Rượu Hà Nội | 6.000 | 350 | 675 | Bã rượu | Mương Trần Khắc Chân |
4. | Dệt 8/3 | 10.000 | 80 | 250 | Các chất tẩy, nhuộm | Sông Kim Ngưu |
5. | Cao su Sao vàng | 5.000 | 140 | 380 | Các chất lưu hóa | Sông Tô Lịch |
6. | Xà phòng Hà Nội | 5.000 | 35 | 295 | NaOH | Sông Tô Lịch |
7. | Nhà máy công cụ số 1 | 3.600 | 25 | 70 | Ni, Cr, Cu | Sông Tô Lịch |
8. | Pin Văn Điển | 2.000 | 28 | 65 | Mn, Fe, Pb | Sông Kim Ngưu |
9. | Phân lân Văn Điển | 5.000 | 40 | 95 | PO43- | Sông Kim Ngưu |
10. | Nhà máy sơn tổng hợp | 1.200 | 30 | 47 | Se, dầu, Fe2O3 | Sông Tô Lịch |
Bảng 3. Thành phần hóa học nước thải của Vedan, Vissan, đường Hiệp Hòa
Chỉ tiêu | Đơn vị | Vedan | Vissan | Đường Hiệp Hòa | |
1. | pH | 4,60 | 7,3 | 3,2 | |
2. | SS | mg/l | - | 530 | 180 |
3. | Tổng N | mg/l | 1.170,00 | 212 | 20 |
4. | N-NH4 | mg/l | 61,00 | 77 | 78 |
5. | Tổng P | mg/l | 571,00 | 30 | 20 |
COD | mg/l | 370.000,00 | 3.400 | 146.000 | |
7. | BOD5 | mg/l | 70.000,00 | 1.800 | 26.000 |
8. | Mg2+ | mg/l | 2.600,00 | 5,6 | 800 |
9. | Ca2+ | mg/l | 6.400,00 | 35 | 5.600 |
10. | - HCO3 | mg/l | 6,00 | 50 | 55 |
11. | Pb2+ | mg/l | 0,01 | <0,01 | - |
12. | Zn2+ | mg/l | 3,31 | <0,01 | - |
13. | Cd2+ | mg/l | 0,01 | <0,01 | <0,01 |
14. | Hg+ | g/l | <0,20 | - | - |
15. | Cl- | mg/l | - | - | 19.150 |
16. | Na+ | mg/l | - | - | 200 |
6.
a) Vedan
Nguồn nước thải của Công ty Vedan từ các nguồn như: Nước chảy tràn; Nước thải sinh hoạt của cán bộ công nhân viên và nước thải sản xuất.
Nước thải sản xuất bao gồm:
![]()
Nước thải từ phân xưởng sản xuất Lysin và phân Vedagro trong dây chuyền lên men (phương pháp sinh học hiếu khí) chứa hàm lượng cao các chất hữu cơ (BOD, COD), chất dinh dưỡng (N, P), SS và các acid.
![]()
Nước thải từ phân xưởng sản xuất tinh bột và nước đường (phương pháp sinh học hiếu khí kết hợp kỵ khí). Nước thải chủ yếu có chứa hàm lượng cao chất hữu cơ (BOD, COD), xơ vỏ của sắn, đặc biệt có CN-.
![]()
Nước thải từ phân xưởng sản xuất bột ngọt và phân Vedagro có chứa hàm lượng cao NH3, COD, BOD5.
Lượng nước thải của nhà máy vào khoảng 1.000–1.200 m3/ngày. Nguồn nước thải của khu lên men là khu có nguồn nước thải rất lớn 1.250m3/ngày.
b) Công ty súc sản Vissan
Nước thải của công ty chủ yếu là huyết, phân (trâu, bò, heo) và một số phế phẩm như da, lông, các phần hư hỏng loại bỏ của khâu chế biến.v.v… Các nguồn nước thải: