hủy nhiệt theo phản ứng: 2NH3 = 3H2 + 2Nng. tử
Tiến hành ở nhiệt độ thấp nên sự khuếch tán khó khăn và chậm nên lớp thấm mỏng, thời gian thấm dài.
Sau khi thấm không tôi và mài
Phải dùng thép chuyên dụng để thấm (38CrMoAlA), trước khi thấm phải nhiệt luyện hóa tốt thành xoocbit ram.
Lớp thấm cứng hơn và giữ được ở nhiệt độ đến 5000C và cao hơn.
Hai nhóm công nghệ thấm hay dùng là:
Thấm nitơ nhiệt độ thấp (4800-5500C) thời gian thấm dài (ở nhiệt thấp khuếch tán xảy ra chậm). Tùy theo thời gian thấm chiều dài lớp thấp có thể đạt 0,4mm.
Thấm nitơ ở nhiệt độ cao (5500-6500C) thời gian thấm ngắn (để hạt nitơrit không
bị thô to lên và không làm hỏng tổ chức của thép sau khi tôi) chỉ tạo được lớp thấm mỏng chiều dày thường không quá 0,2mm.
Để tăng tốc độ thấm người ta tìm cách tăng diện tích tiếp xúc giữa các chi tiết và
Có thể bạn quan tâm!
-
 Đối Với Thép Trước Cùng Tích Và Thép Cùng Tích ( ≤ 0,8%c)
Đối Với Thép Trước Cùng Tích Và Thép Cùng Tích ( ≤ 0,8%c) -
 Tốc Độ Làm Nguội Trong Các Môi Trường Khác Nhau
Tốc Độ Làm Nguội Trong Các Môi Trường Khác Nhau -
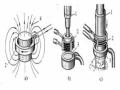
 Chi Tiết Tôi, 2. Vòng Cảm Ứng, 3. Vòng Phun Nước, 4. Đường Sức Từ Trường
Chi Tiết Tôi, 2. Vòng Cảm Ứng, 3. Vòng Phun Nước, 4. Đường Sức Từ Trường -
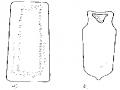
 S Ơ Đ Ồ Cấu Tạo Của Thỏi Đúc Thép Sôi (A) Và Thép Lặng (B).
S Ơ Đ Ồ Cấu Tạo Của Thỏi Đúc Thép Sôi (A) Và Thép Lặng (B). -
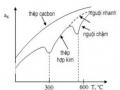
 Ảnh Hưởng Của Nguyên Tố Hợp Kim Đến Quá Trình Nhiệt Luyện
Ảnh Hưởng Của Nguyên Tố Hợp Kim Đến Quá Trình Nhiệt Luyện -
 Khái Niệm, Đặc Điểm Và Phân Loại Thép Kết Cấu
Khái Niệm, Đặc Điểm Và Phân Loại Thép Kết Cấu
Xem toàn bộ 193 trang tài liệu này.
môi trường thấm bằng cách tạo ra nhiều nhấp nhô bề mặt phun cát, xâm thực hóa học...
c. Công dụng
Thấm nitơ để tăng độ cứng và tính chống mài mòn
Trước khi thấm nitơ, chi tiết phải qua nhiệt luyện (tôi+ram cao) để tăng độ bền và độ dẻo dai của lòi. Đối với chi tiết mỏng và có hình dáng phức tạp thường thấm ni tơ ở nhiệt độ 500-5200C thời giam thấm phụ thuộc vào chiều sâu lớp thấm.
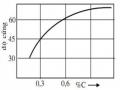
Khi thấm ở nhiệt độ500-5200C, để có chiều sâu lớp thấm 0,3-0,6mm phải mất
24-90 giờ. Thời gian thấm quá dài là nhược điểm của thấm nitơ, để làm nhanh quá trình có thể dùng phương pháp thấm hai cấp đầu tiên thấm ở nhiệt độ 500- 5200C, sau đó tăng lên 540- 5600C.
Độ cứng của lớp thấm phụ thuộc vào thành phần hóa học của thép và nhiệt độ thấm.
Đối với tất cả các loại thép nhiệt độ thấm càng cao thì độ cứng đạt được càng thấp.
Thấm nitơ để tăng tính chống ăn mòn
Với mục đích này thì có thể thấm ở nhiệt độ 600- 7000C, đối với chi tiết nhỏ thời gian thấm là 15 phút, chi tiết lớn thời gian thấm khoảng 6-10 giờ. Sau khi thấm trên bề mặt chi tiết tạo thành một lớp mỏng pha ε (0,01-0,03mm) có tính chống gỉ cao. Trong lớp thấm nitơ có ứng suất nén dư, giá trị ứng suất khoảng 60-80kG/mm2 nên nó làm tăng tính chống mỏi của chi tiết. Khả năng chống mỏi cao nhất đạt được sau khi thấm ở nhiệt độ 500- 5200C .
Thấm nitơ ở trạng thái lỏng
Thấm nitơ ở trạng thái lỏng tiến hành trong bể muối có thành phần 40%KCNO + 60%NaCN, qua bể muối cho luồng không khí đi qua. Nhiệt độ thấm là 5700C, với thời gian 0,5-3,0 giờ. Sau khi thấm trên bề mặt tạo thành một lớp mỏng cacbit-nitrit
Fe3(N,C) có khả năng chống mài mòn cao và không bị phá hủy dòn. Ưu điểm của phương pháp là ít thay đổi kích thước, chi tiết không bị cong vênh. Nhược điểm của phương pháp này là độc và giá muối xianua đắt.
Thấm nitơ dùng cho các chi tiết cần độ cứng và tính chống mài mòn rất cao. Tuy nhiên chịu tải không cao (do lớp thấm mỏng) như: một số loại trục, sơ mi, xy lanh máy bay, dụng cụ cắt, nòng súng, khuôn dập...Thấm nitơ làm tăng đáng kể giới hạn mỏi.
1.6.3.4. Thấm cacbon- nitơ
a. Định nghĩa
Thấm C-N là quá trình bão hoà và khuếch tán đồng thời hai nguyên tố C và N lên bề mặt chi tiết nhằm mục đích làm tăng độ cứng, khả năng chống mài mòn đồng thời phát huy khả năng chịu uốn, xoắn, chịu mỏi cho chi tiết.
b. Nguyên lý thấm cácbon-nitơ
Dùng hỗn hợp thấm để tạo ra môi trường có Cacbon và Nitơ nguyên tử. Ở nhiệt độ thích hợp, các nguyên tử C, N có thể khuếch tán vào bề mặt thép tạo nên lớp thấm có thành phần hoá học khác với lòi. Môi trường thấm có thể ở trạng thái lỏng, bột nhão hoặc thể khí. Tuy nhiên trong thời gian hiện nay môi trường thể khí được sử dụng nhiều nhất vì môi trường lỏng và bột nhão gây độc hại cho con người.
Có 2 phương pháp thấm C-N cơ bản là thấm C-N ở nhiệt độ thấp (thường được tiến hành ở thể lỏng) và thấm C-N ở nhiệt độ cao (thường được tiến hành thấm ở thể khí). Thấm C-N ở nhiệt độ cao (trên dưới 8500C), sự khuếch tán của cacbon mạnh, lớp thấm chủ yếu là cacbon (ít nitơ), do đó có tính chất gần với thấm cacbon tuy nhiên có nhiều ưu điểm hơn thấm cacbon. Thấm C-N ở nhiệt độ thấp (trên dưới 560oC), sự khuếch tán của cacbon yếu, lớp thấm chủ yếu là nitơ, tính chất gần với thấm nitơ nhưng lại kém hơn thấm nitơ.
Khác với thấm C-N nhiệt độ thấp không cần nhiệt luyện sau thấm, thấm C-N ở nhiệt độ cao phải nhiệt luyện sau thấm để đảm bảo độ cứng và khả năng chống mài mòn cao cho chi tiết.
Quá trình thấm C-N là quá trình khuếch tán đồng thời cả cacbon và nitơ vào bề mặt chi tiết. Cơ sở của quá trình này là sự chênh lệch giữa hoạt độ cacbon, nitơ của môi trường (ký hiệu lần lượt là (aC) và (aN)) với hoạt độ cacbon, nitơ trên bề mặt chi tiết (ký hiệu là [aC] và [aN]).
Trong quá trình thấm, hàm lượng C, N trên bề mặt chi tiết sẽ tăng dần cho tới khi hoạt độ của nó phù hợp với hoạt độ của môi trường. Khi đó cân bằng nhiệt động sẽ được thiết lập.
Trong công nghệ thấm C-N nhiệt độ cao, hoạt độ cacbon đóng vai trò chủ yếu. Tuy nhiên hoạt độ của nitơ cũng là m ột thông số ảnh hưởng đến quá trình thấm nó có tác dụng tăng tốc độ thấm. Có thể nói hoạt độ C, N chính là cơ sở của quá trình thấm C-N.
c. Phương pháp thấm C-N có nhiều ưu điểm nổi bật
Thấm C - N có thể được thực hiện trong một phạm vi nhiệt độ tương đối rộng (từ 7800C -9000C).
Nhiệt độ thấm tương đối thấp hơn so với thấm cacbon, áp dụng cho thép cacbon thấp và thép hợp kim thấp nhằm tăng độ cứng và tính chống mài mòn, đồng thời giảm khả năng biến dạng cho chi tiết. Nhiệt độ thấm thấp hơn do đó hạn chế được biến dạng, thoát cacbon hạn chế sự lớn hạt.
Sự bão hoà nitơ ảnh hưởng đến độ bão hoà và chiều sâu khuếch tán của cacbon. Nitơ và cacbon khi có mặt đồng thời có khả năng tăng hoạt tính lẫn nhau. Ngoài ra nitơ có tác dụng thu hẹp sự tồn tại của ferit làm cho quá trình bão hoà cacbon xảy ra mạnh mẽ hơn ở khoảng nhiệt độ thấp hơn so với thấm C, tạo được lớp thấm đồng đều hơn.
Khả năng chống mài mòn của lớp thấm cao hơn, nhờ sự có mặt của nitơ trong lớp thấm cacbon tạo thành pha Fe3(C,N) phân tán rất cứng làm tăng mạnh tính chống mài mòn. Độ cứng lớp thấm C-N từ 59 62 HRC trong khi đó lớp thấm cacbon có thể đạt từ 59 63 HRC.
Có thể tôi trực tiếp từ nhiệt độ thấm vì nhiệt độ thấm gần với nhiệt độ tôi, không cần hạ nhiệt độ trước khi tôi do đó hạn chế thoát cacbon, ôxy hoá và có thể tôi phân cấp vì nitơ làm tăng tính ổn định của austenit quá nguội, điều đó cũng giảm mạnh độ biến dạng.
Lớp thấm C-N không cần dày như lớp thấm C mà vẫn đảm bảo độ cứng và tính chống mài mòn, độ bền.
Thấm C-N có khả năng chống tạo vết nứt tốt hơn so với thấm C vì thấm C-N có tổ chức lớp thấm mịn không có lưới xementit. Còn lớp thấm C có tổ chức hạt thô và lưới xementit do đó trong quá trình tôi, lưới xementit tạo ra vết nứt tế vi và phát triển thành vết nứt của mẫu.
Trong lớp thấm C-N luôn tồn tại một lượng austenit dư làm cho lớp thấm vừa cứng lại vừa dai. Khi chịu tải trọng, nếu trong lớp thấm có một lượng austenit dư nhất định, tải trọng sẽ được phân bố đồng đều hơn và tránh được sự tập trung ứng suất.
So với thấm C tính chất lớp thấm C- N tỏ ra tốt hơn. Tuy nhiên phương pháp
thấm C-N cũng có một số nhược điểm cần lưu ý.
d. Nhược điểm của thấm C- N
Thành phần khí thấm phức tạp, điều khiển thế thấm khó khăn vì môi trư ờng thấm gồm nhiều loại khí. Công nghệ và xử lý lớp thấm phức tạp. Có thể xuất hiện nhiều dạng khuyết tật dạng rỗ khí tế vi, austenit dư hoặc tổ chức phi mactenxit có độ cứng thấp ở trên lớp thấm.
Thực chất nghiên cứu quy trình thấm C-N là nghiên cứu hạn chế khuyết tật trong lớp thấm bằng cách khống chế hàm lượng C, N trên bề mặt lớp thấm. Môi trường thấm hay là hỗn hợp khí thấm là một trong những yếu tố quan trọng nhất, nó góp phần quyết
định hàm lượng C, N trên bề mặt chi tiết và quyết định quá trình tạo pha khi thấm. Sử dụng môi trường thấm hợp lý sẽ điều khiển được hàm lượng C, N theo yêu cầu.[17]
Câu hỏi ôn tập
Câu 1. Thế nào là nhiệt luyện, trình bày các đặc điểm của quá trình nhiệt luyện. Câu 2. Hãy so sánh hai phương pháp nhiệt luyện là ủ và thường hóa.
Câu 3. Thế nào là tôi thép, nêu đặc điểm của phương pháp tôi.
Câu 4. Ram thép là gì, phân loại ram và đặc điểm của các loại ram.
Câu 5. Hóa nhiệt luyện là gì, nêu đặc điểm của phương pháp hóa nhiệt luyện. Câu 6. Trình bày phương pháp hóa bền bề mặt bằng phương pháp cơ học.
Câu 7. Trình bày phương pháp thấm cacbon. Câu 8. Trình bày phương pháp thấm nitơ.
2.1.Thép Cacbon
2.1.1.Thành phần hóa học
CHƯƠNG 2
THÉP VÀ GANG
Trong thực tế, thép cacbon không phải là hợp kim chỉ gồm có Fe và C (trong đó lượng C < 2,14%) mà do điều kiện nấu luyện, có nhiều nguyên tố khác cũng có mặt trong thép, đó là các tạp chất thường có như Mn, Si, P, S, các tạp chất ẩn như H, N, O và các tạp chất ngẫu nhiên như Cr, Ni, Cu, W, Ti, Mo, V, …
Tạp chất thường có là những nguyên tố thường xuyên có mặt trong mọi loại thép, chúng đi vào thép từ quặng sắt, từ nhiên liệu sử dụng khi luyện gang, hoặc từ việc dùng fero để khử oxy khi tinh luyện thép. Trong đó Mn, Si là những tạp chất có lợi, chúng nâng cao cơ tính của thép. Trong các điều kiện thông thường của luyện kim chúng có mặt ở trong thép với lượng chứa Mn ≤ 0,8%; Si ≤ 0,6%. Còn P, S là các tạp chất có hại, chúng làm cho thép bị giòn và khó hàn, cho nên phải tìm cách hạn chế sự có mặt của chúng đến mức có thể được, thép chất lượng càng cao đòi hỏi phải khử càng triệt để hai tạp chất này. Với thép thông thường, lượng chứa của mỗi nguyên tố đó phải nhỏ hơn 0,06%.
Công nghiệp luyện kim sử dụng ngày một nhiều sắt thép vụn (phế liệu) của các ngành kinh tế quốc dân và quốc phòng thải ra (máy móc, xe cộ, vũ khí,…) trong đó nhiều bộ phận làm từ thép hợp kim, nên trong nhiều loại thép cacbon thông thường vẫn có thể có một lượng nhỏ các nguyên tố như: Cr, Ni, Cu (≤ 0,2%), W, Ti, Mo, V (< 0,1%) chúng được gọi là các tạp chất ngẫu nhiên, thường là có lợi vì nâng cao cơ tính cho thép.
Ngoài ra trong thép cacbon thông thường còn hòa tan các khí nitơ, hyđro, oxy với lượng chứa rất nhỏ mà việc xác định chúng rất khó khăn, chúng được gọi là các tạp chất ẩn, với các phương pháp phân tích thông thường khó phát hiện và người ta thường bỏ qua. Nói chung chúng là những tạp chất có hại.
Các nguyên tố kể trên với lượng nhỏ hơn các giới hạn quy định, ảnh hưởng không đáng kể đến tổ chức và tính chất của thép, kể cả nguyên tố có lợi, đều gọi là tạp chất (mà không gọi là nguyên tố hợp kim) bởi vì sự có mặt của chúng với lượng chứa hạn chế, chủ yếu do yêu cầu của quá trình công nghệ đơn giản (cơ bản) nhất mà không có một dụng ý nào.
Tóm lại thành phần hóa học của thép cacbon thông thường, ngoài Fe ra, được giới hạn như sau: C < 2%; Mn ≤ 0,5-0,8%; Si ≤ 0,3-0,6%; P ≤ 0,05-0,06%; S ≤ 0,05- 0,06%.
2.1.2. Ảnh hưởng của Cacbon đến tổ chức và tính chất của thép Cacbon
Cacbon là nguyên tố quan trọng nhất, quyết định chủ yếu đến tổ chức và tính
chất của thép cacbon (và cả thép hợp kim). Từ giản đồ pha Fe-C thấy rằng khi lượng chứa của C trong thép tăng lên, lượng xêmentit cũng tăng lên tương ứng và làm thay đổi tổ chức tế vi của thép. Ở trạng thái cân bằng (trạng thái ủ), tổ chức tế vi của thép cacbon, phụ thuộc vào lượng chứa của C trong nó.
C < 0,8% - thép trước cùng tích, tổ chức là ferit – peclit. C = 0,8% - thép cùng tích, tổ chức là peclit.
C > 0,8% - thép sau cùng tích, tổ chức là peclit – xementit II.
Cơ tính của thép cacbon, phụ thuộc vào lượng chứa của C trong nó, được trình bày trên hình 2.1.
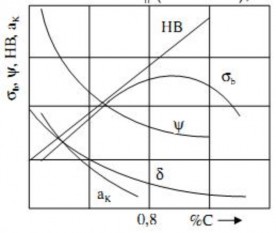
Hình 2.1. Ảnh hưởng của cacbon đến cơ tính của thép cacbon ở trạng thái ủ
Ta thấy khi thành phần cacbon tăng lên, độ bền và độ cứng tăng, còn độ dẻo và
độ dai giảm. Riêng độ bền chỉ tăng và đạt cực đại khi thành phần cacbon vào cỡ 0,8%
– 1,0%, vượt quá giới hạn này độ bền lại giảm đi (và có lẽ đó cũng là lý do trong thực tế ít khi gặp thép có thành phần cacbon vượt quá 1,3%).
Có thể giải thích quy luật trên như sau: khi tăng lượng chứa cacbon, số lượng pha xêmentit (cứng, giòn) tăng lên, lượng peclit tăng lên tương ứng, còn lượng pha ferit (mềm, dẻo) giảm đi. Tổ chức peclit gồm hai pha xêmentit (cứng) và ferit (mềm) xen kẽ nhau, là một tổ hợp pha cho độ bền cao. Như vậy khi tăng lượng chứa cacbon, độ bền và độ cứng tăng, độ dẻo và độ dai giảm xuống. Khi lượng chứa cacbon vượt quá giới hạn 0,8-1,0% trong thép sẽ xuất hiện pha xêmentit II ở dạng lưới, cản trở sự trượt và tạo điều kiện cho việc xuất hiện và phát triển của vết nứt, làm độ bền của thép giảm xuống.
Về mặt định lượng, có thể thấy cứ tăng 0,1%C, làm độ cứng tăng thêm khoảng 20-25 HB, giới hạn bền(σb) tăng thêm khoảng 60-80 MPa, độ giãn dài(δ) giảm đi khoảng 2 – 4%, độ thắt tỷ đối(ψ) giảm đi khoảng 1-5%, độ dai va đập(ak) giảm đi
khoảng 200 Kj/m2,…
Do cacbon ảnh hưởng lớn đến tổ chức và cơ tính của thép như vậy nên thép có thành phần cacbon khác nhau có cơ tính rất khác nhau và do đó được dùng vào các mục đích khác nhau.
- Các thép với thành phần cacbon thấp (≤ 0,25%) nói chung mềm, dẻo, độ bền, độ cứng thấp và hiệu quả hóa bền bằng nhiệt luyện (tôi và ram) cũng không cao, nên được dùng làm các kết cấu xây dựng, chi tiết qua dập nguội (là những sản phẩm cần độ dẻo cao, không cần qua nhiệt luyện). Với các thép này muốn tăng hiệu quả của nhiệt luyện phải qua thấm cacbon lớp bề mặt.
- Các thép với thành phần cacbon trung bình (0,3 - 0,5% C) có cơ tính tổng hợp cao (do có sự kết hợp hài hòa giữa độ bền, độ cứng, độ dẻo và độ dai), do vậy thích hợp cho các chi tiết máy chịu tải trọng tĩnh và va đập cao như trục truyền lực, bánh răng…
- Các thép với thành phần cacbon tương đối cao (0,55 – 0,70%C) có độ cứng cao và giới hạn đàn hồi cao nhất, được dùng làm các chi tiết đàn hồi như lò xo, nhíp,…
- Các thép với thành phần cacbon cao (≥ 0,70%C) có độ cứng và tính chống mài mòn
cao, được dùng làm dụng cụ cắt gọt, dụng cụ đo, khuôn dập nguội,…
Ngoài cơ tính ra, cacbon cũng ảnh hưởng đến một số tính chất hóa lý của thép. Khi tăng lượng cacbon, mật độ (khối lượng riêng γ), độ từ thẩm (µ) và khả năng chống ăn mòn của thép giảm đi, còn điện trở (ρ) và lực khử từ (Hc) tăng lên.
2.1.3. Ảnh hưởng của các nguyên tố khác
a. Mangan(Mn) được cho vào thép khi tinh luyện, dưới dạng fero-Mn, để khử oxy và lưu huỳnh, theo các phản ứng.
FeO + Mn → Fe + MnO (2.1)
FeS + Mn → Fe + MnS (2.2)
MnO và MnS nổi lên, đi vào xỉ và bị đưa ra khỏi lò. Khi hòa tan vào ferit lượng Mn dư thừa sẽ nâng cao độ bền, độ cứng của pha này, do vậy làm tăng cơ tính của thép. Tuy nhiên, do lượng Mn trong thép cacbon ít ( ≤ 0,8% Mn) nên tác dụng này không rò rệt. Tác dụng chủ yếu của Mn trong thép cacbon là để khử oxy và hạn chế sự có mặt của lưu huỳnh như đã nêu ở các phản ứng (2.1) và (2.2)
b. Silic (Si) được cho vào nhiều loại thép để khử oxy một cách triệt để hơn (cùng
với Al), theo phản ứng.
2 FeO + Si → 2 Fe + SiO2 (2.3)
(3 FeO + 2 Al → 3 Fe + Al2O3).
SiO2, Al2O3 nổi lên, đi vào xỉ và bị đưa ra khỏi lò. Lượng Si còn lại hòa tan vào ferit, cũng như Mn, nâng cao độ bền, độ cứng cho pha này. Nhưng trong thép cacbon, lượng Si cũng chỉ trong giới hạn nhỏ hơn 0,6% Si, nên tác dụng này cũng không rò rệt ( còn Al cháy mạnh, hầu như không còn lại trong thép lỏng).
c. Photpho(P)có mặt trong thép từ quặng hay từ than (khi luyện gang). Dù ở dạng hòa tan trong ferit hay ở dạng liên kết Fe3P, nó đều làm cho thép bị giòn, đặc biệt là ở trạng thái nguội, đó là hiện tượng giòn nguội (hay bở nguội), do vậy phải hạn chế sự có mặt của P ở dưới mức cho phép, đối với thép cacbon thông thường
nhỏ hơn 0,06% P. Riêng với thép dễ cắt, để nâng cao khả năng gẫy phoi, lượng P có thể cao tới 0,08-0,15% P.
d. Lưu huỳnh (S) cũng như photpho, lưu huỳnh có mặt trong thép từ quặng và nhất là từ than khi nấu gang. Cùng tinh (Fe + FeS) có nhiệt độ nóng chảy thấp (9880C), nằm ở biên giới hạt. Khi nung nóng thép để gia công áp lực, cùng tinh này bị mềm và chảy ra, làm thép bị đứt ở biên hạt, có cảm tưởng như bị phá hủy giòn, đó là hiện tượng giòn nóng (hay bở nóng), do vậy phải hạn chế sự có mặt của S ở dưới mức cho phép, đối với thép cacbon thông thường nhỏ hơn 0,06%. Riêng với thép dễ cắt, để nâng cao khả năng gẫy phoi, lượng S có thể cao tới 0,08-0,30% S.
2.1.4. Phân loại thép Cacbon
Có nhiều cách phân loại thép khác nhau, nhưng thường gặp các cách sau.
a. Thép chất lượng
Theo chất lượng luyện kim, tức là theo mức độ đồng nhất của thành phần hóa học, tổ chức và tính chất của thép và đặc biệt là mức độ chứa các tạp chất có hại P, S, người ta phân ra các loại thép.
- Thép có chất lượng thường, có thể chứa tới 0,06% S và 0,07% P;
- Thép có chất lượng tốt, chứa không quá 0,04% S và 0,035% P;
- Thép có chất lượng cao, chứa không quá 0,025% mỗi nguyên tố;
- Thép có chất lượng đặc biệt cao, chứa không quá 0,015% S và 0,025% P.
Chất lượng của thép do phương pháp luyện quyết định. Phương pháp Martin (hay phương pháp lò bằng), với tường lò có tính bazơ có thể khử được P, S, luyện được thép với chất lượng tương đối tốt, với tướng lò có tính axit có thể luyện thép có chất lượng cao. Tuy nhiên theo những thông báo mới nhất, phương pháp lò bằng ngày một ít được sử dụng và có thể thay thế bởi các phương pháp khác. Phương pháp L-D (lò thổi oxy từ đỉnh) luyện thép với năng suất cao, chất lượng từ thông thường đến tốt. Phương pháp lò điện (thường là hồ quang) luyện được thép chất lượng cao, có khả năng khử P, S tốt.
Thép cacbon có thể gồm ba loại chất lượng đầu, thép hợp kim có thể gồm ba loại chất lượng sau.
b. Theo phương pháp khử oxy
Theo mức độ khử oxy, phân ra thành thép sôi, thép lặng và nửa lặng.
Thép sôi là thép được khử oxy không triệt để, chỉ dùng fero-Mn. Do vẫn còn FeO, nên nó có thể tác dụng với C trong thép lỏng theo phản ứng.
FeO + C→ Fe + CO (2.4)
Khí CO bay lên làm cho mặt thép lỏng chuyển động giống như nó bị sôi lên, do vậy có tên là thép sôi. Do khí CO vẫn còn tạo thành ngay cả khi rót khuôn nên sẽ tạo thành một số bọt khí trong thỏi thép đúc và gần như không có lòm co tập trung ở phía