Xác định hàm lượng Th4+ bằng phương pháp trắc quang so màu với chỉ thị asenazo(III) 0,005% trong HCl 4 M ở bước sóng 650 nm.
2.3.4. Xác định hàm lượng từng NTĐH
2.3.4.1. Phương pháp sắc kí trao đổi ion kết hợp với chuẩn đ vi lượng
Hàm lượng từng NTĐH trong tổng đất hiếm được xác định bằng phương pháp sắc kí trao đổi ion kết hợp với chuẩn độ vi lượng. Cột sắc kí trao đổi ion có đường kính trong là 0,5 cm, chiều dài cột 100 mm được nhồi bằng nhựa Aminex có kích thước hạt 20 - 50 mesh. Nhựa hấp phụ mẫu phân tích là Wolfatit KPS -
200. Áp suất của hệ sắc kí trao đổi ion được duy trì 1,4 ÷ 1,8 atm. Dung dịch rửa giải được thu vào các đĩa teflon sau đó đem chuẩn độ bằng micropipet 200 L với dung dịch chuẩn DTPA, chất chỉ thị asenazo(III).
Quá trình phân tích được tiến hành như sau:
Rửa sạch cột nhựa bằng dung dịch axit α-hiđroxi isobutyrat 0,36 M ở pH 4,7 sau đó tráng cột bằng nước cất. Dùng phương pháp chuẩn độ để xác định tổng hàm lượng NTĐH trong mẫu để tính toán lượng dung dịch mẫu cần thiết để hấp thụ trên nhựa Wolfatit KPS-200. Nhựa đã hấp thụ được rửa bằng dung dịch NH4Cl 0,1 M rồi sau đó bằng nước cất. Chuyển nhựa Wolfatit KPS-200 lên cột nhựa rồi dùng axit α-hiđroxi isobutyrat ở các nồng độ từ thấp đến cao để rửa giải từng NTĐH ra khỏi cột. Thu các giọt rửa giải trên các đĩa teflon để xác định nồng độ từng NTĐH bằng phép chuẩn độ vi lượng với dung dịch chuẩn DTPA, chất chỉ thị asenazo(III).
4 Phân tích định lượng các nguyên tố bằng ICP - AES
Phương pháp phổ phát xạ nguyên tử cảm ứng plasma (ICP - AES) được dùng để phân tích định lượng các NTĐH riêng rẽ và các kim loại khác trong mẫu từ quá trình chiết bằng dung môi. Hàm lượng các NTĐH và các kim loại khác được đo trên máy Perkin Elmer Elan 9000 của Mỹ tại Viện Công nghệ môi trường, Viện Hàn lâm Khoa học và Công nghệ Việt Nam.
2.3.5. Xác định các thông số của quá trình chiết đất hiếm
2.3.5.1. Hệ số phân bố D của NTĐH
Với giả thiết dung dịch chiết là dung dịch lý tưởng, các pha không trộn lẫn vào nhau và chất tan không phản ứng với dung môi, hệ số phân bố của NTĐH được xác định bằng tỉ số nồng độ NTĐH giữa pha hữu cơ và pha nước tại thời điểm cân bằng chiết được thiết lập. Nồng độ các NTĐH trong pha nước và pha hữu cơ được xác định bằng phương pháp chuẩn độ thể tích sau khi xử lý thích hợp.
2.3.5.2. Xác định dung lượng chiết
Dung lượng chiết của pha hữu cơ được xác định qua đường đẳng nhiệt chiết của hệ. Để xây dựng đường đẳng nhiệt chiết, chúng tôi tiến hành các thí nghiệm sau: Pha các dung dịch ban đầu có thành phần giống nhau về nồng độ axit, nồng độ muối đẩy nhưng nồng độ đất hiếm tăng dần, pha hữu cơ là giống nhau trong mọi thí nghiệm. Sau khi cân bằng chiết được thiết lập, tách riêng biệt hai pha, xác định nồng độ NTĐH trong mỗi pha. Từ kết quả phân tích, lập đồ thị biểu diễn mối quan hệ giữa nồng độ NTĐH ở pha nước và pha hữu cơ. Đoạn đồ thị nằm ngang so với trục hoành tương ứng với đường bão hòa NTĐH trong pha hữu cơ đặc trưng cho dung lượng chiết của pha hữu cơ.
2.3.6. Phương pháp xác định thành phần và tính chất của phức NTĐH(III) với axit lactic
2.3.6.1. Thành phần của phức chất
- Xác định hàm lượng NTĐH: Hàm lượng NTĐH trong phức chất được xác định bằng cách nung nóng một lượng xác định phức rắn ở 8500C trong thời gian 2 giờ. Ở nhiệt độ này, phức chất bị phân hủy chuyển về dạng oxit tương ứng. Hòa tan oxit thu được trong dung dịch HCl, cô dung dịch để đuổi axit dư, hòa tan trong nước cất và định mức đến thể tích cần thiết. Chuẩn độ ion NTĐH thu được bằng dung dịch chuẩn DTPA 1,0.10-3 M, thuốc thử asenazo(III) 0,5%, đệm axetat pH từ 3,8 ÷ 4,0 và 4,0 ÷ 4,2 tùy vào NTĐH.
- Xác định hàm lượng cacbon: Hàm lượng cacbon trong phức chất được xác định trên máy phân tích nguyên tố Analytik.Jena AG (Đức) tại Trung tâm Kỹ thuật Tiêu chuẩn Đo lường chất lượng I, Hà Nội.
- Xác định hàm lượng nước: Hàm lượng nước trong phức chất được xác định bằng thực nghiệm theo phương pháp phân tích nhiệt trên máy phân tích nhiệt Labsys TG/DSC Setaram (Pháp) tại trường Đại học Sư phạm Hà Nội.
2.3.6.2. Đ dẫn điện của dung dịch phức
Nguyên tắc của phương pháp này là có thể xác lập một số trị số trung bình mà độ dẫn điện mol của dung dịch phức chất dao động quanh chúng. Chẳng hạn, nếu lấy những dung dịch chứa 1 milimol phức chất trong 1 lít dung dịch, ở 25oC những phức chất phân li thành hai ion sẽ cho độ dẫn điện mol khoảng 100, nếu phân li thành ba, bốn, năm ion sẽ cho độ dẫn điện mol khoảng 250, 400 và 500. Sở dĩ có được mối quan hệ tương đối đơn giản như trên giữa kiểu phân li ion của phức chất và đại lượng độ dẫn điện mol, vì tất cả các quy luật đặc trưng cho các chất điện ly mạnh thông thường đều được áp dụng cho các phức chất. Trong các dung dịch loãng cỡ mmol.L–1, các muối tan có thể coi như điện li hoàn toàn, cho nên độ dẫn điện mol của chúng là tổng độ dẫn điện của các ion tương ứng [128, 129].
Phương pháp tiến hành đo độ dẫn điện mol của dung dịch trên máy đo độ dẫn điện được tiến hành như sau: Hòa tan một lượng mẫu đã được tính toán trong một thể tích nước rồi định mức thành thể tích dung dịch xác định bằng bình định mức. Cho dung dịch vào cốc thủy tinh rồi nhúng điện cực của máy đo vào, đọc chỉ số độ dẫn điện của 1 mL dung dịch hiển thị trên máy đo.
Độ dẫn điện mol (m) được tính theo công thức:
m = a.V.1000
Trong đó: a là độ dẫn điện của 1 mL dung dịch; V là độ pha loãng, tức là thể tích (lít) trong đó hoà tan 1 mol hợp chất. Độ dẫn điện mol có thứ nguyên là
-1.cm2.mol–1.
2 6 Phương pháp phân tích nhiệt
Phương pháp phân tích nhiệt trong các vật liệu nói chung là phương pháp khảo sát các hành vi nhiệt của vật liệu theo một chương trình nhiệt độ được thiết lập theo thông tin ban đầu về mẫu gồm có các quá trình thu, tỏa nhiệt, quá trình làm thay đổi khối lượng theo thời gian.
Hai kỹ thuật được sử dụng để xác định hành vi nhiệt của vật liệu là phương pháp phân tích nhiệt trong lượng TGA và phương pháp phân tích nhiệt vi sai DTA.
Thông thường trên giản đồ nhiệt, giản đồ biểu thị sự biến đổi tính chất của chất trong hệ toạ độ nhiệt độ - thời gian, có ba đường: đường T chỉ sự biến đổi đơn thuần nhiệt độ của mẫu nghiên cứu theo thời gian, đường DTA (đường phân tích nhiệt vi sai) chỉ sự biến đổi nhiệt độ của mẫu nghiên cứu so với mẫu chuẩn trong lò và đường TGA chỉ hiệu ứng mất khối lượng của mẫu nghiên cứu khi xảy ra những quá trình làm mất khối lượng như thoát khí, thăng hoa, bay hơi… do sự phân huỷ nhiệt của mẫu.
Giản đồ nhiệt của phức chất là rất đa dạng và phức tạp. Khi nghiên cứu các phức chất bằng phương pháp phân tích nhiệt quan trọng nhất là rút ra các kết luận về độ bền nhiệt của chúng và các yếu tố ảnh hưởng đến độ bền nhiệt đó. Độ bền nhiệt của phức chất ở trạng thái rắn được xác định bằng biến thiên năng lượng tự do khi tạo thành nó từ muối đơn giản và các phối tử. Nhưng để đặc trưng cho độ bền nhiệt của các phức chất người ta thường dựa vào nhiệt tạo thành của chúng. Nhiệt tạo thành của phức chất trước hết phụ thuộc vào đặc điểm của liên kết ion trung tâm - phối tử. Vì bản chất của liên kết này được xác định bởi các tính chất của kim loại tạo phức (kích thước, điện tích, các tính chất phân cực) cũng như của phối tử (kích thước, điện tích, momen lưỡng cực), cho nên độ bền nhiệt của phức chất cũng phụ thuộc vào các tính chất đó. Ngoài ra, độ bền nhiệt của phức chất và các phản ứng phân huỷ nhiệt còn được quyết định bởi tính chất của các ion ở cầu ngoại (kích thước, cấu trúc vỏ electron, khuynh hướng của chúng tạo liên kết cộng hoá trị với ion trung tâm).
2.3.6.4. Phương pháp phổ hồng ngoại
Đa số các phổ dao động và phổ quay của các phân tử đều nằm trong vùng hồng ngoại thường có các dải bước sóng từ 4.000 ÷ 667 cm-1; dải 12.500 ÷ 4.000 cm-1 gọi là vùng hồng ngoại gần, còn dải 667 ÷ 50 cm-1 gọi là vùng hồng ngoại xa. Vì vậy, để xác định các nhóm chức đặc trưng và dự đoán một phần cấu tạo của phức chất chúng tôi sử dụng phương pháp phổ hồng ngoại.
Khi chiếu một chùm tia đơn sắc có bước sóng trong vùng từ 400 ÷ 4000 cm-1 qua mẫu phức chất cần phân tích, một phần năng lượng bị hấp thụ làm giảm cường độ của ánh sáng tới. Sự hấp thụ này tuân theo định luật Lambert- Beer [128, 129]:
A = lg I0
I
= .l.C
Trong đó: A là mật độ quang, là hệ số hấp thụ, l là chiều dài cuvet, C là nồng độ chất nghiên cứu, I0/I (%) là độ truyền quang.
Để ghi phổ, ta đặt mẫu nghiên cứu trên đường đi của tia hồng ngoại trong
phổ kế và đo sự phụ thuộc cường độ tương đối của các tia đi qua (và do đó của cả những tia được hấp thụ) vào độ dài sóng (hoặc số sóng). Để có tia đơn sắc người ta sử dụng lăng kính, hoặc cách tử nhiễu xạ có khả năng phân giải cao. Thuỷ tinh và thạch anh hấp thụ mạnh trong toàn bộ vùng phổ hồng ngoại nên không thể dùng chúng để chế tạo cuvet. Với mục đích này người ta thường dùng các halogenua kim loại như natri clorua hoặc xezi bromua.
Để ghi phổ của hợp chất rắn người ta thêm muối halogenua của một kim loại kiềm (thường dùng là kali bromua): lấy khoảng 1 mg chất và 100 ÷ 200 mg KBr, trộn, nghiền kỹ, sấy khô và ép dưới áp suất cao. Khi đó sẽ thu được một viên nhỏ trong suốt, đường kính khoảng 10 mm, dày 1 ÷ 2 mm, thực tế là dung dịch rắn của chất với kali bromua. Trong phổ hồng ngoại của các phức chất, người ta chia ra vùng tần số cao (4.000 ÷ 650 cm-1) và vùng tần số thấp (650 ÷ 50 cm-1, vùng hồng ngoại xa). Trong vùng tần số cao, người ta sử dụng những tần số đặc trưng của các nhóm cho của phối tử, ví dụ >C=O, –O–H... Sự chuyển dịch các tần số so với dạng tự do của phối tử chỉ ra có sự tạo thành liên kết. Khi đó sẽ thu được những thông tin về các nguyên tử liên kết với kim loại. Trong
vùng tần số thấp, khi tạo thành phức chất xuất hiện các dải dao động kim loại - phối tử, cho phép đánh giá hằng số lực của liên kết kim loại - phối tử. Việc xác định các dải này gặp khó khăn, vì trong vùng này còn có các dải dao động biến dạng của các phối tử vòng, các dao động con lắc và các dao động của mạng.
Phổ hấp thụ hồng ngoại của các phức chất cho ta những thông tin về kiểu và mức độ của những biến đổi mà phối tử phải chịu khi nó nằm ở trạng thái liên kết phối trí, về cấu trúc của phân tử, về đối xứng của cầu phối trí, về độ bền của liên kết kim loại - phối tử, về độ đồng nhất của chất... [129].
2.3.7. Phương pháp xử lý và phân tích dữ liệu đánh giá năng suất, chất lượng cây trồng
Xử lý số liệu nhằm hoàn chỉnh, tinh gọn số liệu cho phù hợp với những phân tích sau này. Việc xử lý số liệu có thể bao gồm một hoặc một số bước sau:
+ Sắp xếp và tổ chức và hiệu chỉnh dữ liệu giúp chúng ta thực hiện đúng định dạng yêu cầu của các phần mềm thống kê, tinh gọn (clean) những số liệu không cần thiết, loại trừ những số liệu đột biến, xử lý những số liệu thiếu sót, mất mát trong quá trình thực hiện thí nghiệm, đổi sang những đơn vị đo lường thông dụng hoặc chuyển đổi số liệu sang dạng phân bố chuẩn…
+ Nhập số liệu (data input) để đưa số liệu thô thứ cấp vào trong các phần mềm thống kê theo yêu cầu của mỗi một phần mềm thống kê được sử dụng.
+ Phân tích dữ liệu: Có thể có các kiểu khác nhau như: phân tích định lượng có tác dụng liệt kê hoặc phân tích sự thay đổi, diễn biến của 1 chỉ tiêu nào đó trong nghiên cứu (theo bảng biểu hoặc đồ thị); phân tích thống kê bao gồm: Phân tích biến lượng (ANOVA) nhằm tìm hiểu sự khác biệt giữa các nghiệm thức, các lần lặp lại có ý nghĩa thống kê hay không, trắc nghiệm phân hạng nhằm sắp xếp thứ hạng các nghiệm thức và mức độ khác biệt giữa các nghiệm thức có ý nghĩa thống kê hay không. Tùy theo từng loại thí nghiệm mà chọn lựa kiểu trắc nghiệm phân hạng phù hợp, phân tích tương quan - hồi quy, phân tích so sánh trung bình (T-test/F-test), phân tích, đánh giá tính độc lập (Chi square).
+ Đánh giá kết quả: Việc đánh giá kết quả thí nghiệm không chỉ mang tính chất thống kê mà còn đánh giá các vấn đề liên quan tới năng suất, hiệu quả đầu tư và đặc biệt cần phải chú ý đến vấn đề môi trường, tiện ích cho cộng đồng.
Chương 3
KẾT QUẢ VÀ THẢO LUẬN
3.1. Nghiên cứu làm giàu đất hiếm từ bã thải tuyển quặng đồng Sin Quyền
Bã thải tuyển quặng đồng Sin Quyền là bùn quặng có kích thước hạt 0,074 mm chứa 0,63% tổng oxit đất hiếm được tiến hành lấy mẫu để phân tích và nghiên cứu làm giàu đất hiếm.
3.1.1. Kết quả phân tích thành phần bã thải
Sau tuyển trọng lực, tuyển nổi và tuyển từ thu nhận tinh quặng đồng, vàng, sắt, lưu huỳnh… phần còn lại trong quặng thải chủ yếu là các khoáng vật silicat và alumosilicat nhóm amphibon (actinolit, feropargasit…) mica (biotit, muscovic, kinoshitalit…), plagiocla (albit), thạch anh… Bản thân octit - khoáng vật đất hiếm chủ yếu của mỏ đồng Sin Quyền cũng là một khoáng vật silicat.
Pha Ferropargasit NaCa2Fe4AlSi6Al12O22(OH)2 Pha Kinoshitalit BaMg3Al2Si2O10(OH)2
Pha Albit NaAlSi3O8
Pha Kaolinit Al2Si2O5(OH)4 Pha Quartz SiO2
Hình 3.1. Giản đồ nhiễu xạ tia X của mẫu quặng nghiên cứu làm giàu đất hiếm.
Sự có mặt của các khoáng vật này được thể hiện rất rõ trong giản đồ nhiễu xạ tia X ở hình 3.1. Hàm lượng khoáng vật octit rất ít và không được ghi nhận trên giản đồ nhiễu xạ tia X.
Hàm lượng tổng oxit NTĐH (Ln2O3) và các nguyên tố khác trong mẫu nghiên cứu làm giàu đất hiếm được trình bày trong bảng 3.1.
ảng 1. Thành phần hóa học của mẫu quặng tuyển làm giàu đất hiếm
Chỉ tiêu | Thành phần, % | TT | Chỉ tiêu | Thành phần, % | |
1 | Al2O3 | 12,65 | 8 | CuO | 0,45 |
2 | CaO | 7,75 | 9 | TiO2 | 0,43 |
3 | Fe2O3 | 17,02 | 10 | BaO | 0,06 |
4 | Na2O | 1,52 | 11 | U3O8 | 0,006 |
5 | MgO | 3,51 | 12 | ThO2 | 0,002 |
6 | SiO2 | 48,6 | 13 | Ln2O3 | 0,63 |
7 | MnO2 | 0,22 | 14 | Kích thước hạt | 0,074 mm |
Có thể bạn quan tâm!
-
 Tách Các Ntđh Bằng Phương Pháp Chiết Lỏng - Lỏng
Tách Các Ntđh Bằng Phương Pháp Chiết Lỏng - Lỏng -
 Giới Thiệu Về Cây Chè Và Một Số Loại Rau Phổ Biến Ở Đà Lạt
Giới Thiệu Về Cây Chè Và Một Số Loại Rau Phổ Biến Ở Đà Lạt -
 Phương Pháp Tổng Hợp Phức Chất Đất Hiếm Với Axit Lactic
Phương Pháp Tổng Hợp Phức Chất Đất Hiếm Với Axit Lactic -
 Sơ Đồ Thí Nghiệm Và Kết Quả Làm Giàu Đất Hiếm Từ Mẫu Nghiên Cứu Tuyển Từ Ở Cường Độ Thấp Tách Được Khoáng Vật Có Từ Tính Mạnh Như
Sơ Đồ Thí Nghiệm Và Kết Quả Làm Giàu Đất Hiếm Từ Mẫu Nghiên Cứu Tuyển Từ Ở Cường Độ Thấp Tách Được Khoáng Vật Có Từ Tính Mạnh Như -
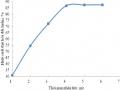
 Ảnh Hưởng Của Thời Gian Phân Hủy Đến Hiệu Suất Thu Hồi Đất Hiếm
Ảnh Hưởng Của Thời Gian Phân Hủy Đến Hiệu Suất Thu Hồi Đất Hiếm -
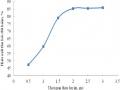
 Sự Phụ Thuộc Hiệu Suất Thu Hồi Đất Hiếm Vào Nồng Độ Dung Dịch Naoh Từ Hình 3.16 Có Thể Nhận Thấy Hiệu Suất Thu Hồi Đất Hiếm Tăng Lên Theo
Sự Phụ Thuộc Hiệu Suất Thu Hồi Đất Hiếm Vào Nồng Độ Dung Dịch Naoh Từ Hình 3.16 Có Thể Nhận Thấy Hiệu Suất Thu Hồi Đất Hiếm Tăng Lên Theo
Xem toàn bộ 149 trang tài liệu này.

Kết quả cho biết hàm lượng tổng hiếm Ln2O3 0,63%. Với hàm lượng tổng hiếm này, có thể giải thích vì sao trên giản đồ nhiễu xạ tia X không có vạch nhiễu xạ đặc trưng cho pha tinh thể chứa đất hiếm.
3.1.2. Kết quả thí nghiệm tuyển làm giàu đất hiếm
Thu nhận tinh quặng đất hiếm hay một sản phẩm giàu đất hiếm từ quặng thải của nhà máy tuyển đồng Sin Quyền là quá trình tuyển tách khoáng vật đất hiếm ra khỏi một khối lượng lớn các khoáng vật silicat và alumosilicat khác mà giữa chúng không chỉ tương đồng về cấu trúc mà còn giống nhau về nhiều tính chất cơ - lý - hóa quan trọng như độ cứng - tỷ trọng, từ tính, tính nổi, mức độ phong hóa, biến đổi trong quá trình tồn tại, khi khai thác, chế biến…
Tỷ trọng của các khoáng vật gần giống nhau, do kích thước hạt nhỏ nên phương pháp tuyển trọng lực sẽ không hiệu quả. Trong quy trình tuyển, chúng tôi kết hợp tuyển từ - tuyển nổi để làm giàu đất hiếm. Sơ đồ tuyển và kết quả đạt được thể hiện ở hình 3.2 và bảng 3.2.