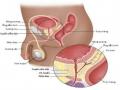
- Siêu âm: Siêu âm qua trực tràng có một tỉ lệ phát hiện UTTTL, siêu âm ổ bụng có giá trị định hướng chẩn đoán, đánh giá di căn trong ổ bụng. Không phải lúc nào cũng có thể thấy được hình ảnh kinh điển của một vùng giảm âm ở ngoại vi của tuyến tiền liệt qua siêu âm. Siêu âm qua trực tràng không thể phát hiện vùng UTTTL với độ tin cậy đầy đủ.
- Cộng hưởng từ tiểu khung có giá trị góp phần vào chẩn đoán, định hướng cho việc sinh thiết TTL. Ngoài ra giúp cho chẩn đoán mức độ xâm lấn của khối u vào tổ chức xung quanh và hạch vùng.
- Chụp cắt lớp vi tính vừa cho phép chẩn đoán mức độ xâm lấn tại chỗ của khối u (T), đồng thời cho phép chẩn đoán di căn, đặc biệt là di căn hạch chậu. Giá trị chẩn đoán của chụp cắt lớp vi tính ngày càng được nâng cao nhờ vào các kỹ thuật chụp mới.
- Xạ hình xương và PET/CT: phát hiện di căn, tái phát, đánh giá hiệu quả phương pháp điều trị.
Sinh thiết TTL
Chỉ định sinh thiết tuyến tiền liệt dựa trên cơ sở nồng độ PSA và/hoặc có nghi ngờ khi thăm khám trực tràng. Cũng cần phải xem xét đến các yếu tố tuổi, bệnh kèm theo và hậu quả điều trị nếu chẩn đoán quá mức. Sinh thiết qua trực tràng là phương pháp được đề nghị trong hầu hết các trường hợp nghi ngờ UTTTL.
Phân độ mô học
Phân độ mô học theo hệ thống thang điểm Gleason đang được sử dụng rộng rãi hiện nay. Điểm Gleason là tổng độ mô học Gleason chiếm ưu thế thứ nhất và thứ nhì. Hệ thống phân loại mô bệnh học mới nhất của UTTTL dựa trên hội nghị đồng thuận của Hiệp hội Quốc tế về Bệnh học Tiết niệu 2014 chia ra 5 độ dựa trên điểm Gleason như sau: Độ 1: ≤ 6 điểm; Độ 2: 3 + 4 = 7
điểm; Độ 3: 4 + 3 = 7 điểm; Độ 4: 8 điểm; Độ 5: 9 – 10 điểm [3].
Có thể bạn quan tâm!
-
 Nhận xét một số đặc điểm lâm sàng, cận lâm sàng của bệnh nhân ung thư tuyến tiền liệt kháng cắt tinh hoàn - 1
Nhận xét một số đặc điểm lâm sàng, cận lâm sàng của bệnh nhân ung thư tuyến tiền liệt kháng cắt tinh hoàn - 1 -
 Nhận xét một số đặc điểm lâm sàng, cận lâm sàng của bệnh nhân ung thư tuyến tiền liệt kháng cắt tinh hoàn - 2
Nhận xét một số đặc điểm lâm sàng, cận lâm sàng của bệnh nhân ung thư tuyến tiền liệt kháng cắt tinh hoàn - 2 -
 Một Số Khái Niệm Sử Dụng Trong Nghiên Cứu
Một Số Khái Niệm Sử Dụng Trong Nghiên Cứu -
 Liên Quan Giữa Triệu Chứng Đau Xương Và Di Căn Xương
Liên Quan Giữa Triệu Chứng Đau Xương Và Di Căn Xương -
 Sự Khác Biệt Thời Gian Từ Thời Điểm Cắt Tinh Hoàn Tới Thời Điểm Kháng Cắt Tinh Hoàn Giữa Các Nhóm Bệnh Nhân
Sự Khác Biệt Thời Gian Từ Thời Điểm Cắt Tinh Hoàn Tới Thời Điểm Kháng Cắt Tinh Hoàn Giữa Các Nhóm Bệnh Nhân
Xem toàn bộ 86 trang tài liệu này.
LIỆT
1.2.5 Chẩn đoán giai đoạn
Đánh giá giai đoạn theo AJCC lần thứ 8 – 2017 (Phụ lục).
1.3 ĐIỀU TRỊ NỘI TIẾT TRONG UNG THƯ TUYẾN TIỀN
Sự phát triển và tiến triển của ung thư tuyến tiền liệt phần lớn phụ
thuộc vào thụ thể Androgen. Trong ung thư tuyến tiền liệt nhạy cảm với hormone, liệu pháp điều trị nội tiết cắt bỏ Androgen kích hoạt tế bào ung thư chết theo chương trình [12].
ADT đóng vai trò cơ bản trong điều trị UTTTL di căn. Tuy nhiên, ADT gây ra sự giảm mạnh nồng độ testosterone huyết thanh, do đó nó có nhiều tác dụng phụ như bốc hỏa, rối loạn chức năng tình dục, mệt mỏi, suy giảm chức năng nhận thức, giảm chất lượng giấc ngủ, thiếu máu,... [42]. Liệu pháp ức chế Androgen bao gồm cắt tinh hoàn ngoại khoa hay cắt tinh hoàn nội khoa bằng các thuốc đồng vận thụ thể GnRH (Gosereline, Triptoreline, Leuprorelin acetate) hoặc đối vận (Degarelix) cho hiệu quả tương đương. Thuốc đối vận thụ thể GnRH được ưu tiên cho các trường hợp di căn xương có chèn ép tủy, các trường hợp cần kiểm soát nhanh các triệu chứng rầm rộ do nó có khả năng làm giảm nhanh Testosterone trong máu.
Mặc dù ADT là lựa chọn hàng đầu cho nam giới bị ung thư tuyến tiền liệt giai đoạn cuối nhưng phần lớn bệnh sẽ tiến triển trong khi điều trị ADT và tình trạng bệnh được gọi là ung thư tuyến tiền liệt kháng cắt tinh hoàn [33].
1.4 UNG THƯ TUYẾN TIỀN LIỆT KHÁNG CẮT TINH HOÀN
1.4.1 Định nghĩa kháng cắt tinh hoàn
Theo Hiệp hội Tiết niệu Châu Âu EAU, Testosterone huyết thanh ở ngưỡng cắt tinh hoàn: dưới 50 ng/dL hoặc dưới 1,7 nmol/L và kèm theo ít nhất một trong hai tiêu chuẩn:
1) Tiến triển sinh học: PSA tăng ở 3 lần thử liên tiếp cách nhau mỗi tuần, ít nhất hai lần tăng trên 50% so với mức thấp nhất (nadir), và một lần PSA tăng trên 2 ng/mL.
2) Tiến triển hình ảnh: Xuất hiện từ hai tổn thương xương mới trên xạ hình trở lên hoặc tiến triển các tổn thương không phải xương theo tiêu chuẩn RECIST 1.1.
1.4.2 Triệu chứng lâm sàng UTTTL kháng cắt tinh hoàn
Tại chỗ: Tiểu máu, rối loạn tiểu tiện, xuất tinh máu,…
Hạch: nổi hạch vùng hoặc hạch ở xa
Di căn xa:
- Di căn xương: Là vị trí di căn phổ biến của ung thư tuyến tiền liệt. Nhiều tổn thương xương di căn gây ra ít hoặc không có triệu chứng [46].
Đau: Đau là biểu hiện phổ biến nhất của di căn xương. Đau do di căn xương khi khởi phát thường âm ỉ sau đó tăng dần [38]. Mặc dù đau do di căn thường được mô tả là đau nhức, tuy nhiên chèn ép rễ thần kinh có thể gây ra đau rát. Đau ở xa đầu gối hoặc khuỷu tay ít có khả năng ác tính hơn đau ở gần hoặc trung tâm vì ung thư thường di căn đến các vùng xương có chức năng tủy hoạt động. Đau khớp có nhiều khả năng khu trú ở các khớp hơn là đau do di căn xương, nhưng chỉ dựa vào tính chất đau thì không đủ tin cậy để phân biệt đau do ung thư di căn hay không [38].
Gãy xương bệnh lý
Chèn ép tủy sống: Di căn đốt sống đặc biệt phổ biến ở nam giới bị ung thư tuyến tiền liệt di căn. Di căn đốt sống có thể gây ra chèn ép tủy sống. Đau là triệu chứng đầu tiên của chèn ép tủy, sau đó có thể có yếu vận động, rối loạn cảm giác,... [38]
- Ít gặp hơn có di căn gan, phổi, não với các triệu chứng: vàng da, gan to, ho, đau ngực, dấu hiệu thần kinh khu trú, đau đầu, nôn,…
Toàn thân: gầy sút cân, thiếu máu,...
1.4.3 Triệu chứng cận lâm sàng UTTTL kháng cắt tinh hoàn
a. Tăng PSA: PSA tăng ở 3 lần thử liên tiếp cách nhau mỗi tuần, ít nhất 2 lần tăng trên 50% so với mức thấp nhất (nadir), và một lần PSA tăng trên 2 ng/mL.
b. Chẩn đoán hình ảnh
X quang:
- Phim X quang thường được sử dụng như bước đầu để đánh giá các vùng có triệu chứng. Do độ nhạy kém, X quang thường không được dùng để sàng lọc di căn xương. Tuy nhiên X quang cột sống có thể được sử dụng để đánh giá cột sống. Các tổn thương xương có thể xuất hiện dưới dạng các vùng giảm đậm độ hoặc mất [46].
- Mặc dù ung thư tuyến tiền liệt di căn xương thường là nguyên bào nuôi nhưng cấu trúc của xương nguyên bào có thể bất thường và thường có sự phá hủy đáng kể của vỏ xương bình thường [38].
Hình 1. 2 Hình ảnh X quang gãy xương bệnh lý ở bệnh nhân nam 89 tuổi ung thư biểu mô tuyến tiền liệt di căn [46]
Chụp cắt lớp vi tính được sử dụng để chẩn đoán di căn xương nếu bệnh nhân có chống chỉ định với MRI, ví dụ trường hợp có máy tạo nhịp tim,… [46]
- Để đánh giá tính toàn vẹn của vỏ xương tại vị trí đã biết có di căn xương, CT được ưu tiên sử dụng. CT có thể phát hiện tổn thương di căn xương trước khi tổn thương đủ rõ ràng để thấy được trên X quang [46].
- Ưu điểm khác của CT so với X quang là nó cho phép phát hiện bệnh mô mềm liên quan và cung cấp hình ảnh dựng ba chiều [46].
Hình 1. 3 Hình ảnh CT của 3 bệnh nhân di căn xương [46]
MRI nhạy hơn CT trong việc phát hiện di căn, cho pháp xác định rõ hơn phạm vi của khối u, đặc biệt hữu ích cho bệnh nhân di căn cột sống để đánh giá mức độ của bệnh lý tủy và ngoài tủy.
Tủy xương bình thường thường chứa một tỉ lệ mỡ cao và có cường độ tín hiệu cao trên xung T1. Tổn thương di căn hiển thị giảm tín hiệu trên xung T1, ngược lại trên xung T2W nó có tín hiệu cao hơn so với tủy bình thường xung quanh [46].
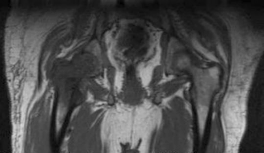
Hình 1. 4 Hình ảnh MRI cho thấy tín hiệu trên xung T1 giảm bất thường ở xương đùi bên phải, cho thấy sự thay thế mỡ tủy bằng khối u [11]
Xạ hình xương: Là phương pháp được sử dụng rộng rãi nhất để phát hiện di căn xương vì nó cung cấp hình ảnh của toàn bộ bộ xương. 99m- Tc-methylene diphosphonate ( 99m Tc-MDP) là chất đánh dấu được sử dụng phổ biến nhất. Nó tích tụ trong các khu vực tăng hoạt động của nguyên bào xương, giúp kiểm tra tổng thể bộ xương và đáng tin cậy để phát hiện di căn trong các bệnh như ung thư tuyến tiền liệt [46].
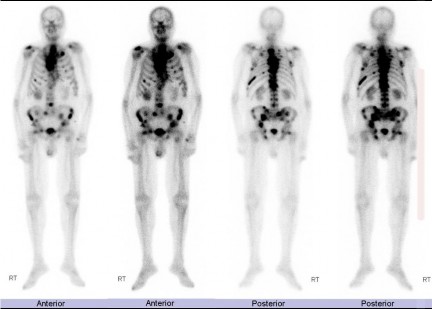
Hình 1. 5 Xạ hình hạt nhân phóng xạ technetium Tc-99m methylene diphosphonate cho thấy nhiều ổ hấp thu bất thường trong toàn bộ khung xương, ví dụ như xương bả vai 2 bên, nhiều xương sườn 2 bên, cột sống thắt lưng, xương chậu 2 bên và cổ xương đùi thứ phát [18]
PET/CT: Ghi hình khối u bằng PET có độ nhạy và độ đặc hiệu cao hơn nhiều so với các phương pháp chẩn đoán hình ảnh khác, đặc biệt là khả năng phát hiện các khối u ở giai đoạn rất sớm khi mà các phương pháp chẩn đoán khác chưa phát hiện thấy. Nguyên lý ghi hình khối u bằng PET dựa trên tính chuyển hóa nhanh hơn nhiều của khối u ác tính so với tổ chức lành. Lợi ích của PET/CT so với xạ hình xương là khả năng sàng lọc di căn tại các
vị trí khác ngoài xương. Do đó, PET/CT được dùng để đánh giá di căn xa ở tất cả các vị trí, bao gồm cả xương.
1.4.4 Điều trị UTTTL kháng cắt tinh hoàn
Lựa chọn phương pháp điều trị phụ thuộc vào nhiều yếu tố, bao gồm các phương pháp điều trị toàn thân trước đó, vị trí, triệu chứng, thời gian tăng gấp đôi PSA [33].
Liệu pháp ức chế Androgen vẫn cần tiếp tục để duy trì Testosterone ở mức cắt tinh hoàn. Bên cạnh đó, Zoledronic acid hoặc Denosumab được sử dụng nếu bệnh nhân di căn, với trường hợp bệnh nhân đau xương có thể xạ trị ngoài để giảm đau [3].
Đối với bệnh nhân chưa có di căn tạng:
- Ức chế sinh tổng hợp Androgen: Abirateron acetate. Các nội tiết tố androgen được tạo ra trong tinh hoàn, tuyến thượng thận và các tế bào khối u có thể gây ra tín hiệu ―autocrine/paracrine‖ đẫn dến sự phát triển của khối u. Abiratone là 1 phân tử nhỏ được sử dụng qua đường uống có tác dụng ức chế không thể đảo ngược các sản phẩm của gen CYP17[33].
- Enzalutamide: Là các tác nhân dùng đường uống có tác dụng tại nhiều vị trí trong con đường truyền tín hiệu của thụ thể Androgen, bao gồm ngăn chặn sự liên kết của Androgen với thụ thể Androgen,… [33]
- Hoá trị: Docetaxel + Prednisone. Phương pháp này được sử dụng với những bệnh nhân có triệu chứng tiến triển tương đối nhanh mà các phương pháp sử dụng Abirateron acetate hay Enzalutamide không phải là lựa chọn thích hợp. Docetaxel (75 mg/m2) chu kì 21 ngày kết hợp với Prednisone dùng hàng ngày (5 mg chia 2 lần/ngày). Docetaxel gây suy tuỷ đáng kể, chống chỉ định bao gồm rối loạn chức năng gan hoặc chức năng tuỷ xương bị tổn thương [33].
- Radium – 223 được sử dụng cho bệnh nhân di căn xương có triệu chứng.
- Nội tiết bậc 2 khác nếu chưa có di căn.
Đối với bệnh nhân đã có di căn tạng:
- Tương tự bệnh nhân chưa có di căn tạng, ở bệnh nhân đã có di căn tạng cũng có các phương pháp sử dụng Docetaxel + Prednisone, Enzalutamide, Abirateron acetate, hoá trị khác và nội tiết bậc 2 khác ( điều trị nội tiết bậc 2 đối với bệnh nhân có di căn triệu chứng nhẹ hoặc trung bình).
- Ngoài ra còn có nhóm thuốc ức chế PARP: Olaparib (bệnh nhân có đột biến gen sửa chữa tái tổ hợp tương đồng dạng gây bệnh hoặc nghi ngờ gây bệnh tiến triển sau điều trị abiratone acetate hoặc enzalutamide) [3].
1.5. TÌNH HÌNH NGHIÊN CỨU VỀ UTTTL KHÁNG CẮT TINH HOÀN
1.5.1. Một số nghiên cứu về UTTTL kháng cắt tinh hoàn trên thế
giới
Trên thế giới đã có rất nhiều nghiên cứu về UTTTL kháng cắt tinh hoàn,
chủ yếu tập trung vào cơ chế, yếu tố tiên lượng và điều trị. Theo nghiên cứu
―Ung thư tuyến tiền liệt kháng cắt tinh hoàn: Tình trạng hiện tại và khả năng‖ của Joan Carles và cộng sự, hóa trị với Docetaxel là một bước ngoặt trong CRPC, vì lần đầu tiên nó làm tăng thời gian sống sót so với Mitoxantrone và prednisone. Điều trị phối hợp Docetaxel và Prednisone là phương pháp điều trị đầu tiên được lựa chọn [14].
Nghiên cứu ―Tỷ lệ tử vong ở nam giới bị ung thư tuyến tiền liệt kháng cắt tinh hoàn — Một cuộc theo dõi dài hạn của một nhóm thuần tập trên thế giới‖ của Khoshkar Y và cộng sự [26] năm 2022 cho thấy các biến dự đoán như thời gian PSA tăng gấp đôi và PSA tại thời điểm kháng cắt tinh hoàn có thể có giá trị để phân loại bệnh nhân thuộc nhóm nguy cơ thấp hay cao, từ đó lựa chọn phương pháp điều trị phù hợp.
1.5.2. Một số nghiên cứu về UTTTL kháng cắt tinh hoàn tại Việt
Nam
Nghiên cứu ―Đánh giá kết quả điều trị ung thư tuyến tiền liệt kháng cắt
tinh hoàn bằng phác đồ Docetaxel - Prenisolone tại Bệnh viện K‖ [6] của tác