oxy thì càng làm tăng tính tan trong nước của chất hoạt động bề mặt này. hi tăng nhiệt độ, ethoxylat alcohol trở nên kém tan trong nước hơn do sự hydrat hóa nhóm ethoxylat giảm và sự tăng kích thước của mixen. Tính HĐBM của chúng không bị ảnh hưởng bởi các ion có trong nước cứng. Tuy nhiên độ tan của chúng tăng lên khi có mặt HCl và ion Ca2+. Nồng độ chất điện ly cao, đặc biệt ion Na+ lại làm giảm độ tan do hiệu ứng đẩy của muối. Ethoxylat alcohol có thể tạo ra hiệu ứng hợp trội khi
phối trộn chung với chất hoạt động bề mặt anion.
1.2.1.2. Chất hoạt động bề mặt fluor hóa
Chất HĐBM fluor hóa là thành phần quan trọng trong nghiên cứu chế tạo chất tạo bọt chữa cháy, nó còn được gọi là “chất siêu hoạt động bề mặt” do khả năng khả năng làm giảm sức căng bề mặt của nước xuống thấp hơn so với sử dụng chất HĐBM hydrocarbon [44-46]. Cũng giống như chất HĐBM hydrocarbon, chất HĐBM fluor hóa được phân ra thành các loại: anion, cation, nonion và lưỡng tính dựa trên cấu trúc hóa học của nhóm ưa nước. Ngoài ra, chất HĐBM fluor hóa cũng có những khác biệt so với chất HĐBM hydrocarbon. Mặc dù nhóm đầu phân cực của chất fluor hóa và hydrocarbon có thể giống nhau, nhưng phần đuôi không phân cực của chất fluor hóa có cả tính chất kỵ nước và kỵ dầu, trong khi chất HĐBM hydrocarbon chỉ có tính kỵ nước [47]. Do vậy, chất fluor hóa thể hiện cả đặc tính kỵ nước và kỵ dầu trong các ứng dụng chữa cháy giúp nâng cao tính hiệu quả của chúng. Mặt khác, các chất HĐBM fluor hóa còn giúp tăng độ bền bọt, chống bị hòa tan trong nước và chất lỏng không phân cực như nhiên liệu hydrocarbon (hình 1.6).
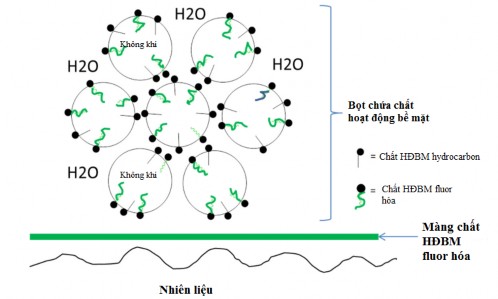
Hình 1.6: Bọt chứa chất HĐBM fluor hóa trên bề mặt nhiên liệu [48]
Chất HĐBM fluor hóa còn có hoạt tính bề mặt lớn hơn so với chất HĐBM hydrocarbon tương tự do fluor có độ phân cực thấp hơn hydro dẫn tới tương tác giữa các chuỗi fluor hóa và lực hút liên phân tử thấp. Vì vậy, các chất HĐBM fluor hóa có xu hướng tập hợp trên bề mặt phân cách không khí và nước lớn giúp giảm sức căng bề mặt tốt hơn. Việc kết hợp các thành phần với chất HĐBM fluor hóa trong AFFF sẽ làm tăng hệ số lan truyền trên bề mặt nhiên liệu hydrocarbon, do đó chữa cháy hiệu quả hơn [49-52]. Một số chất hoạt động fluor hóa thường được sử dụng để chế tạo chất tạo bọt chữa cháy được trình bày trong bảng 1.4.
Bảng 1.4: Chất hoạt động fluor hóa sử dụng trong chế tạo chất tạo bọt chữa cháy [34]
Cấu trúc | |
Chất HĐBM fluor hóa lưỡng tính | O O - S + O R NH N O O O O R S Na(+) S NH - O OH + S N Cl(-) R O R S NH2 n H2N O R S n m - H2N O O O Na(+) O O - S + O R NH N |
Chất HĐBM fluor hóa anion | |
Chất HĐBM fluor hóa cation | |
Chất HĐBM fluor hóa | |
Chất HĐBM fluor hóa | |
Chất HĐBM fluor hóa N - oxide |
Có thể bạn quan tâm!
-
 Nghiên cứu xây dựng hệ chất hoạt động bề mặt bền nhiệt ứng dụng trong công nghệ sản xuất chất tạo bọt chữa cháy - 1
Nghiên cứu xây dựng hệ chất hoạt động bề mặt bền nhiệt ứng dụng trong công nghệ sản xuất chất tạo bọt chữa cháy - 1 -
 Nghiên cứu xây dựng hệ chất hoạt động bề mặt bền nhiệt ứng dụng trong công nghệ sản xuất chất tạo bọt chữa cháy - 2
Nghiên cứu xây dựng hệ chất hoạt động bề mặt bền nhiệt ứng dụng trong công nghệ sản xuất chất tạo bọt chữa cháy - 2 -
![Bọt Chữa Cháy Tạo Màng Nước Chữa Cháy Bể Xăng Dầu Và Trạm Xăng Dầu [9]](data:image/svg+xml,%3Csvg%20xmlns=%22http://www.w3.org/2000/svg%22%20viewBox=%220%200%2075%2075%22%3E%3C/svg%3E) Bọt Chữa Cháy Tạo Màng Nước Chữa Cháy Bể Xăng Dầu Và Trạm Xăng Dầu [9]
Bọt Chữa Cháy Tạo Màng Nước Chữa Cháy Bể Xăng Dầu Và Trạm Xăng Dầu [9] -
![Mô Tả Quá Trình Hình Thành Bọt Chữa Cháy [92] Các Bước Phối Trộn Chất Tạo Bọt Chữa Cháy:](data:image/svg+xml,%3Csvg%20xmlns=%22http://www.w3.org/2000/svg%22%20viewBox=%220%200%2075%2075%22%3E%3C/svg%3E) Mô Tả Quá Trình Hình Thành Bọt Chữa Cháy [92] Các Bước Phối Trộn Chất Tạo Bọt Chữa Cháy:
Mô Tả Quá Trình Hình Thành Bọt Chữa Cháy [92] Các Bước Phối Trộn Chất Tạo Bọt Chữa Cháy: -
 Phương Pháp Xác Định Tính Chất Hóa Lý Của Chất Tạo Bọt Chữa Cháy
Phương Pháp Xác Định Tính Chất Hóa Lý Của Chất Tạo Bọt Chữa Cháy -
 Nghiên Cứu Lựa Chọn Chất Hoạt Động Bề Mặt Fluor Hóa Và Hydrocarbon
Nghiên Cứu Lựa Chọn Chất Hoạt Động Bề Mặt Fluor Hóa Và Hydrocarbon
Xem toàn bộ 136 trang tài liệu này.
Mặc dù chất HĐBM fluor hóa có nhiều tính chất bề mặt hữu ích và đóng vai trò quan trọng trong nhiều ứng dụng, tuy nhiên chúng không thân thiện với môi trường. Nghiên cứu [53-55] đã chứng minh mối nguy hiểm của các chất HĐBM fluor hóa với môi trường do chứa perfluorooctan carboxylat (-C7F15COO-) và perfluorooctan sulfonat (-C8F17SO3-) [56, 57]. Những chất này cực kỳ bền trong môi trường, không bị thủy phân, không phân hủy sinh học. Từ năm 2006, PFOS bị cấm sử dụng ở các nước Liên minh Châu Âu [58] do độc tính và khả năng tích tụ sinh học của nó và từ năm 2009 PFOS được Quốc tế phân loại vào nhóm chất gây ô nhiễm hữu cơ bền vững (POP) [59]. Sau đó PFOS đã được thay thế bằng polyfluorinated (PFC), tuy nhiên hợp chất này cũng không được chấp nhận vì nó khó phân hủy và ảnh hưởng đến môi trường. Để cải thiện khả năng phân hủy sinh học và giảm độc tính của các chất HĐBM fluor hóa, trong luận án sử dụng chất fluor hóa có số nguyên tử C trong gốc perfluorinat từ C8-C10 xuống còn C4-C6 được chứng minh là an toàn với môi trường, phối hợp với các chất HĐBM hydrocarbon giảm bớt hàm lượng chất fluor hóa trong công thức bọt.
1.2.2. Chất trợ HĐBM và các polyme bền rượu
1.2.2.1. Chất trợ HĐBM
Đây là các chất hầu như không có khả năng HĐBM khi đứng riêng lẻ, nhưng lại có khả năng tăng cường hoạt động của các chất HĐBM khác có trong dung dịch và giảm sức căng bề mặt liên diện xuống giá trị thấp hơn. Chúng thường là các polyme, polyme biến tính và các dung môi hữu cơ tan trong nước. Việc kết hợp chất HĐBM với chất trợ HĐBM không những giúp tăng cường khả năng độ bền của bong bóng bọt (thông qua thời gian bán hủy) mà còn được sử dụng để chế tạo các chất tạo bọt đậm đặc hơn.
1.2.2.2. Polyme bền rượu
Thường là các polyme tan trong nước, các polyme này có thể kết tủa khi tiếp xúc với nhiên liệu tan trong nước tạo ra lớp màng bảo vệ giữa nhiên liệu và bọt. Polyme có trong thành phần chất tạo bọt chữa cháy giúp ngăn chặn bọt vỡ ra trên nhiên liệu phân cực và kéo dài thời gian tiết nước. Các polyme thường dùng bao gồm: Diutan gum, Xanthan gum, Guar gum;
- Xanthan gum
Là một polysaccharid, ở dạng bột màu trắng hoặc kem, có khả năng tan trong
nước, không hòa tan trong các dung môi hữu cơ. Khối lượng phân tử ≈ 2.000.000. Độ nhớt của dung dịch 1% là 1500Cp ở 25°C.
- Diutan gum
Diutan gum là một polysaccharid ngoại bào, có cấu trúc mạch thẳng với sự lặp lại của các tetrasaccharid, có khối lượng phân tử ≈ 500.000. Diutan gum thương mại dạng bột màu trắng, tan trong nước tạo gel, không tan trong ethanol.
Các polyme polysaccharide được sử dụng để làm tăng độ nhớt và thời gian tiết nước [60, 61].
1.2.3. Các chất phụ gia
Các chất phụ gia trong thành phần chất tạo bọt chữa cháy gồm chất chống đông, chống lắng; chất tăng độ nhớt, độ linh động; chất tạo màng tăng cường, tăng độ bền bọt; chống oxy hóa, chống ăn mòn. Các thành phần này phải đảm bảo không làm ảnh hưởng đến tính chất HĐBM và độ bền nhiệt của sản phẩm:
+ pH của chất tạo bọt thường được điều chỉnh ở mức trung tính hoặc hơi kiềm giúp ngăn chặn sự ăn mòn và phân hủy (thủy phân) của các thành phần hoạt động khác nhau. Dung dịch NaOH 50% và CH3COOH thường được sử dụng để thay đổi pH trong bọt chữa cháy;
+ Muối (NaCl) có thể được thêm vào để bảo vệ chất HĐBM anion tại bề mặt giao diện không khí/nước và làm các nhóm acid khác yếu đi chẳng hạn như polysaccharid và chất HĐBM;
+ Ethylendiamintetraacetic acid hoặc citric acid có thể có trong công thức bọt với vai trò là chất đệm pH
+ Các chất ức chế ăn mòn được thêm vào để ngăn chặn sự ăn mòn của các thùng chứa và thiết bị mà bọt có thể tiếp xúc.
+ Urea được thêm vào giúp làm giảm độ nhớt của các polysaccharid có trong bọt chữa cháy AR-AFFF, ngoài ra nó cũng có vai trò như một chất chống đông.
+ Natri benzoat được sử dụng để ngăn cản sự tấn công của vi sinh vật trong các chuỗi polysaccharid và các thành phần khác giúp tăng thời gian sử dụng của bọt chữa cháy.
1.2.4. Ứng dụng một số hợp chất chứa silic trong bọt chữa cháy
Ngày nay, vật liệu có kích thước nano đang thu hút sự quan tâm của nhiều nhà khoa học do những tính chất vật lý và hóa học đặc biệt cũng như những ứng
dụng tiềm năng trong nhiều lĩnh vực công nghệ (hóa học, luyện kim, gốm sứ, y dược, lý sinh học, y sinh học, ...). Trong đó, có nhiều công trình nghiên cứu về hạt nano chứa silic ứng dụng trong lĩnh vực phòng cháy chữa cháy [33, 48, 57, 59].
Khả năng hấp phụ các hạt nano trên giao diện lỏng-lỏng (dầu/nước) và khí- lỏng (không khí/nước) đã được nghiên cứu. Trong nhiều trường hợp, các hạt nano có vai trò giống như các chất HĐBM khi được hấp phụ trên các giao diện này. Tính ưa dầu hoặc ưa nước của các hạt nano có thể được xác định thông qua tính dính ướt của chúng qua bằng cách đo góc tiếp xúc với giao diện lỏng-lỏng. Sự khác biệt quan trọng giữa chất HĐBM và các hạt nano là các hạt nano có khả năng hấp phụ mạnh hơn trên bề mặt giao diện.
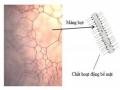
Gần đây, nhiều công trình nghiên cứu và ứng dụng hạt nano SiO2 (Polysilicon Nanoparticle - PN) trong bọt chữa cháy được tiến hành với nhiều kết quả khả quan. Trong đó, nghiên cứu lớp vật liệu sol-gel, với tính chất chữa cháy độc đáo ngày càng được quan tâm. Vật liệu hỗn hợp sol-gel từ lâu được biết đến là chất hấp phụ vật liệu hữu cơ như polyme, thuốc nhuộm, phân tử sinh học…[62]. Mesoporous silica được sử dụng trong các trường hợp này do khả năng giữ nguyên cấu trúc sau khi xử lý với nhiệt [63-66] và thường ở dạng xốp (có vô số các khoang rỗng li ti bên trong). Chúng mang lại nhiều lợi ích hơn so với các polyme tổ hợp do các hạt nano silica có thể dễ dàng tách khỏi nhau, tương tác với các chất HĐBM, không độc hại và có thể phân hủy sinh học. Quá trình hình thành bọt nano silica trong vòi phun được trình bày như hình 1.7.
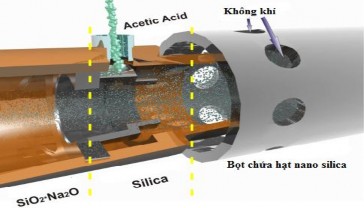
Hình 1.7. Quá trình hình thành bọt silica [95]
Các chất HĐBM fluor hóa và dẫn xuất siloxan đều là những chất có khả năng giảm sức căng bề mặt của dung dịch xuống giá trị thấp. Tuy nhiên, khi chất HĐBM fluor hóa mạch dài bị cấm sử dụng do ảnh hưởng xấu đến môi trường nên
siloxan được xác định là hợp chất tiềm năng sử dụng trong công thức AFFF và được lựa chọn làm đối tượng nghiên cứu của luận án. Kết quả nghiên cứu [47] trình bày trong bảng 1.5 cho thấy, chất HĐBM siloxan làm giảm sức căng bề mặt của nước xuống giá trị thấp (20 mN/m), chỉ đứng sau chất fluor hóa (15 mN/m) và tốt hơn các chất HĐBM hydrocarbon (28 mN/m). Hệ số lan truyền của siloxan đạt giá trị dương (5 mN/m), do đó, nó có khả năng nổi lên và lan truyền trên bề mặt nhiên liệu lỏng. Vì vậy, siloxan có thể phù hợp cho công thức bọt chữa cháy.
Bảng 1.5: Sức căng bề mặt nhỏ nhất và hệ số lan truyền của các dung dịch ở nhiệt độ phòng [47]
Sức căng bề mặt nhỏ nhất | Hệ số lan truyền trên Cyclohexan | Phù hợp cho AFFF | |
Chất HĐBM fluor hóa | 15 mN/m | + 10 mN/m | Có |
Siloxan | 20 mN/m | + 5 mN/m | Có thể |
Alkyl | 28 mN/m | - 3 mN/m | Không |
Nước tinh khiết | 73 mN/m | - 48 mN/m | Không |
Tác động sinh học của siloxan thấp hơn so với chất HĐBM fluor hóa bởi phần kỵ nước của siloxan không chứa các liên kết C-F bền vững và không phân hủy sinh học. Trong chất HĐBM siloxan nhóm siloxan cùng tên tạo thành phần kỵ nước. Nhóm này chủ yếu gồm các liên kết silicon-methyl và silicon-oxy. Các liên kết này dễ bị phân hủy trong tự nhiên như liên kết silicon-oxy có thể bị thủy phân bởi nước và các vi sinh vật tạo thành các sản phẩm hữu cơ trong tự nhiên [47].
Nhiều cơ chế được đề xuất để giải thích sự ổn định của bọt chứa hỗn hợp các chất HĐBM và hạt nano silica [67]; các cơ chế đó bao gồm năng lượng gắn kết hạt [68], áp suất mao quản cực đại của kết tụ [69, 70], sự sắp xếp hạt trên lớp màng và vùng khoảng cách giữa các bong bóng bọt [71], và tương tác phân tử [72]. Binks và cộng sự đề xuất rằng các hạt nano silica được hấp phụ vào bề mặt phân cách không khí/chất lỏng. Quá trình này là không thể đảo ngược [73, 74] do năng lượng (E) cần thiết để đẩy các hạt nano silica khỏi bề mặt phân cách không khí/lỏng rất cao. Năng lượng E phụ thuộc vào góc tiếp xúc được hình thành khi hạt nano silica hấp phụ trên bề mặt phân cách không khí/chất lỏng. Năng lượng gắn/tách rời có thể được tính như sau:
E = πR2 σaw (1 ± cos θ)2
Trong đó R là bán kính hạt, θ là góc tiếp xúc, và σaw là sức căng bề mặt không khí/chất lỏng. Tuy nhiên, Vatanparast và các cộng sự đã chứng minh được các nano silica ưa nước không có xu hướng hấp phụ tại bề mặt phân cách không khí/chất lỏng [109]. Việc bổ sung các chất HĐBM, đặc biệt là chất fluor hóa giúp làm giảm sức căng bề mặt của hỗn hợp. Phương trình trên cho thấy việc thêm chất HĐBM dẫn đến kết quả E thấp. Do đó, sự thay đổi độ ổn định của bọt do thêm các hạt nano silica không thể được giải thích bằng cơ chế năng lượng gắn hạt.
Một cơ chế khác cũng được đề xuất để giải thích sự ổn định màng của bọt chứa các hạt nano silica là tương tác phân tử. Carn và cộng sự chỉ ra rằng sự hình thành các hạt mixen do tương tác giữa các hạt nano silica và chất HĐBM cation làm tăng độ nhớt màng lỏng. Do đó, làm giảm tốc độ thoát nước và tăng cường độ ổn định của bọt [72]. Nguyen và Schulze [76]; Kim và cộng sự [77] cho rằng các phân tử chất HĐBM có thể được hấp phụ lên bề mặt của các nano silica để tạo thành một lớp đơn phân tử, giúp tăng cường tính kỵ nước của các hạt nano silica và làm cho chúng hoạt động tốt hơn trên bề mặt. Do đó, các hạt nano này có thể bị hấp phụ mạnh tại bề mặt phân cách không khí/chất lỏng và làm ổn định các bong bóng. Tuy nhiên, các kết quả này chỉ chứng minh được sự tương tác giữa các hạt nano silica và chất HĐBM làm tăng tốc độ thoát nước của bọt và đóng cặn khi ở nồng độ thấp. Do đó, việc tăng độ ổn định của bọt không thể do tương tác phân tử.
Một số nghiên cứu cho thấy hạt nano silica có xu hướng hình thành các cấu trúc phân lớp trong màng nước mỏng, dẫn đến sự chậm vỡ của các bong bóng bọt [78-80]. Singh và cộng sự thông qua kính hiển vi phát hiện ra rằng các hạt nano silica tồn tại ở vùng không gian khoảng cách giữa các bong bóng bọt và làm chậm quá trình thoát nước bọt [74]. Các cơ chế giải thích tính ổn định và bền bọt của bọt chữa cháy có thành phần nano silica cũng được đề xuất trong một số nghiên cứu tương tự [72, 79].
1.3. Vai trò và nguyên lý dập cháy của bọt chữa cháy
1.3.1. Nguyên nhân hình thành đám cháy chất lỏng
Quá trình cháy là những quá trình lý – hóa học phức tạp của phản ứng giữa chất cháy và chất oxy hóa tạo thành sản phẩm cháy, tỏa nhiệt và phát sáng. Để đám cháy có thể xảy ra, phải hội tụ đủ ba yếu tố: chất cháy, oxy và nguồn nhiệt. Trong
đó chất cháy dạng lỏng ở đây là nhiên liệu: xăng dầu, dung môi hữu cơ... [81]. Khi hội tụ đủ ba yếu tố cần thiết nói trên, sự cháy sẽ xảy ra với điều kiện:
+ Thứ nhất: nồng độ của chất cháy và chất oxy hóa ở trong phạm vi nồng độ bốc cháy.
+ Thứ hai: nguồn nhiệt phải đáp ứng yêu cầu nung nóng được hỗn hợp chất cháy và chất oxy hóa – hỗn hợp cháy tới một nhiệt độ nhất định là nhiệt độ tự bốc cháy của hỗn hợp. Sự cháy được mô tả bằng mô hình 1.8.
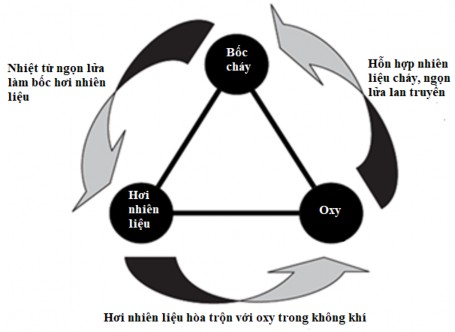
Hình 1.8: Mô hình cháy kiểu tam giác [34]
Từ mô hình nhận thấy, khi nhiên liệu cháy được cung cấp một nguồn nhiệt nhất định thì nhiên liệu sẽ được nung nóng và bốc hơi, hơi nhiên liệu kết hợp với O2 có trong không khí với vai trò là chất oxy hóa sẽ tạo thành hỗn hợp chất cháy, đám cháy sẽ xảy ra khi hỗn hợp được cấp nhiệt đến nhiệt độ cháy. Quá trình cháy là phản ứng oxy hóa giữa chất cháy và O2 sẽ tạo ra nhiệt lượng lớn tiếp tục cấp nhiệt cho quá trình bốc cháy của nhiên liệu cho đến khi hết nhiên liệu.
1.3.2. Nguyên lý dập cháy của bọt chữa cháy
Không giống như các chất chữa cháy thông thường, chất tạo bọt chữa cháy đóng vai trò làm mát bề mặt nhiên liệu cháy, hạn chế nguồn cấp oxy thông qua sự bốc hơi của nước do nhiệt độ cao của đám cháy [82-84]. Chất tạo bọt chữa cháy được sử dụng cho các đám cháy chất rắn hoặc các vật liệu lỏng dễ cháy giúp dập tắt và ngăn chặn sự cháy lại. Một tính năng quan trọng của hầu hết các bọt chữa cháy là khả năng lan truyền, bao phủ một cách tự nhiên trên bề mặt của vật liệu cháy, tạo


![Bọt Chữa Cháy Tạo Màng Nước Chữa Cháy Bể Xăng Dầu Và Trạm Xăng Dầu [9]](https://tailieuthamkhao.com/uploads/2022/07/13/nghien-cuu-xay-dung-he-chat-hoat-dong-be-mat-ben-nhiet-ung-dung-trong-3-1-120x90.jpg)
![Mô Tả Quá Trình Hình Thành Bọt Chữa Cháy [92] Các Bước Phối Trộn Chất Tạo Bọt Chữa Cháy:](https://tailieuthamkhao.com/uploads/2022/07/13/nghien-cuu-xay-dung-he-chat-hoat-dong-be-mat-ben-nhiet-ung-dung-trong-5-1-120x90.jpg)