0,57 ± 0,06 | 1,35 ± 0,04 | 2,50 ± 0,11 |
Có thể bạn quan tâm!
-
 Liên Kết Hydro Nội Phân Tử Của Các Dẫn Xuất 2-(5(6)-Substituted-1H- Benzimidazol-2-Yl)-Phenol
Liên Kết Hydro Nội Phân Tử Của Các Dẫn Xuất 2-(5(6)-Substituted-1H- Benzimidazol-2-Yl)-Phenol -
![[(4-Methoxy-Phenyl)-Pyrrolidin-1-Yl-Methyl]-1H-Indole-2- Carboxylic Acid (Cpm – Chất Mới)](data:image/svg+xml,%3Csvg%20xmlns=%22http://www.w3.org/2000/svg%22%20viewBox=%220%200%2075%2075%22%3E%3C/svg%3E) [(4-Methoxy-Phenyl)-Pyrrolidin-1-Yl-Methyl]-1H-Indole-2- Carboxylic Acid (Cpm – Chất Mới)
[(4-Methoxy-Phenyl)-Pyrrolidin-1-Yl-Methyl]-1H-Indole-2- Carboxylic Acid (Cpm – Chất Mới) -
![Bromo-3-[(4-Methoxy-Phenyl)-Pyrrolidin-1-Yl-Methyl]-1H-Indole (Bpm)](data:image/svg+xml,%3Csvg%20xmlns=%22http://www.w3.org/2000/svg%22%20viewBox=%220%200%2075%2075%22%3E%3C/svg%3E) Bromo-3-[(4-Methoxy-Phenyl)-Pyrrolidin-1-Yl-Methyl]-1H-Indole (Bpm)
Bromo-3-[(4-Methoxy-Phenyl)-Pyrrolidin-1-Yl-Methyl]-1H-Indole (Bpm) -
 Các Mô Hình Gắn Kết Phân Tử Docking Của Các Dẫn Xuất Benzimidazole Và Indole
Các Mô Hình Gắn Kết Phân Tử Docking Của Các Dẫn Xuất Benzimidazole Và Indole -
 Nghiên cứu tổng hợp và đánh giá hoạt tính gây độc tế bào các dẫn xuất của benzimidazole và indole - 21
Nghiên cứu tổng hợp và đánh giá hoạt tính gây độc tế bào các dẫn xuất của benzimidazole và indole - 21 -
 Nghiên cứu tổng hợp và đánh giá hoạt tính gây độc tế bào các dẫn xuất của benzimidazole và indole - 22
Nghiên cứu tổng hợp và đánh giá hoạt tính gây độc tế bào các dẫn xuất của benzimidazole và indole - 22
Xem toàn bộ 186 trang tài liệu này.
(a): dòng tế bào ung thư biểu mô tuyến phổi ở người, (b): tế bào ung thư biểu mô tuyến vú ở người, (c): tế bào ung thư biểu mô tuyến tiền liệt ở người
Bảng 3.3 thể hiện hoạt tính của 64 dẫn xuất benzimidazole ức chế các dòng tế bào ung thư phổi A549, ung thư vú MDA-MB-231 và ung thư tuyến tiền liệt PC3 và sử dụng camptothecin làm chất chứng dương. Kết quả được thể hiện dưới hình thức giá trị IC50 (µM) và độ lệch chuẩn (± SD), trong đó độ lệch chuẩn được tính toán dựa trên 3 lần đo độc lập với nhau. Dựa vào kết quả trên có thể thấy đối với dòng tế bào A549 có 7/64 dẫn xuất có giá trị IC50 < 50 µM, ở dòng MDA-MB-231 và PC3 lần lượt là 9/64 và 2/64 dẫn xuất, chứng tỏ các dẫn xuất 2-phenylbenzimidazole có xu hướng ức chế tốt dòng tế bào MDA-MB-231 hơn hai dòng tế bào A549 và PC3.
Khi vị trí số 5 trên khung benzimidazole là hydro, các dẫn xuất 1- hầu như đều thể hiện hoạt tính ức chế tế bào không tốt trên cả 3 dòng tế bào thử nghiệm, kết quả IC50 cho thấy đa số đều lớn hơn 100 µM. Khi thay thế nguyên tử hydro ở vị trí số 5 bởi nhóm thế đẩy điện tử methyl và nhóm thế rút điện tử chloro và giữ nguyên các nhóm thế trên khung phenyl ở vị trí số 2, dãy chất 2- và 3- đã có sự thay đổi hoạt tính sinh học. Ở dãy dẫn xuất 2DM, 2TM, 2DA và 2IV giá trị IC50 của chúng dao động từ 39,43 µM đến lớn hơn 100 µM, giảm hơn so với dãy dẫn xuất 1DM, 1TM, 1DA và 1IV (IC50 từ 80,67 đến lớn hơn 100 µM) trên cả 3 dòng tế bào, đặc điểm chung của các hợp chất 2DM, 2TM, 2DA và 2IV là có các nhóm thế đẩy điện tử khác nhau (-OCH3, -N(CH3)2, -OH) trên vòng benzene ở vị trí số 2, cùng với đó phải có một nhóm đẩy điện tử (-CH3) ở vị trí số 5 của khung benzimidazole.
Theo những nghiên cứu trước đây [41], nguyên tử halogen ở vị trí số 5 được công nhận như một yếu tố làm tăng hoạt tính sinh học cho các dẫn xuất benzimidazole. Để làm rõ ảnh hưởng này trên các dẫn xuất 2-phenylbenzimidazole, chúng tôi đã thay thế nguyên tử hydro ở vị trí 5 và 6 lần lượt bằng một (dãy chất 3-) và hai nguyên tử chloro (dãy chất 4-) để đánh giá ảnh hưởng nhóm thế trên cả vị trí 5 và 6 cùng với nhóm thế trên vòng phenyl ở vị trí số 2 của khung benzimidazole đến hoạt tính sinh học của các dẫn xuất thu được. Dãy chất 3- có 8 giá trị IC50 < 50 µM (của các dẫn xuất 33H, 3DM, 3TM, 3DA, 3TF, 3BO) trong khi đó ở hai dãy chất 2- là một giá trị và dãy chất 1- hoàn toàn không có giá trị IC50 nào bé hơn 50 µM. Trên dòng tế bào ung thư MDA-MB-231, các hợp chất 2- có IC50 < 100 µM, khi thay đổi
nhóm methyl thành nhóm chloro (3-) thì giá trị IC50 của chúng đều giảm, cụ thể là giá trị IC50 của các cặp chất 33H < 23H, 3DM < 2DM, 3DA < 2DA, 3TF < 2TF và 3BO
< 2BO. Điểm chung là trong cấu trúc phân tử các hợp chất 3 này có sự hiện diện của các nhóm đẩy điện tử như -OH, -OCH3, -N(CH3)2, -O-CH2-Ph ở các vị trí khác nhau trên nhóm thế phenyl ở vị trí số 2 trên khung benzimidazole. Những kết quả trên cho thấy đưa một nguyên tử chloro vào vị trí số 5 trên khung benzimidazole, cùng với sự hiện diện của các nhóm thế đẩy điện tử trên vòng benzene ở vị trí số 2 đã dẫn đến việc gia tăng hoạt tính ức chế tế bào ung thư của dẫn xuất tạo thành so với việc không có nguyên tử chloro, được thể hiện rõ nhất trên dòng tế bào MDA-MB-231. Tuy nhiên, điều tương tự đã không xảy ra đối với dãy chất 4- với hai nguyên tử chloro nằm ở vị trí 5 và 6, các dẫn xuất thu được đều có giá trị IC50 > 100 µM dù trên nhóm thế 2-phenyl có sự hiện diện của nhóm rút hay đẩy điện tử, ngoại trừ duy nhất hợp chất 44H có IC50 = 24.89 µM trên dòng tế bào MDA-MB-231.
Nhằm tìm kiếm các dẫn xuất kháng ung thư mới, hai chuỗi dẫn xuất 5- và 6- chứa lần lượt nhóm thế benzoyl và hydroxylphenylmethyl ở vị trí số 5, đã được tổng hợp và đánh giá hoạt tính ức chế ba dòng tế bào thử nghiệm. Kết quả hoạt tính sinh học của dãy chất 5- và 6- tốt hơn so với dãy chất 4-, trong đó dãy 5- có bốn giá trị IC50 < 50 µM (của dẫn xuất 53H, 5MM), dãy 6- có ba giá trị (dẫn xuất 62H, 63H) và 4- có một giá trị (dẫn xuất 44H). Tuy nhiên chỉ duy nhất chuỗi dẫn xuất 3- và 5- có lần lượt một và bốn giá trị IC50 < 20 µM. Cụ thể trên dòng MDA-MB-231, hợp chất 3BO có IC50 = 19,79 µM, trong khi đó hai hợp chất thuộc dãy dẫn xuất 5- là 53H và 5MM có IC50 lần lượt là 14,90 và 10,82 µM. Mặt khác, khi đã bị khử nhóm carbonyl thành nhóm hydroxyl, hoạt tính của hợp chất 62H, 6TM và 6BO (chứa lần lượt các nhóm thế đẩy điện tử -OH, -OCH3 và -O-CH2-Ph trên nhóm thế 2-phenyl) đã tăng xấp xỉ 2 đến 3 lần so với hợp chất tương ứng 52H (trên 3 dòng tế bào), 5TM (trên dòng A549) và 5BO (trên dòng MDA-MB-231 và PC3). Ở chiều ngược lại, hoạt tính của hợp chất 63H và 6MM bị giảm đi từ 3 đến 10 lần so với khi chưa bị khử nhóm carbonyl thành nhóm hydroxyl (53H và 5MM). Dẫn xuất 53H đã thể hiện khả năng như một tác nhân kháng đa dòng tế bào ung thư, khi ức chế cả 3 dòng tế bào thử nghiệm với giá trị IC50 nằm trong khoảng 14,24 – 17,52 µM, khả năng này bị mất đi khi nhóm carbonyl bị khử thành nhóm hydroxyl ở hợp chất 63H. Như vậy, việc xuất hiện nhóm thế mới benzoyl vào vị trí số 5 trên khung benzimidazole đã mang lại hiệu
133
quả trong việc tìm kiếm tác nhân kháng ung thư mới, có hoạt tính ức chế tế bào ung thư tốt hơn.
Với sự xuất hiện đầy đủ 6 chuỗi dẫn xuất 1-, 2-, 3-, 4-, 5- và 6-, có thể thấy rõ rằng trong số các dẫn xuất chứa nhóm thế rút điện tử (-NO2 và CF3) ở vị trí 2’ trên vòng benzene ở vị trí số 2 trên khung benzimidazole, chỉ duy nhất 3TF có giá trị IC50 lần lượt là 23,92 và 23,38 µM trên dòng MDA-MB231 và PC3, đối với các dẫn xuất còn lại dù vị trí số 5 được gắn với nhiều loại nhóm thế khác nhau (-H, -CH3, -Cl, - CO-Ph, -(OH)CH-Ph) cũng đều thể hiện hoạt tính ức chế tế bào ung thư kém, giá trị IC50 đều lớn hơn 100 µM (12N, 1TF, 22N, 2TF, 32N, 42N, 4TF, 52N, 5TF, 6TF).
Điều này cho thấy ở chuỗi dẫn xuất 2-phenylbenzimidazole này, việc xuất hiện nhóm thế rút điện tử vào vị trí 2’ trên vòng benzene ở vị trí số 2 trên khung benzimidazole là không cần thiết, không mang lại hiệu quả trong việc cải thiện hoạt tính ức chế tế bào ung thư.
Đề xuất cấu trúc của dẫn xuất 2-phenylbenzimidazole cho hoạt tính ức chế tế bào ung thư tốt được tóm tắt trong hình 3.2
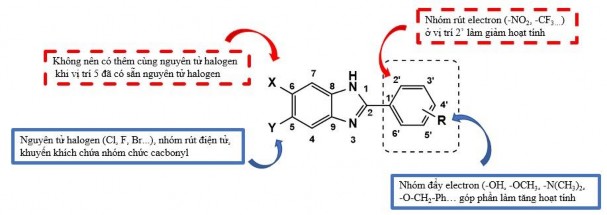
Hình 3.2. Mối quan hệ giữa cấu trúc của các dẫn xuất benzimidazole tổng hợp và hoạt tính ức chế tế bào ung thư
3.3.2. Hoạt tính gây độc tế bào in vitro của các dẫn xuất indole
Các dẫn xuất indole trong nghiên cứu này đều được tạo thành từ phản ứng Mannich đa hợp phần, bao gồm hợp phần indole (indole, indole-2-carboxylic acid, 2- phenylindole và 5-bromoindole), hợp phần amine vòng no (pyrrolidine, morpholine, 1-methylpiperazine và piperidine) và hợp phần aldehyde (aldehyde formic, 4- methoxybenzaldehyde và 4-chlorobenzaldehyde). Các hợp phần này được gắn kết thông qua một cầu nối chữ Y và gắn với hợp phần indole tại vị trí số 3.
![]()
Bảng 3.4. Kết quả gây độc tế bào của các dẫn xuất indole
ÔNG THỨC ẤU TẠO | IC50 ± SD (µM) | |||||||||
A549a | MDA-MB-231b | PC3c | ||||||||
CMF | > 100 | > 100 | > 100 | |||||||
CAF | > 100 | > 100 | > 100 | |||||||
CIF | H N COOH | > 100 | > 100 | > 100 | ||||||
H2C N | ||||||||||
CPF | > 100 | > 100 | > 100 | |||||||
PPF | > 100 | > 100 | > 100 | |||||||
PMF | 88,01 ± 1,27 | 50,65 ± 0,93 | > 100 | |||||||
PAF | H N CH2 N N H3C | > 100 | > 100 | > 100 |
CPM
> 100
> 100
> 100
CMM
> 100
> 100
> 100
CIM
> 100
> 100
> 100
H N
PPM
CH
N
OCH3
29,37 ± 0,47 38,72 ± 0,98 > 100
H N
IPM
CH OCH3 19,25 ± 0,56 19,71 ± 0,24 21,11 ± 0,34
N
BPM
8,83 ± 0,43
9,24 ± 0,15
9,90 ± 0,28
BPC
> 100
> 100
> 100
Camptothecin 0,57 ± 0,06 1,35 ± 0,04 2,50 ± 0,11
(a): dòng tế bào ung thư biểu mô tuyến phổi ở người, (b): tế bào ung thư biểu mô tuyến vú ở người, (c): tế bào ung thư biểu mô tuyến tiền liệt ở người
Bảng 3.4 thể hiện khả năng gây độc tế bào in vitro của 14 dẫn xuất thế vị trí số 3 trên khung indole (hay còn gọi là các dẫn xuất 3-aminoalkylated indole) ức chế ba dòng tế bào ung thư A549, MDA-MB-231 và PC3, sử dụng camptothecin làm chất chứng dương. Từ giá trị IC50 trên ba dòng tế bào của hợp chất IPM lần lượt là 19,25; 19,71 và 21,11 µM; giá trị IC50 của BPM lần lượt là 8,83; 9,24 và 9,90 µM, có thể thấy hai hợp chất này có xu hướng ức chế tốt trên cả ba dòng tế bào ung thư thử nghiệm, thể hiện khả năng như là những tác nhân kháng đa dòng tế bào ung thư. Một điểm trong đặc tính ức chế tế bào của các dẫn xuất indole ở đây là đều thể hiện hoạt tính kém trên dòng tế bào PC3 (ngoại trừ IPM và BPM), toàn bộ giá trị IC50 của chúng đều lớn hơn 100 µM, điều này cho thấy các dẫn xuất 3-aminoalkylated indole không phải là các tác nhân tiềm năng ức chế dòng tế bào ung thư tuyến tiền liệt PC3. Ngoài ra, các dẫn xuất indole này còn thể hiện một đặc điểm thú vị đó là khả năng ức chế đồng đều trên cả 3 dòng tế bào ung thư khác nhau. Các số liệu cho thấy ngoại trừ hợp chất PMF, PPM có các giá trị IC50 khác nhau trên ba dòng tế bào, các dẫn xuất còn lại đều có giá trị IC50 xấp xỉ như nhau trên cả ba dòng tế bào thử nghiệm: hoặc đều lớn hơn 100 µM (CMF, CAF, CIF, CPF, PPF, PAF, CPM, CMM, CIM và
BPC) hoặc xấp xỉ bằng nhau (IPM và BPM).
Mặt khác các dẫn xuất CPF, CMF, CAF, CIF, CPM, CMM, và CIM với giá trị IC50 đều lớn hơn 100 µM trên cả ba dòng tế bào ung thư, chúng có chung đặc điểm cấu trúc là có nhóm carboxyl ở vị trí số 2 trên khung indole, dù cho vị trí số 3 trên khung indole có chứa amin vòng no nào (pyrrolidine, morpholine, 1- methylpiperazine hay piperidine), cũng như chứa hợp phần được tạo từ aldehyde formic hay 4-methoxybenzaldehyde ở cầu nối, thì việc xuất hiện nhóm thế carboxyl ở vị trí số 2 trên khung indole làm cho các sản phẩm đều có hoạt tính ức chế tế bào ung thư kém. Điều đó chứng tỏ sự có mặt của nhóm carboxyl ở vị trí số 2 là không cần thiết cho hoạt tính ức chế tế bào ung thư của các dẫn xuất 3-aminoalkylated indole. Ngược lại, vị trị số 5 chứa một nguyên tử halogen (bromo) đã làm tăng hoạt tính của dẫn xuất BPM (IC50 = 9,24 µM trên dòng MDA-MB-231) lên gấp 2 đến 3 lần so với chỉ có nguyên tử hydro (IPM với IC50 = 19,71 µM) hoặc gấp 3 đến hơn 10 lần so với chứa nhóm phenyl ở vị trí số 2 (PPM với IC50 = 38,72 µM), và hợp chất BPM cũng là dẫn xuất indole có hoạt tính ức chế tốt nhất và đồng đều nhất trên cả 3 dòng tế bào thử nghiệm.
Xét vai trò của hợp phần aldehyde, trong số 7 dẫn xuất indole có hợp phần aldehyde formic trong phản ứng Mannich ban đầu, chỉ có 2/21 giá trị IC50 < 100 µM trên cả 3 dòng tế bào thử nghiệm (của dẫn xuất PMF), ở 7 dẫn xuất indole chứa hợp phần 4-methoxybenzaldehyde có đến 8/21 giá trị IC50 < 40 µM (của dẫn xuất PPM, IPM và BPM). Ngoài ra khi thay thế hợp phần 4-methoxybenzaldehyde (chứa nhóm đẩy điện tử trên vòng phenyl) ở dẫn xuất BPM bằng hợp phần 4-chlorobenzaldehyde (chứa nhóm thế rút điện tử trên vòng phenyl) để tạo ra dẫn xuất BPC thì kết quả nhận được không như mong đợi, hoạt tính kháng tế bào của dẫn xuất BPC bị giảm hoàn toàn trên cả 3 dòng tế bào thử nghiệm, các giá trị IC50 đều lớn hơn 100 µM. Đồng thời chứa nguyên tử brom ở vị trí số 5 nhưng hợp phần 4-methoxybenzaldehyde được thay bằng hợp phần 4-chlorobenzaldehyde thì hoạt tính ức chế tế bào hoàn toàn bị mất đi. Điều đó cho thấy hợp phần 4-methoxybenzaldehyde đóng vai trò quan trọng trong việc gia tăng hoạt tính ức chế tế bào ung thư của các dẫn xuất thu được, hay nói cách khác, nhóm thế đẩy điện tử (nhóm methoxy) trên vòng benzene trong hợp phần benzaldehyde đã đóng góp vào việc làm tăng hoạt tính chung của dẫn xuất 3- aminoalkylated indole và đóng góp này lớn hơn so với nhóm thế rút điện tử (chloro). Ngoài ra, từ bảng dữ liệu có thể thấy riêng rẽ một amine bất kỳ nào (pyrroline, morpholine, 1-methylpiperazine hoặc piperidine) đều không gây ảnh hưởng rõ rệt đến hoạt tính sinh học cuối cùng của dẫn xuất. Tuy nhiên, khi kết hợp với sự hiện diện của hợp phần 4-methoxybenzaldehyde, các dẫn xuất indole chứa pyrrolidine như PPM, IPM và BPM (ngoại trừ CPM) đã thể hiện sự vượt trội về hoạt tính ức chế tế bào ung thư hơn các dẫn xuất indole chứa amine vòng no khác (morpholine, 1-
methylpiperazine hoặc piperidine).
Đề xuất cấu trúc của dẫn xuất 3-aminoalkylated indole có thể cho hoạt tính ức chế tế bào ung thư tốt được tóm tắt ở hình 3.3.
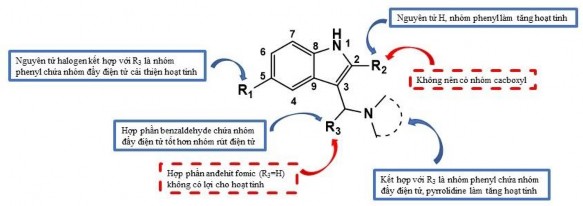
Hình 3.3. Mối quan hệ giữa cấu trúc của các dẫn xuất indole tổng hợp và hoạt tính ức chế tế bào ung thư
3.3.3. Đánh giá khả năng gây độc tế bào thường của các dẫn xuất benzimidazole và indole có hoạt tính ức chế tế bào ung thư tốt nhất
Các dẫn xuất có hoạt tính ức chế tế bào ung thư tốt nhất (53H, 5MM, IPM và BPM) được đánh giá khả năng gây độc tế bào thường HEK 293 (tế bào thận gốc phôi ở người), kết quả được trình bày ở bảng 3.5.
Bảng 3.5. Kết quả gây độc tế bào ung thư và tế bào thường của các dẫn xuất 53H, 5MM, IPM và BPM
IC50 ± SD (µM) | ||||
A549 | MDA-MB-231 | PC3 | HEK 293 | |
53H | 14,24 ± 0,33 | 14,90 ± 0,42 | 17,52 ± 0,28 | 19,17 ± 0,24 |
5MM | > 100 | 10,82 ± 0,35 | > 100 | 51,86 ± 0,62 |
IPM | 19,25 ± 0,56 | 19,71 ± 0,24 | 21,11 ± 0,34 | 89,87 ± 2,38 |
BPM | 8,83 ± 0,43 | 9,24 ± 0,15 | 9,90 ± 0,28 | 17,94 ± 0,4 |
Camptothecin | 0,57 ± 0,06 | 1,35 ± 0,04 | 2,50 ± 0,11 | 1,41 ± 0,04 |
Bốn dẫn xuất 53H, 5MM, IPM và BPM có giá trị IC50 trên dòng tế bào HEK 293 từ 17,94 đến 89,87 µM, cao hơn so với chứng dương camptothecin IC50 = 1,41
µM, hay bốn dẫn xuất này thể hiện khả năng ức chế trên tế bào thường kém hơn camptothecin. Điều này cho thấy các dẫn xuất benzimidazole và indole này có tiềm năng cao trở thành các tác nhân chống ung thư mới, do độc tính trên tế bào thường của chúng thấp hơn 12 đến 63 lần so với tác nhân chống ung thư đang có camptothecin.


![[(4-Methoxy-Phenyl)-Pyrrolidin-1-Yl-Methyl]-1H-Indole-2- Carboxylic Acid (Cpm – Chất Mới)](https://tailieuthamkhao.com/uploads/2022/09/02/nghien-cuu-tong-hop-va-danh-gia-hoat-tinh-gay-doc-te-bao-cac-dan-xuat-17-120x90.jpg)
![Bromo-3-[(4-Methoxy-Phenyl)-Pyrrolidin-1-Yl-Methyl]-1H-Indole (Bpm)](https://tailieuthamkhao.com/uploads/2022/09/02/nghien-cuu-tong-hop-va-danh-gia-hoat-tinh-gay-doc-te-bao-cac-dan-xuat-18-120x90.jpg)