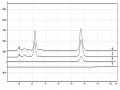
Bảng 3.8. Số liệu phổ NMR (δ ppm) của SD8 và hợp chất tham khảo
a,c δH | a,b δC | #δC | &δC | |
1 | - | 141,7 | 141,6 | 142,1 |
2 | - | 145,2 | 145,1 | 146,6 |
3 | 6,87 s | 106,8 | 106,7 | 106,8 |
3a | - | 127,4 | 127,5 | 126,2 |
4 | 3,21 t (6,0) | 30,7 | 30,8 | 28,9 |
5 | 3,27 t (6,0) | 50,6 | 50,5 | 53,5 |
6a | - | 143,9 | 144,1 | 61,8 |
6b | - | 118,3 | 118,3 | 126,4 |
7 | 6,88 s | 106,8 | 106,7 | 26,7 |
7a | - | 129,4 | 129,5 | 129,6 |
8 | - | 141,7 | 141,6 | 145,9 |
9 | - | 150,2 | 150,2 | 152,0 |
10 | 7,01 d (9,0) | 108,8 | 108,5 | 110,3 |
11 | 8,64 d (9,0) | 123,4 | 123,4 | 123,1 |
11a | - | 118,8 | 118,6 | 124,6 |
11b | - | 117,5 | 117,4 | 116,5 |
12 | 6,18 s | 100,9 | 100,8 | 100,6 |
8-OCH3 | 3,97 s | 60,6 | 60,5 | 60,7 |
9-OCH3 | 3,98 s | 56,2 | 56,2 | 55,7 |
6-NCH3 | 3,12 s | 40,6 | 40,5 | 43,7 |
Có thể bạn quan tâm!
-
 Trình Tự Các Mồi Đặc Hiệu Được Sử Dụng Cho Rt‐Qpcr
Trình Tự Các Mồi Đặc Hiệu Được Sử Dụng Cho Rt‐Qpcr -
 Chiết Xuất, Phân Lập Và Xác Định Cấu Trúc Của Một Số Hợp Chất Từ Thân Lá Cây Củ Dòm
Chiết Xuất, Phân Lập Và Xác Định Cấu Trúc Của Một Số Hợp Chất Từ Thân Lá Cây Củ Dòm -
 Số Liệu Phổ Nmr (Δ Ppm) Của Sd3 Và Hợp Chất Tham Khảo
Số Liệu Phổ Nmr (Δ Ppm) Của Sd3 Và Hợp Chất Tham Khảo -
 Tỷ Lệ (%) Diện Tích Pic Của Oxostephanin Khi Chạy Hplc Bằng Các Pha Động Khác Nhau
Tỷ Lệ (%) Diện Tích Pic Của Oxostephanin Khi Chạy Hplc Bằng Các Pha Động Khác Nhau -
 Thẩm Định Phương Pháp Định Lượng Oxostephanin Bằng Hplc
Thẩm Định Phương Pháp Định Lượng Oxostephanin Bằng Hplc -
 Hình Thái Các Dòng Tế Bào Thử Nghiệm Dưới Tác Dụng Của Sd1, Sd2, Sd3, Sd4 Và Sd5 Tại Thời Điểm 48H (Vk 10X, Zoom 5,6)
Hình Thái Các Dòng Tế Bào Thử Nghiệm Dưới Tác Dụng Của Sd1, Sd2, Sd3, Sd4 Và Sd5 Tại Thời Điểm 48H (Vk 10X, Zoom 5,6)
Xem toàn bộ 368 trang tài liệu này.

a CDCl3, b 500 MHz, c 125 MHz
# δC của dehydrocrebanin đo trong CDCl3 &δC của SD7 đo trong CDCl3 [123]
Dữ liệu phổ NMR cho thấy, SD8 tương tự như SD7 ngoại trừ cấu trúc của vòng C với sự thay đổi lớn về độ chuyển dịch hóa học của C-6a (- 82,1 ppm), C- 6b (+ 8,1 ppm), C-7 (- 80,1 ppm) và C-11a (+ 5,8 ppm). Phổ 13C-NMR và HSQC
cho thấy sự xuất hiện nhóm -CH=C< (δC 106,8 và 143,9) trong vòng C thay vì nhóm methin và methylen như trong cấu trúc của SD7. Điều này cũng được quan sát trên phổ 1H-NMR với sự xuất hiện của proton olefinic tại δH 6,88 (s). Phổ
HMBC cũng cho thấy sự tương tác của proton này với C-6b, C-11a và C-8. Với những phân tích dữ liệu như trên và so sánh với tài liệu tham khảo đã công bố, có thể xác định được hợp chất SD8 là dehydrocrebanin [123] (Hình 3.9).
Hình 3.9. Cấu trúc của hợp chất SD8
3.1.2.9. Hợp chất SD9
Hợp chất SD9 được phân lập từ dưới dạng chất rắn màu trắng. Phổ ESI-MS xuất hiện pic ion giả phân tử tại m/z 120,8 [M-H]- phù hợp với công thức phân tử là C7H6O2. Phổ 1H-NMR (500 MHz, CD3OD) và 13C-NMR (125 MHz, CD3OD):
Xem bảng 3.9.
Bảng 3.9. Số liệu phổ NMR (δ ppm) của SD9 và hợp chất tham khảo
a,b δH | a,c δC | #δC | |
1 | - | 130,0 | 130,3 |
2, 6 | 7,79 d (9,0) | 133,5 | 133,5 |
3, 5 | 6,92 d (9,0) | 117,1 | 116,9 |
4 | - | 165,8 | 165,2 |
7 | 9,77 s | 192,8 | 192,9 |
a CD3OD, b 500 MHz, c 125 MHz
# δC của 4-hydroxybenzaldehyd đo trong CD3OD [125]
Phổ 1H-NMR xuất hiện hai cặp tín hiệu proton olefin tại δH 7,79 (2H, d, J
= 9,0 Hz, H-2, H-6) và 6,92 (2H, d, J = 9,0 Hz, H-3, H-5) đặc trưng cho hệ vòng thơm dạng AAʹBBʹ. Ngoài ra, phổ proton cũng xuất hiện tín hiệu của nhóm aldehyd tại δH 9,77 (1H, s, H-7). Phổ 13C-NMR và DEPT cho thấy tín hiệu cuả 7 carbon, trong đó 6 carbon của vòng thơm tại δC 130,0 (C-1), 133,4 (C-2, C-6), 117,0 (C-3, C-5) và 165,7 (C-4). Tín hiệu tại δC 192,7 (C-7) đặc trưng cho nhóm aldehyd.
Với những phân tích dữ liệu phổ trên và so sánh với tài liệu tham khảo đã công bố, có thể xác định SD9 là 4-hydroxybenzaldehyd [125] (Hình 3.10).
Hình 3.10. Cấu trúc của hợp chất SD9
3.1.2.10. Hợp chất SD10
Hợp chất SD10 được phân lập dưới dạng bột vô định hình màu trắng. Phổ ESI-MS xuất hiện pic ion giả phân tử tại m/z 292,9 [M+Na]+ phù hợp với công thức phân tử C13H18O6. Phổ 1H-NMR (500 MHz, CD3OD) và 13C-NMR (125
MHz, CD3OD): Xem bảng 3.10.
Bảng 3.10. Số liệu phổ NMR (δ ppm) của SD10 và hợp chất tham khảo
a,b δH | a,c δC | #δC | |
1 | - | 139,0 | 139,1 |
2, 6 | 7,41 m | 129,2 | 129,3 |
3, 5 | 7,31 m | 129,1 | 129,2 |
4 | 7,26 m | 128,6 | 128,6 |
7 | 4,66 d (12,0) 4,92 d (12,0) | 71,7 | 71,8 |
1ʹ | 4,35 d (8,0) | 103,2 | 103,3 |
2ʹ | 3,23-3,30 m | 75,1 | 75,1 |
3ʹ | 77,9 | 78,1 | |
4ʹ | 71,6 | 71,7 | |
5ʹ | 3,34 m | 78,0 | 78,1 |
6ʹ | 3,69 dd (6,0, 12,0) 3,89 dd (2,5, 12,0) | 62,8 | 62,8 |
a CD3OD, b 500 MHz, c 125 MHz
# δC của benzyl β-D-glucopyranosid đo trong CD3OD [126]
Phổ 1H-NMR xuất hiện tín hiệu của 5 proton thơm tại δH 7,41 (2H, m, H-2, H-6), 7,31 (2H, m, H-3, H-5) và 7,26 (1H, m, H-4) gợi ý sự có mặt của vòng benzen thế ở vị trí 1. Ngoài ra, trên phổ proton còn xuất hiện tín hiệu của nhóm oxymethylen tại δH 4,66 (1H, d, J = 12,0 Hz, H-7) và 4,92 (1H, d, J = 12,0 Hz, H- 7). Bên cạnh đó, sự xuất hiện của gốc đường β-D-glucopyranosyl cũng được thể hiện qua tín hiệu của proton anomeric với hằng số ghép cặp lớn [δH 4,35 (1H, d, J = 8,0 Hz)], proton nhóm hydroxymethylen [δH 3,69 (1H, d, J = 6,0; 12,0 Hz), 3,89 (1H, d, J = 2,5; 12,0 Hz)] và các proton nhóm hydroxymethin [δH 3,23 – 3,34 (4H, m)]. Phổ 13C-NMR cho thấy tín hiệu của 13 carbon trong đó 6 carbon của gốc đường β-D-glucopyranosyl [δC 103,2, 75,1, 77,9, 71,6, 78,0 và 62,8]. Vị trí của gốc đường này được xác định tại vị trí C-7 thông qua tương tác HMBC giữa H-1′ (δH 4,35) với C-7 (δC 71,7). Với những phân tích dữ liệu phổ trên và so sánh với tài liệu tham khảo đã công bố, có thể xác định hợp chất SD10 là benzyl β-D- glucopyranosid [126] (Hình 3.11).
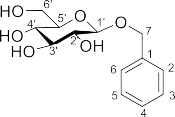
Hình 3.11. Cấu trúc của hợp chất SD10
3.1.2.11. Hợp chất SD11
Hợp chất SD11 thu được dưới dạng bột vô định hình màu trắng. Phổ ESI- MS xuất hiện pic ion giả phân tử tại m/z 409 [M+Na]+ phù hợp với công thức phân tử C19H30O8. Phổ 1H-NMR (500 MHz, CD3OD) và 13C-NMR (125 MHz,
CD3OD): Xem bảng 3.11.
Bảng 3.11. Số liệu phổ NMR (δ ppm) của SD11 và hợp chất tham khảo
a,b δH (J = Hz) | a,c δC | # δC | &δC | $δC | @δC | |
1 | - | 42,4 | 42,5 | 42,5 | 42,5 | 42,4 |
2 | 2,18 m/2,61 m | 50,7 | 50,7 | 50,8 | 50,8 | 50,7 |
3 | - | 201,2 | 201,2 | 210,3 | 201,3 | 201,1 |
4 | 5,89 br s | 127,1 | 127,2 | 127,1 | 127,2 | 127,2 |
- | 167,0 | 167,3 | 167,4 | 167,2 | 166,9 | |
6 | - | 80,0 | 80,0 | 80,0 | 80,1 | 80,0 |
7 | 6,99 d (15,5) | 133,7 | 131,6 | 131,7 | 134,7 | 134,1 |
8 | 5,75 d (15,5) | 133,7 | 135,3 | 135,1 | 133,8 | 133,8 |
9 | 4,55 m | 74,6 | 77,3 | 76,9 | 74,7 | 74,7 |
10 | 1,31 d (6,5) | 22,2 | 21,22 | 21,2 | 22,3 | 22,2 |
11 | 1,06 s | 23,4 | 23,5 | 23,4 | 23,5 | 23,5 |
12 | 1,03 s | 24,7 | 24,7 | 24,6 | 24,7 | 24,8 |
13 | 1,96 d (1,5) | 19,5 | 19,6 | 19,7 | 19,6 | 19,4 |
1ʹ | 4,29 d (7,5) | 101,2 | 102,8 | 102,6 | 100,3 | 100,9 |
2ʹ | 3,21 t (8,0) | 74,9 | 75,3 | 75,2 | 75,0 | 75,0 |
3ʹ | 3,25-3,30 m | 78,3 | 78,2 | 78,0 | 78,4 | 78,3 |
4ʹ | 3,25-3,30 m | 71,6 | 71,7 | 71,5 | 71,7 | 71,8 |
5ʹ | 3,17 m | 78,1 | 78,1 | 78,0 | 78,3 | 78,1 |
6ʹ | 3,66 dd (6,0, 11,5) 3,87 dd (2,0, 11,5) | 62,8 | 62,9 | 62,6 | 62,9 | 62,9 |
a CD3OD, b 500 MHz, c 125 MHz
# δC của (6S,9R)-roseosid, & δC của (6R,9R)-roseosid, $ δC của (6S,9S)- roseosid và @ δC của (6R,9S)-roseosid đo trong CD3OD [127]
Phổ 1H-NMR của hợp chất SD11 xuất hiện tín hiệu của một proton olefin dạng C=CH tại δH 5,89 (1H, br s, H-4) và một nối đôi khác thế hai lần (CH=CH) dạng trans tại δH 6,99 (1H, d, J = 15,5 Hz, H-7) và 5,75 (1H, dd, J = 15,5 Hz, H- 8); 3 nhóm methyl bậc 3 [δH 1,03 (3H, s, H-12), 1,06 (3H, s, H-11) và 1,96 (3H,
d, J = 1,5 Hz, H-13)] và 1 nhóm methyl bậc hai [δH 1,31 (3H, d, J = 6,5 Hz, H- 10)]; 1 nhóm methylen [δH 2,18 (1H, m, H-2a)/2,61 (1H, m, H-2b)]; 1 nhóm oxymethin [δH 4,55 (1H, t, J = 6,8 Hz, H-9)]. Ngoài ra, phổ 1H-NMR còn xuất hiện tín hiệu của một proton anomeric tại δH 4,29 (1H, d, J = 7,5 Hz, H-1ʹ), 2 proton hydroxymethylen tại δH 3,66 (1H, dd, J = 6,0, 11,5 Hz, H-6ʹ), 3,87 (1H, dd, J = 2,0; 11,5 Hz, H-6ʹ) và các proton hydroxymethin nằm trong vùng trường 3,17 - 3,21 ppm, gợi ý sự có mặt của một gốc đường hexose. Giá trị độ dịch chuyển
hóa học của phần đường cùng với hằng số tương tác lớn của proton anomeric H- 1'/H-2' (J1′-2′ = 7,5 Hz) gợi ý gốc đường là O-β-D-glucopyranosyl.
Phổ 13C-NMR và HSQC của hợp chất SD11 xuất hiện tín hiệu cộng hưởng của 19 carbon, bao gồm 13 carbon đặc trưng cho khung megastigman: 1 nhóm carbonyl tại δC 201,2 (C-3), 2 nhóm methin olefin của nối đôi (CH=CH) tại δC 133,7 (C-7)/133,7 (C-8), 2 tín hiệu carbon olefin khác của nối đôi CH=C tại 127,1 (C-4)/167,0 (C-5), 4 nhóm methyl tại δC 19,5 (C-13), 22,2 (C-10), 23,4 (C-11),
24,6 (C-12), 1 nhóm methylen tại δC 50,7 (C-2), 1 carbon không mang hydro liên kết với oxy tại δC 80,0 (C-6), nhóm oxymethin tại δC 74,6 (C-9) và sáu carbon đặc trưng cho gốc đường tại δC 101,2 (C-1ʹ) và 5 tín hiệu các nhóm oxymethin/oxymethylen trong vùng từ δC 62,8 - 78,3.
Phân tích phổ HMBC của SD11 cho thấy vị trí của 2 nhóm methyl bậc ba tại C-1 và C-5 được xác định dựa vào tương tác giữa H3-11/H3-12 với C-1/C-2/ C-6, giữa H3-13 với C-4/C-5/C-6; vị trí của 1 nhóm methyl bậc hai còn lại tại C- 9 được xác định dựa vào các tương tác HMBC giữa H3-10 với C-8/C-9. Bằng cách xác định tương tự mối tương quan giữa các tương tác, vị trí của nhóm keton (C-
3) được xác định dựa vào các tương tác HMBC giữa proton H-2/H-4 với C-3. Tương tác HMBC giữa proton anomeric H-1ʹ với C-9, xác định vị trí của liên kết của phần đường tại C-9.
Cấu hình 6R, 9S được xác định dựa trên độ chuyển dịch hóa học của carbon tại các vị trí C-7, C-8 và C-9 (Bảng 3.11). Từ các phân tích trên kết hợp so sánh số liệu phổ NMR với hợp chất (6R,9S)-roseosid đã được công bố trước đó [127], có thể khẳng định SD11 là (6R,9S)-roseosid (Hình 3.12).
![]()
![]()
Hình 3.12. Cấu trúc (A) và các tương tác HMBC (B) của hợp chất SD11
Như vậy từ thân lá cây củ dòm đã chiết xuất, phân lập và xác định cấu trúc của 11 hợp chất. Thông tin cơ bản của các hợp chất này được tóm tắt trong bảng 3.12.
Bảng 3.12. Các hợp chất phân lập được từ thân lá cây củ dòm
Tên hợp chất | CTPT – KLPT | Cấu trúc hoá học | ||
1 | Stedieltin A (SD1) | C19H15NO6 | O | |
M = 353,0899 | O | N | ||
O OCH3 | ||||
OH | ||||
OCH3 | ||||
2 | Stedieltin B (SD2) | C17H11NO4 | O | |
M = 293,0688 | O | N | ||
O | ||||
OCH3 | ||||
3 | Oxostephanin (SD3) | C18H11NO4 | O | |
M =305 | O | N | ||
O | ||||
OCH3 | ||||
4 | Oxostephanosin (SD4) | C17H9NO4 M = 291 | O O | N O OH |
5 | Oxocrebanin (SD5) | C19H13NO5 | O | |
M = 335 | O | N | ||
O | ||||
OCH3 | ||||
OCH3 | ||||
6 | Aristolactam (SD6) | C17H11NO4 | O | O |
M = 293 | O | NH | ||
OCH3 |
Crebanin (SD7) | C20H21NO4 | O | ||||
M = 339 | O N CH 3 | |||||
OCH3 | ||||||
OCH3 | ||||||
8 | Dehydrocrebanin | C20H19NO4 | O | |||
(SD8) | M = 337 | O N CH 3 | ||||
OCH3 | ||||||
OCH3 | ||||||
9 | 4-hydroxy benzaldehyd (SD9) | C7H6O2 M = 122 | O H OH | |||
10 | Benzyl β-D- glucopyranosid (SD10) | C13H18O6 M = 270 | HO O O HOHOOH | |||
11 | (6R,9S)-roseosid (SD11) | C19H30O8 M = 386 | O | OHO O OH | OH | OH OH |
3.2. BƯỚC ĐẦU NGHIÊN CỨU XÂY DỰNG PHƯƠNG PHÁP PHÂN LẬP VÀ PHƯƠNG PHÁP ĐỊNH LƯỢNG ĐỂ THEO DÕI HÀM LƯỢNG OXOSTEPHANIN TRONG DƯỢC LIỆU THEO THỜI GIAN THU HÁI
3.2.1. Phân lập và sơ bộ đánh giá độ tinh khiết của oxostephanin
3.2.1.1. Phân lập oxostephanin
Nguyên liệu là thân lá cây củ dòm khô (hàm ẩm 5,6%) (5 kg) được nghiền nhỏ và đem ngâm chiết với MeOH (35 lít) ở nhiệt độ phòng, sau 3 ngày tách dịch chiết ra, cô cạn trên máy cất chân không thu được cắn MeOH. Tiến hành lặp lại thêm hai lần chiết với dùng dung môi trên thì thu được cắn MeOH, ký hiệu là M (0,45 kg, hiệu suất 9,0% so với khối lượng nguyên liệu thân lá củ dòm khô).