500
(a)
Nồng độ MB 50 mg/L
500

Dung löôïng hấp phụ q (mg/g)
Có thể bạn quan tâm!
-
 Nghiên cứu than hóa phụ phẩm nông nghiệp vỏ hạt cà phê, lõi bắp bằng phương pháp carbon hóa thủy nhiệt, ứng dụng làm vật liệu hấp phụ và xúc tác - 13
Nghiên cứu than hóa phụ phẩm nông nghiệp vỏ hạt cà phê, lõi bắp bằng phương pháp carbon hóa thủy nhiệt, ứng dụng làm vật liệu hấp phụ và xúc tác - 13 -
 Nghiên cứu than hóa phụ phẩm nông nghiệp vỏ hạt cà phê, lõi bắp bằng phương pháp carbon hóa thủy nhiệt, ứng dụng làm vật liệu hấp phụ và xúc tác - 14
Nghiên cứu than hóa phụ phẩm nông nghiệp vỏ hạt cà phê, lõi bắp bằng phương pháp carbon hóa thủy nhiệt, ứng dụng làm vật liệu hấp phụ và xúc tác - 14 -
 Nghiên cứu than hóa phụ phẩm nông nghiệp vỏ hạt cà phê, lõi bắp bằng phương pháp carbon hóa thủy nhiệt, ứng dụng làm vật liệu hấp phụ và xúc tác - 15
Nghiên cứu than hóa phụ phẩm nông nghiệp vỏ hạt cà phê, lõi bắp bằng phương pháp carbon hóa thủy nhiệt, ứng dụng làm vật liệu hấp phụ và xúc tác - 15 -
 Nghiên cứu than hóa phụ phẩm nông nghiệp vỏ hạt cà phê, lõi bắp bằng phương pháp carbon hóa thủy nhiệt, ứng dụng làm vật liệu hấp phụ và xúc tác - 17
Nghiên cứu than hóa phụ phẩm nông nghiệp vỏ hạt cà phê, lõi bắp bằng phương pháp carbon hóa thủy nhiệt, ứng dụng làm vật liệu hấp phụ và xúc tác - 17 -
 Nghiên cứu than hóa phụ phẩm nông nghiệp vỏ hạt cà phê, lõi bắp bằng phương pháp carbon hóa thủy nhiệt, ứng dụng làm vật liệu hấp phụ và xúc tác - 18
Nghiên cứu than hóa phụ phẩm nông nghiệp vỏ hạt cà phê, lõi bắp bằng phương pháp carbon hóa thủy nhiệt, ứng dụng làm vật liệu hấp phụ và xúc tác - 18 -
 Nghiên cứu than hóa phụ phẩm nông nghiệp vỏ hạt cà phê, lõi bắp bằng phương pháp carbon hóa thủy nhiệt, ứng dụng làm vật liệu hấp phụ và xúc tác - 19
Nghiên cứu than hóa phụ phẩm nông nghiệp vỏ hạt cà phê, lõi bắp bằng phương pháp carbon hóa thủy nhiệt, ứng dụng làm vật liệu hấp phụ và xúc tác - 19
Xem toàn bộ 180 trang tài liệu này.
(b)
Nồng độ MB 100 mg/L
500

Dung löôïng hấp phụ q (mg/g)
(c)
Nồng độ MB 200 mg/L
Dung löôïng hấp phụ q (mg/g)
400CHhydro CChydro CHmagnet CCmagnet
CHimpreg CCimpreg
400
CHhydro CChydro
CHmagnet CCmagnet
CHimpreg CCimpreg
400
CHhydro CChydro
CHmagnet CCmagnet
CHimpreg CCimpreg
300
200
CHactiv CCactiv
CHbiochar CCbiochar
300
200
CHactiv CCactiv
CHbiochar CCbiochar
300
200
CHactiv CCactiv
CHbiochar CCbiochar
100 100
100
0
0 120 240 360 480 600 720 840 960
Thời gian (phút)
0
0 120 240 360 480 600 720 840 960

Thời gian (phút)
0
0 120 240 360 480 600 720 840 960

Thời gian (phút)

500
Dung löôïng hấp phụ q (mg/g)
400
(d)
Nồng độ MB 300 mg/L
500
Dung löôïng hấp phụ q (mg/g)
400
(e)
Nồng độ MB 400 mg/L
500
Dung löôïng hấp phụ q (mg/g)
400
(f)
300 300 300
200
CHhydro CChydro
200
CHhydro CChydro
200
Nồng độ MB 500 mg/L
CHhydro CChydro
CHmagnetCCmagnet
100 CHimpreg CCimpreg
CHactiv CCactiv
CHmagnet CCmagnet
100CHimpreg CCimpreg
CHactiv CCactiv
CHmagnet CCmagnet
100CHimpreg CCimpreg
CHactiv CCactiv
0 CHbiochar CCbiochar
0 120 240 360 480 600 720 840 960
Thời gian (phút)
0 CHbiochar CCbiochar
0 120 240 360 480 600 720 840 960
Thời gian (phút)
0 CHbiochar CCbiochar
0 120 240 360 480 600 720 840 960
Thời gian (phút)
Hình 3.37. Ảnh hưởng của thời gian tiếp xúc và nồng độ MB ban đầu (50 – 500 mg/L) trên các mẫu than sinh học hoạt hóa.
102
3.4.5. Phương trình đường đẳng nhiệt hấp phụ
Đường đẳng nhiệt hấp phụ mô tả và giải thích mối tương quan giữa chất hấp phụ và chất bị hấp phụ, điều này rất quan trọng để tối ưu hóa quá trình hấp phụ [158]. Các phương trình đẳng nhiệt hấp phụ mô tả sự phân bố của chất hấp phụ giữa pha lỏng và pha rắn khi quá trình hấp phụ đạt được trạng thái cân bằng [158]. Việc khớp dữ liệu thực nghiệm với các mô hình đẳng nhiệt khác nhau là một bước quan trọng trong việc xác định mô hình phù hợp cho thiết kế quy trình hấp phụ [158, 161]. Mô hình đẳng nhiệt Langmuir và Freundlich được sử dụng rộng rãi trong các nghiên cứu khoa học và chúng được sử dụng trong nghiên cứu này để phân tích dữ liệu cân bằng hấp phụ thực nghiệm. Tính phù hợp của các mô hình được xác định
bằng cách đánh giá các hệ số tương quan R2 và so sánh giá trị tính toán của dung
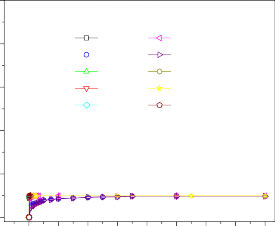
lượng hấp phụ MB tối đa từ mô hình đã chọn với dữ liệu thực nghiệm [158]. Kết quả trên Hình 3.38 cho thấy các đường hấp phụ đẳng nhiệt xanh methylen của các loại vật liệu than sinh học hoạt hóa.
CHhydro
CChydro
CHmagnet CCmagnet
CHimpreg CHactiv
CHbiochar
CCimpreg CCactiv
CCbiochar
500
400
qe(mg/ g)
300
200
100
0
0 50 100 150 200 250
Ce (mg/ L)
Hình 3.38. Sự hấp phụ đẳng nhiệt MB trên các mẫu than sinh học hoạt hóa
Kết quả trên Hình 3.38 cho thấy dung lượng hấp phụ (qe) của tất cả các loại vật liệu tăng nhanh chóng tại thời điểm nồng độ (Ce) trong dung dịch có giá trị thấp, khi Ce lớn hơn thì dung lượng hấp phụ tăng chậm. Khả năng hấp phụ của các vật liệu được sắp xếp theo thứ tự giảm dần Hydrochar hoạt hóa > Hydrochar hoạt hóa thủy nhiệt > Hydrochar hoạt hóa ngâm tẩm ≥ Biochar hoạt hóa > Hydrochar từ tính. Mẫu Hydrochar từ tính có khả năng hấp phụ MB kém nhất so với các loại vật liệu khác (CCmagnet đạt 271,27 mg/g và CHmagnet đạt 263,21 mg/g), có thể do diện tích bề mặt riêng của Hydrochar từ tính giảm bởi các phân tử Fe3O4 đã xâm nhập
vào các lỗ xốp và chiếm diện tích bề mặt trống. Tuy phương pháp điều chế Hydrochar từ tính không hiệu quả trong việc xử lý MB nhưng sẽ hiệu quả trong việc thu hồi. Mẫu Hydrochar hoạt hóa có khả năng hấp phụ MB tốt nhất (CCactiv đạt 481,58 mg/g và CHactiv đạt 475,43 mg/g), có thể do Hydrochar hoạt hóa trực tiếp từ nguyên liệu thô trong môi trường KOH có diện tích bề mặt riêng lớn và hàm lượng các nhóm chứa oxy nhiều đã phân tích trong phần đặc trưng của vật liệu. Diện tích bề mặt riêng lần lượt là CCactiv đạt 965,9 m2/g, CHactiv đạt 950,4 m2/g và hàm lượng các nhóm chứa oxy nhiều là CCactiv đạt 1,825 mmol/g, CHactiv đạt 1,813 mmol/g.
Mô hình Langmuir được thiết lập theo công thức (2.10) với giả thiết rằng chỉ xảy ra hiện tượng hấp phụ đơn lớp và các vị trí hấp phụ là giống nhau và tương đương về mặt năng lượng. Từ đó Qm và KL được xác định từ đồ thị tuyến tính của Ce/qe so với Ce, cho ra phương trình đường thẳng có hệ số góc 1/Qm (từ Hình 3.39 a đến Hình 3.43 a). Ngược lại, mô hình Freundlich được thiết lập cho các hệ thống năng lượng bề mặt không đồng nhất với sự hấp phụ phân rã theo cấp số nhân theo công thức (2.8). Từ đó KF và n có thể được xác định từ đồ thị tuyến tính của logqe so với logCe, cho phương trình đường thẳng có hệ số góc 1/n (từ Hình 3.39 b đến Hình 3.43 b). Các thông số hấp phụ của các mô hình trình bày trong Bảng PL 5.
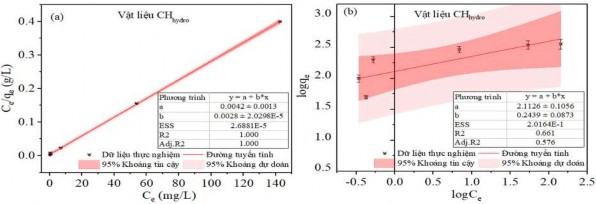
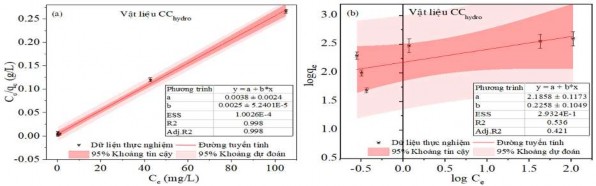
Hình 3.39. (a) Đồ thị đẳng nhiệt Langmuir, (b) Freundlich và hệ số tương quan hồi quy cho sự hấp phụ MB trên Hydrochar hoạt hóa thủy nhiệt.
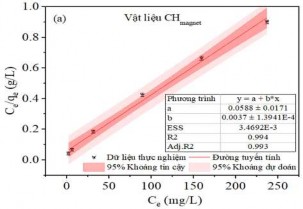
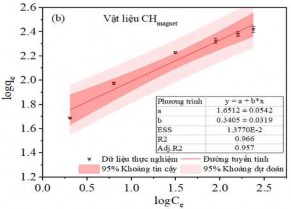
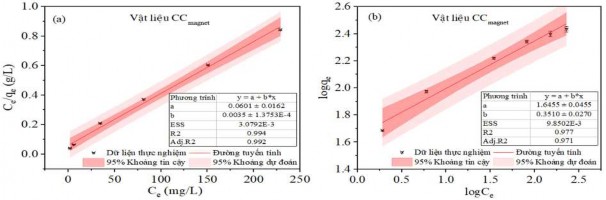
Hình 3.40. (a) Đồ thị đẳng nhiệt Langmuir, (b) Freundlich và hệ số tương quan hồi quy cho sự hấp phụ MB trên Hydrochar từ tính
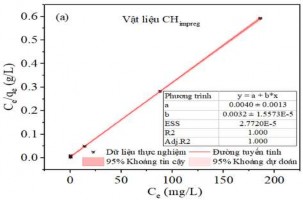
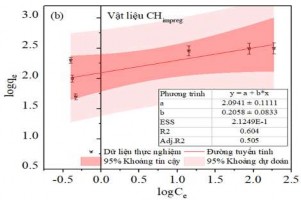
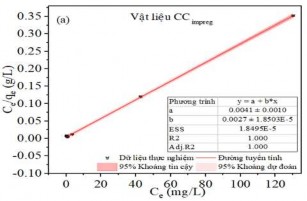
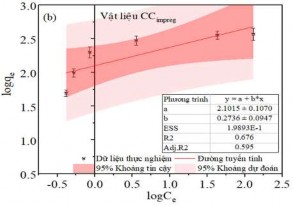
Hình 3.41. (a) Đồ thị đẳng nhiệt Langmuir, (b) Freundlich và hệ số tương quan hồi quy cho sự hấp phụ MB trên Hydrochar hoạt hóa ngâm tẩm.
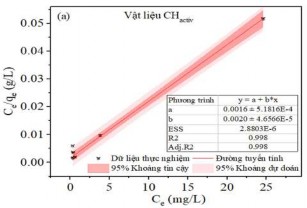

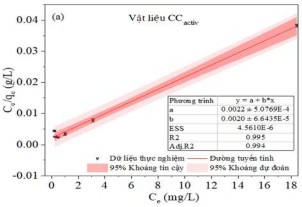
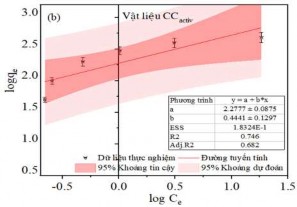
Hình 3.42. (a) Đồ thị đẳng nhiệt Langmuir, (b) Freundlich và hệ số tương quan hồi quy cho sự hấp phụ MB trên Hydrochar hoạt hóa.
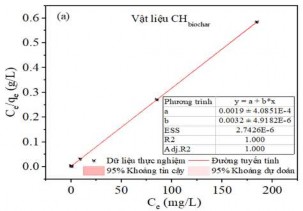
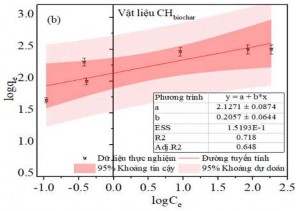
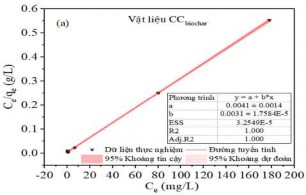
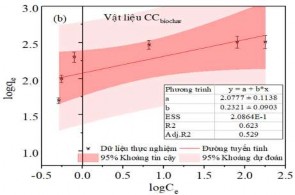
Hình 3.43. (a) Đồ thị đẳng nhiệt Langmuir, (b) Freundlich và hệ số tương quan hồi quy cho sự hấp phụ MB trên Biochar hoạt hóa.
Kết quả trên Bảng PL 5 cho thấy quá trình hấp phụ MB trên các mẫu Hydrochar hoạt hóa, Hydrochar hoạt hóa thủy nhiệt, Hydrochar hoạt hóa ngâm tẩm, Biochar hoạt hóa đều giá trị hệ số tương quan R2 theo mô hình đẳng nhiệt Freundlich thấp (R2 < 0,9), chứng tỏ mô hình đẳng nhiệt Freundlich không phù hợp. Ngoại trừ, Hydrochar từ tính có giá trị hệ số tương quan R2 theo mô hình đẳng nhiệt Freundlich lần lượt CHmagnet (R2 = 0,966) và CCmagnet (R2 = 0,977). Tuy nhiên, các giá trị qe,cal lý thuyết theo mô hình Freundlich của các vật liệu này chênh lệch lớn với các dữ liệu thực nghiệm qexp, độ chênh lệch CHmagnet (qe = 19,86 mg/g), và CCmagnet (qe = 16,78 mg/g). Do đó, quá trình hấp phụ MB trên tất cả các loại vật liệu đều không phù hợp với mô hình đẳng nhiệt Freundlich.
Mặt khác, kết quả trên Bảng PL 5 cho thấy hệ số tương quan R2 của mô hình hấp phụ đẳng nhiệt Langmuir mô tả sự hấp phụ MB trên tất cả các mẫu than sinh học hoạt hóa đều rất tốt R2 > 0,99, chứng tỏ quá trình hấp phụ MB phù hợp với mô hình Langmuir. Hơn nữa, dung lượng hấp phụ MB tối đa (Qm) theo mô hình Langmuir của các mẫu than rất gần với các dữ liệu thực nghiệm qexp trong Bảng 3.7. Dung lượng hấp phụ MB tối đa (Qm) theo mô hình Langmuir của các mẫu than được sắp xếp theo thứ tự giảm dần: CHactiv (500,00 mg/g) > CCactiv (500,00 mg/g) > CChydro (400,00 mg/g) > CCimpreg (359,71 mg/g) > CHhydro (357,14 mg/g) > CCbiochar (322,58 mg/g) > CHbiochar (316,46 mg/g) > CHimpreg (312,50 mg/g) > CCmagnet (285,71 mg/g) > CHmagnet (270,27 mg/g). Kết quả cho thấy quá trình hấp phụ MB trên tất cả các mẫu than hoàn toàn phù hợp với mô hình đẳng nhiệt Langmuir. Do đó, quá trình hấp phụ MB trên tất cả các mẫu than trên là một quá trình hấp phụ hóa học, ái lực hấp phụ trong phạm vi trên bề mặt nhóm chức và năng lượng liên kết. Cơ chế hấp phụ của MB trên bề mặt than được đề xuất dựa theo Hình 3.44 cho các tương tác khác nhau: (i) tương tác tĩnh điện giữa các nhóm chức tích điện âm trên bề mặt than với cation MB bị hấp phụ mạnh từ dung dịch ( Hình 3.44 a), (ii) liên kết hydro giữa các nhóm chức có sẵn trên bề mặt than và các nguyên tử nitơ của MB (Hình 3.44 b), (iii) sự tương tác xếp chồng π - π giữa các vòng thơm của MB và khung của than (Hình 3.44 c). Các kiểu tương tác giữa than và MB khác nhau giúp tăng cường hấp phụ MB trên bề mặt các mẫu than. Kết quả hoàn toàn phù hợp với các nghiên cứu khác đã công bố [159, 160],

Hình 3.44. Cơ chế đề xuất các tương tác có thể xảy ra giữa than sinh học hoạt hóa và MB: (a) tương tác thu hút tĩnh điện, (b) tương tác liên kết hydro, và (c) tương tác xếp chồng π-π
Hơn nữa, mô hình Langmuir đã được xác định tham số cân bằng RL để đánh giá các xu hướng của quá trình hấp phụ [162, 163]. Tham số RL được tính dựa trên giá trị KL không đổi như sau:
𝑅
=ଵ
ଵାಽ
(3.2)
Trong đó: Co (mg/L): nồng độ chất bị hấp phụ trong dung dịch ban đầu; KL (L/mg) là hằng số cân bằng hấp phụ Langmuir.
Giá trị RL đánh giá các xu hướng của quá trình hấp phụ: khi RL = 0 thì quá trình hấp phụ không thuận nghịch, khi RL trong khoảng (0 < RL <1) thì quá trình hấp phụ thuận lợi, khi RL = 1 thì quá trình hấp phụ tuyến tính, khi RL > 1 thì quá trình hấp phụ không thuận lợi [158]. Kết quả thu được trong Bảng PL 5 cho thấy tất cả các vật liệu đều có giá trị RL đáp ứng 0 < RL < 1. Chứng tỏ, sự phù hợp của mô hình đẳng nhiệt Langmuir hấp thụ xanh methylen trên tất cả các vật liệu. Tóm lại, các loại vật liệu than trong nghiên cứu này đều có lợi cho việc hấp phụ thuốc nhuộm MB và phù hợp với mô hình đẳng nhiệt Langmuir.
Ngoài ra, Bảng 3.7 so sánh các mẫu than sinh học hoạt hóa với các loại vật liệu khác có nguồn gốc từ sinh khối khác về khả năng hấp phụ thuốc nhuộm MB.
Kết quả trình bày trong Bảng 3.7 cho thấy Hydrochar hoạt hóa có khả năng hấp phụ MB tốt nhất: mẫu CCactiv đạt 481,58 mg/g và CHactiv đạt 475,43 mg/g. Hơn nữa, các mẫu than khác trong công trình này đều có khả năng hấp phụ MB cạnh tranh với các than hoạt tính khác trong Bảng 3.7. Chứng tỏ, phương pháp HTC là phương pháp đầy hứa hẹn, thân thiện với môi trường và tiềm năng với điều kiện nhiệt độ thấp dễ tiếp cận để tạo than sinh học hoạt hóa hiệu quả. Ưu điểm chính của phương pháp điều chế Hydrochar hoạt hóa là kết hợp quá trình hoạt hóa trong quá trình HTC rút ngắn được giai đoạn hoạt hóa. Hoạt hóa bằng phương pháp thủy nhiệt chỉ tiêu tốn một lượng nhỏ KOH được sử dụng. Lượng dung dịch KOH dư sau khi thủy nhiệt có thể tái sử dụng cho lần hoạt hóa sau. Một ưu điểm nữa là kết hợp đồng thời quá trình hoạt hóa hóa học và nhiệt phân. Lượng KOH bị giữ lại trong sản phẩm thủy nhiệt tiếp tục hoạt động như tác nhân hoạt hóa trong quá trình nhiệt phân. Đặc biệt là quá trình HTC trong môi trường KOH có thể tạo ra nhiều nhóm chức chứa oxy trên bề mặt than sinh học hoạt hóa làm tăng khả năng hấp phụ cũng như hoạt tính xúc tác. Kết quả này tương tư như nghiên cứu khác đã báo cáo [138]. Do đó, vỏ hạt cà phê/ lõi bắp là một trong những nguyên liệu tiềm năng cho việc nghiên cứu điều chế vật liệu hấp phụ rẻ tiền có khả năng hấp phụ thuốc nhuộm trong dung dịch nước hiệu quả.






