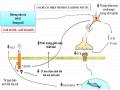
n-butanol liều 100 mg/kg/ngày làm giảm các biểu hiện trầm cảm trên chuột UCMS một cách rõ rệt, tương đương IMP liều 8,0 mg/kg/ngày, tiêm phúc mạc, như: cải thiện hành vi giảm hứng thú (anhedonia) gồm giảm đáp ứng với phần thưởng trong thử nghiệm tiêu thụ saccharose (SPT) và giảm hành vi chải lông trong thử nghiệm môi trường mở (OFT), giảm hành vi tuyệt vọng trong TST, FST và tăng hành vi trốn thoát có định hướng trong FST, đồng thời không gây ảnh hưởng đến vận động tự nhiên của chuột trong OFT. Như vậy, cao chiết phân đoạn n-butanol có chứa thành phần hoạt chất đóng vai trò quan trọng đối với tác dụng chống trầm cảm của hương nhu tía.
- Cơ chế tác dụng chống trầm cảm của cao chiết phân đoạn n-butanol trên chuột UCMS một phần thông qua tác động lên hệ monoaminergic, cụ thể là hệ serotonergic (thử nghiệm sử dụng chất đối kháng DL-ρ-chlorophenyl alanin (PCPA)), noradrenergic và domapinergic (thử nghiệm sử dụng chất đối kháng α-methyl-ρ- tyrosin (AMPT)).
ĐỀ XUẤT
Các kết quả trong luận án cho thấy, hương nhu tía có khả năng cải thiện trí nhớ và chống trầm cảm trên thực nghiệm. Hiện nay, nguồn dược liệu hương nhu tía trong nước khá dồi dào, đã được trồng quy mô và theo tiêu chuẩn hóa. Để có thể khai thác và sử dụng hương nhu tía có hiệu quả hơn nữa trong công tác dự phòng và điều trị các bệnh lý rối loạn tâm thần – thần kinh như trầm cảm và Alzheimer, tác giả xin đề xuất:
- Tiếp tục tìm hiểu sâu hơn về cơ chế chống trầm cảm của các chất phân lập được từ phân đoạn n-butanol hương nhu tía.
- Xây dựng quy trình chiết xuất và tiêu chuẩn hóa cao chiết hương nhu tía
- Xác định độc tính cấp và độc tính bán trường diễn của cao tiêu chuẩn hương nhu tía để hướng đến khả năng phát triển thành thực phẩm chức năng hoặc sản phẩm hỗ trợ dự phòng và điều trị sa sút trí tuệ và/hoặc trầm cảm.
DANH MỤC CÔNG TRÌNH ĐÃ CÔNG BỐ
LIÊN QUAN ĐẾN LUẬN ÁN
Có thể bạn quan tâm!
-
 Tác Dụng Cải Thiện Trí Nhớ Của Các Cao Chiết Phân Đoạn Hương Nhu Tía
Tác Dụng Cải Thiện Trí Nhớ Của Các Cao Chiết Phân Đoạn Hương Nhu Tía -
 Bàn Luận Chung Về Vai Trò Của Acid Ursolic Và Acid Oleanolic Đối Với Tác Dụng Cải Thiện Trí Nhớ Của Os
Bàn Luận Chung Về Vai Trò Của Acid Ursolic Và Acid Oleanolic Đối Với Tác Dụng Cải Thiện Trí Nhớ Của Os -
 Dự Đoán Thành Phần Hóa Học Có Thể Đóng Vai Trò Quan Trọng Trong Tác Dụng Chống Trầm Cảm Của Os
Dự Đoán Thành Phần Hóa Học Có Thể Đóng Vai Trò Quan Trọng Trong Tác Dụng Chống Trầm Cảm Của Os -
 Nghiên cứu tác dụng cải thiện suy giảm trí nhớ và chống trầm cảm của Hương nhu tía Ocimum sanctum L. trên thực nghiệm - 20
Nghiên cứu tác dụng cải thiện suy giảm trí nhớ và chống trầm cảm của Hương nhu tía Ocimum sanctum L. trên thực nghiệm - 20 -
 Nghiên cứu tác dụng cải thiện suy giảm trí nhớ và chống trầm cảm của Hương nhu tía Ocimum sanctum L. trên thực nghiệm - 21
Nghiên cứu tác dụng cải thiện suy giảm trí nhớ và chống trầm cảm của Hương nhu tía Ocimum sanctum L. trên thực nghiệm - 21 -
 Nghiên cứu tác dụng cải thiện suy giảm trí nhớ và chống trầm cảm của Hương nhu tía Ocimum sanctum L. trên thực nghiệm - 22
Nghiên cứu tác dụng cải thiện suy giảm trí nhớ và chống trầm cảm của Hương nhu tía Ocimum sanctum L. trên thực nghiệm - 22
Xem toàn bộ 187 trang tài liệu này.
“NGHIÊN CỨU TÁC DỤNG CẢI THIỆN SUY GIẢM TRÍ NHỚ VÀ CHỐNG TRẦM CẢM CỦA HƯƠNG NHU TÍA (Ocimum sanctum L.) TRÊN THỰC NGHIỆM

1. Nguyen Thu Hien, Le Thi Xoan, Phung Nhu Hoa, Nguyen Van Tai, Nguyen Minh Khoi (2020), “Putative constituents contributing to the antidepressant-like effects of Ocimum sanctum on olfactory bulbectomized-mice”, Journal of medicinal materials, 25(3), pp. 186-192.
2. Xoan Thi Le, Hien Thu Nguyen, Tai Van Nguyen, Hang Thi Nguyet Pham, Phuong Thi Nguyen, Khoi Minh Nguyen, Ba Van Nguyen, Kinzo Matsumoto (2021), Ocimum sanctum Linn. extract improves cognitive deficits in olfactory bulbectomized mice via the enhancement of central cholinergic systems and VEGF expression, Evidence-Based Complementary and Alternative Medicine. 2021, P. 6627648.
3. Thu Hien Nguyen, Thi Xoan Le, Van Tai Nguyen, Thi Nguyet Hang Pham, Minh Khoi Nguyen, Matsumoto Kinzo (2021), The antidepressant-like effects of an n- butanol fraction of Ocimum sanctum Linn. extract in unpredictable chronic mild stress- induced depression in mice, Vietnam Journal Science, Technology and Engineering, 63(4), pp. 55-61.
4. Hien Thu Nguyen, Xoan Thi Le, Hoa Nhu Phung, Tai Van Nguyen, Hang Thi Nguyet Pham, Khoi Minh Nguyen, Matsumoto Kinzo (2022), Ursolic acid and its isomer oleanolic acid are responsible for the anti-dementia effects of Ocimum sanctum in olfactory bulbectomized mice, Journal of Natural Medicines, https://doi.org/10.1007/s11418-022-01609-2, 1-13.
TÀI LIỆU THAM KHẢO
1. Australia, D., S. Baker, and S. Banerjee (2019), "Alzheimer’s Disease International. World Alzheimer Report 2019: Attitudes to dementia", Alzheimer’s Disease International; Alzheimer’s Disease International: London, UK.
2. Association, A.s., 2021 Alzheimer’s disease facts and figures. 2021: Alzheimers Dement.
3. Depression, W. (2017), "Other Common Mental Disorders: Global Health Estimates", Geneva: World Health Organization, pp. 1-24.
4. Nguyễn Bích Ngọc (2014), "Chất lượng cuộc sống của bệnh nhân Alzheimer, người chăm sóc và đánh giá hiệu quả của một số biện pháp can thiệp không dùng thuốc", Luận án Tiến sĩ Y học.
5. Bộ Y tế (2017), "Niên giám Thống kê Y tế".
6. Wilson, R.S., A.W. Capuano, P.A. Boyle, G.M. Hoganson, L.P. Hizel, R.C. Shah, S. Nag, J.A. Schneider, S.E. Arnold, and D.A. Bennett (2014), "Clinical- pathologic study of depressive symptoms and cognitive decline in old age", Neurology. 83(8), pp. 702-709.
7. Modrego, P.J. (2010), "Depression in Alzheimer's disease. Pathophysiology, diagnosis, and treatment", Journal of Alzheimer's Disease. 21(4), pp. 1077- 1087.
8. Dybedal, G.S., L. Tanum, K. Sundet, T.L. Gaarden, and T.M. Bjølseth (2013), "Neuropsychological functioning in late-life depression", Frontiers in psychology. 4, pp. 381.
9. Castaneda, A.E., A. Tuulio-Henriksson, M. Marttunen, J. Suvisaari, and J. Lönnqvist (2008), "A review on cognitive impairments in depressive and anxiety disorders with a focus on young adults", Journal of affective disorders. 106(1-2), pp. 1-27.
10. Ahmad, A., M.M. Khan, S.S. Raza, H. Javed, M. Ashafaq, F. Islam, M.M. Safhi, and F. Islam (2012), "Ocimum sanctum attenuates oxidative damage and neurological deficits following focal cerebral ischemia/reperfusion injury in rats", Neurological sciences. 33(6), pp. 1239-1247.
11. Joshi, H. and M. Parle (2006), "Evaluation of nootropic potential of Ocimum sanctum Linn. in mice".
12. Sampath, S., S. Mahapatra, M. Padhi, R. Sharma, and A. Talwar (2015), "Holy basil (Ocimum sanctum Linn.) leaf extract enhances specific cognitive
parameters in healthy adult volunteers: A placebo controlled study", Indian J Physiol Pharmacol. 59(1), pp. 69-77.
13. Kusindarta, D.L., H. Wihadmadyatami, and A. Haryanto (2016), "Ocimum sanctum Linn. stimulate the expression of choline acetyltransferase on the human cerebral microvascular endothelial cells", Veterinary world. 9(12), pp. 1348.
14. Trần Đình Năng, Nguyễn Hoàng Giao, Dương Phước An, Nguyễn Thị Thu Vân, and T.P.H. Yến (2011), "Khảo sát khả năng cải thiện sự suy giảm trí nhớ của cao chiết lá Hương nhu tía (Ocimum sanctum) trên chuột nhắt", Y Học TP. Hồ Chí Minh. 15(Phụ bản số 1), tr. 124-129.
15. Jothie Richard, E., R. Illuri, B. Bethapudi, S. Anandhakumar, A. Bhaskar, C. Chinampudur Velusami, D. Mundkinajeddu, and A. Agarwal (2016), "Anti‐stress activity of Ocimum sanctum: Possible effects on hypothalamic– pituitary–adrenal axis", Phytotherapy Research. 30(5), pp. 805-814.
16. Le Thi Xoan, N.H.A. (2015), "Antidepressant-like effect of Ocimum sanctum in Olfactory bulbectomized mice", Tạp chí Dược liệu. 20(5), pp. 311-316.
17. Association, A.s. (2012), "2012 Alzheimer’s disease facts and figures", Alzheimer's & Dementia. 8(2), pp. 131-168.
18. Bi, C., S. Bi, and B. Li (2019), "Processing of mutant β-amyloid precursor protein and the clinicopathological features of familial Alzheimer’s disease", Aging and disease. 10(2), pp. 383.
19. H Ferreira-Vieira, T., I. M Guimaraes, F. R Silva, and F. M Ribeiro (2016), "Alzheimer's disease: targeting the cholinergic system", Current neuropharmacology. 14(1), pp. 101-115.
20. Wenk, G.L. (2003), "Neuropathologic changes in Alzheimer's disease", Journal of Clinical Psychiatry. 64, pp. 7-10.
21. Khyade, V.B., S.V. Khyade, and S.G. Jagtap (2016), "Alzheimer’s Disease: Overview", International Academic Journal of Social Sciences. 3(12), pp. 23- 38.
22. Priller, C., T. Bauer, G. Mitteregger, B. Krebs, H.A. Kretzschmar, and J. Herms (2006), "Synapse formation and function is modulated by the amyloid precursor protein", Journal of Neuroscience. 26(27), pp. 7212-7221.
23. Iqbal, K., A.d.C. Alonso, S. Chen, M.O. Chohan, E. El-Akkad, C.-X. Gong, S. Khatoon, B. Li, F. Liu, and A. Rahman (2005), "Tau pathology in Alzheimer disease and other tauopathies", Biochimica et Biophysica Acta (BBA)- Molecular Basis of Disease. 1739(2-3), pp. 198-210.
24. Li, X., X. Bao, and R. Wang (2016), "Experimental models of Alzheimer's disease for deciphering the pathogenesis and therapeutic screening", International journal of molecular medicine. 37(2), pp. 271-283.
25. Udo, H., Y. Yoshida, T. Kino, K. Ohnuki, W. Mizunoya, T. Mukuda, and H. Sugiyama (2008), "Enhanced adult neurogenesis and angiogenesis and altered affective behaviors in mice overexpressing vascular endothelial growth factor 120", Journal of Neuroscience. 28(53), pp. 14522-14536.
26. Wada, T., J.J. Haigh, M. Ema, S. Hitoshi, R. Chaddah, J. Rossant, A. Nagy, and
D. van der Kooy (2006), "Vascular endothelial growth factor directly inhibits primitive neural stem cell survival but promotes definitive neural stem cell survival", Journal of Neuroscience. 26(25), pp. 6803-6812.
27. Inada, C., Y. Niu, K. Matsumoto, X.T. Le, and H. Fujiwara (2014), "Possible involvement of VEGF signaling system in rescuing effect of endogenous acetylcholine on NMDA-induced long-lasting hippocampal cell damage in organotypic hippocampal slice cultures", Neurochemistry international. 75, pp. 39-47.
28. Mateo, I., J. Llorca, J. Infante, E. Rodríguez‐Rodríguez, C. Fernández‐Viadero,
N. Pena, J. Berciano, and O. Combarros (2007), "Low serum VEGF levels are associated with Alzheimer's disease", Acta Neurologica Scandinavica. 116(1), pp. 56-58.
29. Provias, J. and B. Jeynes (2014), "Reduction in vascular endothelial growth factor expression in the superior temporal, hippocampal, and brainstem regions in Alzheimer’s disease", Current neurovascular research. 11(3), pp. 202-209.
30. Garcia, K.d.O., F.L. Ornellas, P. Matsumoto, C.d.L. Patti, L.E. Mello, R. Frussa-Filho, S.W. Han, and B.M. Longo (2014), "Therapeutic effects of the transplantation of VEGF overexpressing bone marrow mesenchymal stem cells in the hippocampus of murine model of Alzheimer’s disease", Frontiers in aging neuroscience. 6, pp. 30.
31. Wang, P., Z.-H. Xie, Y.-J. Guo, C.-P. Zhao, H. Jiang, Y. Song, Z.-Y. Zhu, C. Lai, S.-L. Xu, and J.-Z. Bi (2011), "VEGF-induced angiogenesis ameliorates the memory impairment in APP transgenic mouse model of Alzheimer’s disease", Biochemical and biophysical research communications. 411(3), pp. 620-626.
32. Hohman, T.J., S.P. Bell, A.L. Jefferson, and A.s.D.N. Initiative (2015), "The role of vascular endothelial growth factor in neurodegeneration and cognitive decline: exploring interactions with biomarkers of Alzheimer disease", JAMA neurology. 72(5), pp. 520-529.
33. Rodríguez, J.J. and A. Verkhratsky (2011), "Neurogenesis in Alzheimer’s disease", Journal of anatomy. 219(1), pp. 78-89.
34. Kulason, S., E. Xu, D.J. Tward, A. Bakker, M. Albert, L. Younes, and M.I. Miller (2020), "Entorhinal and transentorhinal atrophy in preclinical Alzheimer's disease", Frontiers in Neuroscience. 14, pp. 804.
35. Bevan-Jones, W.R., T.E. Cope, P.S. Jones, S.S. Kaalund, L. Passamonti, K. Allinson, O. Green, Y.T. Hong, T.D. Fryer, and R. Arnold (2020), "Neuroinflammation and protein aggregation co-localize across the frontotemporal dementia spectrum", Brain. 143(3), pp. 1010-1026.
36. Stampfer, M. (2006), "Cardiovascular disease and Alzheimer's disease: common links", Journal of internal medicine. 260(3), pp. 211-223.
37. Cholerton, B., L.D. Baker, and S. Craft (2013), "Insulin, cognition, and dementia", European journal of pharmacology. 719(1-3), pp. 170-179.
38. Gorelick, P.B., A. Scuteri, S.E. Black, C. DeCarli, S.M. Greenberg, C. Iadecola,
L.J. Launer, S. Laurent, O.L. Lopez, and D. Nyenhuis (2011), "Vascular contributions to cognitive impairment and dementia: a statement for healthcare professionals from the American Heart Association/American Stroke Association", Stroke. 42(9), pp. 2672-2713.
39. Association, A.s. (2013), "2013 Alzheimer's disease facts and figures", Alzheimer's & dementia. 9(2), pp. 208-245.
40. Food, U., Drug Administration FDA grants accelerated approval for Alzheimer’s drug. 2021.
41. May, P.C., R.A. Dean, S.L. Lowe, F. Martenyi, S.M. Sheehan, L.N. Boggs,
S.A. Monk, B.M. Mathes, D.J. Mergott, and B.M. Watson (2011), "Robust central reduction of amyloid-β in humans with an orally available, non-peptidic β-secretase inhibitor", Journal of Neuroscience. 31(46), pp. 16507-16516.
42. Golde, T.E., E.H. Koo, K.M. Felsenstein, B.A. Osborne, and L. Miele (2013), "γ-secretase inhibitors and modulators", Biochimica et Biophysica Acta (BBA)- Biomembranes. 1828(12), pp. 2898-2907.
43. MacLeod, R., E.-K. Hillert, R.T. Cameron, and G.S. Baillie (2015), "The role and therapeutic targeting of α-, β-and γ-secretase in Alzheimer's disease", Future science OA. 1(3).
44. Hefti, F., W.F. Goure, J. Jerecic, K.S. Iverson, P.A. Walicke, and G.A. Krafft (2013), "The case for soluble Aβ oligomers as a drug target in Alzheimer's disease", Trends in Pharmacological Sciences. 34(5), pp. 261-266.
45. Yamaguchi, M. (2018), Drosophila models for human diseases. Vol. 1076. Springer.
46. Dey, A., R. Bhattacharya, A. Mukherjee, and D.K. Pandey (2017), "Natural products against Alzheimer's disease: Pharmaco-therapeutics and biotechnological interventions", Biotechnology Advances. 35(2), pp. 178-216.
47. Chauhan, N.B. (2006), "Effect of aged garlic extract on APP processing and tau phosphorylation in Alzheimer's transgenic model Tg2576", Journal of ethnopharmacology. 108(3), pp. 385-394.
48. Park, S.J., J.M. Jung, H.E. Lee, Y.W. Lee, D.H. Kim, J.M. Kim, J.G. Hong,
C.H. Lee, I.H. Jung, and Y.-B. Cho (2012), "The memory ameliorating effects of INM-176, an ethanolic extract of Angelica gigas, against scopolamine-or Aβ1–42-induced cognitive dysfunction in mice", Journal of ethnopharmacology. 143(2), pp. 611-620.
49. Zhang, Z., R. Zhao, J. Qi, S. Wen, Y. Tang, and D. Wang (2011), "Inhibition of glycogen synthase kinase‐3β by Angelica sinensis extract decreases β‐amyloid‐induced neurotoxicity and tau phosphorylation in cultured cortical neurons", Journal of Neuroscience Research. 89(3), pp. 437-447.
50. Kim, H.-K.K. and D.-H. Shinate (2000), "Inhibitory effect of Artemisia asiatica alkaloids on acetylcholinesterase activity from rat PC12 cells", Mol Cells. 10(3), pp. 253-62.
51. Le, X.T., H.T.N. Pham, T. Van Nguyen, K.M. Nguyen, K. Tanaka, H. Fujiwara, and K. Matsumoto (2015), "Protective effects of Bacopa monnieri on ischemia-induced cognitive deficits in mice: the possible contribution of bacopaside I and underlying mechanism", Journal of ethnopharmacology. 164, pp. 37-45.
52. Ruan, C.-J., J.-Y. Si, L. Zhang, D.-H. Chen, G.-H. Du, and L. Sun (2009), "Protective effect of stilbenes containing extract-fraction from Cajanus cajan L. on Aβ25–35-induced cognitive deficits in mice", Neuroscience letters. 467(2), pp. 159-163.
53. Lee, J.W., Y.K. Lee, J.O. Ban, T.Y. Ha, Y.P. Yun, S.B. Han, K.W. Oh, and J.T. Hong (2009), "Green tea (-)-epigallocatechin-3-gallate inhibits β-amyloid- induced cognitive dysfunction through modification of secretase activity via inhibition of ERK and NF-κ B pathways in mice", The Journal of nutrition. 139(10), pp. 1987-1993.
54. Mazza, M., A. Capuano, P. Bria, and S. Mazza (2006), "Ginkgo biloba and donepezil: a comparison in the treatment of Alzheimer's dementia in a randomized placebo‐controlled double‐blind study", European Journal of Neurology. 13(9), pp. 981-985.