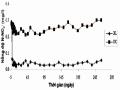
3.7.4.2. Mật độ tảo
Sự biến động về mật độ tảo và vi khuẩn lam trong hồ Hoà Mục ở khu vực đối chứng và khu vực xử lý bằng B90-La được chỉ ra trong Hình 3.59. Sau khi xử lý, mật độ tảo và vi khuẩn lam trong hồ giảm rõ rệt. Sự suy giảm mật độ chủ yếu do số lượng tế bào tảo lục và vi khuẩn lam giảm, còn số lượng tế bào của các loài tảo khác chiếm số lượng không đáng kể. Điều này cho thấy nước hồ đã trong và sạch hơn sau khi được xử lý nhưng vẫn đảm bảo sự đa dạng loài cần thiết (thể hiện ở số lượng loài vẫn được bảo đảm). Ngược lại, ở khu vực đối chứng, mật độ tế bào tảo tăng mạnh mà nguyên nhân chủ yếu do sự tăng số lượng tế bào vi khuẩn lam, còn số lượng tảo lục giảm. Điều này có thể khẳng định, có sự chuyển dịch từ ngành tảo lục sang vi khuẩn lam trong thời gian khảo sát.

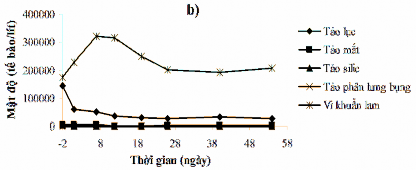
Hình 3.59. Biến đổi mật độ tảo của nước hồ Hoà Mục trước và sau khi xử lý bằng B90-La: a) khu vực xử lý, b) khu vực đối chứng.
Sự biến động của tổng số mật độ tế bào tảo và vi khuẩn lam của hồ Hoà Mục trước và sau khi xử lý bằng B90-La được trình bày trong Hình 3.60. So sánh sự biến động mật độ tế bào tảo và vi khuẩn lam ở khu vực xử lý và khu vực đối chứng cho thấy mật độ tế bào ở khu vực đối chứng cao hơn hẳn khu vực xử lý. Như vậy việc xử lý hồ bằng B90-La đã cho hiệu quả tốt với nước hồ.
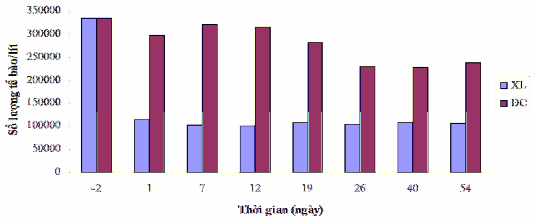
Có thể bạn quan tâm!
-
 Thành Phần Hoá Học Và Tính Chất Bề Mặt Của Vật Liệu Sau Khi Hấp Phụ
Thành Phần Hoá Học Và Tính Chất Bề Mặt Của Vật Liệu Sau Khi Hấp Phụ -
 Sự Biến Đổi Nồng Độ Pht Trong Cột Đối Chứng Và Cột Xử Lý Với Tỉ Lệ B90- La:p Là 230:1, 340:1 Và 450:1.
Sự Biến Đổi Nồng Độ Pht Trong Cột Đối Chứng Và Cột Xử Lý Với Tỉ Lệ B90- La:p Là 230:1, 340:1 Và 450:1. -
 Nồng Độ N-No2- (Mg/l) Của Khu Vực Xử Lý Và Khu Vực Đối Chứng Trong Thời Gian Thử Nghiệm: (♦) Khu Vực Xử Lý, (■) Khu Vực Đối Chứng.
Nồng Độ N-No2- (Mg/l) Của Khu Vực Xử Lý Và Khu Vực Đối Chứng Trong Thời Gian Thử Nghiệm: (♦) Khu Vực Xử Lý, (■) Khu Vực Đối Chứng. -
 Nghiên cứu điều chế, tính chất của vật liệu bentonit biến tính và ứng dụng hấp phụ phốtpho trong nước - 19
Nghiên cứu điều chế, tính chất của vật liệu bentonit biến tính và ứng dụng hấp phụ phốtpho trong nước - 19 -
 Nghiên cứu điều chế, tính chất của vật liệu bentonit biến tính và ứng dụng hấp phụ phốtpho trong nước - 20
Nghiên cứu điều chế, tính chất của vật liệu bentonit biến tính và ứng dụng hấp phụ phốtpho trong nước - 20 -
 Nghiên cứu điều chế, tính chất của vật liệu bentonit biến tính và ứng dụng hấp phụ phốtpho trong nước - 21
Nghiên cứu điều chế, tính chất của vật liệu bentonit biến tính và ứng dụng hấp phụ phốtpho trong nước - 21
Xem toàn bộ 213 trang tài liệu này.
Hình 3.60. So sánh mật độ tảo ở khu vực đối chứng và khu vực xử lý hồ Hoà Mục bằng B90-La.
3.7.5. Kết luận về quá trình xử lý hồ Hoà Mục bằng vật liệu B90-La
Trên cơ sở khảo sát sự thay đổi nồng độ PHT và sự biến đổi một số chỉ tiêu sinh hoá của hồ Hoà Mục trong suốt thời gian xử lý bằng B90-La từ tháng 4/2011 đến tháng 12/2011, một số kết luận được rút ra:
- Nồng độ phốtpho hoà tan giảm nhanh trong khu vực xử lý trong 12 ngày đầu sau khi xử lý và khu vực đối chứng thay đổi không đáng kể. Tuy nhiên lượng mưa cao bất thường 35 ngày sau xử lý, dẫn đến một lượng nước lớn chảy tràn vào hồ làm nồng độ PHT tăng lên một ít, sau đó giảm xuống duy trì ở mức 0,03 mg/l trong suốt thời gian khảo sát từ tháng 5/2011 đến 12/2011.
- Nồng độ kim loại trong nước hồ Hoà Mục và trong lớp bùn đáy thay đổi không đáng kể trong thời gian trước và sau khi thử nghiệm. Quan sát được số lượng tảo trên bề mặt giảm thể hiện qua nồng độ Chl a giảm trong khu vực xử lý. Trong khi đó ở khu vực đối chứng thì nồng độ Chl a ít thay đổi.
- Thành phần tảo có biến động lớn trong thời gian xử lý hồ. Thành phần loài có sự biến động mạnh, đặc biệt đối với tảo lục và vi khuẩn lam là 2 ngành chiếm ưu thế trong hồ Hoà Mục. Sau xử lý mật độ tảo và tảo lam trong hồ giảm rõ rệt, sự suy giảm này chủ yếu do số lượng tế bào tảo lục và tảo lam giảm trong suốt thời gian xử lý. Điều này cho thấy nước hồ đã trong và sạch hơn sau khi xử lý nhưng vẫn đảm bảo sự đa dạng loài cần thiết. Như vậy việc xử lý hồ bằng B90-La đã cho hiệu quả tốt.
KẾT LUẬN
Với mục đích nghiên cứu của luận án là điều chế vật liệu bentonit biến tính từ nguồn bentonit Bình Thuận và các tác nhân biến tính (La, Al, Fe, Al/La, Al/Fe), và khảo sát khả năng hấp phụ phốtpho trong nước của vật liệu điều chế và rút ra một số kết luận dưới đây:
1. Đã tổng hợp được các loại vật liệu bentonit biến tính bằng tác nhân kim loại (La) và tác nhân polyoxocation kim loại (Al, Fe, Al/La, Al/Fe) trên nền bentonit Bình Thuận với các đặc tính vượt trội so với bentonit nguyên liệu là: khoảng cách lớp tăng từ 12,6Å của B90 lên đến 15 – 16Å (B90-La, B40-La, BFe), 17 – 19Å (BAl, BAlLa, BAlFe). Khoảng cách lớp giữa mở rộng đáng kể so với bentonit nguyên liệu từ 3Å lên 5 – 11Å tuỳ thuộc vào loại vật liệu bentonit biến tính. Diện tích bề mặt, tổng thể tích lỗ xốp, tâm hoạt động của bentonit biến tính tăng lên đáng kể so với bentonit chưa biến tính, phù hợp cho các ứng dụng hấp phụ.
2. Đã khảo sát một số yếu tố ảnh hưởng đến quá trình hấp phụ phốtpho trong dung dịch nước trên bentonit biến tính cho thấy: khả năng hấp phụ phốtpho trên vật liệu B90-La, B40-La, BAl, BFe, BAlLa và BAlFe xảy ra nhanh và đạt cân bằng sau 4 giờ. Dung lượng hấp phụ P thay đổi không đáng kể trong khoảng pH từ 3 đến 6 và dung lượng hấp phụ P giảm khi pH tăng từ 7 đến 11. Động học hấp phụ phốtpho trên bentonit biến tính phù hợp với mô hình động học biểu kiển bậc 2. Đường đẳng nhiệt mô tả quá trình hấp phụ P trên bentonit biến tính phù hợp tốt với phương trình đẳng nhiệt Langmuir. Quá trình hấp phụ phốtpho của bentonit biến tính tự xảy ra trong điều kiện nhiệt động và thu nhiệt.
3. Đã khảo sát khả năng làm giảm nồng độ phốtpho trong nước hồ phú dưỡng bằng vật liệu bentonit biến tính theo mô hình cột. Nồng độ phốtpho trong nước hồ Hoà Mục giảm là do bentonit biến tính lantan đã hấp phụ và giữ chúng trong cấu trúc lớp.
4. Kết quả ứng dụng xử lý phú dưỡng tại hồ Hoà Mục thấy nồng độ phốtpho hoà tan giảm hơn 80% sau 12 ngày xử lý. Mật độ tảo và vi khuẩn lam trong hồ giảm và có sự thay đổi thành phần loài tảo theo hướng làm sạch môi trường nước hồ. Bentonit biến tính không chỉ hấp phụ làm giảm phốtpho hoà tan trong cột nước, mà còn hấp thu, kéo tế bào tảo và vi khuẩn lam xuống lớp bùn đáy hồ.
DANH MỤC CÁC CÔNG TRÌNH ĐÃ CÔNG BỐ
1. Trần Văn Quy, Lê Bá Thuận, Bùi Văn Thắng, Trần Văn Sơn, Thân Văn Liên (2010), Nghiên cứu điều chế vật liệu bentonit biến tính lantan ứng dụng xử lý phốtpho trong môi trường nước, Tạp chí Khoa học ĐHQGHN, Khoa học Tự nhiên và Công nghệ, 26, số 5S, 836 – 842.
2. Lê Bá Thuận, Bùi Văn Thắng, Trần Văn Sơn (2010), Nghiên cứu công nghệ xử lý phú dưỡng nước hồ Hoàn Kiếm bằng vật liệu bentonit biến tính lantan, Tạp chí hoá học, T.48, 4C, 384 – 389.
3. Lê Bá Thuận, Bùi Văn Thắng, Nguyễn Mạnh Trường, Trần Văn Sơn, Thân Văn Liên (2010), Nghiên cứu hấp phụ phốtpho trong dung dịch nước bằng vật liệu bentonit biến tính lantan, Tạp chí hoá học, T.48, 4C, 402 – 407.
4. Lê Bá Thuận, Bùi Văn Thắng, Trần Văn Sơn (2011), Nghiên cứu điều chế, tính chất của vật liệu La/Al chống bentonit và ứng dụng hấp phụ phốtphat trong nước. Phần I. Nghiên cứu điều chế, tính chất của vật liệu, Tạp chí hoá học, T.49, 3A, 302 – 306.
5. Lê Bá Thuận, Bùi Văn Thắng (2011), Nghiên cứu điều chế, tính chất của vật liệu La/Al chống bentonit và ứng dụng hấp phụ phốtphat trong nước. Phần II. Khảo sát hấp phụ phốtphat, Tạp chí hoá học, T.49, 3A, 307 – 312.
6. Bùi Văn Thắng, Lê Bá Thuận (2012), Nghiên cứu điều chế và đặc trưng cấu trúc của vật liệu Fe chống bentonit, Tạp chí hoá học, T.50, 5B, 18-23.
7. Bùi Văn Thắng, Lê Bá Thuận (2012), Đặc trưng cấu trúc của Al-, Fe-, Al/Fe- chống bentonit và khảo sát hấp phụ phốtphat trong nước, Tạp chí hoá học, T.50, 5B, 24-29.
8. Lê Bá Thuận, Bùi Văn Thắng (2012), Nghiên cứu điều chế và khảo sát tính chất của vật liệu Al/Fe chống bentonit, Tạp chí hoá học, T.50, 5B, 30-35.
9. Lê Bá Thuận, Bùi Văn Thắng (2012), Nghiên cứu hấp phụ phốtpho trong nước bằng vật liệu bentonit biến tính lantan nhằm ngăn chặn và kiểm soát phú dưỡng trong các thuỷ vực, Tạp chí hoá học, T.50, 5B, 36-41.
I. TIẾNG VIỆT
TÀI LIỆU THAM KHẢO
[1] Nguyễn Thị Diệu Cẩm (2010), Nghiên cứu biến tính bentonit và ứng dụng hấp phụ, xúc tác phân huỷ các hợp chất phenol trong nước bị ô nhiễm, Luận án Tiến sĩ, Đại học Khoa học Tự nhiên, Hà Nội.
[2] Cao Anh Dũng và cộng sự (2005), Một số kết quả nghiên cứu tổng hợp sét hữu cơ từ sét Bình Thuận để sử dụng cho ngành dầu khí, Tuyển tập báo cáo Hội nghị KHCN “30 năm dầu khí Việt Nam cơ hội mới thách thức mới”.
[3] Nguyễn Hữu Đĩnh, Trần Thị Đà (1999), Ứng dụng một số phương pháp phổ nghiên cứu cấu trúc phân tử, NXB Giáo Dục, Hà Nội.
[4] Thân Văn Liên và cộng sự (2006), Nghiên cứu qui trình xử lý, hoạt hoá bentonite Việt Nam để sản xuất bentonite xốp dùng cho xử lý nước thải có chứa kim loại nặng, Viện Cộng nghệ Xạ - Hiếm, Hà Nội.
[5] Thân Văn Liên và Cộng sự (2009), Nghiên cứu công nghệ chế tạo montmorillonite (MMT) từ nguồn khoáng thiên nhiên làm nguyên liệu cho nanoclay, Báo cáo kết quả nghiên cứu đề tài KHCN cấp Nhà Nước, mã số KC02-06/06/10, Hà Nội.
[6] Đào Thế Minh, Hoàng Tuấn Hưng, Đỗ Quang Kháng, Nguyễn Văn Hội (2006), Chế tạo vật liệu nanocompozit trên cơ sở cao su blend nhiệt dẻo polyvinyl/cao su nitril – butadien và clay hữu cơ bằng phương pháp lưu hoá động, Tuyển tập các báo cáo Khoa học Hội nghị KHCN nano và ứng dụng trong quân sự, Hà Nội.
[7] Phan Thanh Sơn Nam, Vương Quang Thạo (2008), Nghiên cứu sử dụng bentonite Bình Thuận biến tính làm xúc tác cho phản ứng ghép đôi Heck giữa iodotoluen và styrene, Tạp chí phát triển KHCN, tập 11, số 8, 19-23.
[8] Nguyễn Đức Nghĩa (2007), Hoá học nano công nghệ nền và vật liệu nguồn, NXB Khoa học Tự nhiên và Công nghệ, pp 349 – 384.
[9] Nguyễn Trọng Nghĩa (2011), Điều chế sét hữu cơ từ khoáng bentonite Bình Thuận và khảo sát khả năng ứng dụng của chúng, Luận án Tiến sĩ, Đại học Khoa học Tự nhiên, Hà Nội.
[10] Nguyễn Hữu Phú (1998), Hấp phụ và xúc tác bề mặt vật liệu vô cơ mao quản, NXB KHKT, Hà Nội.
[11] Đỗ Quý Sơn (1987), Nghiên cứu khả năng ứng dụng các chất trao đổi ion trên cơ sở các aluminosilicate tự nhiên để hấp phụ một số ion kim loại nặng, Báo cáo đề tài nghiên cứu khoa học, Viện Cộng nghệ Xạ - Hiếm, Hà Nội.
II. TIẾNG ANH
[12] Adams J.M. and Evans S. (1979), Determination of the cation-exchange capacity (layer charge) of small quantities of clay minerals by nephelometry, Clay and Clay Minerals, Vol. 27, No. 2, 137-139.
[13] Adebowale K.O., Unuabonah E.I., Olu-Owolabi B.I. (2008), Kinetic and thermodynamic aspects of the adsorption of Pb2+ and Cd2+ ions on tripolyphosphate
- modified kaolinite clay, Chemical Engineering Journal, 136, 99 – 107.
[14] Afsar A. and Groves S. (2008), Alum and Phoslock: Comparison of the factors that affect their performances, Phoslock Water Solution Limited, Report number: IR 015/08.
[15] Afsar A. and Groves S. (2009), Comparison of P-inactivation efficacy and ecotoxicity of Alum and Phoslock, Phoslock Water Solution Limited, Report number: IR 015/09.
[16] Altunlu M. and Yapar S. (2007), Effect of OH-/Al3+ and Al3+/clay ratios on the
adsorption properties of Al-pillared bentonites, Colloids and Surfaces A: Physiscochem. Eng. Aspects 306, 88 – 94.
[17] Balci S. and Gökçay E. (2002), Effects of drying methods and calcination temperatures on the physical properties of iron intercalated clays, Material Chemistry and Physics, 76, 46-51.
[18] Balci S. and Gökçay E. (2009), Pore structure and surface acidity evaluation of Fe-PILC, Turk J Chem, 33, 843-856.
[19] Banković P., Milutionvić-Nikolić A., Jović-Jovičić N., Dostanić J., Čupić Ž., Lončarević D., Jovanović D. (2009), Synthesis, characterization and appilcation of Al,Fe-pillared clays, Acta Physica Polonica A, Vol. 115, No. 4, 811 – 815.
[20] Bartram (1999), Introduction. Toxic Cyanobacteria in Water: A guide to their public health consequences, monitoring and management. I Chorus & J. Bartham, E & FN Spon Publishers.
[21] Bergaoui L., Lambert J.F., Franck R., Suquet H., Robert J.L. (1995), Al- pillared saponites. Part 3. – Effect of parent clay layer charge on the intercalation-pillaring mechanism and structural properties, Journal of the Chemical Society, Faraday Transactions, 91, 2229-2239.
[22] Bergaya F., Theng B.K.G., Lagaly G. (2006), Handbook of Clay Science, Developments in Clay Science, Elsevier, 1197p.
[23] Berkheiser V.E. and Mortland M.M. (1977), Hectorite Complexes with Cu(II) and Fe(II)-1,10-Phenanthroline Chelates, Clays and Clay Minerals, 25, 105-112.
[24] Best (1999), Environmental pollution studies, Liverpool University Press, p. 29.
[25] Borgnino L., Giacomelli C.E., Avena M.J., De Pauli C.P. (2010), Phosphate adsorbed on Fe(III) modified montmorillonite: Surface complexation studied by ATR-FTIR spectroscopy, Colloids and Surfaces A: Physicochem.Eng.Aspects, 353, 238-244.
[26] Brindley G.W. and Sempels R.E. (1977), Preparation and properties of some hydroxy-aluminum beidellites, Clay Minerals, Vol. 12, 229-237.
[27] Caglar B., Afsin B., Tabak A., Eren E. (2009), Characterization of the cation- exchanged benonites by XRD, XRPD, ATR, DTA/TG analyses and BET measurement, Chemical Engineering Journal, 149, 242-248.
[28] Carrado K.A., Kostapapas A. and Suib S.L. (1986), Physical and chemical stabilities of pillared clays containing transitition metal ions, Solid State Ionics, 22, 117 – 125.
[29] Carriazo J.G., Centeno M.A., Odriozola J.A., Moreno S., Molina R. (2007), Effect of Fe and Ce on Al-pillared bentonite and their performance in catalytic oxidation reactions, Applied Catalysis A: General, 317, 120-128.
[30] Chae H.J., Nam I.N., Ham S.W. Hong S.B. (2001), Physicochemical charateristics of pillared interlayered clays, Catalysis Today, 68, 31-40.
[31] Chapman D. (1996). Water quality assessments – A Guide to Use of Biota, Sediments and Water in Environmetal Monitoring, 2st Ed, UNESCO/WHO/UNEP, Great Britain.
[32] Chen J. and Zhu L. (2009), Comparative study of catalytic of different Fe- pillared bentonites in the presence of UV light and H2O2, Separation and Purification Technology, 67, 282-288.
[33] Chen Q., Wu P., Dang Z., Zhu N., Li P., Wu J., Wang X. (2010), Iron pillared vermiculite as a heterogeneous photo-Fenton catalyst for photocatalytic degradation of azo dye reactive brilliant orange X-GN, Separation and Purification Technology, 71, 315-323.
[34] Chorus I. & Mur L. (1999), Preventative measures. Toxic Cyanobacteria in Water: A guide to their public health consequences, monitoring and management. I. Chorus & J. Bartham, E & FN Spon Publishers.
[35] Clem A.G. and Doehler R.W. (1963), Industrial application of bentonite, Clays and Clay minerals, Vol. 10, 272 – 283.
[36] Coelho A.V., Poncelet G. (1991), Gallium, aluminium and mixed gallium- aluminium pillared montmorillonite. Preparation and characterization, Applied Catalysis, 77, 303-314.
[37] Cooke G.D., Welch E.B., Peterson S.A., Nichols S.A. (2005), Restoration and Management of Lakes and Reservoirs. 3rd edition. Editor – Cooke G.D, Taylor an Francis, Boca Raton, Florida. 591 p.
[38] Danh Nguyen-Thanh, Block K., Bandosz T.J. (2005), Adsorption of hydrogen sulfide on montmorillonites modified with iron, Chemosphere, 59, 343-353.
[39] De la Noüe J. and De Pauw N. (1988). The potential of microalgal biotechnology: a review of production and uses of microalgae, Biotechnology Advanvance, 6, 725–770.
[40] Dimov V.I., Ilieva A.V., Khaltakova N.G., Filizova L.D. (2000), Structural Model of Al13-pillared montmorillonite, Clays and Clay Minerals, Vol. 48, No. 1, 1-9.
[41] Ding W., Huang X., Zhang L. (2003), Removal of phosphorous from aqueous solution by lanthanum hydrate, Environmental Science, 24, 110-113.
[42] Domínguez J.M., Botello-Pozos J.C., López-Ortega A., Ramíze M.T., Sandoval-Floros G., Rojas-Hernández (1998), Study of pillar precursors [Ga(III)-Al(III), Ln(III)-Al(III), Zr(IV)] for hydrothermally stable pillared clays, Catalysis Today, 43, 69 – 77.
[43] Edzwald J.K., Toensing D.C., Leung M.C-Y. (1976), Phosphate adsorption reactions with clay minerals, Environmental Science & Technology, 10, 485–490.