Bảng 3.20. Các mô hình ước tính điểm số Ishak 60
Bảng 3.21. Các tham số được ước tính từ mô hình đa biến rút gọn 61
Bảng 3.22. Liên quan giữa độ thanh lọc ICG và suy gan sau phẫu thuật cắt gan lớn
...................................................................................................................................63
Bảng 3.23. Liên quan giữa độ thanh lọc ICG và mức độ suy gan sau phẫu thuật cắt gan lớn 64
Bảng 3.24. Thể tích gan bảo tồn trong nhóm cắt gan lớn 65
Bảng 3.25. Liên quan giữa thể tích gan bảo tồn và suy gan sau phẫu thuật cắt gan lớn 65
Bảng 3.26. Liên quan giữa thể tích gan bảo tồn và mức độ suy gan 66
Bảng 3.27. Liên quan giữa mức độ xơ gan và suy gan sau phẫu thuật cắt gan lớn 67
Bảng 3.28. Thể tích gan bảo tồn ở nhóm RLV/SLV < 40% 68
Có thể bạn quan tâm!
-
 Giá trị tiên lượng chức năng gan của độ thanh lọc indocyanine green trong phẫu thuật cắt gan - 1
Giá trị tiên lượng chức năng gan của độ thanh lọc indocyanine green trong phẫu thuật cắt gan - 1 -
 Đánh Giá Chức Năng Gan Trước Phẫu Thuật Cắt Gan
Đánh Giá Chức Năng Gan Trước Phẫu Thuật Cắt Gan -
 Liên Quan Giữa Độ Thanh Lọc Icg Và Tăng Áp Lực Tĩnh Mạch Cửa
Liên Quan Giữa Độ Thanh Lọc Icg Và Tăng Áp Lực Tĩnh Mạch Cửa -
 Tỉ Lệ Suy Chức Năng Gan Sau Mổ Theo Isgls Của Các Tác Giả (%)
Tỉ Lệ Suy Chức Năng Gan Sau Mổ Theo Isgls Của Các Tác Giả (%)
Xem toàn bộ 138 trang tài liệu này.
Bảng 3.29. Độ thanh lọc ICG ở nhóm RLV/SLV < 40% 68
Bảng 3.30. So sánh tỉ lệ suy gan giữa hai nhóm RLV/SLV trên và dưới 40% 68
Bảng 3.31. So sánh mức độ suy gan giữa hai nhóm RLV/SLV trên và dưới 40% ..69 Bảng 3.32. So sánh tỉ lệ suy gan theo tiêu chuẩn 50-50 giữa hai nhóm RLV/SLV trên và dưới 40% 69
Bảng 3.33. So sánh độ thanh lọc ICG và thể tích gan bảo tồn giữa hai nhóm suy gan và không suy gan trong nhóm RLV/SLV dưới 40% 70
Bảng 3.34. Các mô hình ước tính nguy cơ suy gan sau phẫu thuật cắt gan lớn 71
Bảng 3.35. Các tham số ước tính nguy cơ suy gan từ mô hình đa biến rút gọn 72
Bảng 4.1. So sánh tỉ lệ các mức độ suy gan với các tác giả khác 80
Bảng 4.2. So sánh hiệu quả của các mô hình tiên lượng suy gan sau phẫu thuật cắt gan lớn 94
DANH MỤC CÁC HÌNH
Hình 1.1. Cấu trúc hóa học của Indocyanine Green 3
Hình 1.2. Máy đo độ thanh lọc ICG bằng phương pháp LiMON 6
Hình 1.3. Thể tích gan trái bảo tồn đo bằng chụp X quang cắt lớp vi tính 17
Hình 1.4. Thể tích gan trái bảo tồn đo bằng chụp cộng hưởng từ 17
Hình 2.1. Sưởi ấm tay bệnh nhân và gắn cảm biến của máy và cảm biến SpO2 32
Hình 2.2. Bảng kết quả độ thanh lọc ICG 33
Hình 2.3. Cách xác định ranh giới gan trái khi đánh giá thể tích gan 34
Hình 2.4. Gan trái trước (24/03/2020) và sau PVE (09/04/2020) 35
Hình 2.5. Gan trái trước (21/03/2019) và sau ALPPS thì một (09/04/2019) 35
Hình 2.6. Tổn thương gan 0/6 theo Ishak 36
Hình 2.7. Tổn thương gan 1/6 theo Ishak 36
Hình 2.8. Tổn thương gan 2/6 theo Ishak 36
Hình 2.9. Tổn thương gan 3/6 theo Ishak 37
Hình 2.10. Tổn thương gan 4/6 theo Ishak 37
Hình 2.11. Tổn thương gan 5/6 theo Ishak 37
Hình 2.12. Tổn thương gan 6/6 theo Ishak 38
DANH MỤC CÁC SƠ ĐỒ
Sơ đồ 1.1. Lựa chọn bệnh nhân phẫu thuật cắt gan kết hợp giữa lâm sàng, nồng độ bilirubin máu và ICG-R15 16
Sơ đồ 3.1. Nomogram ước tính điểm số Ishak từ các thông số trong mô hình đa biến rút gọn 62
Sơ đồ 3.2. Nomogram ước tính nguy cơ suy gan sau phẫu thuật cắt gan từ các thông số của mô hình đa biến rút gọn 73
DANH MỤC CÁC BIỂU ĐỒ
Biểu đồ 1.1. Tương quan giữa ICG-R15 và số lượng tiểu cầu 14
Biểu đồ 3.1. Liên quan giữa giới tính và điểm số Ishak 51
Biểu đồ 3.2. Tương quan giữa tuổi và điểm số Ishak 51
Biểu đồ 3.3. Tương quan giữa ICG-R15 trước phẫu thuật và điểm số Ishak 52
Biểu đồ 3.4. Liên quan giữa điểm Child-Pugh và điểm số Ishak 53
Biểu đồ 3.5. Tương quan giữa nồng độ albumin máu trước phẫu thuật và điểm số Ishak 54
Biểu đồ 3.6. Tương quan giữa nồng độ bilirubin máu trước phẫu thuật và điểm số Ishak 54
Biểu đồ 3.7. Tương quan giữa INR trước phẫu thuật và điểm số Ishak 55
Biểu đồ 3.8. Tương quan giữa số lượng tiểu cầu trước phẫu thuật và điểm số Ishak
...................................................................................................................................55
Biểu đồ 3.9. Liên quan giữa ICG-R15 và suy gan sau phẫu thuật cắt gan 57
Biểu đồ 3.10. Liên quan giữa ICG-R15 và mức độ suy gan sau phẫu thuật cắt gan 58
Biểu đồ 3.11. Liên quan giữa ICG-R15 và suy gan sau phẫu thuật cắt gan lớn 63
Biểu đồ 3.12. Liên quan giữa ICG-R15 và mức độ suy gan sau phẫu thuật cắt gan lớn 64
Biểu đồ 3.13. So sánh thể tích gan bảo tồn ở hai nhóm suy gan và không suy gan sau phẫu thuật cắt gan lớn 66
Biểu đồ 3.14. So sánh thể tích gan bảo tồn ở các mức độ suy gan sau phẫu thuật cắt gan lớn 67
Biểu đồ 3.15. So sánh thể tích gan bảo tồn giữa hai nhóm suy gan và không suy gan sau phẫu thuật cắt gan lớn ở nhóm RLV/SLV dưới 40% 70
Biểu đồ 3.16. So sánh ICG-R15 giữa hai nhóm suy gan và không suy gan sau phẫu thuật cắt gan lớn trong nhóm RLV/SLV dưới 40% 70
Biểu đồ 3.17. Hiệu quả của mô hình ước tính nguy cơ suy gan sau phẫu thuật cắt gan lớn 72
ĐẶT VẤN ĐỀ
Suy gan sau phẫu thuật cắt gan là một biến chứng nặng, đe dọa mạng sống bệnh nhân [5], [6], [7], [8], [28], [30], [33], [71], [72], [77], [78], [83],
[101], [102], [103]. Phẫu thuật viên cắt gan phải luôn luôn cân nhắc giữa tính triệt để về mặt ung thư học (cắt gan đủ rộng) và chức năng gan bảo tồn (phần gan còn lại đủ lớn và đảm bảo đủ chức năng).
Đa số phẫu thuật cắt gan tại Việt Nam là để điều trị ung thư tế bào gan, thường xuất hiện trên nền tổn thương gan mạn tính hoặc gan xơ. Vì vậy, việc đánh giá chức năng gan trước phẫu thuật để tiên lượng và ngăn ngừa biến chứng suy gan sau phẫu thuật hết sức quan trọng vì biến chứng này tuy tỉ lệ không cao [1], [5], [6], [7], [8], [28], [72], [102], [103] nhưng tỉ lệ tử vong có thể lên đến
80-100% [7], [72].
Cho đến gần đây, ở nước ta, mặc dù đã có nghiên cứu chứng minh thang điểm Child-Pugh không có mối tương quan với mức độ xơ gan [3] nhưng đây vẫn là phương tiện thường dùng nhất để đánh giá chức năng gan trước phẫu thuật cắt gan. Bên cạnh đó, siêu âm đàn hồi gan và đo thể tích gan bảo tồn cho phép phẫu thuật viên có thể đánh giá được một phần chức năng gan [1], [4] nhưng các phương tiện này chỉ nói lên hình thái chứ không phản ánh được chức năng gan thật sự.
Hiện nay, độ thanh lọc chất Indocyanine green (ICG) được xem là phương pháp đánh giá chức năng gan rất tốt, được ứng dụng rất nhiều trên thế giới, nhất là tại khu vực Châu Á - Thái Bình Dương và được xem là một trong những tiêu chuẩn để quyết định phẫu thuật cũng như mức độ cắt gan, đặc biệt là những trường hợp cần cắt gan lớn (từ 4 hạ phân thùy) [17], [26], [27], [43], [55], [58], [59], [60], [68]. Tuy vậy, điều này vẫn chưa được thống nhất bởi các
tác giả khác [41], [57], [72], [93], [102].
Từ tháng 5 năm 2016, Bộ Y tế Việt Nam đã cho phép sử dụng chất ICG trong đánh giá chức năng gan (Phụ lục) dựa trên những lợi ích mà xét nghiệm này mang lại. Đây là lần đầu tiên trong cả nước, xét nghiệm độ thanh lọc ICG được ứng dụng để đánh giá chức năng gan trước phẫu thuật cắt gan.
Đa phần các trường hợp bệnh nhân có khối u ác tính ở gan nói chung và ung thư tế bào gan (UTTBG) nói riêng tại Việt Nam nhập viện khi bệnh ở giai đoạn muộn, khối u có kích thước lớn, cần phải phẫu thuật cắt gan lớn theo giải phẫu mới có thể đạt được điều trị triệt để cho bệnh nhân. Vì vậy, vai trò đánh giá mức độ xơ gan và tiên lượng suy chức năng sau phẫu thuật cắt gan của độ thanh lọc ICG ở người Việt Nam cần được đặt ra:
“Độ thanh lọc ICG có tương quan với mức độ xơ gan không? Độ thanh lọc ICG có tốt hơn thang điểm Child-Pugh trong đánh giá chức năng gan trước phẫu thuật cắt gan không? Độ thanh lọc ICG có giúp đánh giá tốt nguy cơ suy gan sau phẫu thuật cắt gan không?”
Từ đó, chúng tôi tiến hành đề tài nghiên cứu “Giá trị tiên lượng chức năng gan của độ thanh lọc indocyanine green trong phẫu thuật cắt gan” với ba mục tiêu nghiên cứu sau:
1. Xác định mối tương quan giữa độ thanh lọc ICG và mức độ xơ gan trên giải phẫu bệnh theo thang điểm Ishak.
2. So sánh độ thanh lọc ICG với thang điểm Child-Pugh trong đánh giá chức năng gan trước phẫu thuật cắt gan.
3. Xác định mối liên quan giữa độ thanh lọc ICG và thể tích gan bảo tồn với biến chứng suy chức năng gan sau phẫu thuật cắt gan lớn.
Chương 1. TỔNG QUAN
1.1 Đại cương về Indocyanine green
1.1.1 Giới thiệu về ICG
Indocyanine green (ICG) là chất màu tan trong nước có cấu trúc tricarbocyanin với phổ hấp thụ cực đại tại bước sóng 800nm.
Công thức hóa học của ICG là C43H47N2NaO6S2 với tên hóa học là Sodium 4-[(2Z)-2-[(2E,4E,6E)-7-[1,1-dimethyl-3-(4-sulfonatobutyl)benzo [e]indol-3-ium-2-yl]hepta-2,4,6-trienylidene]-1,1-dimethylbenzo[e]indol-3- yl]butane-1-sulfonate, trọng lượng phân tử là 774, 96g/mol.
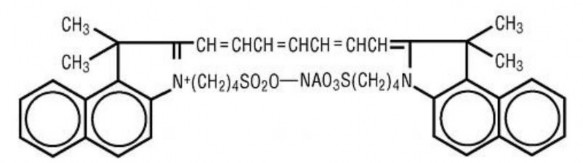
Hình 1.1. Cấu trúc hóa học của Indocyanine Green
1.1.2 Dược lý lâm sàng
Sau khi tiêm tĩnh mạch, ICG sẽ nhanh chóng gắn kết với protein huyết tương, mà albumin là thành phần chuyên chở chính (95%). ICG đi qua tuần hoàn ngoài gan và tuần hoàn gan ruột không đáng kể; định lượng cùng lúc ở máu động mạch và tĩnh mạch cho thấy chất màu này được hấp thu không đáng kể ở thận, ngoại biên, phổi hay não-tủy sống.
ICG được hấp thụ từ huyết tương hầu hết được thải trừ hoàn toàn bởi tế bào gan và xuất tiết hoàn toàn vào đường mật. Khi có tắc nghẽn đường mật, chất màu này xuất hiện trong hệ bạch huyết của gan một cách độc lập với dịch mật, gợi ý rằng niêm mạc đường mật ngăn chặn hoàn toàn sự thấm nhập của
chất màu này mặc dù cho phép bilirubin thấm nhập. Những tính chất này làm cho ICG trở thành một công cụ hữu ích để đánh giá chức năng gan.
Sau khi tiêm tĩnh mạch ICG với liều 0,25-0,5mg/kg thể trọng trên người lớn khỏe mạnh, nồng độ thuốc trong huyết tương giảm theo cấp số nhân. Đường cong thời gian - nồng độ cho thấy thuốc thải qua hai pha với pha thải trừ nhanh trong vòng 15 phút đầu tiên, tiếp theo là pha thải trừ chậm. Trên người lớn khỏe mạnh, thời gian bán thải sinh học của ICG là 3-4 phút.
1.1.3 Ứng dụng của ICG
Chẩn đoán các bệnh lý gan và tiên lượng khả năng hồi phục của gan: xét nghiệm chức năng gan (đo tỉ lệ thải trừ khỏi huyết tương, tỉ lệ còn lại trong máu và dòng máu gan).
Chẩn đoán các bệnh lý tim mạch: xét nghiệm chức năng tim mạch (đo cung lượng tim, thời gian lưu thông trung bình của dòng máu bất thường).
Đánh giá tưới máu của mạch máu và mô.
Xác định hạch bạch huyết canh gác trong các bệnh: ung thư vú, melanoma ác tính.
1.1.4 Chống chỉ định của ICG
ICG không được sử dụng ICG cho người dị ứng với các thành phần của thuốc, và nên được sử dụng thận trọng ở người có tiền sử dị ứng với iod.
1.1.5 Độ an toàn của ICG
ICG được Cục quản lý Thuốc và Thực phẩm của Mỹ (U.S. Food and Drug Administration: FDA) cho phép sử dụng từ năm 1959.
Tác dụng không mong muốn được ghi nhận khi dùng ICG bao gồm:
(1) Rối loạn hệ miễn dịch: sốc phản vệ, phù Quinck
(2) Rối loạn hệ mạch: sốc




