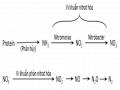
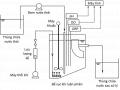
CHƯƠNG 3. KẾT QUẢ VÀ THẢO LUẬN
3.1. Kết quả đánh giá đặc tính nước thải đầu vào
3.1.1. Kết quả nghiên cứu quá trình chuẩn bị mẫu nước.
Do nước thải nghiên cứu là nguồn nước thải nhân tạo được pha chế từ các hóa chất công nghiệp nên đòi hỏi cần có giai đoạn chuẩn bị nước thải thông qua việc pha chế nhiều lần để tìm ra được liều lượng phù hợp nhất cho quá trình vận hành sau này. Thí nghiệm được thực hiện trên cốc đong với thể tích 1 L, lượng hóa chất được tính toán giả định theo lý thuyết và điều chỉnh cho phù hợp sau mỗi lần phân tích. Kết quả thí nghiệm pha chế nước thải điều chỉnh các thông số COD và NH4+ được thể hiện trên Bảng 2.
Bảng 2. Kết quả thí nghiệm điều chế nước thải
COD (mg/L) | NH4+ (mg/L) | ||
Cồn công nghiệp (ml) | NH4Cl (g) | ||
0,62 | 0,446 | 1001,0 | 123,2 |
0,60 | 0,550 | 952,1 | 146,0 |
0,58 | 0,553 | 923,6 | 148,6 |
0,56 | 0,555 | 899,7 | 152,3 |
0,56 | 0,555 | 905,0 | 153,4 |
0,56 | 0,555 | 896,3 | 151,0 |
Có thể bạn quan tâm!
-
 Nghiên cứu Xử lý nước thải giàu chất hữu cơ và Nitơ bằng phương pháp sục khí luân phiên - ĐH Quốc gia Hà Nội - 1
Nghiên cứu Xử lý nước thải giàu chất hữu cơ và Nitơ bằng phương pháp sục khí luân phiên - ĐH Quốc gia Hà Nội - 1 -
 Nghiên cứu Xử lý nước thải giàu chất hữu cơ và Nitơ bằng phương pháp sục khí luân phiên - ĐH Quốc gia Hà Nội - 2
Nghiên cứu Xử lý nước thải giàu chất hữu cơ và Nitơ bằng phương pháp sục khí luân phiên - ĐH Quốc gia Hà Nội - 2 -
 Ứng Dụng Phương Pháp Sục Khí Luân Phiên Trong Xử Lý Nước Thải
Ứng Dụng Phương Pháp Sục Khí Luân Phiên Trong Xử Lý Nước Thải -
 Phương Pháp Phân Tích, Đánh Giá, Xử Lý Số Liệu Thực Nghiệm
Phương Pháp Phân Tích, Đánh Giá, Xử Lý Số Liệu Thực Nghiệm -
 Nghiên cứu Xử lý nước thải giàu chất hữu cơ và Nitơ bằng phương pháp sục khí luân phiên - ĐH Quốc gia Hà Nội - 6
Nghiên cứu Xử lý nước thải giàu chất hữu cơ và Nitơ bằng phương pháp sục khí luân phiên - ĐH Quốc gia Hà Nội - 6 -
 Nghiên cứu Xử lý nước thải giàu chất hữu cơ và Nitơ bằng phương pháp sục khí luân phiên - ĐH Quốc gia Hà Nội - 7
Nghiên cứu Xử lý nước thải giàu chất hữu cơ và Nitơ bằng phương pháp sục khí luân phiên - ĐH Quốc gia Hà Nội - 7
Xem toàn bộ 64 trang tài liệu này.
Ngoài các thông số ô nhiễm chính là COD và NH4+, trong quá trình pha chế nước thải cần bổ sung thêm soda nhằm tăng pH cho nước thải đầu vào, tạo điều kiện tối ưu cho quá trình nitrat hóa diễn ra triệt để. Ngoài ra cũng cần phải bổ sung dinh dưỡng photpho cho vi sinh vật để quá trình xử lý đạt hiệu quả tối
ưu nhất. Trong quá trình thí nghiệm, việc điều chỉnh pH sử dụng soda công nghiệp Na2CO3 đã được tiến hành thử nghiệm nhiều lần. pH của nước thải khi chưa bổ sung soda thường dao động trong khoảng 7,0 – 7,2 và cần điều chỉnh trong khoảng 7,8 – 8,5. Sau nhiều lần tiến hành điều chỉnh pH với các liều lượng Na2CO3 khác nhau, từ đó đi đến kết quả: cần bổ sung cho mỗi 1 L nước thải khoảng 5 ml dung dịch Na2CO3 100 g/L để nâng pH của nước thải ổn định trong khoảng 8,0 – 8,5. Đối với photpho, dựa trên tỷ lệ thực nghiệm C:N:P = 100:5:1 tối ưu cho quá trình xử lý sinh học hiếu khí, tùy theo nồng độ NH4+ mà ta bổ sung photpho bằng muối KH2PO4 cho thích hợp. Trong hầu hết các lần pha, đối với nồng độ NH4+ là 150 mg/l sẽ bổ sung một lượng khoảng 1 ml dung dịch KH2PO4 100 g/L cho mỗi lít nước thải pha.
3.1.2. Kết quả diễn biến các thành phần ô nhiễm trong nước thải
Sau khi tìm được lượng hóa chất phù hợp sử dụng cho việc pha chế nước thải, tiếp tục tiến hành theo dõi diễn biến của các thành phần ô nhiễm trong nước thải theo thời gian. Sỡ dĩ phải theo dõi diễn biễn thành phần ô nhiễm là bởi điều kiện bảo quản nước thải không được đáp ứng tốt (không có nắp đậy thùng nước thải), hơn nữa bản chất của thành phần hữu cơ trong nước thải là cồn công nghiệp, khi để tiếp xúc trong không khí sẽ dễ dàng bị bay hơi. Diễn biến của thành phần COD trong nước thải được thể hiện trong Hình 4.
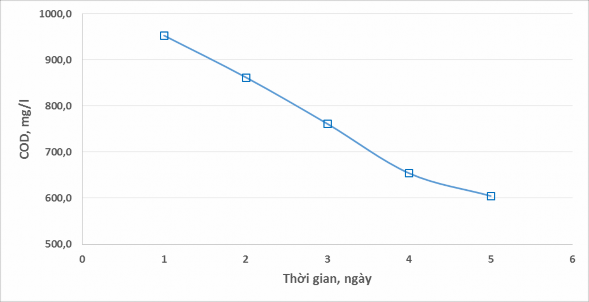
Hình 4. Diễn biến thành phần COD trong nước thải pha
Dựa vào hình vẽ ta có thể dễ dàng nhận thấy giá trị COD của mẫu nước thải pha có sự thay đổi khá rõ rệt qua từng ngày và cụ thể là có xu hướng giảm đều. Sau khoảng thời gian 5 ngày, giá trị COD đã giảm từ 953,0 mg/l trong ngày đầu tiên xuống còn 604,8 mg/l trong ngày thứ 5, bình quân mỗi ngày lượng chất hữu cơ giảm khoảng 10% so với lượng ban đầu. Nguyên nhân của sự biến đổi giá trị COD trong nước thải qua từng ngày là do thùng chứa nước thải không được che đậy cẩn thận khiến ethanol dễ dàng bay hơi thất thoát vào trong môi trường.
Hình 5 thể hiện diễn biến của thành phần NH4+ trong nước thải pha.
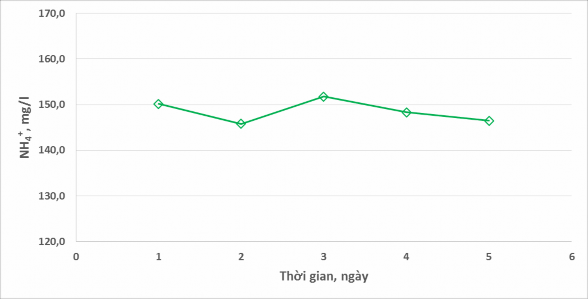
Hình 5. Diễn biến thành phần NH4+ trong nước thải pha
Đối với nồng độ NH4+ nhận thấy gần như không có sự thay đổi qua các ngày ( 150 mg/l). Dựa vào kết quả phân tích được thể hiện trên Hình 5, sở dĩ có sự dao động nhỏ về nồng độ NH4+ là do sai số mắc phải trong quá trình lấy mẫu và phân tích từng ngày. Rõ ràng NH4Cl không phải là hóa chất có thể dễ dàng bay hơi và phân hủy trong điều kiện thường, vì thế nên nồng độ NH4+ trong nước thải không bị thay đổi theo thời gian.
Diễn biến của thông số pH trong nước thải được thể hiện trên Hình 6.
Từ Hình 6 nhận thấy đại lượng pH không có chiều hướng thay đổi theo thời gian. Sau 5 ngày theo dõi, giá trị pH của nước thải vẫn ổn định (8,0 – 8,2).
Có thể giải thích điều này bởi chất hữu cơ có trong nước thải là ethanol không có khả năng thủy phân tạo môi trường kiềm hay axit từ đó làm ảnh hưởng đến pH của nước thải.
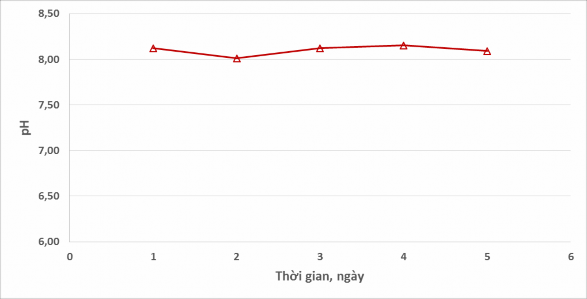
Hình 6. Diễn biến giá trị pH của nước thải pha
Từ các kết quả nghiên cứu về đặc tính cũng như diễn biến của nước thải đã đề cập ở trên dẫn đến quyết định: trong quá trình thực nghiệm hằng ngày, nước thải sẽ được pha mới liên tục với một lượng vừa đủ (trong chế độ khởi động mỗi ngày pha 30 L và trong 2 chế độ 1; 2 mỗi ngày chỉ pha 20 L) tránh lãng phí hóa chất cũng như nguồn nước sạch, đồng thời giảm thiểu tối đa sự biến đổi về thông số ô nhiễm, đặc biệt là COD.
3.2. Kết quả nghiên cứu ảnh hưởng của chu kỳ sục khí – ngừng sục khí đến hiệu suất xử lý chất hữu cơ và Nitơ
3.2.1. Hiệu suất xử lý chất hữu cơ
Sự dao động của các thông số COD đầu vào, đầu ra và hiệu suất xử lý ở điều kiện tỷ lệ (COD/T – N) > 3 của chu kỳ sục khí – ngừng sục khí luân phiên được trình bày trên Hình 7.
Kết quả ở Hình 7 cho thấy COD đầu vào biến động trong khoảng 650 – 1500 mg/l, trong khi đó COD đầu ra ổn định hơn và dao động trong khoảng nhỏ 20 – 150 mg/l, gần như không phụ thuộc vào các chu kỳ sục khí – ngừng
sục khí khác nhau. Hiệu suất xử lý COD trong cả ba chế độ đều ổn định và đạt trong khoảng 85 – 98%. Kết quả này chứng tỏ khi thay đổi chu kỳ sục khí – ngừng sục khí không có sự ảnh hưởng đến hiệu suất xử lý COD, bởi bản chất thành phần chất hữu cơ trong nước thải đầu vào là cồn công nghiệp C2H5OH – một dạng chất hữu cơ rất dễ phân hủy và còn bay hơi theo thời gian.
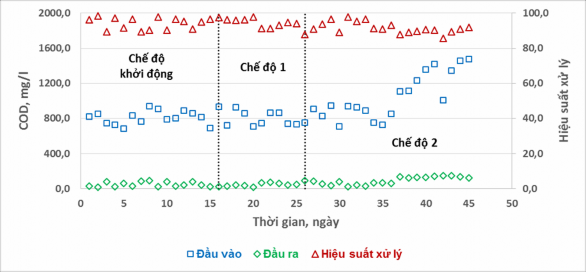
Hình 7. Ảnh hưởng của chu kỳ sục khí – ngừng sục khí đến hiệu suất xử lý COD
So sánh kết quả của nghiên cứu này với các nghiên cứu liên quan khác được thể hiện trên Bảng 3.
Bảng 3. So sánh hiệu quả xử lý COD giữa các nghiên cứu khác nhau
Hiệu suất xử lý (%) | Chu trình xử lý (giờ) | |
Trần Thị Thu Lan (2013) | 80 – 88 | 12 |
Kousei Sasaki (1994) | 95 | 2 |
Yang P. Y. (1999) | 98 | 6 |
Nghiên cứu này | 93 | 6 |
3.2.2. Hiệu suất xử lý Nitơ
a. Hiệu quả xử lý amoni
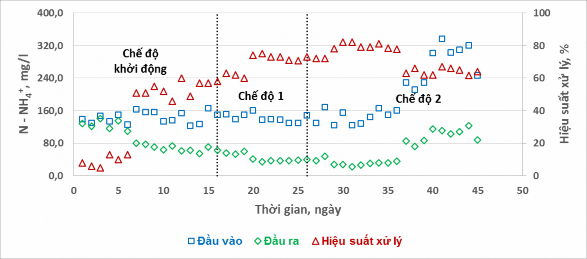
Nồng độ NH4+ trong nước thải đầu vào, trong nước thải sau xử lý và hiệu suất xử lý N – NH4+ ở hai chế độ thí nghiệm được thể hiện trên Hình 8.
Hình 8. Nồng độ N – NH4+ đầu vào, đầu ra và hiệu suất xử lý ở các chế độ khác nhau
Dựa vào biểu đồ có thể nhận thấy các chu kỳ sục khí – ngừng sục khí luân phiên khác nhau có ảnh hưởng khá rõ rệt đến hiệu suất xử lý N – NH4+. Trong chế độ khởi động, hiệu quả xử lý N – NH4+ từ những ngày đầu là rất thấp, gần như không xử lý được. Trong 3 ngày đầu tiên, hiệu suất xử lý chỉ đạt 5 – 8%. Nguyên nhân của việc không xử lý được N – NH4+ trong nước thải của hệ thí nghiệm được cho là pH trong bể phản ứng quá thấp 5,5 – 6,0 không tạo được điều kiện tối ưu cho quá trình nitrat hóa. Vì vậy, trong quá trình thực nghiệm sau này đã lưu ý đến việc điều chỉnh pH nước thải đầu vào và trong bể phản ứng. Trong 3 ngày tiếp theo (ngày thứ 4 đến ngày thứ 6), mặc dù đã điều chỉnh pH cho phù hợp nhưng hiệu suất xử lý mang lại vẫn gần như không thay đổi, chỉ đạt từ 10 – 12%. Nguyên nhân tiếp theo được xác định ở đây là do thiếu nguồn dinh dưỡng photpho cho quá trình xử lý vi sinh, bùn gặp phải tình trạng khó lắng. Chính vì vậy, trong những ngày tiếp theo đã bổ sung thành phần photpho trong nước thải đầu vào. Kể từ ngày thứ 7 sau khi đã đồng thời điều chỉnh pH và bổ sung photpho, hiệu suất xử lý N – NH4+ đạt được đã có dấu
+
hiệu khả quan hơn 46 – 60%. Tuy hiệu suất xử lý đã tăng nhiều so với những ngày đầu vận hành nhưng kết quả đạt được chưa thực sự cao. Điều này có thể giải thích là do thời gian sục khí trong chế độ khởi động vẫn chưa đủ cho quá trình nitrat hóa xảy ra hoàn toàn (90 phút). Từ đó, chế độ thí nghiệm về sau đã được chuyển sang 6 giờ/chu trình làm việc với thời gian sục khí tăng lần lượt là 3 giờ và 4 giờ. Sau quá trình thay đổi chế độ, dễ dàng nhận thấy qua biểu đồ hiệu quả xử lý N – NH4+ đã được cải thiện đáng kể. Hiệu suất xử lý N – NH4 trong chế độ 1 dao động trong khoảng 60 – 75% trong khi đó chế độ 2 đạt kết quả tốt hơn 72 – 82% (với cùng tải trọng NH4+).
b. Hiệu quả xử lý T – N
Nồng độ T – N đầu vào, đầu ra và hiệu suất xử lý T – N của các chế độ thí nghiệm được thể hiện trên Hình 9.
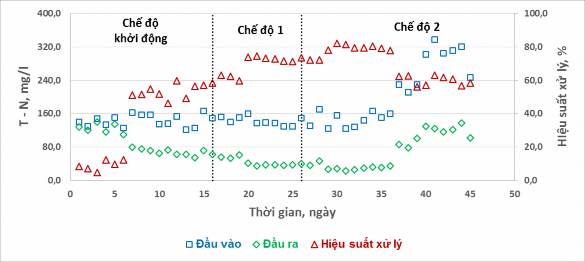
Hình 9. Hiệu quả xử lý T – N ở các chế độ thí nghiệm khác nhau
Kết quả trên Hình 9 cho thấy, chu kỳ sục khí – ngừng sục khí khác nhau có ảnh hưởng đến hiệu suất xử lý T – N. Trong chế độ khởi động, hiệu suất xử lý T – N đạt 47 – 60% trong những ngày ổn định, những ngày đầu vận hành chưa điều chỉnh pH và bổ sung photpho thì hiệu quả xử lý còn rất thấp. Khi chuyển sang vận hành chế độ 1, hiệu suất xử lý T – N đã tăng lên rõ rệt, dao động trong khoảng 60 – 75%. Điều này có thể giải thích do thời gian sục khí trong chế độ 1 lâu hơn chế độ khởi động (3 giờ và 1,5 giờ), thời gian lưu nước lâu hơn (2 ngày và 1 ngày) nên hiệu quả xử lý tốt hơn. Hiệu quả xử lý đạt được
ở chế độ 2 là khả quan hơn cả (72 – 82% khi so sánh với cùng tải trọng) do thời gian sục khí trong chế độ 2 lâu hơn so với chế độ 1 (4 giờ và 3 giờ) nên quá trình nitrat hóa hiệu quả hơn.
So sánh kết quả của nghiên cứu này với các nghiên cứu liên quan khác được thể hiện trên Bảng 4.
Bảng 4. So sánh hiệu quả xử lý T – N với các nghiên cứu khác
Hiệu suất xử lý (%) | Chu trình xử lý (giờ) | |
Trần Thị Thu Lan (2013) | 99,0 | 12 |
Kousei Sasaki (1994) | 89,4 | 2 |
Yang P. Y. (1999) | 92,4 | 6 |
Koottatep S. (1994) | 45,0 | 12 |
Katsuto Inomae (1987) | 81,0 | 0,75 |
Nghiên cứu này | 78,1 | 12 |
c. Sự chuyển hóa nitrat và nitrit của quá trình
Sự thay đổi tổng nồng độ nitrat và nitrit trong hệ thí nghiệm ở hai chế độ được thể hiện trên Hình 10.
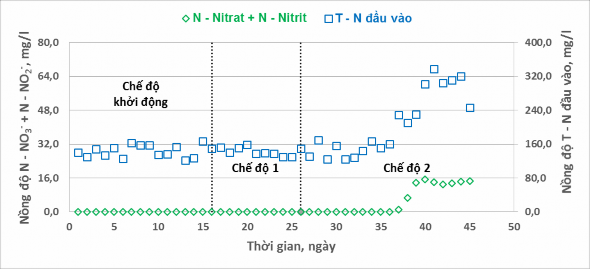
Hình 10. Quá trình chuyển hóa nitrit và nitrat ở các chế độ khác nhau