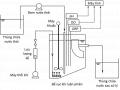
Nghiên cứu hiệu quả xử lý COD, N – NH4+, T – N bằng phương pháp sục khí luân phiên.
Đánh giá nồng độ các thành phần NH4+, NO3-, NO2-, T – N và COD qua từng bước xử lý cũng như tính ổn định của hệ thống và khả năng ứng dụng phương pháp trong điều kiện việt nam
CHƯƠNG 1. TỔNG QUAN
1.1. Chất hữu cơ và hợp chất chứa Nitơ trong nước thải
1.1.1. Các chất hữu cơ
Dựa vào khả năng có thể phân hủy nhờ vi sinh vật có trong nước mà ta có thể phân các chất hữu cơ thành hai nhóm:
a. Các chất hữu cơ dễ bị phân hủy
Có thể bạn quan tâm!
-
 Nghiên cứu Xử lý nước thải giàu chất hữu cơ và Nitơ bằng phương pháp sục khí luân phiên - ĐH Quốc gia Hà Nội - 1
Nghiên cứu Xử lý nước thải giàu chất hữu cơ và Nitơ bằng phương pháp sục khí luân phiên - ĐH Quốc gia Hà Nội - 1 -
 Ứng Dụng Phương Pháp Sục Khí Luân Phiên Trong Xử Lý Nước Thải
Ứng Dụng Phương Pháp Sục Khí Luân Phiên Trong Xử Lý Nước Thải -
 Phương Pháp Phân Tích, Đánh Giá, Xử Lý Số Liệu Thực Nghiệm
Phương Pháp Phân Tích, Đánh Giá, Xử Lý Số Liệu Thực Nghiệm -
 Kết Quả Đánh Giá Đặc Tính Nước Thải Đầu Vào
Kết Quả Đánh Giá Đặc Tính Nước Thải Đầu Vào -
 Nghiên cứu Xử lý nước thải giàu chất hữu cơ và Nitơ bằng phương pháp sục khí luân phiên - ĐH Quốc gia Hà Nội - 6
Nghiên cứu Xử lý nước thải giàu chất hữu cơ và Nitơ bằng phương pháp sục khí luân phiên - ĐH Quốc gia Hà Nội - 6 -
 Nghiên cứu Xử lý nước thải giàu chất hữu cơ và Nitơ bằng phương pháp sục khí luân phiên - ĐH Quốc gia Hà Nội - 7
Nghiên cứu Xử lý nước thải giàu chất hữu cơ và Nitơ bằng phương pháp sục khí luân phiên - ĐH Quốc gia Hà Nội - 7
Xem toàn bộ 64 trang tài liệu này.
Đó là các hợp chất protein, hidratcacbon, chất béo có nguồn gốc động vật và thực vật. Đây là các chất gây ô nhiễm chính có nhiều trong nước thải sinh hoạt, nước thải từ các xí nghiệp chế biến thực phẩm. Các hợp chất này chủ yếu làm suy giảm oxy hòa tan trong nước dẫn đến suy thoái tài nguyên thủy sản và làm giảm chất lượng nước cấp sinh hoạt.
b. Các chất hữu cơ khó bị phân hủy
Các chất loại này thuộc các chất hữu cơ có vòng thơm (hidrocacbua của dầu khí), các chất đa vòng ngưng tụ, các hợp chất clo hữu cơ, photpho hữu cơ… Trong số các chất này có nhiều hợp chất là các chất hữu cơ tổng hợp. Hầu hết chúng là các chất có độc tính đối với sinh vật và con người. Chúng tồn lưu lâu dài trong môi trường và cơ thể sinh vật gây độc tích lũy, ảnh hưởng nguy hại đến cuộc sống.
Trong nguồn nước tự nhiên, hàm lượng các chất hữu cơ rất thấp, ít có ảnh hưởng đến nước sinh hoạt, nuôi trồng thủy sản và tưới tiêu thủy lợi. Khi bị ô nhiễm thì hàm lượng các chất hữu cơ có trong nước sẽ tăng cao.
1.1.2. Các hợp chất chứa Nitơ
Hợp chất chứa Nitơ trong nước thường tồn tại ở ba dạng: hợp chất hữu cơ, amoniac và dạng oxi hóa (nitrat, nitrit). Các dạng này là các khâu trong chuỗi phân hủy hợp chất chứa Nitơ hữu cơ, ví dụ: protein và hợp phần của protein.
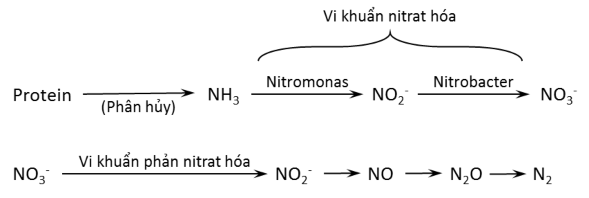
Hình 1. Chuỗi phân hủy hợp chất chứa Nitơ hữu cơ
Nếu nước chứa hầu hết các hợp chất Nitơ hữu cơ, amoniac hoặc NH4OH thì chứng tỏ nước mới bị ô nhiễm. NH3 trong nước sẽ gây độc với cá và sinh vật khác trong nước.
Nếu trong nước có hợp chất N chủ yếu là nitrit (NO2-) là nước đã bị ô nhiễm một thời gian dài hơn.
Nếu nước chủ yếu là hợp chất N ở dạng nitrat (NO3-) chứng tỏ quá trình phân hủy đã kết thúc. Tuy vậy, các nitrat chỉ bền ở điều kiện hiếu khí, khi ở điều kiện thiếu khí hoặc kỵ khí các nitrat dễ bị khử thành N2O, NO và Nitơ phân tử tách khỏi nước bay vào không khí.
Amoniac (NH3): amoniac trong nước tồn tại ở dạng NH3 và NH4+ (NH4OH, NH4NO3, (NH4)2SO4...) tùy thuộc vào pH của nước vì nó là một bazơ yếu. NH3 và NH4+ có trong nước cùng với photphat sẽ thúc đẩy quá trình phú dưỡng của nước.
Nitrat (NO3-): là sản phẩm cuối cùng của quá trình phân hủy các hợp chất hữu cơ chứa N có trong nước thải của người và động vật.
1.2. Ảnh hưởng của Nitơ đối với môi trường và sức khỏe con người
Amoni hầu như không có ảnh hưởng trực tiếp tới sức khoẻ con người, nhưng trong quá trình khai thác, lưu trữ và xử lý...amoni được chuyển hoá thành nitrit (NO2-) và nitrat (NO3-) là những chất có tính độc hại đối với con người. Nitrit là chất rất độc vì nó có thể chuyển hoá thành nitroamin, chất này có khả
năng gây ung thư cho con người. Nitơ tồn tại trong hệ thuỷ sinh ở nhiều dạng hợp chất vô cơ và hữu cơ, các dạng Nitơ vô cơ cơ bản tồn tại với tỉ lệ khác nhau tuỳ thuộc vào điều kiện của môi trường nước. Nitrat là muối Nitơ vô cơ trong môi trường nước được sục khí đầy đủ và liên tục, nitrit tồn tại trong điều kiện đặc biệt, còn amoniac (NH3) và ion NH4+ tồn tại trong điều kiện kỵ khí. Amoniac hoà tan trong nước tạo thành dạng hyđrôxit amoni (NH4OH) và sẽ phân ly thành ion NH4+ và OH-. Quá trình oxi hoá có thể chuyển tất cả các dạng Nitơ vô cơ thành ion nitrat, còn quá trình khử sẽ chuyển hoá chúng thành dạng ion amoni.
Nitơ không những chỉ có thể gây ra các vấn đề phì dưỡng mà khi chỉ tiêu N – NO3- trong nước cấp sinh hoạt vượt quá 45 mg/l sẽ gây ra mối đe doạ nghiêm trọng đối với sức khỏe con người. Một số nghiên cứu ở Nepan đã khẳng định khi hàm lượng NO3- trên 45 mg/l sẽ khiến cho dân cư dùng thường xuyên nguồn nước này bị mắc các bệnh ung thư về dạ dày, thực quản và bệnh tiểu đường.
Trong đường ruột trẻ nhỏ thường tìm thấy loại vi khuẩn có thể chuyển hoá nitrat thành nitrit. Nitrit có ái lực với hồng cầu trong máu mạnh hơn oxy, khi nó thay thế oxy sẽ tạo thành methermoglobin, hợp chất này không thể nhận oxy và gây ra bệnh xanh xao ở trẻ nhỏ (methermoglobinemia), thậm chí có thể gây tử vong. Những đứa trẻ sơ sinh trong giai đoạn mới được 6 tháng tuổi dễ bị mắc căn bệnh này vì hàm lượng enzym methaemoglobin reductase tương đối thấp – đây là một loại enzym có khả năng chuyển hoá methermoglobin trở lại thành hemoglobin.
Ngoài Mỹ, một số nước Đông Âu, mức độ nhiễm độc nguồn nước sinh hoạt lấy từ giếng lên cũng rất cao. Ví dụ tại Transylvania ở Rumani trong thời gian từ 1990 – 1994 trung bình cứ 100.000 trẻ em sơ sinh thì có tới 24 đến 363 ca nhiễm độc. Độ nguy hiểm của NO3- đã khiến người Mỹ quy định trong Đạo luật về An toàn Nguồn nước Sinh hoạt của Mỹ (SDWA – Safe Drinking Water Act) hàm lượng N – NO3- tối đa là 10 mg/l [15].
Ngoài ra, nếu trong nước tồn tại amoni sẽ làm giảm hiệu quả của khâu clo hoá sát trùng là bước cuối cùng trong quá trình xử lý nước hiện hành, nhằm
đảm bảo nước hoàn toàn an toàn về mặt vi sinh khi đến tay người tiêu dùng. Khi có mặt amoni, hợp chất này phản ứng ngay với clo tạo thành cloramin (bao gồm monochloramine, dichloramine, trichloramine, organochloramine) có tính sát khuẩn kém hàng trăm lần so với clo nguyên tố. Bên cạnh đó amoni là nguồn dinh dưỡng cho các sinh vật nước, tảo sinh trưởng và phát triển. Sự phát triển này làm ô nhiễm nước thứ cấp trong quá trình lưu trữ, đồng thời sinh ra các chất độc nitrit và nitrat.
1.3. Các phương pháp xử lý chất hữu cơ và Nitơ trong nước thải
1.3.1. Các phương pháp xử lý chất hữu cơ
Người ta sử dụng các phương pháp sinh học để làm sạch nước thải khỏi các chất hữu cơ hòa tan và một số chất vô cơ như H2S, các sunfit, amoniac, Nitơ,… Phương pháp này dựa trên cơ sở sử dụng hoạt động của vi sinh vật để phân hủy các chất hữu cơ gây ô nhiễm trong nước thải. Các vi sinh vật sử dụng các chất hữu cơ và một số chất khoáng làm nguồn dinh dưỡng và tạo năng lượng. Trong quá trình dinh dưỡng, chúng nhận các chất dinh dưỡng để xây dựng tế bào, sinh trưởng và sinh sản nên sinh khối của chúng được tăng lên. Quá trình phân hủy các chất hữu cơ nhờ vi sinh vật gọi là quá trình oxy hóa sinh hóa .
Như vậy, nước thải có thể được xử lý bằng phương pháp sinh học sẽ được đặc trưng bởi chỉ tiêu BOD hoặc COD. Để có thể xử lý bằng phương pháp này, nước thải sản xuất cần không chứa các chất độc và tạp chất, các muối kim loại nặng hoặc nồng độ của chúng không được vượt quá nồng độ cực đại cho phép và có tỷ số BOD/COD ≥ 0,5.
Các quá trình sinh học dùng trong xử lý nước thải đều có xuất sứ trong tự nhiên. Nhờ thực hiện các biện pháp tăng cường hoạt động của vi sinh vật trong các công trình nhân tạo, quá trình làm sạch các chất bẩn diễn ra nhanh hơn. Trong thực tế hiện nay người ta vẫn tiến hành xử lý nước thải bằng phương pháp sinh học ở điều kiện tự nhiên và điều kiện nhân tạo tùy thuộc vào khả năng kinh phí, yêu cầu công nghệ, địa lý cùng hàng loạt các yếu tố khác. Nói chung, các quá trình sinh học trong xử lý nước thải gồm 5 nhóm quá trình chủ yếu sau:
Quá trình hiếu khí
Quá trình kỵ khí
Quá trình trung gian – anoxic
Quá trình tùy nghi
Quá trình ở ao hồ
Từ những quá trính chủ yếu này lại thêm các quá trình phụ, như quá trình sinh trưởng lơ lửng, sinh trưởng dính bám...
1.3.2. Các phương pháp xử lý Nitơ
Để xử lý amoni trong nước thải có thể sử dụng các phương pháp hóa lý (sục khí đuổi amoniac trong môi trường kiềm, hấp phụ, trao đổi ion...), hóa học (oxi hóa bằng các chất oxi hóa gốc clo), các phương pháp lọc màng (UF – Nano, RO), hoặc phương pháp sinh học.
a. Phương pháp clo hóa tới điểm đột biến
Bản chất của phương pháp là quá trình oxy hóa – khử xảy ra giữa clo khi hòa tan vào trong nước có chứa amoniac và amoni tạo thành các cloramin. Nếu clo dư, các cloramin sẽ bị phân hủy thành khí N2. Tuy phương pháp clo hóa nhìn chung rất đơn giản và rẻ về mặt thiết bị cũng như xây dưng cơ bản nhưng rất khó áp dụng vì dư lượng clo nếu quá lớn sẽ gây khó khăn cho các nhà máy trong việc giải quyết vấn đề an toàn sức khỏe.
b. Phương pháp thổi khí ở pH cao
Amoni ở trong nước tồn tại dưới dạng cân bằng:
4
NH+ ⇌ NH
3 (khí hòa tan)
+ H+ với pK
= 9,5 (1.1)
a
Như vậy, ở pH gần 7 chỉ có một lượng rất nhỏ khí NH3 so với amoni. Nếu ta nâng pH tới 9,5; tỷ lệ [NH3]/[NH4+] = 1, và càng tăng pH cân bằng càng chuyển về phía tạo thành NH3. Khi đó nếu áp dụng các kỹ thuật sục hoặc thổi khí thì NH3 sẽ bay hơi theo định luật Henry, làm dịch chuyển cân bằng về phía phải:
4
NH+ + OH- ⇌ NH3
↑ + H2
O (1.2)
Trong thực tế pH phải nâng lên xấp xỉ 11, lượng khí cần để đuổi NH3 ở mức 1600 m3 không khí/1m3 nước và quá trình rất phụ thuộc vào nhiệt độ môi trường. Phương pháp này áp dụng được cho nước thải, tuy nhiên khó có thể xử lý triệt để N – amoni và cũng không có khả năng xử lý Nitơ trong các hợp chất hữu cơ.
c. Phương pháp sinh học
Để xử lý nước thải người ta có thể sử dụng phương pháp vật lý, hóa lý và hóa học; nhưng xu hướng ngày nay thường sử dụng phương pháp sinh học cho các hệ xử lý nói chung bởi những tính năng ưu việt mà phương pháp này mang lại. Trong rất nhiều nghiên cứu, các nhà khoa học đã chứng minh xử lý bằng phương pháp sinh học đã mang lại cho con người những lợi điểm như sau: hiệu suất xử lý cao: từ 80 – 90% và có thể là 90 – 99%, ít sử dụng hoá chất, chi phí năng lượng cho một đơn vị thể tích xử lý thấp so với các phương pháp khác và do những ưu điểm trên nên phương pháp sinh học mang tính kinh tế rất cao.
Trong phương pháp này, amoni sẽ bị chuyển hoá thành nitrat rồi thành N2 nhờ hoạt tính của vi sinh vật trong tự nhiên. Trong quá trình xử lý, vi sinh vật sẽ được tạo các điều kiện về dinh dưỡng cũng như các yếu tố khác để có thể đạt được hoạt tính cao nhất… Ở phương pháp sinh học có thể thực hiện bao gồm hai quá trình nối tiếp là nitrat hoá và khử nitrat hoá.
Như đã nói ở trên, công nghệ xử lý Nitơ trong nước thải bằng phương pháp sinh học đã được nghiên cứu và đưa vào ứng dụng thực tế từ những năm 1960. Trên thực tế, có rất nhiều quy trình công nghệ xử lý Nitơ bằng phương pháp sinh học khác nhau. Chúng giống nhau ở nguyên lý là thực hiện các quá trình nitrat hoá và khử nitrat hoá nhưng khác nhau ở cách sắp xếp trình tự các quá trình trong sơ đồ xử lý và nguồn cacbon sử dụng. Các quá trình này có thể là các quá trình sinh trưởng lơ lửng, sinh trưởng bám dính hay sinh trưởng lơ lửng – bám dính kết hợp. Sau đây là một số qui trình cơ bản thường được ứng dụng trong xử lý Nitơ trong nước thải.
Trong quy trình (a) Hình 2 cho hiệu suất xử lý cao (70 – 90%) vì toàn bộ nitrat sinh ra trong bể hiếu khí sẽ được đưa qua quá trình khử nitrat. Trong quy trình này, quá trình tái sục khí tiếp theo quá trình khử nitrat là cần thiết nhằm xử lý thành phần hữu cơ dư sau khử nitrat. Quy trình công nghệ này có nhược điểm là phức tạp, cần phải bổ sung cơ chất hữu cơ cho quá trình khử nitrat.
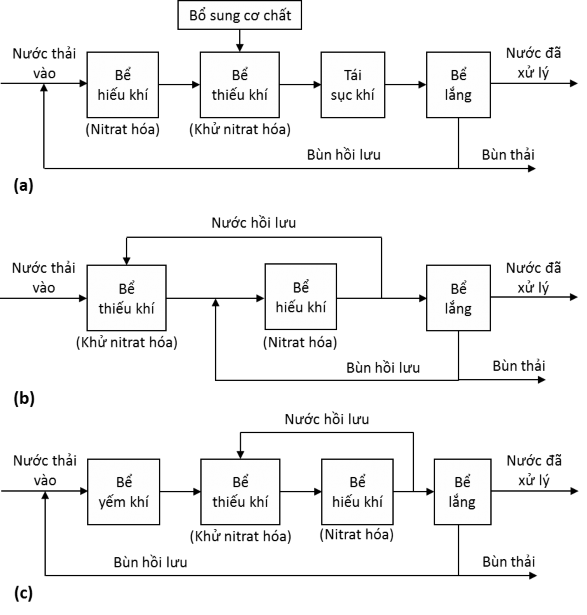
Hình 2. Một số quy trình công nghệ xử lý Nitơ trong nước thải