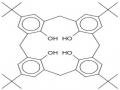
NMR của hợp chất calixaren tương đối đơn giản vì phân tử của chúng có tính chất đối xứng. Trong cấu hình dạng cone xuất hiện cặp pic đôi ở 3,2 ppm và 4,9 ppm là dao động của các proton trong cầu nối metylen. Dao động của các proton trong nhân thơm trong khoảng 7-8 ppm, proton của nhóm -OH cho dao động trong khoảng từ 8- 10 ppm, tùy thuộc vào kích thước phân tử calixaren [65].
1.1.6. Vài nét về ứng dụng của calixaren
Như chúng tôi đã trình bày ở trên, có hai hướng chính để tổng hợp dẫn xuất calixaren là tạo dẫn xuất lower rim và dẫn xuất upper rim. Đối với hướng lower rim, các dẫn xuất tạo ra thường được phát triển các dẫn xuất calixaren mới có tính ứng dụng cao trong trong phân tích và tách chiết. Ngoài ra, calixaren còn được sử dụng trong các lĩnh vực khác như nghiên cứu điện hóa, cảm biến hóa học, sắc kí, màng vận chuyển…
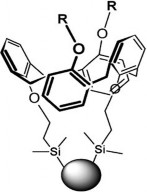
Hình 1.5. Cấu trúc của pha tĩnh silica-calix[4]aren trong kĩ thuật HPLC.
Trong các ứng dụng nêu trên, sử dụng dẫn xuất lower rim calixaren làm tác nhân chiết thu hút được rất nhiều sự quan tâm của các nhà khoa học. Các nghiên cứu đã công bố cho thấy khả năng chiết, tách của các dẫn xuất lower rim calixaren rất phong phú và đa dạng. Trong phần này, chúng tôi chỉ trình bày một số nghiên cứu nổi bật trong tách chiết và làm giàu trong thời gian gần đây. Chẳng hạn, chiết các ion kim loại nhóm IA như Li+, Na+, K+ đặc biệt là Cs+ đã được nghiên cứu bởi tác giả Li và cộng sự với dẫn xuất calixaren, hiệu suất chiết đặc biệt cao đối với ion Cs+ (hình 1.6) [40] hoặc nghiên cứu của Yatifan cho biết đã chiết được Na+, K+, Cs+ bằng một loại dẫn xuất calixaren [161]. Chiết ion kim loại chuyển tiếp được các nhà
Có thể bạn quan tâm!
-
 Nghiên cứu khả năng tạo phức của một số dẫn xuất mới của azocalixaren với ion kim loại và ứng dụng trong phân tích - 1
Nghiên cứu khả năng tạo phức của một số dẫn xuất mới của azocalixaren với ion kim loại và ứng dụng trong phân tích - 1 -
 Phức Hai Nhân Của Azocalixaren (22) Với Ion Kim Loại.
Phức Hai Nhân Của Azocalixaren (22) Với Ion Kim Loại. -
 Vài Nét Về Hóa Học Siêu Phân Tử Và Phức Host-Guest
Vài Nét Về Hóa Học Siêu Phân Tử Và Phức Host-Guest -
 Một Số Thuốc Thử Hữu Cơ Dùng Để Xác Định Chì
Một Số Thuốc Thử Hữu Cơ Dùng Để Xác Định Chì
Xem toàn bộ 130 trang tài liệu này.
hóa học quan tâm hàng đầu, chẳng hạn như Gong và cộng sự đã chiết thành công ion Hg(II) bằng 1,3-dipropyn-2-yl-oxycalix[4]aren với hiệu suất chiết rất cao đến 99,1% [66]. Agrawal và nhóm nghiên cứu sử dụng dẫn xuất 37, 38, 39, 40, 41, 42- hexahydroxy-7,25,31-calix[6]crown hydroxamic acid để khảo sát cơ chế chiết Cr(VI), Mo(VI), W(VI) [21]. Torgov và cộng sự lại dùng calixaren phosphin để chiết Zn(II) và Ru(II) [153]. Alpoguz và nhóm nghiên cứu nghiên cứu thành công việc dùng màng lỏng chứa dẫn xuất calix[4]aren để tách Hg(II) từ dung dịch [24].
Tác giả Kostin và cộng sự sử dụng calix[4,6]aren với 4 hoặc 6 nhóm phosphin oxit tại vị trí upper và lower rim để chiết các ion kim loại chuyển tiếp hóa trị II. Hằng số chiết của quá trình này cũng đã được khảo sát với ion Cu(II), Co(II) và Ni(II). Do kích thước của dẫn xuất upper rim phosphoryl calix[4]aren lớn nên tạo được phức dạng M2L. Trong khi đó, phức chất ML2 được hình thành với dẫn xuất lower rim phosphorylated calix[4]aren [88]. Ludwig sử dụng calix[4,6,8]aren với nhóm chức pyridino tại vòng dưới để chiết Tc(VII) [106].
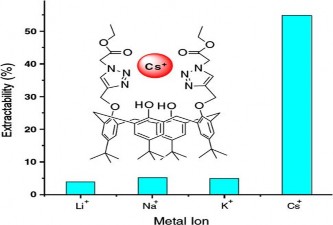
Hình 1.6. Chiết Cs+ từ nước thải phóng xạ bằng triazol calix[4]dietyleste.
Chiết tách ion kim loại nhóm lantanit và actinit cũng được quan tâm nghiên cứu. Sansone và cộng sự sử dụng calix[6]aren và calix[8]aren với vai trò là phối tử để chiết Ln(III) từ nước thải phóng xạ [134]. Matulkova ở Czech đã tổng hợp calix[4]aren với 4 nhóm chức chứa axit phosphoric tại vị trí lower rim để chiết nhóm La(III), Eu(III) và Yb(III) [109]. Tác giả Jain chiết được U(VI) và Th(IV) từ
dung dịch bằng calix[4]aren-o-vanillinsemicarbazon [73]. Một nhóm nghiên cứu khác đã tổng hợp được loại nhựa mới khi phối hợp p-octasulfonato-calix[8]aren và polyvinylamin. Sau đó sử dụng nhựa này để chế tạo màng hấp thụ các ion nguyên tố đất hiếm từ dung dịch muối clorua (LaCl3, CeCl3, PrCl3 và SmCl3) [117]. Tác giả Yaftian đã chiết Th(IV) và Eu(III) bằng dẫn xuất phosphoryl calix[4]aren vào diclometan [162].
Ngoài ra, các nghiên cứu về khả năng chiết đa dạng của calixaren cũng đã được khẳng định trong các bài báo tổng quan. Arora và cộng sự đã tổng kết các công trình ứng dụng của calixaren trong cảm biết hóa học và tách chiết [26]. Creaven và cộng sự đã công bố một bài báo tổng hợp các nghiên cứu trên tạp chí Coordination Chemistry Reviews; theo đó, các tác giả đã có bức tranh toàn cảnh về các ứng dụng của calixaren từ trên 300 bài báo về lĩnh vực này trên các tạp chí khác nhau như tách chiết, trắc quang, điện hóa, cảm biến, màng vận chuyển, sắc kí [40]. Tác giả Ludwig đã có một bài tổng quan dựa trên 487 tài liệu tham khảo về ứng dụng trong phân tích và tách chiết của calixaren trên tạp chí Fresenius. J. Anal. Chem. [105]. Các công trình của tác giả Sliwa được tập hợp từ trên 200 bài báo nghiên cứu khác nhau cho thấy khả năng ứng dụng rất phong phú của các lower calixaren với các ion kim chuyển tiếp, ion nhóm lantan và nhóm actini [143-145]. Từ đó đến nay đã có thêm rất nhiều công trình nghiên cứu được công bố trên các tạp chí khoa học uy tín. Điều đó cho thấy ưu thế vượt trội của calixaren trong tách chiết và làm giàu.
1.2. Tổng quan về azocalixaren
Đối với hướng upper rim, một trong những loại dẫn xuất được các nhà khoa học quan tâm nhiều đó là tạo ra các nhóm chức mang màu như nhóm azo N=N. Với một hoặc nhiều nhóm azo liên hợp với nhân thơm, loại dẫn xuất này có nhiều tên gọi khác nhau như azocalixaren hoặc dẫn xuất diazotizated calixaren. Trong phần này, chúng tôi trình bày một số vấn đề về tổng hợp, đặc tính phổ, khả năng tạo phức, tách chiết và cảm biến hóa học của azocalixaren.
1.2.1. Tổng hợp azocalixaren
Azocalixaren đầu tiên được tổng hợp bởi Shinkai vào những năm 1990 của thế kỉ trước [140]. Nhóm nghiên cứu này đã thực hiện phản ứng azo hóa giữa calix[4]aren với ion benzendiazonium trong tetrahydrofuran ở nhiệt độ 5oC trong pyridin. Kết quả thu được là các dẫn xuất azocalixaren với các nhóm thế khác nhau. Sau đó, Nomura và cộng sự cũng tổng hợp được một số dẫn xuất azocalixaren mới và nghiên cứu khả năng tạo phức của các hợp chất này với ion kim loại [121]. Tùy theo các nhóm thế khác nhau, mỗi azocalixaren được tổng hợp theo những quy trình
khác nhau. Tuy nhiên, nguyên tắc tổng hợp chung là dùng phản ứng azo hóa giữa calix[n]aren với các hợp chất hữu cơ. Chẳng hạn như quy trình tổng hợp của nhóm tác giả Karci thuộc Khoa Hoá - Trường Đại học Pamukakale-Thổ Nhĩ Kì công bố như sau: Chuẩn bị dung dịch muối 2-chlorophenyldiazonium clorua bằng cách cho 2-cloroanilin (1,28 g,10 mmol), NaNO2 (0,69 g, 10 mmol) và HCl (7 mL) vào 25
mL H2O, sau đó thêm từ từ vào dung dịch ở 5oC chứa calix[4]aren (1,0 g, 2,36
mmol) và CH3COOONa.3H2O (4,08 g, 30 mmol) trong dung môi hỗn hợp H2O- DMF (26 mL, 5:8 v/v). Sản phẩm thu được là các dẫn xuất azocalixaren (2)(13) có màu vàng sậm [80]. Tác giả người Trung Quốc là Ma và cộng sự tổng hợp được 5,17-bis(quinolyl-8-azo)-25,26,27,28-tetrahydroxycalix[4]aren (1) bằng cách cho 8- aminoquinolin phản ứng với calix[4]aren trong DMF ở nhiệt độ 0-5oC [107]. Một nghiên cứu khác của Karci và cộng sự cho biết họ tổng hợp được một loạt dẫn xuất o-, m-, p-cloroanilin, o-, m-, p-nitroanilin, o-, m-, p-toluidin, m-, p-anisidin và anilin azocalix[6]aren (14–19) (xem hình 1.7 và 1.8) [81].
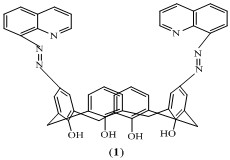
Hình 1.7. Dẫn xuất 5,17-bis(quinolyl-8-azo)-25,26,27,28-tetrahydroxycalix[4]aren.
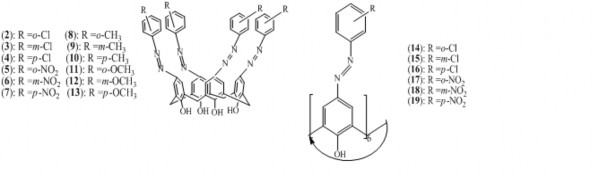
Hình 1.8. Công thức cấu tạo của một số azocalix[4]aren và azocalix[6]aren.
Nhóm nghiên cứu của Sener đã tổng hợp được 6 dẫn xuất azocalixaren bằng cách cho nitrosyl sulphuric phản ứng với calix[4]aren. Sau đó, nhóm này cũng dùng quy trình tương tự để tổng hợp hetarylazo calix[6]aren [136-138]. Một công trình nghiên cứu thú vị của Bonvallet và cộng sự cho biết họ đã tổng hợp được một dẫn xuất azobenzen calix[4]aren 2 nhân và nghiên cứu khả năng tồn tại của hai đồng phân cis-trans dựa vào các thông số nhiệt động (hình 1.9) [33].
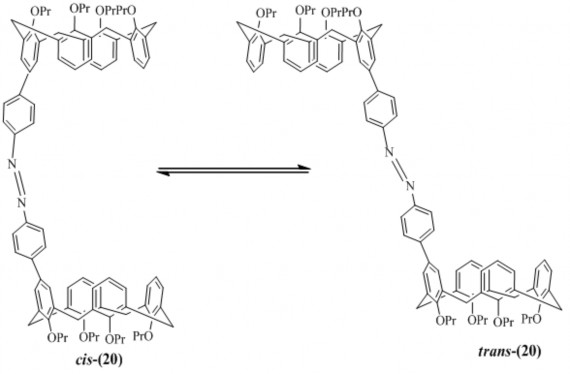
Hình 1.9. Hai dạng tồn tại cis và trans của azocalixaren (20).
1.2.2. Tính chất phổ của azocalixaren
Cấu trúc của azocalixaren được xác định thông qua tính chất phổ của chúng như UV, 1H-NMR, FT-IR, MS…Phổ UV của các dẫn xuất này có dải phổ cực đại trong khoảng 285-298nm với rất cao. Đây là kết quả của sự dịch chuyển của các electron từ π π* [48,140].
Phổ hồng ngoại IR của các dẫn xuất này có dải dao động hoá trị trong khoảng 3200-3500 cm-1 của nhóm –OH. Giá trị này có thể cao hay thấp phụ thuộc vào độ bền liên kết hydro của các nhóm –OH. Một số dao động đặc trưng như số sóng 3100-3000 cm-1 (arom, CCH), 2950-2900 cm-1 (aliph, CH), 1700-1600 cm-1 (arom C=C) và 1600-1500 cm-1 (N=N) [81].
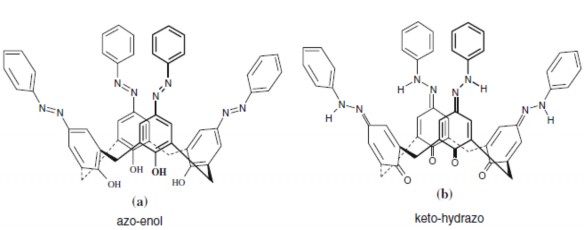
Hình 1.10. Hai dạng đồng phân hỗ biến của một azocalix[4]aren.
Bằng số liệu phổ IR, các tác giả Delegoz [48], Karakus [78,79] và Karci [80] đã chỉ ra rằng trong trạng thái rắn azocalixaren chỉ tồn tại dạng azo-enol duy nhất. Trong phổ này các hợp chất đều có dao động của nhóm –OH trong khoảng 3340-3320 cm-1 và dải dao động hoá trị của nhóm –CO tại 1196-1063 cm-1. Ngược lại, trong dung dịch chúng có thể tồn tại ở hai dạng đồng phân hỗ biến là azo-enol và keto-hydrazo (xem hình 1.10). Hai dạng tồn tại của cũng được chứng minh bằng phổ 1H-NMR qua các nghiên cứu của Ho và cộng sự [70]. Trong dung môi DMSO-d6, azocalixaren xuất hiện các tín hiệu của proton nhóm –OH ( =10,82-11,67) và của nhóm NH (
=13,56-11,57). Khi hai dạng này tách proton sẽ cho ra một anion tương ứng. Sự hỗ biến của hai dạng này phụ thuộc rất nhiều vào dung môi hoà tan và pH của môi trường. Do đó, cực đại hấp thụ của azocalixaren cũng tùy thuộc vào hai yếu tố này.
Cấu trúc của azocalixaren ở trạng thái tinh thể cũng đã được nhiều nhà khoa học quan tâm nghiên cứu. Tinh thể azocalixaren đầu tiên được công bố bởi Ehlinger và cộng sự khi kết tinh azocalixaren. Bằng kĩ thuật X-ray, nhóm nghiên cứu đã xác định được các độ dài liên kết, góc liên kết của azocalixaren [57]. Mới đây, nhóm nghiên cứu của Chang cũng đã dùng kĩ thuật X-ray để xác định được cấu trúc tinh thể của một azocalixaren [34] (xem hình 1.11).
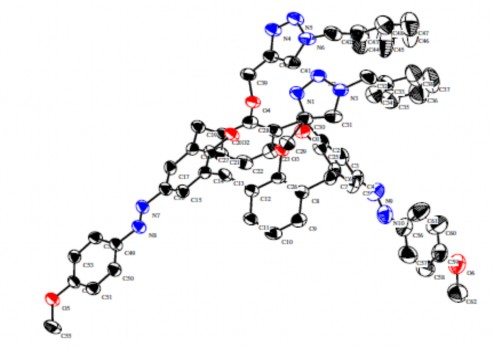
Hình 1.11. Cấu trúc tinh thể của một azocalixaren.
1.2.3. Ứng dụng của azocalixaren trong phân tích
1.2.3.1. Trong nghiên cứu tạo phức và phân tích trắc quang
Điểm nổi bật của các azocalixaren là khả năng thay đổi màu sắc của chúng khi tương tác với các ion kim loại, ion vô cơ, hữu cơ…Chính vì thế, các dẫn xuất này được các nhà hóa học phát triển ứng dụng theo hướng phân tích trắc quang hoặc huỳnh quang. Trong thời gian vừa qua, nhiều công trình nghiên cứu về ứng dụng
phức màu của các azocalixaren trong phân tích đã được công bố. Kubinyi và cộng sự cũng đã tổng hợp được 3 dẫn xuất azocalixaren và nghiên cứu khả năng tạo phức của các dẫn xuất này với các ion kim loại nhóm IA [90]. Tác giả Lang và cộng sự đã tổng hợp được một loạt dẫn xuất azocalix[4]aren và thiacalix[4]aren. Thông qua việc khảo sát phổ UV-VIS, các dẫn xuất này cho thấy có khả năng tương tác rất tốt với các ion kim loại nhóm IA [96]. Chang và cộng sự đã tổng hợp được dẫn xuất azocalix[4]aren (21) có khả năng tạo phức với Ca2+, Pb2+ (xem hình 1.12) [34].
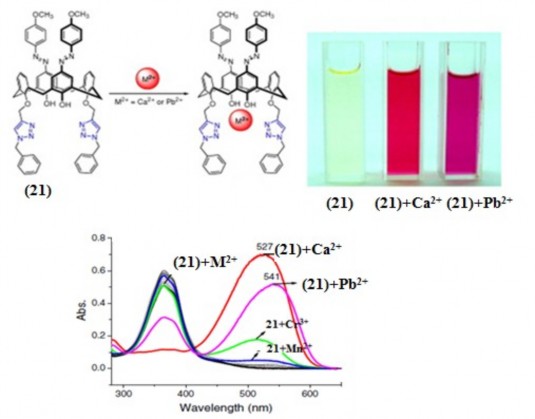
Hình 1.12. Phức màu của azocalixaren (21) với Ca2+ và Pb2+.
Trong khi đó, Chen và Chung cũng tổng hợp được dẫn xuất azocalixaren để nhận biết Ca2+ và Ba2+ [37]. Một nghiên cứu của Dong và cộng sự đã cho biết hợp chất calix[4]aren nitrophenylazo và distal etyl este có khả năng tạo phức chọn lọc với Ca2+ [53]. Khả năng tương tác của azocalixaren với các ion kim loại nặng, có độc tính cao như Hg2+, Pb2+ cũng được nhiều nhà hóa học công bố như Bingol và cộng sự đã phát triển được một bột kit kiểm tra nhanh hàm lượng Hg2+ dựa vào phức