RE
DANH MỤC BẢNG
Bảng 1. 1. Dạng tồn tại, tính chất và tính độc hại của thủy ngân 32
Bảng 3. 1. Giá trị cụ thể của các thông số trong phương trình Randle – Sevcik 54
Bảng 3. 2. Kết quả nghiên cứu các phương pháp chế tạo composit 54
Bảng 3. 3. Diện tích hoạt động điện hóa của điện cực AuNP/GCE và AuNP-GO/GCE
...................................................................................................................................59
Bảng 3. 4. Giá trị điện lượng Q trên các điện cực biến tính bởi SAM trên nền AuNP- GO 65
Bảng 3. 5. Giá trị thống kê nghiên cứu độ bền điện cực PET-SAM/AuNP 75
Bảng 3. 6. Giới hạn phát hiện và độ thu hồi thủy ngân trên điện cực PET-SAM/AuNP
Có thể bạn quan tâm!
-
 Nghiên cứu biến tính điện cực than thuỷ tinh bằng vật liệu có cấu trúc nano ứng dụng để xác định thuỷ ngân trong môi trường nước - 1
Nghiên cứu biến tính điện cực than thuỷ tinh bằng vật liệu có cấu trúc nano ứng dụng để xác định thuỷ ngân trong môi trường nước - 1 -
 Mục Đích, Phạm Vi Và Đối Tượng Nghiên Cứu Của Đề Tài
Mục Đích, Phạm Vi Và Đối Tượng Nghiên Cứu Của Đề Tài -
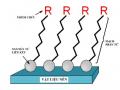
![Sơ Đồ Các Giai Đoạn Hấp Phụ Heptanethiol Trên Cu (110) [ 57]](data:image/svg+xml,%3Csvg%20xmlns=%22http://www.w3.org/2000/svg%22%20viewBox=%220%200%2075%2075%22%3E%3C/svg%3E) Sơ Đồ Các Giai Đoạn Hấp Phụ Heptanethiol Trên Cu (110) [ 57]
Sơ Đồ Các Giai Đoạn Hấp Phụ Heptanethiol Trên Cu (110) [ 57] -
![Ảnh Sem Graphen Được Chế Tạo Bằng Phương Pháp Cvd [98].](data:image/svg+xml,%3Csvg%20xmlns=%22http://www.w3.org/2000/svg%22%20viewBox=%220%200%2075%2075%22%3E%3C/svg%3E) Ảnh Sem Graphen Được Chế Tạo Bằng Phương Pháp Cvd [98].
Ảnh Sem Graphen Được Chế Tạo Bằng Phương Pháp Cvd [98].
Xem toàn bộ 138 trang tài liệu này.
...................................................................................................................................77
Bảng 3. 7. Giá trị thống kê độ lặp lại của các điện cực PET-AET-SAM/ AuNP 82

Bảng 3. 8. Kết quả phân tích hàm lượng Hg (II) trong cùng một mẫu trong hai ngày liên tiếp 82
Bảng 3. 9. Giá trị thống kê nghiên cứu độ bền điện cực PET-AET-SAM/AuNP 83
Bảng 3. 10. Giới hạn phát hiện và độ thu hồi thủy ngân trên điện cực PET-AET- SAM/AuNP 85
Bảng 3. 11. Giá trị dòng píc thủy ngân trên các điện cực khác nhau 88
Bảng 3. 12. Giá trị thống kê độ lặp lại của các điện cực PET-AET-SAM/AuNP-GO
...................................................................................................................................89
Bảng 3. 13. Giá trị thống kê nghiên cứu độ bền điện cực PET-SAM/ AuNP-GO và PET-AET-SAM/AuNP-GO 89
Bảng 3. 14. Giới hạn phát hiện và độ thu hồi thủy ngân trên điện cực PET-AET- SAM/AuNP-GO 91
Bảng 3. 15. Kết quả phân tích mẫu giả sử dụng phương pháp điện hóa 93
Bảng 3. 16. So sánh kết quả phân tích Hg (II) trong mẫu giả giữa phương pháp điện hóa và phương pháp AAS 93
Bảng 3. 17. Kết quả phân tích Hg (II) trong mẫu thực 96
DANH MỤC HÌNH VẼ
Hình 1. 1. Minh họa sự hình thành SAM trên bề mặt vật liệu nền 5
Hình 1. 2. Cấu trúc decanthiolat trên tinh thể Au (111) [45] 9
Hình 1. 3. Mô hình hấp phụ thiol trên Au (110) (hình A) và Au (100) (hình B) [52] 9 Hình 1. 4. Mô hình cấu trúc thiol trên Ag (111) [23] 10
Hình 1. 5. Sơ đồ các giai đoạn hấp phụ heptanethiol trên Cu (110) [57] 11
Hình 1. 6. Cấu trúc đề xuất của đơn lớp n-alkanoic trên bạc oxit (hình a), đồng oxit và nhôm oxit (hình b) [61] 12
Hình 1. 7. Mô hình chế tạo SAM bằng phương pháp in phun [67] 13
Hình 1. 8. Sự hình thành lớp vàng nano điện kết tủa trên bề mặt GCE [97] 17
Hình 1. 9. Ảnh SEM graphen được chế tạo bằng phương pháp CVD [98]. 18
Hình 1. 10. Ảnh SEM của SAM chế tạo theo phương pháp tạo khuôn. Vùng A: nền Au. Vùng B: dibutylamin. Vùng C: diethanolamin. Vùng D: HN(C10H21)- (C8H2F15) [99] 18
Hình 1. 11. Hình ảnh SEM của CFC-AuNDs được chuẩn bị bằng phương pháp dòng tĩnh với thời gian 240 giây [100] 19
Hình 1. 12. Mô hình phương pháp TEM 19
Hình 1. 13. Ảnh TEM của graphen [101] 20
Hình 1. 14. Nguyên lý quét thế vòng theo thời gian và phổ đồ quét thế vòng 22
Hình 1. 15. Đường CV của điện cực vàng (a) và điện cực DMTD/Au (b) trongdung dịch Fe(CN)63-/ Fe(CN)62- [103] 23
Hình 1. 16. Đường CV ảnh hưởng của thời gian ngâm khác nhau của điện cực vàng biến tính bởi C16SH nồng độ 1mM trong dung dịch Fe(CN)63-/ Fe(CN)62-[104] 23 Hình 1. 17. Đường CV của AuNP kích thước 250nm và 30 nm trong dung dịch KOH 0,5 M [105] 23
Hình 1. 18. Ảnh SEM các điện cực AuNP được chế tạo bằng các phương pháp khác nhau: áp thế cố định (a) [117], quét thế vòng (b) [120], hấp phụ hóa học (c) [119] 26 Hình 1. 19. Ảnh SEM các điện cực AuNP được chế tạo bằng các phương pháp điện hóa khác nhau: phương pháp thế tĩnh (CA) (a), quét thế vòng (CV) (b), thế tĩnh xung kép (PDP) (c) [87] 26
Hình 1. 20. Đường CV của điện cực AuNP/GCE trong dung dịch H2SO4 0,5 M [106]
...................................................................................................................................27
Hình 1. 21. (A): đường CV của điện cực Au và Au/AuNP trong dung dịch đệm photphat; (B): Ảnh SEM của điện cực Au và AuNP; (C): đường CV của điện cực Dopamin/Au và Dopamin/Au/AuNP trong dung dịch đệm photphat [22] 28
Hình 1. 22. Khảo sát bề mặt GO bằng phương pháp đo thế zeta và UV-VIS [132].29 Hình 1. 23. (a) Sự biến thiên thế theo thời gian, (b) Dạng đường von-ampe hòa tan trong kỹ thuật von-ampe xung vi phân. 35
Hình 2. 1. Hệ thống thiết bị phân tích điện hoá đa năng CPA-HH* 39
Hình 2. 2. Điện cực cacbon thủy tinh trước (a) và sau khi tạo lớp vàng nano dạng hạt: điện cực AuNP/GCE (b) 41
Hình 3. 1. Ảnh SEM của AuNP trên bề mặt GCE được xử lý bằng các kỹ thuật điện hóa khác nhau: PP1 (a), PP2 (b), PP3 (c), PP4 (d) 49
Hình 3. 2. Ảnh SEM của AuNP trên bề mặt điện cực GCE với thời gian tạo vàng khác nhau: 50 giây (a), 300 giây (b), 600 giây (c) 50
Hình 3. 3. Ảnh SEM của AuNP trên bề mặt điện cực GCE với thời gian với thời gian 600 giây trong điều kiện không khuấy (a) và có khuấy ở tốc độ 60 vòng/phút (b). .50 Hình 3. 4. Giản đồ XRD của AuNP điện kết tủa lên bề mặt GCE ở các điều kiện E = 0,5 V trong 600 giây 51
Hình 3. 5. Đường CV của các điện cực chế tạo bằng phương pháp khác nhau: PP1 (■), PP2 (▲), PP3 (▼) và AuNP/GCE (●) trong dung dịch K3(Fe(CN)6) 5 mM/PBS 0,1 M pH=7 với tốc độ quét 0,1 V/s. 53
Hình 3. 6. Ảnh hưởng của nồng độ muối vàng (a), lượng GO phân tán (b) và thời gian áp thế điện kết tủa (c) đến tín hiệu dòng Hg (II) 55
Hình 3. 7. Ảnh hưởng của pH dung dịch điện phân đến tín hiệu thủy ngân 56
Hình 3. 8. Phổ FTIR của AuNP/GCE (a) và AuNP-GO/GCE (b) 57
Hình 3. 9. Ảnh SEM của điện cực AuNP/GCE được chế tạo bằng cách áp thế 0,5 V, thời gian áp thế 600 giây trong dung dịch HAuCl4 (a) và AuNP-GO/GCE (b) được chế tạo bằng cách áp thế 0,5 V, thời gian áp thế 600 giây trong hỗn hợp dung dịch HAuCl4+GO.(thay ảnh SEM) 58
Hình 3. 10. Đường CV trên điện cực AuNP (●) và AuNP-GO (■) trong dung dịch K3(Fe(CN)6) 5 mM/PBS 0,1 M pH=7 với tốc độ quét 0,1 V/s. 58
Hình 3. 11. Phổ von-ampe vòng khử hấp phụ của PET-SAM/Au-NP/GCE (■) và AuNP/GCE (●) đo trong dung dịch KOH 0,5 M, v = 0,1 V/s. PET-SAM được chế tạo từ dung dịch PET có nồng độ 1 mM, thời gian ngâm 12 tiếng 60
Hình 3. 12. Phổ von-ampe vòng khử hấp phụ của AET-SAM/AuNP/GCE (●) và AuNP/GCE (■) đo trong dung dịch KOH 0,5 M, v = 0,1 V/s. AET-SAM được chế tạo từ dung dịch AET có nồng độ 1 mM, thời gian ngâm 12 tiếng 62
Hình 3. 13. Phổ von-ampe vòng khử hấp phụ của PET-AET-SAM/AuNP/GCE (■) và AuNP/GCE (●), đo trong dung dịch KOH 0,5 M, v = 0,1 V/s. PET-AET-SAM được chế tạo từ dung dịch PET có nồng độ 1 mM, thời gian ngâm 12 tiếng và AET có nồng độ 0,1 mM, thời gian ngâm 20 phút 64
Hình 3. 14. Phổ von-ampe vòng khử hấp phụ của điện cực AET-SAM/ AuNP-GO (■), PET-SAM/AuNP-GO (●) và PET-AET-SAM/AuNP-GO(▲) AET-SAM và
PET-SAM được chế tạo từ dung dịch tương ứng có nồng độ 3 mM, thời gian ngâm 3 tiếng. PET-AET-SAM được chế tạo từ dung dịch PET có nồng độ 3 mM, thời gian ngâm 3 tiếng và AET có nồng độ 0,1 mM, thời gian ngâm 20 phút đo trong dung dịch KOH 0,5 M, v = 0,1 V/s 65
Hình 3. 15. Phổ DPASV phát hiện Hg (II) đo trong dung dịch KCl 0,1 M và HCl, pH
= 3 sử dụng điện cực PET-SAM (hình trái), AET-SAM (hình phải), trong dung dịch Hg (II) nồng độ 1ppb với thời gian làm giàu 30 phút. 69
Hình 3. 16. Sự ảnh hưởng của chiều quét Von-Ampe đến chiều cao píc: quét chiều catot (●) và quét theo chiều anot (■). Các phổ xung vi phân được đo với PET- SAM/AuNP/GCE làm giàu trong dung dịch Hg (II) 1 ppb với thời gian ngâm 30 phút
...................................................................................................................................70
Hình 3. 17. Ảnh hưởng của thời gian áp thế đến tín hiệu thủy ngân 71
Hình 3. 18. Phổ DPASV phát hiện Hg (II) của PET-SAM/Au đĩa (■) và PET- SAM/AuNP (●) sau khi làm giàu trong dung dịch Hg (II) 1 ppb với thời gian ngâm 30 phút, ghi đo trong dung dịch KCl 0,1 M +HCl, pH=3 72
Hình 3. 19. Sự ảnh hưởng của các cation trong dung dịch đến tín hiệu ipHg(II) 73
Hình 3. 20. Sự ảnh hưởng của các anion Cl-(●), SO42- (▼) và NO3- (■) đến tín hiệu ipHg(II) 74
Hình 3. 21. Sự biến đổi dòng píc Hg (II) ở nồng độ 1 ppb theo số lần sử dụng của điện cực PET-SAM/AuNP 75
Hình 3. 22. Phổ DPASV và đường chuẩn theo chiều cao píc trên điện cực PET- SAM/AuNP khi nồng độ thủy ngân tăng dần từ 100 ppt đến 1000 ppt 76
Hình 3. 23. Phổ DPASV phát hiện thủy ngân ở nồng độ 1ppb sử dụng PET-AET- SAM/Au-NP/GCE được chuẩn bị bằng cách ngâm PET- SAM trong 0,1 mM AET với thời gian khác nhau (Hình nhỏ: Sự phụ thuộc của tín hiệu dòng thủy ngân vào thời gian ngâm trong dung dịch AET ở nồng độ 0,1 mM) 78
Hình 3. 24. Phổ DPASV phát hiện thủy ngân ở nồng độ 1ppb sử dụng PET-AET- SAM/Au-NP/GCE được chuẩn bị bằng cách ngâm PET- SAM trong dung dịch AET 20 phút với nồng độ ngâm khác nhau. (Hình nhỏ: Sự phụ thuộc của tín hiệu dòng thủy ngân vào nồng độ ngâm trong dung dịch AET với thời gian ngâm 20 phút) 79
Hình 3. 25. Phổ DPASV phát hiện Hg (II) sử dụng điện cực AET-SAM(▲), PET- SAM (●), PET-AET-SAM (■) trong dung dịch Hg (II) nồng độ 1 ppb với thời gian làm giàu 30 phút 80
Hình 3. 26. Sự phụ thuộc giưa tín hiệu dòng và số lần đo lặp lại (7 lần) trên điện cực AuNP tại cùng nồng độ Hg(II) 1 ppb trong dung dịch KCl 0,1 M + HCl pH = 3 81
Hình 3. 27. Sự biến đổi dòng píc Hg (II) ở nồng độ 1 ppb theo số lần sử dụng của điện cực PET-AET-SAM/AuNP 83
Hình 3. 28. Phổ DPASV và đường chuẩn theo chiều cao píc trên điện cực PET-AET- SAM/AuNP khi nồng độ thủy ngân tăng dần từ 50 ppt đến 2000 ppt 84
Hình 3. 29. Ảnh hưởng của nồng độ PET (a), nồng độ AET (b), thời gian ngâm PET (c), thời gian ngâm AET (d) đến tín hiệu thủy ngân 86
Hình 3. 30. Ảnh hưởng thời gian ngâm đến tín hiệu thủy ngân 87
Hình 3. 31. Phổ DPASV phát hiện Hg (II) sử dụng điện cực PET-AET-SAM/AuNP- GO (■), PET-SAM/AuNP-GO (▲) và PET-AET-SAM/AuNP (●) trong dung dịch Hg (II) nồng độ 1ppb với thời gian ngâm 30 phút. 87
Hình 3. 32. Độ lặp lại của các điện cực PET-AET-SAM/ AuNP-GO qua 7 lần đo trong dung dịch Hg (II) nồng độ 1ppb 88
Hình 3. 33. Sự biến đổi dòng píc Hg (II) ở nồng độ 1 ppb theo số lần sử dụng của điện cực PET-SAM/ AuNP-GO và PET-AET-SAM/AuNP-GO 89
Hình 3. 34. Phổ DPASV và đường chuẩn theo chiều cao píc trên điện cực PET-AET- SAM/ AuNP-GO khi nồng độ thủy ngân tăng dần từ 30 ppt đến 3500 ppt 90
Hình 3. 35. Phổ DPASV của điện cực PET-SAM trước (●) và sau (■) khi làm sạch bằng phương pháp điện hóa. Phổ Von-Ampe đo với mẫu có chứa Hg 1ppb 92
Hình 3. 36. Đường thêm chuẩn (hình trái) và phổ DPASV (hình phổ) của phép phân tích mẫu giả có nồng độ 1 ppb 93
Hình 3. 37. Đồ thị thêm chuẩn (hình trái) và phổ DPASV (hình phải) xác định Hg (II) trong mẫu nước biển Hải Tiến (Thanh Hóa) 94
Hình 3. 38. Đồ thị thêm chuẩn (hình trái) và phổ DPASV (hình phải) xác định Hg (II) trong mẫu nước biển Lạch Vạn (Nghệ An). 95
Hình 3. 39. Đồ thị thêm chuẩn (hình trái) và phổ DPASV (hình phải) xác định Hg (II) trong mẫu nước thải nhà máy bóng đèn phích nước Rạng Đông (Hà Nội) 95
Hình 3. 40. Phổ DPASV phat hiện Hg (II) của mẫu nước không qua xử lý (■) và được xử lý điện hóa (●), sử dụng điện cực PET-AET-SAM / AuNP - GO 97
Hình 3. 41. Ảnh hưởng của thế áp (a); nồng độ KCl (b); Thời gian điện phân (c); và thời gian khuấy (d) đến tín hiệu Hg (II) 98
Hình 3. 42. Đồ thị thêm chuẩn (hình trái) và phổ DPASV (hình phải) xác định Hg (II) trong mẫu nước song Tô Lịch đã qua xử lý 99
MỞ ĐẦU
1. Lý do lựa chọn đề tài
Vấn đề ô nhiễm môi trường ngày càng trở nên đáng báo động ở nhiều quốc gia trên thế giới, đặc biệt là ô nhiễm nguồn nước do ảnh hưởng trực tiếp tới sức khỏe cộng đồng. Một trong các tác nhân gây ảnh hưởng đó là sự có mặt của kim loại nặng trong các nguồn nước. Trong đó, thủy ngân và các hợp chất của thủy ngân là một trong những tác nhân ô nhiễm có độc tính cao, có thể gây ảnh hưởng xấu tới sức khỏe con người khi xâm nhập vào cơ thể ở một lượng lớn hơn cho phép. Đặc biệt, khi tiếp xúc với nồng độ thủy ngân mặc dù ở nồng độ thấp nhưng nếu kéo dài vẫn có thể dẫn đến các vấn đề ở hệ tiêu hóa, hệ thống thần kinh, tiết niệu... Chính vì vậy, tổ chức Y tế Thế giới đã quy định giới hạn cho phép thủy ngân trong nước uống phải nằm trong khoảng hàm lượng vết (1 g / L) [1]. Do hàm lượng thủy ngân bị giới hạn ở mức thấp nên các phương pháp phân tích cần có độ nhạy và độ chính xác cao.
Một số phương pháp phân tích sử dụng thiết bị hiện đại đa tính năng cho phép phân tích phát hiện thủy ngân ở hàm lượng siêu vết được sử dụng phổ biến là: quang phổ tử ngoại – khả kiến (UV-VIS) [2], huỳnh quang tia X (XRF) [3], quang phổ hấp thụ nguyên tử (AAS) [4,5], huỳnh quang nguyên tử (AFS) [6], phổ khối plasma cảm ứng (ICP-MS) [7], hay quang phổ phát xạ nguyên tử cảm ứng (ICP-AES) [8,9]. Các phương pháp hiện đại này có độ chính xác cao. Tuy nhiên, việc đầu tư trang thiết bị ban đầu rất lớn, quy trình xử lý mẫu và vận hành máy phức tạp. Do đó, phương pháp phân tích điện hóa đã được đưa vào sử dụng với mục đích giảm giá thành phân tích cũng như trang thiết bị ban đầu, đơn giản hóa việc xử lý mẫu phân tích mà vẫn có độ chính xác, độ nhạy cao và độ lặp lại tốt.
Trong phương pháp phân tích điện hóa, để phân tích được hàm lượng vết đều phải qua quá trình làm giàu bằng phương pháp điện hóa. Thông thường, việc làm giàu các kim loại nặng thường được tiến hành nhờ dòng điện để khử các ion kim loại nặng trong mẫu nước. Sản phẩm của quá trình này sẽ được tích tụ làm giàu trên bề mặt điện cực. Tuy nhiên, sử dụng điện thế áp trong quá trình làm giàu có thể gây ảnh hưởng đến độ chọn lọc của phương pháp, bởi trong quá trình làm giàu, có thể có các chất đồng thời bị khử cùng các ion kim loại cần phân tích do thế khử của các chất này không khác nhiều so với thế khử làm giàu của các chất cần phân tích. Vì vậy, một kỹ
1


![Sơ Đồ Các Giai Đoạn Hấp Phụ Heptanethiol Trên Cu (110) [ 57]](https://tailieuthamkhao.com/uploads/2022/07/13/nghien-cuu-bien-tinh-dien-cuc-than-thuy-tinh-bang-vat-lieu-co-cau-truc-nano-4-1-120x90.jpg)
![Ảnh Sem Graphen Được Chế Tạo Bằng Phương Pháp Cvd [98].](https://tailieuthamkhao.com/uploads/2022/07/13/nghien-cuu-bien-tinh-dien-cuc-than-thuy-tinh-bang-vat-lieu-co-cau-truc-nano-5-1-120x90.jpg)