Qua đó cho thấy sự bất lợi của quá trình khi thừa sắt. Nồng độ cao của Fe2+ hoặc Fe3+ dẫn đến sự hình thành kết tủa sắt ở các giá trị pH cao hơn (pH> 2,5) và làm giảm hiệu suất dòng điện.
Bên cạnh đó năm 2006, Deng và cộng sự báo cáo khi tăng nồng độ ion Fe2+ cũng làm giảm nồng độ •OH và làm tăng độ dẫn điện của nước thải [61]. Việc đưa vào nồng độ chất xúc tác lớn có thể không hiệu quả vì tạo ra lượng lớn bùn oxit sắt.
Từ các kết quả và đánh giá với công bố trước đây luận án lựa chọn sử dụng [Fe2+] = 0,1mM để nghiên cứu trong quá trình EF tiếp theo.
3.1.5. Ảnh hưởng của nồng độ chất điện li Na2SO4 đến khả năng xử lý glyphosateChất điện li Na2SO4 có ảnh hưởng đến hiệu quả xử lý bằng quá trình EF. Trong nghiên cứu của Ruiz và cộng sự năm 2013 đã khẳng định nồng độ của chất điện phân ảnh hưởng đến hiệu quả xử lý bằng quá trình EF khi nghiên cứu ảnh hưởng của nồng
độ chất điện ly đến tính chất điện hóa của AB5 đối với Ni/MH [150].
Để nghiên cứu ảnh hưởng nồng độ chất điện li các điều kiện thí nghiệm: [glyphosate] = 0,1mM; nồng độ chất xúc tác ban đầu [Fe2+] = 0,1mM; pH = 3; mật độ dòng điện 8,333 mA/cm2; d = 1 cm. Nồng độ chất điện li Na2SO4 lần lượt tại: 0,025M; 0,05M; 0,075M; 0,1M.
Hình 3.8 cho kết quả như sau: khi tăng nồng độ Na2SO4 từ 0,025M ữ 0,05M thì hiệu suất phân hủy glyphosate tăng từ 53,03% lên 80,94%. Điều này được giải thích khi nồng độ Na2SO4 tăng dẫn đến độ dẫn điện cũng tăng, khi đó tốc tộ di chuyển của ion trong dung dịch tăng lên, các ion đi về phía điện cực nhanh hơn qua đó các sản phẩm tạo thành nhanh, đồng thời thúc đẩy khả năng phân hủy glyphosate.
Năm 2007, Zhou công bố khả năng xử lý metyl đỏ tăng từ 56,8% lên đến gần 80% khi nồng độ Na2SO4 tăng. Nồng độ chất điện phân thấp có thể không cung cấp đủ độ dẫn điện cho quá trình EF. Trong báo cáo này kết luận mật độ dòng điện cao khi các dung dịch điện phân có nồng độ Na2SO4 cao, tương ứng với tốc độ sản xuất H2O2 tăng lên góp phần tạo ra nhiều gốc •OH, qua đó nâng cáo hiệu suất của quá trình và giảm tiêu thụ năng lượng [121].
Bờn cạnh đú, kết quả trờn Hỡnh 3.8, khi tăng nồng độ từ 0,05 M ữ 0,1 M thỡ hiệu suất phân hủy glyphosate lại giảm từ 80,94%; 72,93%; 69,06% lần lượt Na2SO4 tại nồng độ 0,05M; 0,075M; 0,1M
0,025 M
Có thể bạn quan tâm!
-
 Bảng Pha Chất Nuôi Bùn Hoạt Tính
Bảng Pha Chất Nuôi Bùn Hoạt Tính -
 Nghiên Cứu Xử Lý Glyphosate Bằng Quá Trình Fenton Điện Hóa
Nghiên Cứu Xử Lý Glyphosate Bằng Quá Trình Fenton Điện Hóa -
 Ảnh Hưởng Của Khoảng Cách Điện Cực Đến Khả Năng Xử Lý Glyphosate
Ảnh Hưởng Của Khoảng Cách Điện Cực Đến Khả Năng Xử Lý Glyphosate -
 Phổ Chuẩn Glyphosate Trên Thư Viện Phổ Của Máy Lcms/ms
Phổ Chuẩn Glyphosate Trên Thư Viện Phổ Của Máy Lcms/ms -
 Nghiên Cứu Các Yếu Tố Ảnh Hưởng Đến Mbr Để Xử Lý Thứ Cấp Glyphosate
Nghiên Cứu Các Yếu Tố Ảnh Hưởng Đến Mbr Để Xử Lý Thứ Cấp Glyphosate -
 Ảnh Hưởng Của Chế Độ S/d Lên Khả Năng Xử Lý Glyphosate
Ảnh Hưởng Của Chế Độ S/d Lên Khả Năng Xử Lý Glyphosate
Xem toàn bộ 229 trang tài liệu này.
0,05 M
0,075 M
0,1 M
100
80
Hiệu suất xử lý TOC (%)
60
40
20
0
0 10 20 30 40 50 60
Thời gian (phút)
Hình 3.8. Ảnh hưởng của nồng độ chất điện li Na2SO4 đến khả năng xử lý glyphosate Điều này giải thích khi nồng độ Na2SO4 tăng trên 0,05M có thể dẫn đến gốc
•OH tham gia phản ứng với Na2SO4 bởi phương trình phản ứng 3.12 và 3.13 [121] qua đó làm giảm gốc •OH tham gia vào phản ứng 1.1 và ảnh hưởng đến hiệu suất quá trình.
•OH+ SO42- → OH- + SO4•- (3.12)
SO4•- + e-→ SO42- (3.13)
Kết quả này so với các công bố khi sử dụng nồng độ chất điện li Na2SO4 0,05M
cụ thể:
Trong nghiên cứu của Ghoneim và cộng sự, hiệu quả của sử dụng chất điện li
KCl, NaCl và Na2SO4 ở cùng nồng độ 0,05M được so sánh và cho tốc độ mất màu tối đa của sunset yellow FCF [58]. Hiệu quả loại bỏ màu đạt 100% trong thời gian lần lượt của Na2SO4 0,05M là 120 phút và của NaCl, KCl là 180 phút.
Năm 2014, nhóm của El – Ghenymy nghiên cứu quá trình xử lý 230 mL sulanilamit 0,006M; pH = 3, I = 300 mA, [Na2SO4] = 0,05M bởi quá trình EF với điện cực Pt/vải C. Sau 360 phút xử lý bằng quá trình EF dung dịch đã được xử lý hoàn toàn [151].
Từ kết quả nghiên cứu trên, luận án lựa chọn nồng độ [Na2SO4] = 0,05M làm cơ sở để nghiên cứu xử lý glyphosate trong quá trình EF.
3.1.6. Ảnh hưởng của nồng độ glyphosate ban đầu đến khả năng xử lý của quá trình Fenton điện hóa
Để nghiên cứu ảnh hưởng của nồng độ glyphosate ban đầu đến khả năng xử lý của quá trình EF, các điều kiện thực hiện tại pH = 3, [Fe2+] = 0,1 mM, mật độ dòng điện: 8,333 mA/cm2, d = 1 cm, nồng độ glyphosate lần lượt: 0,05mM; 0,1mM; 0,2mM; 0,4mM. Thực hiện thí nghiệm trong 60 phút liên tục và tiến hành xác định giá trị TOC tại các thời điểm 0, 10, 20, 30 phút. Từ đó xác định điều kiện phù hợp để thực hiện quá trình EF.
0,05 mM
0,1 mM
0,2 mM
0,4 mM
100
80
Hiệu suất xử lý TOC (%)
60
40
20
0
0 5 10 15 20 25 30
Thời gian (phút)
Hình 3.9. Ảnh hưởng của nồng độ glyphosate ban đầu đến quá trình EF
Sự phụ thuộc của nồng độ TOC vào thời gian điện phân và nồng độ glyphosate được thể hiện trên Hình 3.9.
Hình 3.9 cho thấy rằng khi nồng độ ban đầu của glyphosate càng lớn thì hiệu quả xử lý tăng. Điều này được giải thích: theo định luật tác dụng khối lượng, tốc độ của phản ứng phân hủy glyphosate bởi gốc (•OH) tỷ lệ thuận với nồng độ các chất tham gia, do đó khi nồng độ ban đầu của glyphosate càng lớn, trong khi lượng gốc (•OH) ít thay đổi, thì tốc độ phân hủy glyphosate nhanh, điều này giúp khả năng khoáng hóa glyphosate tăng khi tăng nồng độ ban đầu của chất thamg gia phản ứng (glyphosate).
Mặt khác trên Hình 3.10, cho thấy tỷ lệ loại bỏ chất ô nhiễm đã tăng lên khi tăng nồng độ ban đầu của glyphosate, tuy nhiên tốc độ tăng của hiệu suất không tuyến tính với nồng độ glyphosate. Lúc này, khi tăng nồng độ glyphosate ban đầu thì hiệu quả khoáng hóa giảm dần. Trên Hình 3.10 nhận thấy sau 20 phút điện phân, hiệu suất đạt là 32,6% ở nồng độ 0,05mM; 54,97% tại nồng độ 0,1mM; 69,06% tại nồng độ 0,2mM và 79,63% tại 0,4mM. Kết quả này được giải thích như sau: trong quá trình phân hủy glyphosate trong dung dịch diễn ra không hoàn toàn và tạo ra các sản phẩm phụ. Các sản phẩm tạo ra này tiếp tục tham gia phản ứng với gốc hydroxyl tự do (•OH) và cạnh tranh giữa gốc hydroxyl tự do (•OH) và glyphosate do đó tuy hiệu quả khoáng hóa vẫn tăng khi tăng nồng độ glyphosate ban đầu, tuy nhiên tốc độ tăng chậm dần.
100
Hiệu suất xử lý TOC (%)
80
60
40
4 6 8 10 12 14
Nồng độ glyphosate (mgC/L)
Hình 3.10. Hiệu suất xử lý TOC sau 20 phút khi xử lý glyphosate bằng quá trình EF Năm 2009, nhóm của Rosales đã nghiên cứu xử lý thuốc nhuộm với nồng độ
ban đầu cao dẫn đến tạo ra các sản phẩm trung gian của phản ứng, làm giảm lượng gốc hydroxyl tự do (•OH) để phân hủy các chất ô nhiễm qua đó hiệu suất quá trình EF giảm [152].
Trong báo cáo nghiên cứu của Jasmann năm 2016 cho rằng mặc dù hiệu quả xử lý tăng không tuyến tính khi tăng nồng độ chất ô nhiễm ban đầu nhưng khối lượng chất ô nhiễm được loại bỏ vẫn cao khi tăng nồng độ chất ô nhiễm ban đầu [153].
Xu thế ảnh hưởng nồng độ đầu của glyphosate cũng góp phần giải thích sự biến thiên hiệu suất theo thời gian: trong khoảng thời gian đầu của quá trình điện phân, TOC của dung dịch giảm rất nhanh, nhưng khi thời gian lâu hơn thì khả năng khoáng hóa TOC giảm chậm.
Qua nghiên cứu trên chứng mình quá trình EF sẽ diễn ra nhanh khi nồng độ các chất ô nhiễm hữu cơ ban đầu cao, do đó EF sẽ phù hợp nếu áp dụng trong tiền xử lý các chất ô nhiễm.
3.1.7. Nghiên cứu động học và các sản phẩm phụ của quá trình phân hủy glyphosate
3.1.7.1. Nghiên cứu động học của quá trình phân hủy glyphosate
Trên cơ sở các điều kiện phù hợp cho quá trình EF, tiến hành thí nghiệm điện phân dung dịch glyphosate ở các điều kiện này để đánh giá hiệu quả quá trình oxy hóa và động học quá trình phân hủy glyphosate, cụ thể như sau: nồng độ glyphosate 0,1mM, [Fe2+] = 0,1mM, [Na2SO4] = 0,05M, mật độ dòng điện 8,333 mA/cm2, pH = 3, d = 1 cm. Mẫu được lấy tại: 5 phút, 10 phút, 15 phút, 20 phút, 30 phút, 40 phút để phân tíchTOC và nồng độ còn lại của glyphosate.
Kết quả trên Hình 3.11 cho thấy nồng độ glyphosate và giá trị TOC luôn giảm dần theo thời gian điện phân. Tuy nhiên glyphosate còn lại giảm nhanh hơn nồng độ TOC còn lại. Qua 40 phút điện phân có 91,87% glyphosate được loại bỏ và hiệu suất loại bỏ TOC tương ứng là 79,83%, thấp hơn hiệu quả loại bỏ glyphosate. Kết quả này chứng tỏ có sản phẩm phụ được tạo ra.
Qua cách ước tính nồng độ sản phẩm phụ thu được từ quá trình phân hủy glyphosate thông qua giá trị nồng độ TOC, nồng độ sản phẩm tăng lên trong 15 phút đầu tiên và sau đó gần như không đổi trong quá trình điện phân. Có thể giải thích do một số chất trung gian tương đối bền và làm chậm quá trình phân hủy glyphosate, chẳng hạn như axit cacboxylic được biết là có hằng số tốc độ phản ứng tương đối thấp với gốc (•OH). Ngoài ra, sự tồn tại của một số phức chất của Fe3+ với một số axit cacboxylic nhất định có thể không bị oxy hóa bởi gốc (•OH) trong dung dịch cũng làm chậm quá trình phân hủy glyphosate.
Động học của quá trình phân hủy glyphosate trong điều kiện thích hợp: d = 1 cm; [Fe2+] = 0,1mM, [Na2SO4] = 0,05M; pH = 3, mật độ dòng điện là 8,333 mA/cm2. Vì hằng số tốc độ cho phản ứng của gốc hydroxyl với các hợp chất hữu cơ rất lớn (từ
107 – 1010 L/mol.s) trong khi thời gian tồn tại của nó là rất ngắn (10-9 s). Do đó coi nồng độ (•OH) ổn định trong suốt quá trình EF, động học của phản ứng phân hủy glyphosate được coi là giả bậc nhất.
TOC
Glyphosate
Sản phẩm trung gian
4
3
Nồng độ (mgC/L)
2
1
0
0 10 20 30 40
Thời gian (phút)
Hình 3.11. Nồng độ của glyphosate, sản phẩm trung gian và TOC theo thời gian xử lý bằng quá trình EF
Biểu thức tốc độ phân hủy glyphosate với gốc hydroxyl được viết theo phương trình: Glyphosate + •OH→ sản phẩm
𝑑[𝑔𝑙𝑦𝑝ℎ𝑜𝑠𝑎𝑡𝑒] = kabs.[ •OH].[glyphosate] = kapp[glyphosate]
𝑑𝑡
Trong đó kapp = kabs.[ •OH] và kabs là hằng số tốc độ tuyệt đối của quá trình phân hủy glyphosate bời gốc hydroxyl [•OH].
Kapp là hằng số tốc độ biểu kiến của quá trình phân hủy glyphosate bởi gốc hydroxyl.
Ta có biểu thức tích phân:
𝑑 [𝐺𝑙𝑦𝑝ℎ𝑜𝑠𝑎𝑡𝑒] = kapp.dt
[𝐺𝑙𝑦𝑝ℎ𝑜𝑠𝑎𝑡𝑒]
Tích phân 2 vế của biểu thức ta có:
=
0
𝐶 𝑑[𝐺𝑙𝑦𝑝ℎ𝑜𝑠𝑎𝑡𝑒] 0
∫ 𝑘
.dt
𝐶 [𝐺𝑙𝑦𝑝ℎ𝑜𝑠𝑎𝑡𝑒]
∫𝑡
𝑎𝑝𝑝
Khai triển tích phân 2 vế ta được: Ln(𝐶0) = kapp.t
𝐶
Như vậy theo lý thuyết, Ln(𝐶0) tỷ lệ tuyến tính với t.
𝐶
Thời gian (phút)
Thời gian (phút)
Nồng độ glyphosate (mg/L)
Hình 3.12. Động học của quá trình phân hủy dung dịch glyphosate
Hình 3.12 thể hiện kết quả thực nghiệm của giá trị nồng độ glyphosate theo thời gian. Kết quả cho thấy lượng glyphosate còn lại giảm dần theo thời gian theo hàm số mũ. Cũng trên Hình 3.12, đồ thị giữa Ln (C0/Ct) và thời gian có dạng đường thẳng (với R2 =0,996); chứng tỏ động học của phản ứng phân hủy glyphosate bởi gốc (•OH) là giả bậc nhất. Trong phản ứng giả bậc nhất hằng số tốc độ của phản ứngtheo đồ thị là 0,063 (phút-1). Một số chất có hằng số tốc độ phản ứng sau khi được xử lý bằng quá trình EF cụ thể: thuốc nhuộm DO61 là 0,301 (phút-1) [125], xanh malachit là 0,39 (phút-1), tinh thể tím (0,36 phút-1), xanh metyl là (0,15 phút-1).
3.1.7.2. Sản phẩm của quá trình phân hủy glyphosate sau xử lý bằng quá trình EF
Trong luận án này, tác giả không đi sâu nghiên cứu cơ chế quá trình phân hủy glyphosate bằng quá trình EF mà kế thừa các công bố trước đây để xác định một số sản phẩm phụ (dễ phân hủy sinh học) có thể tạo thành trong quá trình tiền xử lý glyphosate bằng EF làm cơ sở để nghiên cứu quá trình MBR phía sau.
Thật vậy, theo một số nghiên cứu trước đây, công nghệ AOPs có thể phân hủy glyphosate theo hai con đường: tạo thành AMPA và axit glycolic (phân cắt liên kết C–
N) hoặc sarcosine và PO43- (phân cắt liên kết C–P) (Hình 3.13). Theo Yang và cộng sự
[154] quá trình phân hủy glyphosate bằng xúc tác quang đi theo con đường sarcosine,
sản phẩm phụ sinh ra sau đó là glycine, formadehit, axit formic. Theo Balci và cộng sự
[155] quá trình giả EF sử dụng xúc tác Mn2+ phân hủy glyphosate tạo thành các sản phẩm trung gian AMPA và axit glycolic, sau đó tiếp tục bị phân hủy tạo ra các axit cacboxylic. Theo Lan và cộng sự [129] quá trình oxy hóa điện hóa phân hủy glyphosate theo con đường sarcosine, tạo thành các sản phẩm phụ là glycine, axit glycolic, axit oxamic. Còn theo Barrett và cộng sự [156], quá trình oxy hóa bằng MnO2 sẽ phân hủy glyphosate sarcosine, sản phẩm phụ tạo thảnh chủ yếu là glycine và axit formic.
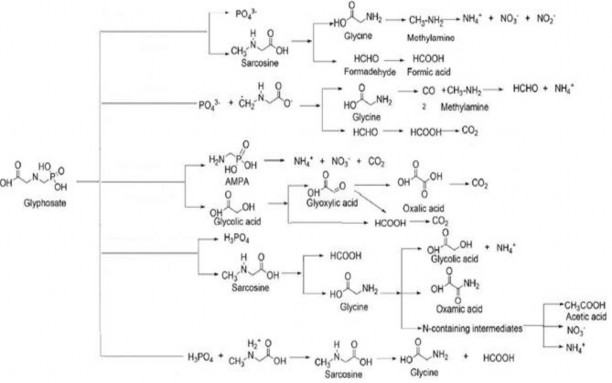
Hình 3.13. Con đường phân hủy glyphosate bằng một số quá trình AOP [129,154]
Có thể thấy rằng phần lớn các quá trình AOP phân hủy glyphosate theo con đường sarcosine, tạo thảnh sản phẩm phụ chủ yếu là glycine. Trong luận án để xác định sản phẩm sinh ra trong quá trình xử lý glyphosate bằng EF, tiến hành thực nghiệm điện phân dung dịch glyphosate với nồng độ đầu 16,9 mg/L, [Fe2+]= 0,1mM, [Na2SO4] = 0,05M, mật độ dòng điện là 8,333 mA/cm2, pH = 3, thời gian điện phân là 60 phút, d = 1,0 cm. Tiến hành lấy mẫu trước điện phân trước và sau khi điện phân 60 phút, mẫu được đo bằng hệ thống sắc ký lỏng khối phổ 2 lần LCMS/MS để xác định glyphosate và sản phẩm thứ cấp của glyphosate.






